аномальное отсутствие почек при рождении кроссворд
Аномалии развития почек
Аномалии развития почек – это внутриутробное нарушение формирования почек, обусловленное генетическими мутациями и воздействием тератогенных факторов на плод в первом триместре беременности. Проявляются болями в поясничной области, приступами почечной колики, повышением температуры, общей слабостью, изменениями в моче и крови. Диагностируются при помощи УЗИ с допплерографией, экскреторной урографии, КТ, МРТ, лабораторных анализов и иных методик. Лечение аномалий развития почек включает уросептики, антибиотики, гипотензивные препараты. По показаниям проводится удаление добавочной почки, удаление кисты и другие операции.
МКБ-10
Общие сведения
Аномалии развития почек – самые распространенные пороки развития. На их долю приходится 30-40% всех врожденных аномалий. Наиболее часто встречается удвоение почек и поликистоз, последний нередко сопровождается кистозной дисплазией соседних органов. Имеются гендерные различия по некоторым порокам. Так, варианты аплазии чаще встречаются у мальчиков, а удвоение почек – в два раза чаще у девочек. Прогноз при данной патологии в большинстве случаев достаточно благоприятный за исключением тяжелых сочетанных пороков и двухсторонних аномалий. Актуальность пороков мочевыделительной системы в современной педиатрии определяется их весомой долей в структуре всех врожденных заболеваний и важностью фильтрационной функции почек, потеря которых требует трансплантации органа со всеми ее сложностями.
Причины
Как и любые пороки, аномалии развития почек формируются внутриутробно вследствие неправильной закладки, дифференцировки тканей и персистенции клеток эмбриональных структур. Патологии могут возникать в результате воздействия на плод вредных факторов: лекарственных препаратов (антибиотиков, ингибиторов АПФ), радиации, инфекционных агентов. Если причиной является генетическая поломка, аномалии развития почек сочетаются с пороками другой локализации, образуя различные синдромы. В зависимости от того, какой именно процесс нарушается, речь может идти о дисплазии, дистопии и других аномалиях.
Классификация
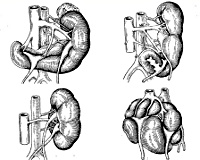
Аномалии развития почек делятся на аномалии количества, структуры, положения и аномалии сосудов. Такие аномалии развития почек часто сочетается с другими пороками мочеполовой системы.
Симптомы аномалий почек
Неправильно развитая или расположенная почка клинически ничем не проявляет себя, патология часто обнаруживается случайно. Двусторонние пороки обычно заметны в короткие сроки после рождения из-за недостаточной функции органа. Наиболее грубые аномалии развития почек (агенезия) даже в одностороннем варианте часто приводят к летальному исходу в первые месяцы и годы жизни не только по причине выраженной почечной недостаточности, но и потому, что почти всегда сопровождаются пороками развития скелета и различных органов.
Гипоплазия, добавочная почка, удвоение и поликистоз почек могут проявляться симптомами пиелонефрита, который возникает в результате нарушения оттока мочи. Ребёнок жалуется на боли в поясничной области, может наблюдаться повышение температуры и признаки интоксикации. Аномалии развития почек часто сопровождаются артериальной гипертензией, поскольку почки участвуют в регуляции артериального давления (ренин-ангиотензиновая система).
Одним из клинических признаков добавочной почки является недержание мочи. Также возможны приступы почечной колики. Пациент или его родители могут предъявлять жалобы на изменения в моче: появление крови, мутная моча, моча цвета «мясных помоев».
Диагностика
Пренатальная диагностика многих аномалий развития почек возможна с 13-17 недели беременности, когда можно заподозрить порок по отсутствию закладки в месте расположения почки либо заметить отсутствие мочевого пузыря, что также является косвенным признаком аномалий почек. Клиническая диагностика осуществляется при наличии симптомов со стороны мочевыделительной системы. В этом случае врач-педиатр назначает анализы мочи и крови, чтобы оценить функцию почек и выявить признаки воспаления. Также можно обнаружить возбудителя вторичного пиелонефрита для проведения прицельной антибиотикотерапии.
Аномалии развития почек подтверждаются при помощи инструментальных методов обследования;
Лечение аномалий развития почек
При отсутствии клинических признаков лечение не требуется. Консервативная терапия включает антибиотики для лечения инфекционного поражения почек, гипотензивные препараты, уросептики. Хирургическое вмешательство показано при выраженном стенозе чашечно-лоханочной системы, дистопии и любых других аномалиях развития почек в случае, если методы консервативной терапии оказываются неэффективными. Проводится удаление добавочной или удвоенной почки, стентирование сосудов и почечных лоханок. Удаление кист не требует оперативного вмешательства с использованием открытого доступа, содержимое эвакуируется путём прокола в процессе эндоскопической операции.
Прогноз и профилактика
Прогноз при аномалиях развития почек чаще благоприятный. Как уже было сказано, функции мочевыделительной системы часто остаются в норме. Медикаментозное и оперативное лечение также быстро приводят к улучшению состояния ребёнка. Исключение составляют грубые сочетанные пороки и двусторонние аномалии, при которых может потребоваться трансплантация почки и регулярный гемодиализ. Профилактика аномалий развития почек проводится во время беременности. Необходимо соблюдение диеты, исключение вредных привычек и коррекция соматического статуса.
Аномальное отсутствие почек при рождении кроссворд
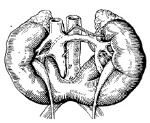
Почка образуется из метанефрогенного тяжа и зачатка мочеточника. Последний возникает на 5-й неделе беременности из мезонефрального (вольфова) протока и проникает в метанефрогенный тяж — область недифференцированной мезенхимы на нефрогенном гребне. Зачаток мочеточника в процессе развития проделывает приблизительно 6 разветвлений и к 20-й неделе образует всю собирательную систему почки — мочеточник, почечную лоханку, чашечки, сосочковые протоки и собирательные трубочки. Под индуцирующим влиянием зачатка мочеточника на 7-й неделе беременности начинается дифференцировка нефрона.
К 20-й неделе, т. е. к моменту образования собирательной системы, имеется около 30 % нефронов. Скорость их образования можно описать экспоненциальной функцией. К 36-й неделе оно полностью завершается.
Агенезия почек
Двусторонняя агенезия почек несовместима с жизнью во внеутробный период. Вскоре после рождения дети погибают от гипоплазии легких. Сочетание агенезии почек и гипоплазии легких известно под названием синдрома Поттпера. Этот синдром сопровождается характерной лицевой дизморфией. «Лицо Поттера» включает гипертелоризм, эпикант, низкое расположение ушных раковин, широкий сплющенный нос, микрогнатию. Кроме того, наблюдаются аномалии конечностей. О двусторонней агенезии почек следует подумать, если при УЗИ определяется маловодие и не удается визуализировать почки и мочевой пузырь плода. Двусторонняя агенезия почек встречается с частотой 1:3000 новорожденных, что составляет 20 % фенотипа Поттера.
Он наблюдается также при кистозной дисплазии почек и обструктивной уропатии, реже при аутосомно-рецессивном (младенческом) поликистозе, гипоплазии или медуллярной дисплазии почек.
Агенезия — врожденное отсутствие почки вследствие аномалии зачатка мочеточника. Ее следует отличать от аплазии — крайней формы дисплазии, при которой бугорок нефункционирующей ткани покрывает нормальный или аномальный мочеточник. Однако клинически дифференцировать их трудно. Термин «наследственная адисплазия почек» относят к случаям, когда в нескольких поколениях одной и той же семьи наблюдается агенезия, дисплазия, мультикистозная дисплазия или их сочетание. «Адисплазия» почек наследуется аутосомно-доминантно с пенетрантностью 50-90 % и вариабельной экспрессией. Наследственная «адисплазия» и двусторонняя агенезия почек сопровождаются пороками развития заднего прохода и прямой кишки, сердечно-сосудистой системы и скелета.
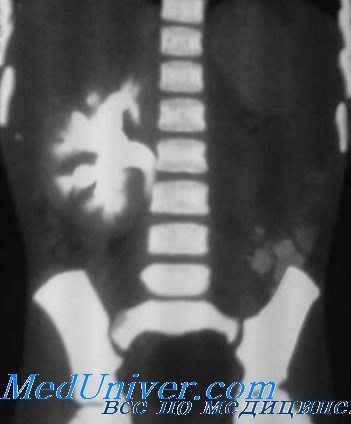
Односторонняя агенезия почки обычно выявляется при обследовании по поводу других пороков развития или заболеваний мочевой системы. Частота односторонней агенезии почек повышена у новорожденных с единственной почечной артерией. При истинной односторонней агенезии отсутствует мочеточник с той же стороны и соответствующая половина треугольника мочевого пузыря. Имеющаяся почка подвергается компенсаторной гипертрофии, отчасти пренатально, но преимущественно постнатально. Приблизительно в 15 % случаев со стороны единственной почки имеется пузырно-мочеточниковый рефлюкс. У мужчин односторонняя агенезия почки в большинстве случаев сопровождается отсутствием вольфова протокают соответственно, семявыносящего протока с той же стороны.
Поскольку вольфов проток тесно связи с мюллеровым, у девочек односторонняя агенезия почки нередко сопровождается пороками развития половых органов, в частности синдромом Майера-Рокитанского-Кюстера-Хаузера: односторонняя агенезия или эктопия почки, порок развития маточных труб и матки и агенезия влагалища. Диагноз односторонней агенезии почки обычно ставят на основании того, что почка не визуализируется при УЗИ и экскреторной урографии. В части случаев при этом имеет место гипоплазия или мультикистозная дисплазия почки с последующим полным кистозным перерождением. В клинических условиях особой необходимости дифференцировать подобные вторичные изменения и истинную одностороннюю агенезию почки нет. Важнее в отсутствии почки по данным УЗИ выполнить экскреторную урографию или сцинтиграфию, чтобы исключить эктопию почки. Если единственная почка сформирована правильно, ее функция может оставаться нормальной на протяжении всей жизни.
Вопрос о том, допустимы ли при односторонней агенезии почки занятия спортом, связанным с риском травмы (футбол, карате), остается спорным. С одной стороны, этим занятиям не препятствует то обстоятельство, что у человека селезенка, печень, головной мозг не являются парными. К тому же утрата одной почки из-за спортивной травмы явление очень редкое. С другой стороны, известно, что единственная почка компенсаторно гипертрофирована, из-за чего недостаточно прикрыта ребрами, поэтому ее тяжелая травма смертельно опасно ААП рекомендует оценивать опасность спортивных занятий в каждом случае индивидуально.
Причины генетического бесплодия
Согласно оценкам экспертов Всемирной организации здравоохранения, около 50 миллионов супружеских пар во всем мире (что составляет примерно 7% от их общего количества) не могут завести ребенка из-за мужского и/или женского бесплодия. На данный момент считается, что в 50% случаев причиной являются генетические нарушения.
Современная наука достигла больших успехов в изучении причин генетического бесплодия, особенно с появлением метода секвенирования нового поколения (next generation sequencing, NGS), позволяющего быстро и с минимальными трудозатратами «читать» последовательность ДНК. Тем не менее, этот вопрос остается сложным, и в имеющихся на данный момент знаниях остается еще немало пробелов.
Существует множество генов, влияющих на мужскую и женскую репродуктивную функцию. Например, в одних только яичках мужчины экспрессируется около 2300 генов. Наука продолжает развиваться, и список доступных анализов ежегодно пополняется новыми генетическими тестами.
Генетические изменения, способные приводить к невозможности зачатия и вынашивания беременности, бывают разными:
Хромосомные аномалии
Хромосомные нарушения представляют большой интерес в аспекте вопросов бесплодия, так как они ответственны более чем за половину всех выкидышей в первом триместре беременности. В большинстве случаев хромосомные аномалии не наследуются – они возникают случайно в половых клетках или клетках эмбриона. При этом происходят выкидыш, мертворождение, либо ребенок рождается с серьезными пороками развития.
В каждой клетке человеческого тела содержится 46 хромосом. В яйцеклетке и сперматозоиде их по 23 – соответственно, ребенок получает половину набора от матери и половину от отца. Состояние, при котором меняется количество хромосом, называется анеуплоидией. Некоторые примеры, связанные с бесплодием:
Помимо изменений количества хромосом, встречаются нарушения их структуры – аберрации.
Их основные разновидности:
Моногенные заболевания
Моногенные заболевания характеризуются возникновением мутации в одном гене, отвечающем за синтез определенного белка. Эти патологии передаются от родителей детям, причем типы наследования бывают разными.
В настоящее время известно много моногенных мутаций, связанных с бесплодием. Их список постоянно пополняется.
Мультифакториальные заболевания
Мультифакториальные, или полигенные заболевания имеют сложный патогенез. В их развитии принимают участие генетические нарушения (как наследственные, так и приобретенные), образ жизни, воздействия внешней среды. На «неправильные» гены накладываются такие факторы, как особенности питания, уровень физической активности, экологическая обстановка, вредные привычки, стрессы, прием различных лекарственных препаратов и пр.
Типичные примеры мультифакториальных заболеваний – сахарный диабет и сердечно-сосудистые патологии. Среди причин женского бесплодия важное значение имеют следующие заболевания:
Эпигенетические изменения
Эпигенетические изменения возникают в результате различных процессов, когда последовательность ДНК остается нормальной, но меняется активность генов. Например, это происходит в результате метилирования – прикрепления особых метильных групп к определенным участкам ДНК. Некоторые научные исследования показали, что эпигенетические механизмы играют роль в развитии бесплодия.
В каких случаях рекомендуется пройти генетическое тестирование?
Обычно врачи направляют пациентов на консультации к клиническим генетикам в следующих случаях:
Генетик собирает семейный анамнез, анализирует родословную и при необходимости назначает анализы. Для диагностики причин генетического бесплодия применяют разные методы: цитогенетический анализ, полимеразную цепную реакцию (ПЦР), флуоресцентную гибридизацию in situ (FISH), микрочипирование, секвенирование нового поколения.
Чтобы выявить распространенные аномалии у плода, на 16–20-й неделях беременности проводят тройной тест. По показаниям выполняют различные инвазивные исследования. Более современный и точный метод диагностики – неинвазивное пренатальное тестирование (НИПТ), во время которого изучают ДНК плода в крови матери.
Если у одного или обоих партнеров из пары, страдающей бесплодием, выявляют генетические нарушения, в ряде случаев могут помочь различные методы лечения или вспомогательные репродуктивные технологии (ЭКО, ИКСИ). Но иногда проблему не удается решить. В таких ситуациях врач предложит рассмотреть возможность использования донорских яйцеклеток или сперматозоидов.
С возрастом репродуктивные возможности уменьшаются, а в клетках накапливаются мутации, которые могут помешать наступлению и вынашиванию беременности, вызвать тяжелые патологии у ребенка. Поэтому женщинам, которые планируют забеременеть после 35 лет, стоит подумать о возможности сохранить свои яйцеклетки в криобанке. В дальнейшем ими можно воспользоваться в любое время – это будет своего рода «страховка» репродуктивной функции.
Если вы решили сохранить собственные половые клетки или воспользоваться донорскими, важно подобрать надежный банк половых клеток. На данный момент Репробанк является одним из крупнейших на территории России и СНГ. Наше криохранилище оснащено новейшим оборудованием, а в каталоге представлено большое количество доноров, среди которых любая пара наверняка сможет подобрать подходящего.
Зиновьева Юлия Михайловна
Ведёт генетическое обследование доноров Репробанка, осуществляет подбор доноров для пар, имеющих ранее рождённых детей с установленной генетической патологией.
Хроническая почечная недостаточность у детей
Содержание статьи
Это патология, при которой почки полностью или частично не справляются с выделительной функцией, утрачивают способность очищать кровь. Симптомы почечной недостаточности у детей более выражены, чем у взрослых. Заболевание протекает тяжело, может быстро прогрессировать, приводить к инвалидности и смерти.
Зная, как проявляется почечная недостаточность у детей, вы сможете своевременно обратиться к врачу и начать лечение. Грамотная диагностика и лечебные мероприятия позволяют избежать последствий и сохранить жизнь.
Общие признаки заболевания
Вас должны насторожить следующие проявления:
Острая почечная недостаточность
Это неспецифический синдром, возникающий при острой утрате гомеостатических функций почек. Симптоматика ярко выражена и проявляется внезапно. Прекращается или резко сокращается объем выводимой мочи. Токсичные вещества из организма ребенка не выводятся, происходит интоксикация продуктами метаболизма. В течение нескольких дней проявляются симптомы, напоминающие отравление – ребенок становится вялым, его тошнит или рвет. Источник:
О.И. Андриянова, Ф.К. Манеров, Ю.А. Чурляев, И.Г. Хамин
Причины и лечение острой почечной недостаточности у детей //
Общая реаниматология, 2007, III, 4, с.70-75
Почему возникает и как протекает заболевание у детей разного возраста
В первые сутки новорожденный может не мочиться, признаком патологии является отсутствие мочи на третьи сутки. Особенности физиологического строения почек в неонатальном периоде не позволяют определить заболевание у младенцев в первые двое суток. Источник:
Iseki K., Ikemiya Y, Iseki C., Takishita S.
Proteinuria and the risk of developing end-stade renal disease //
Kidney Int. 2003; 63:1468-1473
В период новорожденности проблемы могут возникнуть по следующим причинам:
У детей от 1 месяца до 3 лет проблемы возникают на фоне острых кишечных патологий, инфекции почек, гемолиза, нарушения обменных процессов.
Причинами острой почечной недостаточности у детей 3-14 лет являются: тяжелые травмы, отравление лекарственными средствами, инфекционные заболевания, наличие камней или опухолей, которые закупоривают желчевыводящие пути.
Стадии развития и симптомы
Как проводится диагностика?
Главным симптомом острой почечной недостаточности у детей, по которому можно заподозрить патологию, является резкое сокращение объема мочи. Чтобы подтвердить диагноз, необходимо исследование мочи и крови.
При ОПН наблюдается:
Хроническая почечная недостаточность
Патология развивается, если не лечить острую форму. ХПН – это состояние, при котором наблюдается анемия, нарушается фосфорно-кальциевый обмен, повышается артериальное давление. Причиной ХПН у детей может быть отравление лекарствами и тяжелыми металлами, недолеченные инфекции и заболевания мочевыделительной системы:
У детей до 3 лет развитие заболевания часто вызвано аномалиями развития мочевыводящих путей, наследственностью, дисплазией почечной ткани.
Причинами хронической почечной недостаточности у детей от 10 лет являются приобретенные болезни: поражения органов при туберкулезе, сахарном диабете. В группу риска входят дети с нарушением внутриутробного развития, с обструктивными заболеваниями. Источник:
Т.И. Раздолькина
Особенности хронической почечной недостаточности у детей //
Трудный пациент, 2013, №2-3, т.11, с.16-20
Стадии развития ХПН
Лечение заболевания
При острой форме, когда сильная интоксикация организма, необходима неотложная медицинская помощь. Требуется вызывать «скорую» для госпитализации и проведения мероприятий по дезинтоксикации. Врачи промывают желудок, очищают пищевод энтеросорбентами. В случае угрозы жизни делают гемосорбцию или гемодиализ. Лечение хронической почечной недостаточности у детей проводится для восстановления работы почек и замедления патологических процессов. Курс составляется индивидуально с учетом причины и состояния пациента. В зависимости от формы болезни и клинической картины назначают медикаментозное или активное лечение. На вопрос, перерастет ли ребенок ХПН, никто не сможет ответить, необходимо соблюдать предписания и контролировать состояние клубочковой фильтрации.
Консервативные методы
Активные методы
Если лекарства не помогают, показана терапия с помощью специальных аппаратов с целью предотвращения рецидивов и поддержания жизнедеятельности.
Последствия и осложнения
При несвоевременной диагностике и некорректном лечении могут возникнуть тяжелые осложнения. Развитие болезни приводит к сокращению почечных функций, нарушению работы систем и органов, отравлению продуктами обмена, к необратимым последствиям.
Среди опасных осложнений:
При наличии патологии ребенок отстает в развитии, плохо входит в коллектив, имеет трудности в развитии речи.
Профилактика у детей
Внимательное отношение родителей к появлению первых признаков позволяет полностью вылечить заболевание без последствий. Клинические рекомендации по профилактике хронической почечной недостаточности у детей:
При подозрении на патологию нужно немедленно обратиться к врачу. Чтобы не допустить врожденных заболеваний, будущей маме следует придерживаться здорового питания и образа жизни.
Источники:
Все врачи детские нефрологи
Драбовская Наталья Юрьевна
Основная специальность : нефролог
Дополнительная специальность : педиатр
Дунайский пр-т, д. 47 (м. Дунайская)
Цена приёма : 1750 рублей Что входит в стоимость?
Драбовская Наталья Юрьевна
Основная специальность : нефролог
Дополнительная специальность : педиатр
Дунайский пр-т, д. 47 (м. Дунайская)
Цена приёма : 1750 рублей Что входит в стоимость?
Автор:
Акушер-гинеколог, врач ультразвуковой диагностики
Рецензент:
Акушер-гинеколог, врач ультразвуковой диагностики, генетик
Агенезия почки у плода: что это такое
Неблагоприятные внешние факторы, влияющие на беременную женщину, иногда, вопреки всем защитным механизмам, могут приводить к нарушениям внутриутробного развития плода. У ребенка агенезия почки (двусторонняя или, что бывает чаще, односторонняя) встречается в 1 случае из 1100-1200 родов, и иногда эта патология становится довольно серьезным испытанием для родителей.
Что такое агенезия почки
Эта аномалия может быть полной или неполной. При полном отсутствии почки речь идет об агенезии. При наличии хотя бы части органа, говорят о его аплазии. Очень часто одновременно с отсутствием почки отмечается недоразвитие, частичное или полное отсутствие мочеточника. В последнем случае в мочевом пузыре нет даже устья мочеточника.
Чаще отсутствует орган с левой стороны, хотя возможна и правосторонняя аномалия. Двусторонний процесс встречается гораздо реже.
Симптомы аномалии
Одностороннее нарушение может не проявляться даже до достижения зрелого возраста. Нередко его обнаруживают случайно при обследовании по поводу других болезней. Впрочем, это более актуально для взрослых. Современные методы скрининга позволяют выявить аномалию у плода еще на ранних стадиях его развития, хотя это и довольно сложно.
При подозрении на агенезию или аплазию почки с рождения следует брать во внимание наличие таких сопутствующих аномалий, как:
Эти нарушения гораздо более заметны и заставляют опытного врача задуматься — нет ли у малыша и других аномалий, незаметных при обычном осмотре.
В течение жизни всю работу по очистке крови от «мусора» берет на себя вторая почка, которая еще во внутриутробном периоде увеличивается в размерах. Это называется «компенсаторная гипертрофия». Избыточный ее объем повышает риск разного рода заболеваний. Некоторые научные данные свидетельствуют о том, что со временем у таких людей возникает вначале гломерулопатия (ухудшение фильтрационной функции единственной почки), а затем и артериальная гипертензия. Правда, эту теорию еще исследуют.
Дети с аплазией почек (или агенезией) умирают в первые 2 суток от дыхательной недостаточности, так как из-за маловодия у них не развиваются легкие. Известны редкие случаи нормального развития дыхательных органов, но и тогда малыши погибают от почечной недостаточности в первые недели жизни.
Лечение агенезии почек
При двусторонней аномалии лечение невозможно. При односторонней форме агенезии почек у ребенка нет нужды в каком-либо вмешательстве, так как имеющийся орган вполне справляется с функцией очищения крови. Однако из-за того, что такие дети находятся в группе риска по различным почечным заболеваниям, их рано берут на учет нефролог или уролог. В случае развития инфекционных заболеваний их лечат по общим правилам, учитывая факт наличия единственной почки. При травмах врач обязан использовать все возможные методы, чтобы сохранить орган (у здоровых людей иногда удаление одной из почек при ее травме является операцией выбора).
Инвалидность при агенезии почки совсем не обязательна. Зачастую люди проживают вполне нормальную жизнь, ни разу не обратившись к врачу с почечными заболеваниями. Однако если почка начинает не справляться со своими функциями, начинают нарастать явления почечной недостаточности. Когда это состояние достигает 2А-степени (при количестве креатинина в плазме крови равном 0,14-0,44 и скорости клубочковой фильтрации – 20-50%), пациент получает право пройти медико-санитарную экспертизу и получить группу инвалидности. Если у вас возникли вопросы, запишитесь на личный прием к нашим специалистам. Запись на сайте Добробут.ком и по вышеуказанным телефонам.