Чем вредны гормональные уколы
Гормонотерапия в гинекологии: мифы и реальность
Современная гинекология не может обойтись без использования гормональных препаратов. Вместе с тем назначение гормональных средств часто пугает людей, так как о них распространено много недостоверной либо устаревшей информации. Постараемся разобраться в необходимости применения данных препаратов и развеять самые распространенные мифы о гормонотерапии.
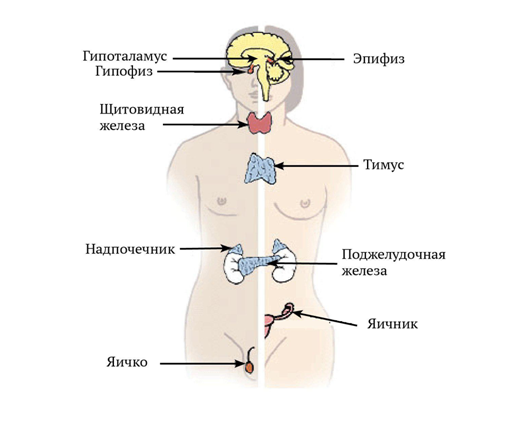
Гормоны – специальные химические посредники, регулирующие работу всего организма. Основная часть гормонов производится в железах внутренней секреции: щитовидной и паращитовидных железах, гипофизе, надпочечниках, поджелудочной железе, яичниках у женщин и яичках у мужчин. Гормональные препараты – не что иное, как синтетические аналоги наших природных гормонов.
В акушерстве и гинекологии гормонотерапия применяется относительно давно и приносит довольно впечатляющие результаты, особенно сегодня, с появлением новых высокоэффективных гормональных препаратов, лишенных серьезных побочных действий своих предшественников.
Гормонотерапия необходима в следующих случаях
Менопаузальная гормональная терапия
Гормонотерапия необходима для поддержания состояния здоровья женщины в период климакса, когда репродуктивная функция организма снижается и происходит угасание выработки гормонов яичниками. Дефицит гормона эстрогена провоцирует нарушения психоэмоционального и физического состояния. Зачастую у женщины возникают проблемы в сексуальной жизни: снижается либидо, беспокоит дискомфорт во время полового контакта.
В основе заместительной гормональной терапии лежит восполнение недостатка либо отсутствия гормонов яичников медикаментозными препаратами, аналогичными по структуре и эффекту, что значительно улучшает качество жизни пациентки.
Гормональная контрацепция
Гормональная контрацепция (оральные контрацептивы, гормоносодержащие спирали, пластыри, импланты, инъекционные контрацептивы) является высокоэффективным методом предохранения от нежелательной беременности. С контрацептивной целью используются синтетические аналоги эстрогенов и прогестерона и их производные. Помимо основной функции защиты данные препараты нормализуют менструальный цикл, снижают вероятность доброкачественных опухолей (миомы матки, эндометриоза, кист яичников), а также оказывают лечебное воздействие при наличии данных и других гинекологических заболеваний (синдром поликистозных яичников).
Гормоны в лечении бесплодия
В настоящее время лечение бесплодия и невынашивания беременности – одно из приоритетных направлений акушерства. Значение гормональных препаратов в программе ЭКО сложно переоценить. Вспомогательные репродуктивные технологии получили распространение и дают высокий процент положительных результатов, то есть наступивших беременностей, в первую очередь благодаря успехам фармацевтических компаний в разработке и производстве высокотехнологичных аналогов эндогенных гормонов. Благодаря им возможна стимуляция суперовуляции для развития нескольких доминантных фолликулов. Такой эффект гормональных препаратов, как торможение функции яичников, также используется в протоколах ЭКО для подавления собственных гонадотропинов и создания оптимального фона для стимуляции экзогенными гонадотропинами. После переноса эмбриона в полость матки необходимо применение препаратов прогестерона, так как его недостаток снижает вероятность имплантации, может привести к прерыванию беременности на ранних сроках. Кроме того, благодаря искусственным гормонам удается наладить работу яичников и избавиться от других проблем, препятствующих зачатию (полипы эндометрия, эндометриоз и др.).
Главные заблуждения
Гормоны прописывают только при очень тяжелых заболеваниях.
Для назначения гормонов нет необходимости дожидаться тяжелых, запущенных стадий заболевания. Более того, грамотная и своевременная гормональная коррекция может избавить от проблемы или приостановить ее развитие при использовании минимально эффективных доз и в кратчайшие сроки.
Если вовремя не выпить гормональную таблетку, ничего страшного не произойдет.
Гормональные препараты, особенно контрацептивы, надо принимать строго по часам. К примеру, противозачаточная гормональная таблетка действует 24 часа, то есть принять ее необходимо раз в день для поддержания эффективной концентрации вещества в сыворотке крови. Опоздание более чем на 12 часов может резко снизить контрацептивный эффект, возможны спонтанная овуляция и наступление незапланированной беременности.
Если принимать гормоны, они накапливаются в организме.
В корне неверно, поскольку требование строгого приема гормонального лекарства как раз и связано с тем, что при попадании в организм гормон сразу распадается на химические соединения, а они, в свою очередь, выводятся из организма.
При беременности гормональные препараты не выписывают.
Выписывают. Если до беременности у женщины были гормональные нарушения, то во время вынашивания плода ей требуется лекарственная поддержка, чтобы уровень половых гормонов был в норме и ребенок нормально развивался. При необходимости назначают и другие гормоны: гормоны щитовидной железы – при гипотиреозе, кортикостероидные гормоны – при некоторых системных заболеваниях, для подавления андрогенов коры надпочечников, инсулин – при диабете и т. д. Отказ от терапии во время беременности из-за страха навредить плоду не имеет под собой научной основы, напротив, плод страдает при отсутствии необходимой коррекции.
У гормональных препаратов много побочных эффектов, в первую очередь, увеличение массы тела.
Препараты первого и второго поколения контрацептивов действительно могли вызвать эффект прибавки в весе из-за большого содержания гормонов. В настоящее время производители выпускают микродозированные противозачаточные средства с видоизмененной структурой активных веществ, что практически не провоцирует колебания веса. Гормональные препараты назначают на достаточно длительный срок, организм к концу первого-второго месяцев адаптируется, и большинство женщин не ощущают никакого дискомфорта.
Гормонам всегда можно найти альтернативу.
Не всегда. Есть ситуации, когда гормональные препараты незаменимы. Скажем, у молодой женщины (до 50 лет) были удалены яичники, в результате она начала быстро стареть и терять здоровье. В этом случае ее организм до 55–60 лет нуждается в обязательной поддержке гормонотерапией. Разумеется, при условии, что основное заболевание (из-за которого были удалены яичники) не имеет противопоказаний к такому назначению.
Гормональные препараты нельзя принимать долгое время.
Главное требование – правильный подбор гормонального препарата. Принимать грамотно подобранный препарат при условии ежегодного контроля можно годами без перерывов. Длительный прием не только не оказывает вредного воздействия на организм, но и, напротив, помогает наладить менструальный цикл, предотвращает развитие доброкачественных заболеваний молочных желез, эндометриоза, миомы, кист яичника, а также улучшает качество волос и кожи.
Десятый миф об аллергии: вред лечения гормонами
Так считают не только пациенты, а и многие врачи.
Стероидофобия (страх перед гормонами)-такая же болезнь, как и сама аллергия. Тут больше вреда не от лечения. Тем более, когда речь о вреде препаратов, не имеющим к гормонам никакого отношения.
Гормональный препарат НЕ равно гормон.
Последние-это биологически активные вещества, которые производит наш организм для управления своими функциями. Поскольку природа экономна, то у одного гормона есть сразу несколько эффектов.
Гормональный препарат-это искусственно созданное вещество с ОДНИМ эффектом природного гормона.
Переводя это на аллергию- с противоаллергическим эффектом.
То, чего боятся больные стероидофобией-это другие эффекты гормонов, типа набора веса, угрей, целлюлита или потери либидо.
Гормональные препараты, созданные для лечения именно аллергии НЕ обладают такими эффектами.
Ещё больные стероидофобией боятся «привыкания к гормонам», хотя с точки зрения медицины речь скорее о зависимости. Имеется в виду факт невозможности отказаться от лечения из-за обострения болезни после отмены.
Обострение аллергической болезни происходит не из-за отмены гормонального препарата, а по причине отсутствия устранения
Для лечения этой поломки существует иммунотерапия в нескольких вариантах.
Провокаторы обострений-это вещества, на которые реагирует поломанный иммунитет производством иммуноглобулинов Е (аллергены) или атакой тучных клеток (триггеры).
Факторы микросреды, способствующие напряжению поломанного иммунитета: курение (пассивное особенно), сухой воздух, пыль, вредная и не по возрасту пища, дефицит свежего воздуха и физических нагрузок, сидячий образ жизни, частое посещение людных мест, эмоциональные и психологические перегрузки.
Заканчивая эту десятку мифов, подчеркну, что их сотни.
Поэтому, аллергику важно найти СВОЕГО врача, который будет давать индивидуальную информацию о его заболевании и подбирать необходимые именно ему методы терапии.
Блок об аллергии закрыт.
Следующий блок мифов будет посвящён вакцинации.
Что такое гормонотерапия: принцип действия, осложнения
Что такое гормоны?
Гормоны – биологически-активные вещества, которые вырабатываются эндокринными железами и переносятся с кровью до органов-мишеней, где выполняют определенные биохимические и физиологические регуляторные функции – отвечают за рост и развитие организма, обмен веществ, половую и репродуктивную функции.
Центральным звеном эндокринной системы являются структуры головного мозга – гипоталамус и гипофиз, которые отправляют сигналы для увеличения или снижения выработки уровня гормонов.
К периферическим эндокринным железам относятся щитовидная железа, паращитовидные железы, надпочечники, поджелудочная железа, яичники у женщин, яички у мужчин. Соответственно, гормонотерапия – это один из видов лечения не только в онкологии, но и в эндокринологии, гинекологии.
В онкологии гормонотерапия – это один из видов противоопухолевого лечения, который блокирует или уменьшает уровень гормонов в организме с целью остановки или прекращения роста опухоли.
Гормонопрепараты применяются только при гормонально-активных опухолях, к которым относятся: рак молочной железы, рак предстательной железы, в некоторых случаях – при раке яичников и раке эндометрия (раке тела матки). Гормонотерапия применяется и с симптоматической целью. Например, глюкокортикостероиды используются с целью премедикации перед проведением химиотерапии и таргетной терапии, или аналоги соматостатина назначаются для уменьшения карциноидного синдрома при нейроэндокринных опухолях.
История развития гормонотерапии в онкологии начинается с 60-х годов, когда доктор Дора Ричардсон разработала формулу препарата тамоксифен в рамках исследования новых противозачаточных препаратов. Но было выявлено, что он не обладает контрацептивным эффектом. О препарате решили забыть, но доктор Артур Валпоулу инициировал другое клиническое исследование по изучению тамоксифена для лечения рака молочной железы. К 80-м годам была доказана высокая эффективность этого препарата не только при лечении распространенных, но и ранних стадий рака молочной железы.
Гормонотерапия при раке молочной железы
Гормонотерапия при раке молочной железы применяется:
Антиэстрогены: тамоксифен, торемифен, ралоксифен
Механизм действия большинства гормональных препаратов довольно схожий. Суть заключается в том, что тамоксифен связывается с рецепторами эстрогена, вытесняет и блокирует его действие.
Таблетки тамоксифена принимаются ежедневно и длительно. В связи с чем, возникают побочные эффекты, например, приливы. Они наблюдатся у 50% пациентов. С приливами можно бороться немедикаментозными методами: изменение образа жизни, отказ от курения и употребления алкоголя, регулярные занятия спортом, уменьшение количества потребляемого кофеина, избегание стрессовых ситуаций.
Если немедикаментозные методы не помогают, то применяются антигипертензивные препараты (препараты, понижающие артериальное давление), антидеприссанты, антиконвульсанты и противосудорожные препараты. Две последние группы препаратов назначаются только врачом-неврологом или врачом-психотерапевтом.
Пациентам обязательно нужно сообщать врачам любых специальностей о том, что они принимают какие-либо препараты. Поскольку, например, тамоксифен может вступать в лекарственное взаимодействие с антидепрессантом пароксетином. Пароксетин – это один из препаратов выбора при лечении приливов. Соответственно, при длительном одновременном употреблении этих препаратов может возникнуть лекарственное взаимодействие, которое приведет к снижению противоопухолевой эффективности тамоксифена.
К побочным эффектам при применении антиэстрогенов относится гиперплазия эндометрия у женщин в постменопаузе. Дело в том, что антиэстрогены являются блокаторами эстрогенов в тканях молочной железы, но в ткани эндометрия они, наоборот, стимулируют действие эстрогенов, и возникают соответствующие побочные эффекты. Поэтому при появлении кровянистых выделений из половых путей, необходимо незамедлительно сообщать об этом лечащему врачу. При дообследовании будет либо продолжаться лечение томаксифеном, либо произойдет смена лекарственной терапии.
Также существуют сведения о повышении риска развития рака эндометрия. Но поскольку было проведено большое количество клинических исследований, которые доказали высокую эффективность тамоксифена для снижения риска развития рецидива рака молочной железы, преимуществ при применении тамоксифена намного больше, чем вероятность развития рака эндометрия.
Также могут возникать тромбоэболические осложнения, поэтому при возникновении боли в нижних конечностях, в грудной клетке и кашля необходимо незамедлительно об этом сообщать врачу. Поскольку это может свидетельствовать о серьезных осложнениях и жизнеугрожающих состояниях.
Под воздействием тамоксифена может возникнуть генитоуринарноый синдром, который характеризуется сухостью влагалища, снижением либидо. Также есть сведения о более частом возникновении депрессивных состояний и о повышении риска развития катаракты у пациентов, принимающих тамоксифен.
Антагонисты рецепторов эстрогена
К антагонистам рецепторов эстрогена относится фулвестрант. Он обладает высоким сродством к рецепторам эстрогена и разрушает их. При этом он не проявляет собственной эстрогеноподобной активности, поэтому у него нет такого побочного эффекта, как гиперплазия эндометрия у женщин в менопаузе.
К побочным эффектам применения антагонистов рецепторов эстрогена относятся реакция в месте введения, приливы, слабость, головные боли.
Фулвестрант – это препарат для инъекций, вводится один раз в месяц. В первый месяц – два раза: в первый и в пятнадцатый дни.
Ингибиторы ароматазы
К ингибиторам ароматазы относятся летрозол, анастразол, эксеместан. Они воздействуют на фермент – ароматазу, который способствуют образованию эстрогенов из андрогенов.
Ароматаза – это основной источник эстрогенов у женщин в постменапаузе. Поэтому ингибитор ароматазы назначается только в постменапаузе либо при дополнительной овариальной супрессии, которая достигается медикаментозным, хирургическим или лучевым методами.
Ингибиторы ароматазы – это таблетки, которые применяются длительно и ежедневно.
К побочным эффектам относятся суставные и мышечные боли. Есть сведения о повышении риска переломов костей, поэтому при необходимости могут быть назначены остеомодифицирующие агенты. Также увеличивается риск развития сердечно-сосудистых заболеваний, может повышаться уровень холестерина в крови.
С целью овариальной супрессии могут использоваться аналоги гонадотропин-релизинг гормона. К ним относятся гозерелин, бусерелин, лейпролерин. Соответственно, они назначаются при сохранной функции яичников при необходимости овариальной супрессии. Они ингибируют секрецию лютеинизирующего гормона и фолликулостимулирующего гормона.
К побочным эффектам их применения относятся увеличение массы тела, приливы, слабость. Эти препараты вводятся подкожно или внутримышечно раз в месяц (но существуют депо-формы, т.е. формы пролонгированного действия, они могут вводиться раз в три месяца).
Гормонотерапия предстательной железы
С целью гормонотерапии рака предстательной железы используется андроген-депривационная (угнетающая) терапия. С этой целью может проводиться двухсторонняя орхиэктомия – хирургическое удаление яичек. Могут применяться агонисты лютеинизирующего гормона релизинг гормона (ЛГРГ) либо лютеинизирующего гормона релизинг гормона.
При приеме агонистов на 3-5 день может возникнуть синдром вспышки, т.е. усиление симптомов, поэтому они назначаются при раке предстательной железы совместно с антиандрогенами.
Гормонотерапия рака предстательной железы назначается при локализованном, местнораспространенном и метастатическом заболевании.
Антагонист лютеинизирующего гормона релизинг гормона – это дегареликс. Механизм его действия заключается в том, что он конкурентно связывается с рецептором ЛГРГ в гипофизе, но при этом не возникает синдрома вспышки. К побочным эффектам его применения относятся приливы, боли в месте инъекции. Инъекция дегареликса выполняется раз в месяц, в первый месяц – два укола в один день, затем каждый месяц – по одному уколу.
Антиандрогены
К антиандрогенам относятся флутамид, бикалутамид, нилутамид, энзалутамид, ципротерона ацетат. Они блокируют рецепторы андрогена и препятствуют связыванию с ними андрогенов, т.е. не происходит влияния андрогенов на деление опухолевых клеток.
Препарат принимается в виде капсул, длительно. К его побочным действиям относятся диарея, увеличение или болезненность грудной железы у мужчин, гинекомастия, гепатотоксичность – печеночная токсичность, возможно возникновение приливов и слабости. Было отмечено, что нилутамид вызывает ночную слепоту и легочную токсичность, поэтому сегодня этот препарат не используется.
Ингибиторы стероидогенеза
К ингибиторам стероидогенеза относится абиратерон ацетат. Он угнетает активность фермента 17-а-гидроксилазы, который необходим для синтеза андрогенов в яичках, надпочечниках и клетках предстательной железы.
К побочным эффектам относятся: снижение уровня калия в крови, отеки, повышение артериального давления. Поэтому абиратерон ацетат назначается вместе с преднизолоном. При воздействии на фермент 17-а-гидроксилазу не только снижается уровень андрогенов, но и повышается уровень минералокортикоидов. К ним относится гормон альдостерон. Он обуславливает возникновение таких симптомов, как отеки, гипокалиемия, повышение артериального давления.
Гормонотерапия рака эндометрия и рака яичников
При раке эндометрия гормонотерапия используется при прогрессировании заболевания с низкой степенью злокачественности опухоли. Могут применяться прогестагены, антиэстрогены или ингибиторы ароматазы.
При раке яичников низкой степени злокачественности в поддерживающем режиме могут применяться прогестагены, антиэстрогены, ингибиторы ароматазы.
К прогестагенам относятся медроксипрогестерон ацетат и мегестрола ацетат. Они воздействуют на секрецию гонадотропинов гипофизом, подавляют продукцию эстрадиола и андростендиона надпочечников.
К побочным эффектам относятся повышение аппетита и увеличение массы тела, поэтому прогестагены применяются не только в гормонотерапии рака эндометрия и рака яичников, но и с целью лечения анорексии (отсутствия аппетита при объективной потребности организма в питании).
Симптоматическая терапия
В симптоматической терапии применяются глюкокортикостероиды: дексаметазон или преднизолон. Они обладают противовоспалительным, противорвотным и иммунодепрессивным и иммуностимулирующим (при применении низких доз) эффектами. Поэтому во многих смехах терапии в целях премедикации перед цитостатиками и таргетными препаратами может присутствовать глюкокортикостероид – дексаметазон.
При возникновении иммуноопосредованных, нежелательных явлений при применении иммунотерапии также могут назначаться глюкокортикостероиды.
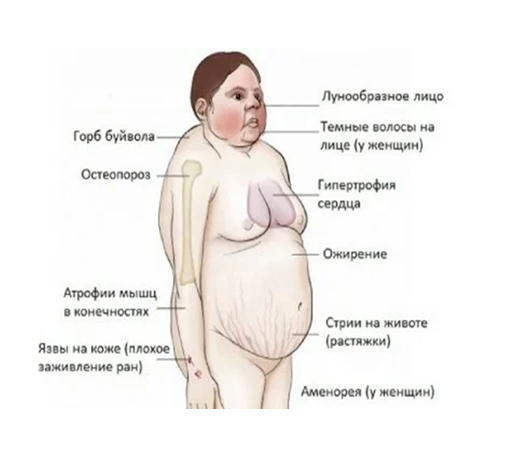
При длительном назначении глюкокортикостероидов могут наблюдаться повышение уровня глюкозы, возникновение язв желудка, увеличение массы тела, перераспределение жировой ткани, остеопороз, гипергликемия, изъязвление слизистой оболочки желудка, повышение артериального давления.
При длительном приеме глюкокортикостероидов отмена их приема должна происходить постепенно, так как резкая отмена может спровоцировать надпочечниковую недостаточность.
Аналоги соматостатина
К аналогам саматостатина относятся октреотид и ланреотид. Они подавляют секрецию гормона роста, инсулина, глюкагона, гастрина, серотонина. Аналоги соматостатина используются при нейроэндокринных опухолях с целью уменьшения симптомов карциноидного синдрома, который характеризуется покраснением лица, верхней части туловища, возникновением диареи, болей в животе, снижением артериального давления и ощущением сердцебиения.
Нейроэндокринные опухоли часто локализуются в желудочно-кишечном тракте и в легких.
Аналоги соматостатина применяются в первые две недели ежедневно, а затем используются депо-формы, которые вводятся один раз в месяц. При низкой степени злокачественности опухоли аналоги соматостатина могут назначаться совместно с иммунотерапией, с интерфероном альфа. При высокой степени злокачественности опухоли они назначаются совместно с химиотерапией.
Заключение
Гормонотерапия обладает высокой эффективностью при лечении гормон-позитивных опухолей. Она характеризуется удовлетворительной переносимостью, меньшим количеством побочных эффектов, чем при применении цитостатиков. При прохождении гормонального терапевтического лечения о любых новых жалобах и симптомах необходимо незамедлительно сообщать лечащему врачу. Также информировать докторов о приеме любых препаратов, так как их лекарственное взаимодействие может снижать эффективность терапии или приводить к усилению побочных эффектов.
Список литературы:
Авторская публикация:
Шарашенидзе Софико Мамуковна, ординатор отделения краткосрочной химиотерапии НМИЦ онкологии им. Н.Н. Петрова
Под редакцией:
Ткаченко Е.В., Заведующий отделением краткосрочной химиотерапии НМИЦ онкологии им. Н.Н. Петрова, врач-онколог, химиотерапевт, к.м.н.
Что вам необходимо сделать
Публикации по теме:
Очень интересная статья, без излишних размывающих суть рассуждений.
Правда, неспециалисту часто приходится отвлекаться на разъяснение терминов. Но это плата за четкость.
Прошу разъяснить, возможно ли консультироваться в «центре» при прохождении гормонотерапии в онкоотделении городской поликлиники.
СПАСИБО.
С уважением — Б.Куперман
Глюкокортикоидная терапия сегодня: эффективность и безопасность
В каких случаях проводится терапия глюкокортикоидами? Какие виды гормональной терапии используются? История применения глюкокортикостероидов (ГКС) в клинической практике насчитывает чуть более полувека, хотя «антиревматическая субстанция Х» была изве
В каких случаях проводится терапия глюкокортикоидами?
Какие виды гормональной терапии используются?
История применения глюкокортикостероидов (ГКС) в клинической практике насчитывает чуть более полувека, хотя «антиревматическая субстанция Х» была известна еще с 20-х годов ХХ столетия. Детальное изучение клинической значимости гормонов коры надпочечников, начатое Edward Calvin Kendall и Tadeus Reichstein, было продолжено только после того, как Philip Hench в конце 40-х годов обратил внимание на улучшение течения ревматоидного артрита при желтухе и беременности. В 1950 году всем троим была присуждена Нобелевская премия за «. открытия в отношении гормонов коры надпочечников, их структуры и биологических эффектов».
В настоящее время к ГКС относятся как естественные гормоны коры надпочечников с преимущественно глюкокортикоидной функцией — кортизон и гидрокортизон (кортизол), так и их синтезированные аналоги — преднизон, преднизолон, метилпреднизолон и др., включая галогенированные (фторированные) производные — триамцинолон, дексаметазон, бетаметазон и др. Широкий спектр физиологических и фармакологических эффектов глюкокортикоидов (адаптогенный, противовоспалительный, обезболивающий и жаропонижающий, неспецифический мембраностабилизирующий и противоотечный, противоаллергический и иммуносупрессивный, гематологический, гемодинамический и противошоковый, антитоксический, противорвотный и др.) делает эти препараты чуть ли не универсальными лекарственными средствами, и сегодня трудно найти такое патологическое состояние, при котором на том или ином этапе развития они не были бы показаны. Среди показаний в первую очередь можно выделить так называемые ревматические заболевания, болезни почек, крови, аллергические заболевания, трансплантации, ургентные состояния.
В зависимости от цели различаются три варианта терапии ГКС; при этом любая из них может быть как ургентной, так и плановой.
В отличие от плановой терапии применение ГКС в ургентных ситуациях носит, как правило, симптоматический, реже патогенетический характер и не заменяет, а дополняет другие методы лечения. В рамках неотложной терапии ГКС применяются при острой надпочечниковой недостаточности, тиреотоксическом кризе, аллергических заболеваниях (сывороточная болезнь, анафилактический шок, бронхиальная астма, крапивница, отек Квинке), заболеваниях печени (печеночно-клеточная недостаточность), неврологических заболеваниях (туберкулезный и бактериальный менингит, некоторые формы отека мозга), различных видах шока (кроме кардиогенного).
Из-за обилия побочных эффектов терапия ГКС направлена в основном на достижение максимального эффекта при назначении минимальных доз, величина которых определяется заболеванием и не зависит от массы тела и возраста; доза корректируется в соответствии с индивидуальной реакцией. Приняты две принципиально разные схемы назначения ГКС:
В зависимости от суточной дозы (в пересчете на преднизолон) и длительности применения ГКС принято выделять несколько видов терапии, имеющих различные показания:
Результат терапии ГКС зависит не только от дозы, но и от режима дозирования. Наиболее перспективными можно считать прерывистые схемы применения, когда за счет увеличения суточной дозы препарат принимается не каждый день. Самой эффективной представляется внутривенная пульс-терапия максимальными дозами, однако она оказывается и самой небезопасной. Значительно более безопасным должен быть признан режим «мини-пульс», который, однако, уступает по эффективности пульс-терапии. Столь же эффективно назначение умеренной/высокой дозы, разделенной на несколько приемов; но по безопасности этот режим уступает «мини-пульсу». Далее по эффективности следуют альтернирующий режим (через день удвоенные суточные дозы с последующим постепенным уменьшением) и режим ежедневного однократного назначения умеренной/высокой дозы; первый из них безопаснее и по этому критерию приближается к «мини-пульсу». Наиболее безопасна терапия низкими дозами, которая, однако, обеспечивает лишь поддерживающий эффект. При всех ежедневных схемах ГКС следует назначать в ранние утренние часы (между 6 и 8 часами); если же одноразовый прием невозможен из-за величины дозы, 2/3 дозы назначаются в 8 часов и 1/3 — днем (около полудня). При любом режиме дозирования по достижении планируемого эффекта доза постепенно снижается до поддерживающей или препарат отменяется вовсе.
Важной проблемой терапии ГКС является выбор препарата. Фармакокинетические и фармакодинамические свойства ГКС, включая их побочные эффекты, существенно различаются у отдельных препаратов (табл. 1, табл. 2). Приняв за единицу выраженность различных эффектов гидрокортизона, можно получить количественные характеристики активности отдельных препаратов. При сравнении ГКС чаще всего анализируется противовоспалительное действие этих препаратов, в соответствии с которым и рассчитывается эквивалентная пероральная доза, снижающаяся по мере увеличения противовоспалительной активности. Ее возрастание, параллельное увеличению длительности действия отдельных ГКС, сопровождается уменьшением минералокортикоидной активности, которой у метилпреднизолона (солу-медрола) и фторированных соединений вообще можно пренебречь.
Соотношение терапевтического и побочных эффектов позволяет утверждать, что в настоящее время препаратом выбора для длительной и пожизненной терапии является метилпреднизолон (солу-медрол). В настоящий момент солу-медрол широко используется в лечении аутоиммунных заболеваний, в трансплантологии и интенсивной терапии. Многообразие форм выпуска позволяет использовать препарат во всех возрастных категориях в оптимальных дозировках.
Вторым по эффективности препаратом остается в большинстве случаев преднизолон. Во многих же ургентных ситуациях определенными достоинствами обладают фторированные соединения: дексаметазон (дексазон, дексона) и бетаметазон (целестон, дипроспан). Однако в случае неотложной терапии, при которой противовоспалительное действие не играет ведущей роли, сравнительная оценка эффективности и безопасности различных препаратов весьма затруднительна по крайней мере по двум причинам:
В связи с вышеуказанными трудностями была предложена условная эквивалентная единица (УЭЕ), за которую принимаются минимальные эффективные дозы. Показано, что выраженные в УЭЕ максимальные суточные эффективные дозы фторированных ГКС (дексаметазона и бетаметазона) в пять раз меньше, чем у негалогенированных препаратов. Это обеспечивает не только более высокую эффективность и безопасность данной группы препаратов, назначаемых в определенных ситуациях, но и их фармакоэкономические преимущества.
Как бы тщательно ни проводился выбор препарата, режима дозирования и вида терапии, полностью предотвратить развитие тех или иных побочных эффектов при применении ГКС не удается. Характер побочных реакций может зависеть от ряда причин (табл. 3).
Вероятность и выраженность подавления оси ГГКН с развитием вначале функциональной недостаточности, а позже и атрофии коры надпочечников определяются дозой и длительностью терапии. Прекращение глюкокортикоидной терапии почти всегда сопряжено с угрозой развития острой надпочечниковой недостаточности.
Частым побочным действием ГКС оказываются инфекционные осложнения, которые в этом случае протекают атипично, что связано с противовоспалительной, аналгетической и жаропонижающей активностью этих средств. Это затрудняет своевременную диагностику и требует проведения ряда профилактических мероприятий. Из-за склонности к генерализации, затяжному течению, тканевому распаду и резистентности к специфической терапии эти осложнения становятся особенно грозными. Столь же коварны и «стероидные язвы», отличающиеся бессимптомным течением и склонностью к кровотечениям и перфорациям. Между тем желудочный дискомфорт, тошнота, другие диспепсические жалобы на фоне приема ГКС чаще не связаны с поражением слизистой. Экзогенный синдром Кушинга как осложнение терапии ГКС встречается далеко не всегда, однако отдельные нарушения метаболизма, гормональной регуляции и деятельности тех или иных систем развиваются почти во всех случаях глюкокортикоидной терапии.
С сожалением приходится отметить, что утверждение Е. М. Тареева, назвавшего терапию ГКС трудной, сложной и опасной, до сих пор справедливо. Как писал Тареев, такую терапию гораздо легче начать, чем прекратить. Однако ответственный подход к лечению позволяет значительно повысить его безопасность. Это достигается благодаря строгому учету противопоказаний (абсолютных среди которых нет) и побочных эффектов ГКС (оценка отношения «ожидаемый эффект/предполагаемый риск»), а также проведению «терапии прикрытия» в группах риска (антибактериальные препараты при хронических очагах инфекции, коррекция доз сахароснижающих средств или переход на инсулин при сахарном диабете и др.). Особое место при длительном применении ГКС занимает метаболическая терапия, которая проводится в целях предупреждения и коррекции нарушений электролитного обмена и катаболических процессов в первую очередь в миокарде (дистрофия) и костной ткани (остеопороз). Однако наиболее надежным путем обеспечения безопасности терапии ГКС остается соблюдение основного принципа клинической фармакологии и фармакотерапии — назначение лечения по строгим показаниям.
В. В. Городецкий, кандидат медицинских наук
А. В. Тополянский, кандидат медицинских наук