Чем выше давление тем ниже температура кипения
Зависимость температуры кипения от давления
Зависимость температуры кипения от давления
Температура кипения воды равна 100 °C; можно подумать, что это неотъемлемое свойство воды, что вода, где бы и в каких условиях она ни находилась, всегда будет кипеть при 100 °C.
Но это не так, и об этом прекрасно осведомлены жители высокогорных селений.
Вблизи вершины Эльбруса имеется домик для туристов и научная станция. Новички иногда удивляются, «как трудно сварить яйцо в кипятке» или «почему кипяток не обжигает». В этих случаях им указывают, что вода кипит на вершине Эльбруса уже при 82 °C.
В чем же тут дело? Какой физический фактор вмешивается в явление кипения? Какое значение имеет высота над уровнем моря?
Этим физическим фактором является давление, действующее на поверхность жидкости. Не нужно забираться на вершину горы, чтобы проверить справедливость сказанного.
Помещая подогреваемую воду под колокол и накачивая или выкачивая оттуда воздух, можно убедиться, что температура кипения растет при возрастании давления и падает при его уменьшении.
Вода кипит при 100 °C только при определенном давлении – 760 мм Hg.
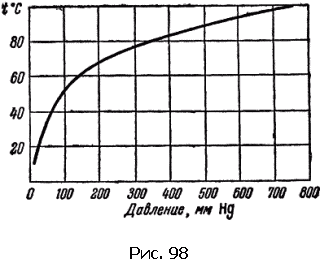
Кривая температуры кипения в зависимости от давления показана на рис. 98. На вершине Эльбруса давление равно 0,5 атм, этому давлению и соответствует температура кипения 82 °C.
А вот водой, кипящей при 10–15 мм Нg, можно освежиться в жаркую погоду. При этом давлении температура кипения упадет до 10–15 °C.
Можно получить даже «кипяток», имеющий температуру замерзающей воды. Для этого придется снизить давление до 4,6 мм Hg.
Интересную картину можно наблюдать, если поместить открытый сосуд с водой под колокол и откачивать воздух. Откачка заставит воду закипеть, но кипение требует тепла. Взять его неоткуда, и воде придется отдать свою энергию. Температура кипящей воды начнет падать, но так как откачка продолжается, то падает и давление. Поэтому кипение не прекратится, вода будет продолжать охлаждаться и в конце концов замерзнет.
Такое кипение холодной воды происходит не только при откачке воздуха. Например, при вращении гребного корабельного винта давление в быстро движущемся около металлической поверхности слое воды сильно падает и вода в этом слое закипает, т.е. в ней появляются многочисленные наполненные паром пузырьки. Это явление называется кавитацией (от латинского слова cavitas – полость).
Снижая давление, мы понижаем температуру кипения. А увеличивая его? График, подобный нашему, отвечает на этот вопрос. Давление в 15 атм может задержать кипение воды, оно начнется только при 200 °C, а давление в 80 атм заставит воду закипеть лишь при 300 °C.
Итак, определенному внешнему давлению соответствует определенная температура кипения. Но это утверждение можно и «перевернуть», сказав так: каждой температуре кипения воды соответствует свое определенное давление. Это давление называется упругостью пара.
Кривая, изображающая температуру кипения в зависимости от давления, является одновременно и кривой упругости пара в зависимости от температуры.
Цифры, нанесенные на график температуры кипения (или на график упругости пара), показывают, что упругость пара меняется очень резко с изменением температуры. При 0 °C (т.е. 273 K) упругость пара равна 4,6 мм Hg, при 100 °C (373 K) она равна 760 мм, т. е, возрастает в 165 раз. При повышении температуры вдвое (от 0 °C, т.е. 273 K, до 273 °C, т.е. 546 K) упругость пара возрастает с 4,6 мм Hg почти до 60 атм, т.е. примерно в 10000 раз.
Поэтому, напротив, температура кипения меняется с давлением довольно медленно. При изменении давления вдвое – от 0,5 атм до 1 атм, температура кипения возрастает от 82 °C (т.е. 355 K) до 100 °C (т.е. 373 K) и при изменении вдвое от 1 атм до 2 атм – от 100 °C (т.е. 373 K) до 120 °C (т.е. 393 K).
Та же кривая, которую мы сейчас рассматриваем, управляет и конденсацией (сгущением) пара в воду.
Превратить пар в воду можно либо сжатием, либо охлаждением.
Как во время кипения, так и в процессе конденсации точка не сдвинется с кривой, пока превращение пара в воду или воды в пар не закончится полностью. Это можно сформулировать еще и так: в условиях нашей кривой и только при этих условиях возможно сосуществование жидкости и пара. Если при этом не подводить и не отнимать тепла, то количества пара и жидкости в закрытом сосуде будут оставаться неизменными. Про такие пар и жидкость говорят, что они находятся в равновесии, и пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Кривая кипения и конденсации имеет, как мы видим, еще один смысл – это кривая равновесия жидкости и пара. Кривая равновесия делит поле диаграммы на две части. Влево и вверх (к большим температурам и меньшим давлениям) расположена область устойчивого состояния пара. Вправо и вниз – область устойчивого состояния жидкости.
Кривая равновесия пар – жидкость, т.е. кривая зависимости температуры кипения от давления или, что то же самое, упругости пара от температуры, примерно одинакова для всех жидкостей. В одних случаях изменение может быть несколько более резким, в других – несколько более медленным, но всегда упругость пара быстро растет с увеличением температуры.
Уже много раз мы пользовались словами «газ» и «пар». Эти два слова довольно равноправны. Можно сказать: водяной газ есть пар воды, газ кислород есть пар кислородной жидкости. Все же при пользовании этими двумя словами сложилась некоторая привычка. Так как мы привыкли к определенному относительно небольшому интервалу температур, то слово «газ» мы применяем обычно к тем веществам, упругость пара которых при обычных температурах выше атмосферного давления. Напротив, о паре мы говорим тогда, когда при комнатной температуре и давлении атмосферы вещество более устойчиво в виде жидкости.
Читайте также
К квантовой теории абсолютного нуля температуры
К квантовой теории абсолютного нуля температуры Ниже помещен перевод заметки» написанной известными физиками и опубликованной в «Natur-wissenschaften». Редакторы журнала «попались на удочку громких имен» и, не вдаваясь в существо написанного, направили полученный материал в
6. Математическая статистика и корреляционная зависимость
6. Математическая статистика и корреляционная зависимость Математическая статистика – наука о математических методах систематизации и использования статистических данных для решения научных и практических задач. Математическая статистика тесно примыкает к теории
К квантовой теории абсолютного нуля температуры
К квантовой теории абсолютного нуля температуры Д. Бак, Г. Бете, В. Рицлер (Кембридж) «К квантовой теории абсолютного нуля температуры» и заметки, переводы которых помещены ниже: К квантовой теории абсолютного нуля температуры Движение нижней челюсти у крупного
Изменение давления с высотой
Изменение давления с высотой С изменением высоты давление падает. Впервые это было выяснено французом Перье по поручению Паскаля в 1648 г. Гора Пью де Дом, около которой жил Перье, была высотой 975 м. Измерения показали, что ртуть в торричеллиевой трубке падает при подъеме на
Влияние давления на температуру плавления
Влияние давления на температуру плавления Если изменить давление, то изменится и температура плавления. С такой же закономерностью мы встречались, когда говорили о кипении. Чем больше давление, тем выше температура кипения. Как правило, это верно и для плавления. Однако
Зависимость температуры кипения воды от давления:
Температура кипения — это температура, при которой происходит кипение жидкости, которая находится под постоянным давлением. Согласно уравнению Клапейрона — Клаузиуса с ростом давления температура кипения увеличивается, а с уменьшением давления температура кипения соответственно уменьшается.
Если жидкость получает теплоту, то она будет нагреваться и через некоторое время начнет кипеть. По наблюдениям этот процесс сопровождается образованием в объеме жидкости пузырьков насыщенного пара. С повышением температуры их количество на стенках сосуда возрастает, а размеры увеличиваются. При определенной температуре давление пара в пузырьках становится равным давлению в жидкости, и они под действием силы Архимеда начинают всплывать. Когда такой пузырек достигает поверхности жидкости, он лопается и выбрасывает пар наружу.
Кипение — это внутреннее парообразование, которое происходит во всем объеме жидкости при температуре, когда давление насыщенного пара равно давлению в жидкости.
Установлено, что при кипении температура жидкости остается постоянной— при достижении температуры кипения все предоставленное количество теплоты идет на парообразование. Если жидкость не получает теплоту, кипение прекратится, поскольку не будет поступать энергия для внутреннего парообразования.
Кипение осуществляется при температуре, когда давление насыщенного пара в пузырьках равно давлению в жидкости.
Каждое вещество имеет собственную температуру кипения. Очевидно, что ее значение определяется давлением насыщенного пара при данной температуре, поскольку кипение наступает тогда, когда давление насыщенного пара уравнивается с давлением в жидкости. Поэтому температура кипения жидкостей зависит от внешнего давления — чем оно выше, тем выше должна быть температура кипения, и наоборот.
Температура кипения воды при этом давлении:
o C
Удельный объем насыщенного пара:
м 3 /кг
Удельная теплота парообразования:
кДж/кг
Температура кипения воды в зависимости от давления: 4 фактора, таблица для расчёта
Многие люди думают, что температура кипения воды составляет 100°C. Однако этот показатель может меняться в зависимости от атмосферного давления.
Например, на горе Эверест на подъеме 8842 метра над уровнем моря вода закипит при +70°C. А в глубокой шахте при достижении температуры + 103°C
В данной статье мы выясним, как будет меняться температура кипения воды в зависимости от давления: в горах, шахте, вакууме. Рассмотрим особенности процесса кипячения с точки зрения физики и химии.
Как будет меняться температура кипения воды: 4 фактора
Температура, при которой кипит жидкость, называется температурой кипения.
Стоит отметить, что она всегда остается неизменной. Поэтому, если увеличить огонь под кипящей кастрюлей с водой, выкипать будет быстрее, но температура при этом не увеличится, так как средняя кинетическая энергия молекул остаётся неизменной.
Рассмотрим 4 фактора, которые влияют на изменение t°:
Рассмотрим более подробно каждый из факторов.
Влияние атмосферного давления
Согласно исследованиям и уравнению Клапейрона — Клаузиуса, градус кипения напрямую зависит от атмосферного давления. С его ростом температура кипения увеличивается, а с уменьшением, наоборот, становится все ниже и ниже.
Атмосферное давление — это давление атмосферы, действующее на все находящиеся на ней предметы и земную поверхность. Оно может меняться в зависимости от места и времени и измеряется барометром.
При нормальном атмосферном давлении 760 мм ртутного столба вода кипит при + 100 °C
В горной местности давление уменьшается, а под землей (в шахте) увеличивается.
Для наглядности предоставлена таблица № 1 из большого химического справочника, источник: Волков А. И, Жарский И. В.
Таблица № 1. «Температура кипения воды от давления».
| Р, кПа | t, °C | Р, кПа | t, °C | Р, кПа | t, °C |
| 5,0 | 32,88 | 91,5 | 97,17 | 101,325 | 100,00 |
| 10,0 | 45,82 | 92,0 | 97,32 | 101,5 | 100,05 |
| 15,0 | 53,98 | 92,5 | 97,47 | 102,0 | 100,19 |
| 20,0 | 60,07 | 93,0 | 97,62 | 102,5 | 100,32 |
| 25,0 | 64,98 | 93,5 | 97,76 | 103,0 | 100,46 |
| 30,0 | 69,11 | 94,0 | 97,91 | 103,5 | 100,60 |
| 35,0 | 72,70 | 94,5 | 98,06 | 104,0 | 100,73 |
| 40,0 | 75,88 | 95,0 | 98,21 | 104,5 | 100,87 |
| 45,0 | 78,74 | 95,5 | 98,35 | 105,0 | 101,00 |
| 50,0 | 81,34 | 96,0 | 98,50 | 105,5 | 101,14 |
| 55,0 | 83,73 | 96,5 | 98,64 | 106,0 | 101,27 |
| 60,0 | 85,95 | 97,0 | 98,78 | 106,5 | 101,40 |
| 65,0 | 88,02 | 97,5 | 98,93 | 107,0 | 101,54 |
| 70,0 | 89,96 | 98,0 | 99,07 | 107,5 | 101,67 |
| 75,0 | 91,78 | 98,5 | 99,21 | 108,0 | 101,80 |
| 80,0 | 93,51 | 99,0 | 99,35 | 108,5 | 101,93 |
| 85,0 | 95, 15 | 99,5 | 99,49 | 109,0 | 102,06 |
| 90,0 | 96,71 | 100,0 | 99,63 | 109,5 | 102,19 |
| 90,5 | 96,87 | 100,5 | 99,77 | 110,0 | 102,32 |
| 91,0 | 97, 02 | 101,0 | 99,91 | 115,0 | 103,59 |
Единицы измерения давления в таблице: кПа.
1 кПа = 1000 Па = 0,00986923 атм = 7, 50062 мм. рт. ст
Нормальное атмосферное давление составляет 765 мм. РТ. Ст. = 101,325 Р, кПа
Температура кипения в горах
При подъеме над поверхностью Земли (в горах), температура кипения воды падает, так как снижается атмосферное давление (на каждые 10, 5 м на 1 мм РТ. С). Пузырькам легче всплывать – процесс происходит быстрее.

Для варки мяса, как и других продуктов, нужны привычные 100 градусов. В обратном случае все компоненты бульона просто останутся сырыми.
Таблица № 2. «Как будет меняться t° кипения с высотой».
| Высота над уровнем моря | t° кипения |
| 0 | 100,0 |
| 500 | 98,3 |
| 1000 | 96,7 |
| 1500 | 95,0 |
| 2000 | 93, 3 |
| 2500 | 91,7 |
| 3000 | 90,0 |
| 3500 | 88,3 |
| 4000 | 86,7 |
| 4500 | 85,0 |
| 5000 | 83,3 |
| 6000 | 80,0 |
Температура кипения воды в шахте
Если спуститься в шахту, то давление будет увеличиваться.
Применение герметической крышки
Герметичные крышки не позволяет образовавшемуся пару ускользнуть. В среднем температура закипания воды увеличивается от 5-20 градусов.
В хозяйстве для приготовления блюд часто используют кастрюли, сковородки с герметичной крышкой. Таким образом, уменьшается время приготовления пищи за счет высокой температуры, а блюда получаются более вкусными. В горных районах с низким давлением это необходимая вещь для приготовления пищи. Так же используют мультиварки и сотейники.
Кипячение воды в вакууме
Вакуум — это среда с газом, с пониженным давлением.
Температура кипения воды в вакууме зависит от того, какое давление в нём.
Разные виды вакуумов поддерживают разное давление. Например, в низком вакууме давление составляет от 760 до 25 мм. РТ. Ст. В абсолютном вакууме давление полностью отсутствует. Для точного расчета нужно знать модель вакуума и давление, которое он поддерживает.
Кипение солёной воды
Солёная вода закипает при более высокой температуре за счет своих свойств.
Соль увеличивает плотность воды, соответственно на процесс требуется больше времени.
t° повышается примерно на 1 градус при добавлении 40 грамм соли на литр воды.
Температура кипения воды в чайнике
Чистая пресная вода закипает в чайнике при t° 100 градусов °C при условиях нормального атм. давления 760 мм ртутного столба.
Удельная теплоемкость
Удельной теплоемкостью вещества называется количество теплоты, которое необходимо подвести к 1 кг этого вещества, чтобы его температура изменилась на 1 градус Цельсия.
Это количество теплоты необходимое для нагревания массы вещества на один градус.

С — удельная теплоемкость;
— масса нагреваемого охлаждающегося вещества;
— ΔT — разность конечной и начальной температур вещества.
Процесс кипячения воды: 3 основных стадии
Кипение – это интенсивное парообразование, которое происходит при нагревании жидкости по всему объёму при определённой температуре.
Весь процесс кипения воды сопровождается выделением пара. Это одно из состояний воды. При парообразовании температура пара и воды остаются постоянными до тех пор, пока жидкость не изменит свое агрегатное состояние. Это явление объясняется тем, что при кипении вся энергия расходуется в преобразование воды в пар.
В воде растворены молекулы воздуха (газов). При нагревании газ превращается в воздушные пузырьки. При достижении достаточной температуры они лопаются, создаётся характерный шум.
Процесс можно разделить на 3 стадии:
Что такое кипячёная вода?
Это вода, ранее доведенная до температуры кипения. Сырая вода в своем составе может содержать различные бактерии, микроорганизмы. В водопроводе больших городов много хлора и различных других химических веществ. Процесс кипячения обезвреживает многие микробы. Однако не все бактерии и тяжёлые металлы убиваются в кипящей воде, поэтому питьевая вода происходит предварительную проверку пригодности.
Выводы и рекомендации
Кипячение необходимый процесс для человечества. С помощью него приготавливают пищу, стирают загрязненную одежду, проводят дезинфекцию.
Градус кипения напрямую зависит от давления, свойств воды и емкости.
Молекулярная физика. Кипение жидкости.
Кипение — это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
В отличие от испарения, которое происходит при любой температуре жидкости, другой вид парообразования — кипение — возможен лишь при совершенно определенной (при данном давлении) температуре — температуре кипения.
При нагревании воды в открытом стеклянном сосуде можно увидеть, что по мере увеличения температуры стенки и дно сосуда покрываются мелкими пузырьками. Они образуются в результате расширения мельчайших пузырьков воздуха, которые существуют в углублениях и микротрещинах не полностью смачиваемых стенок сосуда.
Пары жидкости, которые находятся внутри пузырьков, являются насыщенными. С ростом температуры давление насыщенных паров возрастает, и пузырьки увеличиваются в размерах. С увеличением объема пузырьков растет и действующая на них выталкивающая (архимедова) сила. Под действием этой силы наиболее крупные пузырьки отрываются от стенок сосуда и поднимаются вверх. Если верхние слои воды еще не успели нагреться до 100 °С, то в такой (более холодной) воде часть водяного пара внутри пузырьков конденсируется и уходит в воду; пузырьки при этом сокращаются в размерах, и сила тяжести заставляет их снова опускаться вниз. Здесь они опять увеличиваются и вновь начинают всплывать вверх. Попеременное увеличение и уменьшение пузырьков внутри воды сопровождается возникновением в ней характерных звуковых волн: закипающая вода шумит.
Когда вся вода прогреется до 100 °С, поднявшиеся вверх пузырьки уже не сокращаются в размерах, а лопаются на поверхности воды, выбрасывая пар наружу. Возникает характерное бульканье — вода кипит.
Кипение начинается после того, как давление насыщенного пара внутри пузырьков сравнивается с давлением в окружающей жидкости.
Во время кипения температура жидкости и пара над ней не меняется. Она сохраняется неизменной до тех пор, пока вся жидкость не выкипит. Это происходит потому, что вся подводимая к жидкости энергия уходит на превращение ее в пар.
Температура, при которой кипит жидкость, называется температурой кипения.
Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости. Это объясняется зависимостью давления насыщенного пара от температуры. Пузырек пара растет, пока давление насыщенного пара внутри него немного превосходит давление в жидкости, которое складывается из внешнего давления и гидростатического давления столба жидкости.
Чем больше внешнее давление, тем больше температура кипения.
Всем известно, что вода кипит при температуре 100 ºC. Но не следует забывать, что это справедливо лишь при нормальном атмосферном давлении (примерно 101 кПа). При увеличении давления температура кипения воды возрастает. Так, например, в кастрюлях-скороварках пищу варят под давлением около 200 кПа. Температура кипения воды при этом достигает 120°С. В воде такой температуры процесс варки происходит значительно быстрее, чем в обычном кипятке. Этим и объясняется название «скороварка».
И наоборот, уменьшая внешнее давление, мы тем самым понижаем температуру кипения. Например, в горных районах (на высоте 3 км, где давление составляет 70 кПа) вода кипит при температуре 90 °С. Поэтому жителям этих районов, использующим такой кипяток, требуется значительно больше времени для приготовления пищи, чем жителям равнин. А сварить в этом кипятке, например, куриное яйцо вообще невозможно, так как при температуре ниже 100 °С белок не сворачивается.
У каждой жидкости своя температура кипения, которая зависит от давления насыщенного пара. Чем выше давление насыщенного пара, тем ниже температура кипения соответствующей жидкости, т. к. при меньших температурах давление насыщенного пара становится равным атмосферному. Например, при температуре кипения 100 °С давление насыщенных паров воды равно 101 325 Па (760 мм рт. ст.), а паров ртути — всего лишь 117 Па (0,88 мм рт. ст.). Кипит ртуть при 357°С при нормальном давлении.
Теплота парообразования.
Теплота парообразования (теплота испарения) — количество теплоты, которое необходимо сообщить веществу (при постоянном давлении и постоянной температуре) для полного превращения жидкого вещества в пар.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой r и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты, необходимое для парообразования (или выделяющееся при конденсации). Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования r умножить на массу m:
При конденсации пара происходит выделение такого же количества теплоты: