Чем выводят аскариды у кошек
Аскариды у кошек: причины появления и методы избавления
Бывают ли аскариды у кошек? — вопрос довольно популярный среди любителей домашних животных. Ответ однозначный: да! К тому же эти гельминты встречается гораздо чаще других; относятся они к роду круглых червей — нематодам. Плотоядные заражаются двумя видами паразитов: токсокарами (Toxocara mystax) и токсакаридами (Toxacaris Leonina).
Морфологические признаки гельминтов
Все аскариды у котов визуально очень похожи, отличаются они лишь размерами:
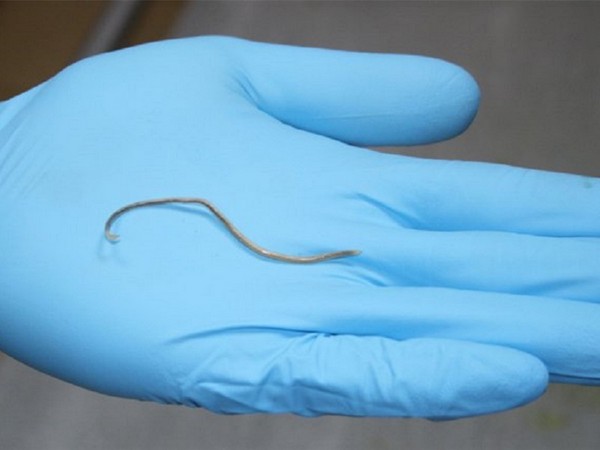
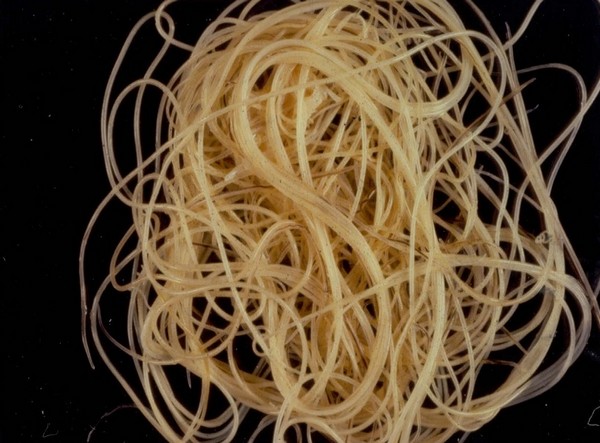
Сами же нематоды желтоватого цвета, гладкие, блестящие, длинные и тонкие черви.
Механизм развития
Жизненный путь возбудителя от яйца до половозрелого гельминта можно представить в виде следующей цепочки взаимосвязей:
Это надо знать? Такой путь развития гельминтной инвазии носит название аскаридного, длится он около месяца.
Кто болеет?
Аскариды распространены повсеместно и могут встречаться как у взрослой кошки, так и у котенка. При этом малыши, не достигшее трехмесячного возраста, переносят болезнь очень тяжело, вплоть до летального исхода.
Источниками инвазии служат больные животные, выделяющие и заражающие окружающие предметы большим количеством яиц.
Заражение глистами
Важно! Исключительно домашний питомец также входит в группу риска. Даже если у него не было прямого контакта с больным животным, он может заразиться через человека, принесшего на обуви или одежде яйца гельминтов.
Признаки болезни
Как правило, при слабой инвазии (2-3 глиста) симптомы аскарид у кошек не характерны. Возможно, болезнь будет проявляться одним или сразу несколькими признаками:
У маленьких котят картина токсокароза более выражена:
Важно! При значительной степени инвазии гельминты закупоривают просвет кишечника, приводя к его непроходимости вплоть до разрыва пищеварительной трубки и летального исхода вследствие перитонита.
Как поставить диагноз?
По внешним признакам можно лишь предположить, что кошка заражена аскаридами. Для уточнения диагноза приходится прибегать к специальному виду исследования.
Для этого в лабораторию отправляются фекалии, где проводится копрологический анализ на яйца глист.
Это надо знать! По возможности отбор проб делают два-три раза в разное время суток и обязательно повторяют исследования через 7-10 дней.
Почему? Секрет кроется в особенности жизнедеятельности гельминтов.
На самом деле в реальности к паразитологическим исследованиям прибегают достаточно редко. Обычно ветеринарный врач предпочитает сделать профилактическую дегельминтизацию, дабы никому не морочить голову. После дачи противоглистной таблетки уже на следующий день будет понятно были гельминты или нет: погибших круглых червей находят или не находят в свежих фекалиях.
Бытует мнение, что глисты под действием таблеток растворяются. На самом деле они просто погибают и уже мертвыми выходят наружу естественным путем.
Что делать, если у кошки глисты?
Лечение аскарид у кошек несложное: достаточно однократно дать противопаразитарный препарат и через две недели повторить его дачу.
При выборе того или иного лекарства следует внимательно изучить инструкцию. В ней обязательно должно быть указано, что действующее вещество эффективно в отношении нематод (круглых червей), в идеале должно быть прописано против каких именно.
Таблетки дают утром натощак или вечером через пару часов после последнего приема пищи. Дополнительно вводить слабительные средства не рекомендуется.
И еще несколько важных моментов:
Важно! В процессе лечения проглистогонить кошку недостаточно. Помимо этого, необходимо провести тотальную дезинвазию в квартире.
Санитарная уборка включает в себя следующие мероприятия:
Это надо знать! Отказ от столь простых правил грозит постоянным перезаражением кошки самой себя.
Безопасны ли препараты от глистов?
Этот вопрос задают довольно часто, так как бывали случаи летального исхода у котят после дачи противоглистных препаратов.
На самом деле, ангельминтные средства, хоть и обладают определенной токсичностью, совершенно не причем и не вызывают серьезных побочных эффектов.
Да действительно котенок может погибнуть, если имеет место быть сильная инвазия. В этом случае вина препарата косвенная, а не прямая. Дело в том, что погибшие глисты, выбрасывают в кровь колоссальное количество токсинов, которые и являются причиной смерти.
Чтобы такого не происходило необходимо вовремя лечить, а лучше профилактировать появление паразитов.
Вопросы профилактики
Предупредить развитие инвазии можно одним единственным способом — периодически (2-4 раза в год) глистогонить любимого питомца. Периодичность зависит от образа жизни животного: уличных готов пролечивают чаще, домашних реже.
Какие именно брать препараты подскажет ветеринарный врач. Как правило, не рекомендуется каждый раз приобретать одни и те же лекарства, а точнее средства на основе одного и того же действующего начала. Почему? Существует мнение, что у глистов может вырабатываться невосприимчивость к часто применяющимся таблеткам.
К сожалению, против глистов иммунитет не вырабатывается, поэтому никаких вакцин от группы этих паразитарных болезней еще не придуманы. Косвенно снизить риск заражения можно путем правильного, полноценного питания и здорового образа жизни питомца. Считается, что в чем лучших условиях обитает животное, тем меньше шанс ему заразиться и выше вероятность победить инвазии силами организма.
Кошачьи аскариды и человек
Очень часто можно услышать вопрос: аскариды кошек передаются человеку? Попробуем на него ответить.
Toxocara mystax и Toxacaris Leonina — облигатные, видовые паразиты, то есть способны жить и развиваться в организме конкретного животного. Но для людей, особенно детей, они все же представляют определенную угрозу. Попадая в человеческий организм, кошачьи аскариды, хоть и не проходят полный путь развития, но все же успевают сильно навредить.
Например, доказано, что у ребенка они могут стать причиной аллергии, частого возникновения простудных болезней из-за снижения иммунитета.
Дабы избежать стольких проблем стоит взять за привычку мыть руки с мылом после общения с домашними и уж тем более дворовыми кошками, да и не надо с ними целоваться — это и не гигиенично, и потенциально опасно для здоровья.
Автор статьи: Чуприна Марина Николаевна,
ветеринарный врач, паразитолог
На вопрос болеют ли люди кошачьим токсокарозом, отвечают специалисты:
Аскариды у кошек: симптомы, лечение и профилактика
Кошка много ест и страдает расстройствами пищеварения?
Узнайте об этих и других признаках заражения аскаридами.
Бонус для тех, кто дочитает до конца: расскажем, как избавиться от паразитических червей.
Какие аскариды встречаются у кошек
Аскариды – крупные круглые паразитические черви, относятся к классу нематод. Кошки заражаются двумя видами аскарид: Toxocara leonina и Toxacara cati.
Toxocara leonina при паразитировании у кошки вызывает болезнь, которую называют токсаскаридоз. Кошка – окончательный хозяин этого гельминта. В редких случаях Toxocara leonina может заразиться человек, но в его организме паразит не достигает половозрелой стадии.
Toxacara cati паразитирует в организме кошек и других представителей семейства кошачьих, вызывая токсокароз. Взрослые особи гельминта локализуются, как правило, в тонком отделе кишечника, личинки могут мигрировать по всему организму.
Человек часто играет роль случайного хозяина данного паразита. В его организме аскариды не проходят полный жизненный цикл, а останавливаются в развитии на стадии личинки и инкапсулируются.
Как выглядят гельминты
Аскариды внешне похожи на шнурки желтоватого цвета. Тело этих паразитов длинное, гладкое, блестящее, заострённое с обеих сторон. В организме кошки они могут вырастать до 20 см в длину. Аскариды – раздельнополые организмы, размножаются половым путём. Самки аскарид всегда крупнее самцов.
Преимущественно обитают гельминты в тонком отделе кишечника, где прикреплены к его слизистой оболочке головным концом. При сильной степени заражения питомца аскариды выходят вместе с калом или рвотой.
Как кошка заражается аскаридами
Источниками заражения паразитами являются больные животные, которые вместе с фекалиями выделяют из кишечника большое количество яиц гельминтов. Здоровый питомец заражается при проглатывании созревших во внешней среде яиц с личинкой.
Чаще всего яйца аскарид попадают в организм питомца:
Хозяин может принести яйца гельминтов на обуви или одежде в дом, поэтому даже полностью домашний питомец рискует заразиться аскаридами.
Биология развития аскарид
Биология развития Toxocara leonina и Toxacara cati отличаются друг от друга. Жизненный цикл развития возбудителя токсаскаридоза достаточно прост. Самка аскариды откладывает яйца, которые выводятся наружу вместе с фекалиями кошки. Личинка, которая расположена внутри яйца, становится заразной через несколько дней нахождения яйца в окружающей среде. Далее яйцо проглатывается животным, в тонком кишечнике из него вылупляется личинка. Затем она растёт, несколько раз линяет и постепенно достигает половой зрелости. Окончательными хозяевами Toxocara leonina являются кошки и собаки, а промежуточными могут выступать грызуны. При поедании заражённого личинками аскариды грызуна кошка заражается токсаскаридозом.
Цикл развития Toxоcara cati сложнее. Окончательными хозяевами этой аскариды являются все представители семейства кошачьих. А промежуточными могут быть не только грызуны, но и насекомые, дождевые черви и даже куры. Кошка проглатывает личинку аскариды вместе с кормом или водой, а также поедая промежуточного хозяина. В кишечнике личинка аскариды внедряется в стенку и проникает в кровеносный сосуд, и вместе с током крови попадает в лёгкие и трахею. Путешествуя по организму, личинки растут, несколько раз линяют. Когда животное кашляет, личинки попадают в ротовую полость и снова проглатываются. Формирование взрослой особи происходит в тонком кишечнике.
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).