Чем заменить сладкое при инсулинорезистентности
Сахарозаменители: как правильно рекомендовать
Подробный гид по заменителям сахара с таблицами: калорийность, безопасность и принципы подбора для покупателя
Нередко людям требуется временно или навсегда отказаться от сахара. Однако необходимость исключить или резко ограничить его употребление создает состояние дискомфорта. Для выстраивания новых правильных пищевых привычек требуется время. Именно в таких ситуациях, когда полный и одномоментный отказ от привычных вкусов невозможен, но по состоянию здоровья необходим (избыточная масса тела, сахарный диабет, различные оздоровительные диеты), диетологи рекомендуют употреблять сахарозаменители, сводя со временем и их применение к минимуму. Рассмотрим основные классы заменителей сахарозы и их свойства.
Классификация
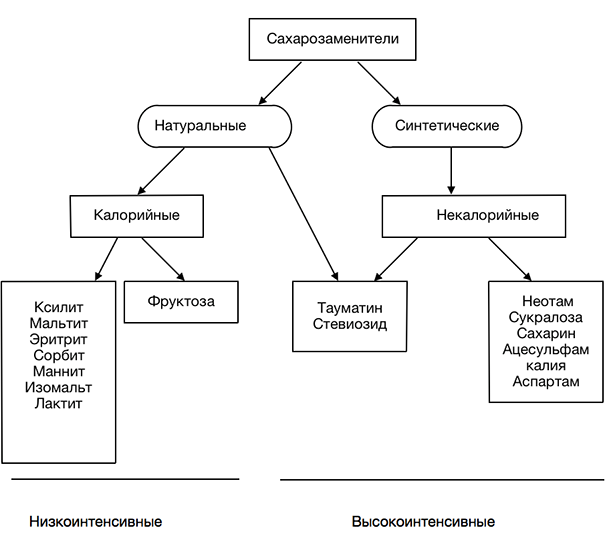
Схема 1. Классификация сахарозаменителей [1]
Существует несколько классификаций сахарозаменителей. Так, например, все сахарозаменители можно разделить на натуральные (вещества, близкие по составу к сахарозе, имеющие схожую с ней калорийность) и синтетические (специально разработанные для подслащивания, имеют низкую калорийность). Также принято сравнивать сладость сахарозаменителя с сахарозой: те подсластители, уровень сладости которых близок к сахарозе, называют низкоинтенсивными, а вещества, во много раз слаще сахарозы — интенсивными [2].
Шипучие таблетки «Стевиозид+Галега»
Натуральный сахарозаменитель с приятным сладким вкусом.
Основное преимущество: отсутствие глюкозы и калорий.
Стевия содержит более 50 ценнейших биологически активных веществ (витамины, микроэлементы, 17 аминокислот, флавоноиды, органические кислоты и другие), легкоусвояемых и нужных организму для поддержания полноценного функционирования.
Экстракт травы галеги содержит: аминокислоты растительного происхождения, витамины — каротин, аскорбиновая кислота; флавоноиды, органические кислоты, рутин.
БАД. Не является лекарственным средством.
Наиболее значимой с точки зрения практического применения и выбора является деление сахарозаменителей на калорийные и бескалорийные.
Табл. 1. Калорийные и бескалорийные подсластители
| Калорийные подсластители (2-4 ккал/г) | Бескалорийные подсластители (0 ккал/г) | |
| Фруктоза | Тауматин | |
| Сахарные спирты | Ксилит | Стевиозид |
| Сорбит | Аспартам | |
| Маннит | Сукрапоза | |
| Изомальт | Сахарин | |
| Мальтит | Ацесульфам калия | |
| Эритрит | Неотам | |
| Лактит | Цикламат | |
Рассмотрим наиболее популярные и распространенные сахарозаменители подробнее. Начнем с натуральных.
Фруктоза
Содержится в ягодах, овощах, фруктах и меде. По сути, это такой же углевод, как и сахароза, только в 1,5 раза слаще. Гликемический индекс фруктозы (степень повышения сахара в крови после употребления продукта) — всего 31, тогда как у обычного сахара — 89. Калорийность фруктозы сопоставима с калорийностью сахара (1 г фруктозы — 3,7 ккал, 1 г сахара — 4 ккал). Несмотря на это, в настоящее время диетологи склонны считать фруктовый сахар вредным продуктом. Некоторые исследования говорят о том, что регулярное употребление фруктозы ведет к нарушению обмена веществ и снижает чувствительность к инсулину, что со временем приводит к ожирению и повышению уровня сахара в крови [3]. Почему это происходит? Дело в том, что в природе фруктоза не встречается изолированно, она всегда идет вместе с клетчаткой. Именно клетчатка позволяет организму медленно усваивать этот сахар без скачков инсулина, тогда как чистая фруктоза вызывает резкое повышение уровня этого гормона. Лишая фруктозу балласта (пищевых волокон), мы превращаем ее в обычный сахар. Сейчас употребление фруктозы как сахарозаменителя считается неоправданным [3]. Максимальная суточная доза — 400–600 мг на 1 кг массы тела (если заменять весь сахар фруктозой).
Стевиозид
Экстракт растения стевия — это сахарозаменитель последнего поколения с нулевой калорийностью. По сладости стевия сравнима с синтетическими заменителями — она в 300 раз слаще сахарозы. Гликемический индекс стевии равен нулю. Приятный вкус стевии и устойчивость к температурам до 200 градусов обусловили ее широкое использование в пищевой промышленности. В стевии содержатся фолиевая кислота, витамин C и все незаменимые аминокислоты за исключением триптофана. Стевиозиды проверены многими наблюдениями на человеке и животных. Они не являются мутагенными, тератогенными и не обладают канцерогенными свойствами [4]. Максимальная суточная доза — 18 мг на 1 кг массы тела.
Тауматин
Низкокалорийный подсластитель и корректор вкуса белковой природы. Этот белок обычно используется именно для коррекции вкуса, а не как заменитель сахара.
Сахарные спирты (ксилит, сорбит, маннит, изомальт, мальтит, эритритол, лактит)
Сахарные спирты являются производными сахаридов. Относятся к калорийным сахарозаменителям. Они содержат меньше калорий по сравнению с сахарами: 1,5–3 ккал на грамм. Сопоставимы по сладости с сахарозой. Сахарные спирты всасываются медленно и не полностью. На всасывание сахарных спиртов влияет время транзита по желудочно-кишечному тракту и степень ферментации кишечными бактериями. Для усвоения организмом сахарных спиртов практически не требуется инсулина, именно поэтому пища, приготовленная с их использованием, может стать альтернативой для людей, страдающих сахарным диабетом. Особенного внимания в этой группе заслуживает эритритол. Его гликемический индекс равен нулю, он не ферментируется бактериями и не вызывает диареи (в отличие от маннита с нулевым гликемическим индексом).
В аптеках, как правило, представлены сахарозаменители в виде комбинации нескольких веществ, нередко с добавлением декстрозы, фруктозы или обычного сахара для достижения приятного вкуса. Поэтому инсулиновый отклик у таких комбинаций может быть выше, чем у моновеществ по причине добавления сахаров.
Сахарные спирты включены в перечень веществ, признанных полностью безвредными [5]. Однако, у некоторых людей избыточное употребление сорбитола и маннитола может вызвать газообразование и слабительный эффект. Максимальная суточная доза — до 600 мг на 1 кг массы тела.
Теперь рассмотрим популярные синтетические сахарозаменители.
Аспартам
Относится к бескалорийным подсластителям. Один из самых распространенных в мире сахарозаменителей. Впервые был синтезирован в 1965 году из двух аминокислот (аспарагина и фенилаланина) с метанолом. Аспартам слаще сахара примерно в 220 раз и не имеет привкуса. В настоящее время аспартам практически не применяется в чистом виде, его обычно смешивают с другими сахарозаменителями, чаще всего с ацесульфамом калия, чтобы добиться вкусовых качеств, максимально приближенных ко вкусу обычного сахара.
Аспартам противопоказан людям, страдающим фенилкетонурией (генетическое заболевание, сопровождающееся нарушением метаболизма фенилаланина).
В настоящее время существует много противоречивой информации касательно безопасности аспартама. Несколько исследований выявили, что аспартам может вызывать головные боли у тех людей, которые склонны к их появлению [6].
Однако, регулирующие органы более 100 стран признали аспартам безопасным. Аспартам до сих пор остается самым спорным сахарозаменителем. Максимальная суточная доза — 50 мг на 1 кг массы тела.
Ацесульфам К
Неусваиваемый, некалорийный подсластитель со степенью сладости 200 единиц. Впервые был получен в 1970‑е гг., одобрен для применения в пищевой промышленности в 1988 г. [2]. В качестве подсластителя пищевых продуктов ацесульфам используют, как правило, в сочетании с другими сахарозаменителями, и прежде всего с аспартамом, а также с углеводами (сахарозой, фруктозой), которые добавляют для лучшей коррекции вкуса.
FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) одобрило ацесульфам. Исследования на лабораторных грызунах, проведенные Национальным институтом здоровья США в 2005 году, не показали увеличения количества опухолей при добавлении в пищу Ацесульфам калия [7]. Безопасная суточная доза — 15 мг на 1 кг веса тела.
Сукралоза
Сукралоза — высокоинтенсивный, некалорийный сахарозаменитель, в 600 раз слаще столового сахара, обладает ярким сладким вкусом без неприятного привкуса. Открыта в 1976 году, одобрена FDA в 1998 году для использования в качестве сахарозаменителя. Сукралоза не усваивается в процессе пищеварения, выводится в практически неизменном виде. На сегодняшний день сукралоза признана безопасным подсластителем и не вызывает каких‑либо побочных эффектов при длительном применении [8]. Максимальная суточная доза — 15 мг на 1 кг массы тела.
Сахарин
Присутствует на рынке более 100 лет и является старейшим бескалорийным сахарозаменителем синтетического происхождения. Сахарин в 200–700 раз слаще сахара (интенсивность изменяется в зависимости от концентрации). Очень широко используется в пищевой и косметической, а также фармацевтической промышленности. Сахарин не метаболизируется в желудочно-кишечном тракте и не влияет на уровень инсулина.
В ходе экспериментов на животных в 1977 году была обнаружена связь между приемом сахарина и возникновением рака мочевого пузыря у лабораторных крыс. Однако позднее эти предположения были опровергнуты [9]. Препарат одобрен Объединенной экспертной комиссией по пищевым добавкам (JECFA) Всемирной организации здравоохранения и Научным комитетом по пищевым продуктам Европейского союза, разрешен более чем в 90 странах (в том числе и в России [1]). Рекомендованной суточной дозой в приеме сахарина является 5 мг на 1 кг массы тела.
Цикламат натрия
Слаще сахара в 30–50 раз. Впервые сладкие свойства этого вещества были обнаружены еще в 1937 году, а использовать в качестве сахарозаменителя начали только в 1950‑х годах. Широко используется для подслащивания пищевых продуктов, напитков и лекарственных средств. Входит в состав большинства продаваемых в России комплексных подсластителей. По данным исследований, цикламат натрия повышает риск развития рака мочевого пузыря у крыс, однако эпидемиологические данные не подтверждают аналогичного риска у людей [9]. Несмотря на данные о безопасности цикламата натрия, он запрещен для использования в США. Дело в том, что FDA наложило запрет на использование этой добавки еще в 1969 году (после публикации результатов первых исследований на крысах), и до сих пор он не снят. Суточная доза — 10 мг на 1 кг массы тела.
Неотам
Относительно новый синтетический бескалорийный сахарозаменитель. Он состоит из фенилаланина и аспарагиновой кислоты, слаще сахара в 7000–13 000 раз. Быстро метаболизируется и полностью выводится из организма. На сегодняшний день никакого негативного влияния этой добавки на организм не выявлено. В настоящее время это самый сладкий из существующих подсластителей. Вещество не входит в список пищевых добавок, разрешенных к применению в пищевой промышленности в Российской Федерации [1].
Спроси и помоги выбрать
Если перед вами покупатель, заинтересованный в покупке сахарозаменителя, стоит задать ему несколько уточняющих вопросов. Основное, что стоит узнать, — какова цель использования и частота возможного применения подсластителя.
Если целью является контроль уровня глюкозы крови (при сахарном диабете, нарушении толерантности к глюкозе, инсулинорезистентности), а прием будет длительным, то предпочтение стоит отдать стевиозиду или эритритолу и их комбинациям. Именно эти подсластители при минимальном инсулиновом ответе и не имеют побочных эффектов при продолжительном приеме.
Если цель применения сахарозаменителя — снижение веса, а использование будет ситуативным, то целесообразно рекомендовать подсластитель с нулевой калорийностью и максимально приближенным к традиционному вкусу: цикламат натрия, аспартам, сукралоза, ацесульфам калия.
Если использовать подсластитель будут часто, то и здесь лучше выбирать натуральные сахарозаменители (стевиозид, сахарные спирты) во избежание возможных нежелательных эффектов.
Также в зависимости от цели использования можно рекомендовать ту или иную форму выпуска: таблетированный сахарозаменитель удобно использовать для подслащивания напитков, порошковый — для выпечки и в виде порционных саше в поездках, а жидкую форму — применять в кулинарии.
К сожалению, никакой самый современный сахарозаменитель не избавит от тяги к сладкому, а лишь усугубит ее. Чувствуя сладость, но не получая в нагрузку глюкозу, организм начинает испытывать определенного рода «голодание», результатом которого становится повышенный аппетит. В нескольких исследованиях были выявлены взаимосвязи между длительным потреблением бескалорийных подсластителей и увеличением массы тела [10].
Большинство диетологов солидарны в мнении о том, что сахарозаменители должны использоваться умеренно и лишь в тех случаях, когда это действительно необходимо.
Табл. 2. Основные качества сахарозаменителей
Диета при инсулинорезистентности. Для кого? Перечень рекомендованных продуктов
Основы диеты при инсулинорезистентности
От чего стоит отказаться полностью, так это от перекусов между основными приемами пищи. Исключить также стоит жареное и газировки. Минимизировать соленое.
Поскольку продукты животного происхождения богаты жирами, они должны занимать не более трети от суточного рациона. Вообще нужно стараться питаться натуральными продуктами, богатыми белком и витаминами. Хотя сложными углеводами и клетчаткой пренебрегать тоже не стоит. Питаться лучше дробно, маленькими порциями до 5 раз в день. Желательно делать это в одно и то же время.
Не стоит забывать и о микроэлементах. Восприимчивость к инсулину повышают продукты, богатые марганцем, магнием, хромом, цинком и медью.
Список рекомендованных продуктов:
● свежие фрукты(кроме банана, черешни и винограда);
● картофель (не более 300 г в день);
● хлопья из зерновых;
● мясо птицы (курица, индейка);
● растительные масла (оливковое, кукурузное, кунжутное).
Список запрещенных продуктов:
● манка, пшено, перловка;
● макароны и мучные полуфабрикаты;
● сладкие газированные напитки;
● магазинные снеки с приправами;
● жареные и жирные блюда.
Питьевой режим при инсулинорезистентности
Чем заменить сладости
Не стоит относиться к диете как к испытанию. Постарайтесь воспринять это как заботу о себе и собственном здоровье. Некоторые ограничения в питании позволят вам не только снизить массу тела и предотвратить развития хронического заболевания (что уже немало), но и в целом оздоровят организм. Например, восстановится работа пищеварительной и сердечно-сосудистой систем.
Диета при инсулинорезистентности
При инсулиновой резистентности, при диабете, а также при повышенном инсулине важно похудеть. В первом случае это поможет избежать развития диабета, а во втором – облегчить общее состояние, улучшить качество жизни.
Лишний вес не только портит фигуру человека, но и является причиной многих серьезных заболеваний. Так, например, уже в состоянии предожирения у человека может снизиться чувствительность к инсулину. Это называется инсулинорезистентность. Клетки перестают должным образом реагировать на воздействие инсулина, что блокирует процесс усвоения глюкозы, поступающей в кровь при потреблении углеводов. В результате поджелудочная железа, чтобы улучшить эффективность процесса расщепления и усвоения глюкозы повышает выработку инсулина. Со временем организму для нормального функционирования нужно все больше инсулина. Когда потребность в нем становится слишком высокой, и организм уже не может сам обеспечить себя нужным количеством, развивается диабет.
При инсулиновой резистентности, при диабете, а также при повышенном инсулине важно похудеть. В первом случае это поможет избежать развития диабета, а во втором — облегчить общее состояние, улучшить качество жизни. Снижение веса, это достаточно сложный процесс, требующий поддержки специалистов. Людям, имеющим такие серьезные проблемы со здоровьем как диабет 2 типа, заниматься похудением самостоятельно просто не безопасно. Нужно обязательно консультироваться с опытными диетологами, реабилитологами, психологами, которые должны выработать индивидуальную комплексную программу по снижению веса. Только в этом случае можно рассчитывать на хороший результат, не рискуя еще больше навредить здоровью. В клинике «Доктор Борменталь» применяется своя запатентованная методика снижения веса и сохранения результата, с помощью которой похудело уже более полумиллиона человек. Подробнее о методике здесь — https://doctorbormental.ru/metodika/.
Диета при инсулинорезистентности
Чтобы снизить риск возникновения диабета, нужно обязательно нормализировать вес. С этой целью составляется специальный рацион питания, в котором предусматривается минимум быстрых углеводов и животных жиров. При этом в нем должны писутсвовать все необходимые для полноценной работы организма вещества в нужном количестве.
Общие правила
Существуют определенные правила, придерживаясь которых можно разработать качественное удобное меню.
Как стабильно снижать вес на 1-2 кг. в неделю,
перепрограммируя свои привычки?
Список разрешенных продуктов
Рацион человека с инсулинорезистентностью или диабетика должен состоять из натуральных продуктов, богатых белками и витаминами. При этом должны присутствовать в достаточном количестве сложные углеводы. Диетологи рекомендуют употреблять следующие продукты:
Можно немного добавлять сливочного масла, но отдавать предпочтение стоит жирам растительного происхождения — масло кукурузное, кунжутное, оливковое.
Очень важно обеспечивать организм микроэлементами, необходимыми для полноценного обмена веществ. Эти вещества повышают восприимчивость к инсулину. К ним относятся: марганец, магний, хром, цинк, медь.
Что можно пить
Напитки, содержащие сахар для людей в состоянии преддиабета находятся под запретом. Поэтому покупные соки, сладкие воды нужно исключить. Пить можно в больших количествах чистую воду, а также приготовленные самостоятельно компоты, отвары и морсы без сахара. Из горячих напитков разрешается кофе (1-2 чашки в день) и зеленый чай. Их тоже нужно пить без сахара. Но можно применять натуральные подсластители, такие как глициризин, фруктоза, стевия или обычный мед. Не стоит использовать синтетические сахарозаменители, так как они могут нанести вред здоровью и ухудшить самочувствие.
Не все разрешенные подсластители можно применять в неограниченном количестве. Самым безвредным является глициризин. Если не получается пить несладкие напитки и подсластьитель приходится применять постоянно, лучше пусть это будет именно глициризин. Мед очень полезен, но может вызывать аллергические реакции, к тому же он не подходит для меню худеющего человека. Его можно употреблять не более 1 чайной ложки в сутки. Фруктоза — это оптимальный заменитель сахара, но больше 25 г в день ее не стоит потреблять.
Список запрещенных продуктов
Не рекомендуются такие продукты, которые содержат жиры и быстрые углеводы, и при этом не имеют полезных веществ:
Если меню человека состоит преимущественно из перечисленных выше позиций, можно смело говорить о нарушении пищевого поведения. Чтобы исправить ситуацию и не довести дело до диабета, следует обратиться к диетологу и откорректировать рацион. Специалисты рекомендуют убирать запрещенные продукты постепенно, по одному пункту за неделю.
В тех случаях, когда у человека есть серьезная зависимость от любимых, но неполезных блюд, переход на новый сбалансированный рацион может оказаться слишком сложным. Нередко все заканчивается срывом и отказом менять пищевые привычки. Чтобы этого избежать рекомендуется не убирать запрещенную еду вообще, а сократить ее потребление до минимума. Например, некоторые диетологи советуют раз в неделю проводить разгрузочный день наоборот — в течение дня есть все привычное и неполезное, но в остальные 6 дней к такой еде не прикасаться вообще.
Узнайте, есть ли у вас нарушения
пищевого поведения
Меню диеты при инсулинорезистентности (Режим питания)
Рацион человека с инсулинорезистентностью должен быть разнообразным и сбалансированным. Нужно включить блюда, которые будут доставлять удовольствие, и обеспечивать организм всеми необходимыми веществами. Ниже приведен примерный вариант меню на неделю. Его можно дополнять и видоизменять в зависимости от личных предпочтений, сезона, возможностей.
Понедельник
Вторник
Среда
Четверг
Пятница
Суббота
Воскресенье
Каждый день в любой из приемов пищи можно съедать 2 кусочка ржаного хлеба. Желательно чтобы хлеб был не свежим, а выпеченным за день или два. Можно заменить хлеб диетическими хлебцами.
Очень важно при любой диете помнить о соблюдении водного баланса. Нужно в течение дня часто пить воду небольшим порциями. В целом следует выпивать около 2 литров воды в день.
Плюсы и минусы диеты
Диета для людей с инсулинорезистентностью предлагается как вариант постоянного правильного питания. По сравнению с краткосрочными диетами с более строгими ограничениями она имеет такие преимущества:
Недостатками диеты можно назвать некоторые сложности, которые возникают на первых этапах ее применения. К ним относят такие явления:
Чем заменить сладости
Для многих людей переход на правильное питание дается очень тяжело именно из-за недостатка сладкого. Сахарасодержащие продукты, тем более выпечка и кондитерские изделия, которые содержат все те же быстрые углеводы и жиры, исключаются при любой диете. Но организм, привыкший к сладостям, начинает «паниковать». Он подает сигнал о том, что питание стало неполноценным, и человек испытывает серьезный дискомфорт, у него ухудшается настроение, возникает состояние депрессии. Поэтому, тем, кто раньше много потреблял сладкого, при переходе на диету нужно продумать полезную замену пирожным, конфетам и булочкам.
Любители творожных десертов могут готовить запеканки из обезжиренного творога. Добавлять можно нежирную сметану, ягоды, орехи. При необходимости подсластить можно фруктозой или стевией.
Хороший диетический вариант — морковная запеканка со сметаной и взбитым белком. Можно делать всевозможные фруктовые салаты и заправлять их нежирным натуральным йогуртом без добавок. Самый простой способ — запечь в духовке яблоки. Можно с творогом, сухофруктами, с добавлением капельки меда. В интернете есть и другие рецепты полезных сладостей. Они намного лучше покупной кондитерки, от них не полнеют, и они не вредят здоровью. Об этом следует помнить, когда появляется желание купить что-то сладкое в магазине.
Для занятых людей, которым некогда самостоятельно готовить десерты, в супермаркетах есть специальные отделы с продуктами для покупателей с диабетом. Это различные сладкие изделия, содержащие безопасные сахарозаменители. Их можно иногда покупать, но злоупотреблять нельзя, так как в них есть другие вредные составляющие — красители, усилители вкуса, консерванты и т. д. Лучше приучить себя к натуральным фруктам, сухофруктам, орехам.
Комментарии диетологов
Предложенная здесь диета, это, по сути, просто правильная система питания, которой желательно придерживаться всем, независимо от состояния здоровья. Людям с инсулинорезистентностью она просто необходима. Естественно, что составлять рацион питания нужно вместе со специалистом, тем более, если проблемы с обменными процессами уже начались. Но общий принцип остается неизменным — убираем быстрые углеводы и животные жиры, повышаем процент продуктов, содержащих витамины, минералы, клетчатку.
Инсулинорезистентность и пути ее коррекции при сахарном диабете 2 типа
Инсулинорезистентность — это недостаточный биологический ответ клеток на действие инсулина при его достаточной концентрации в крови. Биологические эффекты инсулина могут быть объединены в четыре группы: очень быстрые (секунды): гиперполяризация мембран
Инсулинорезистентность — это недостаточный биологический ответ клеток на действие инсулина при его достаточной концентрации в крови. Биологические эффекты инсулина могут быть объединены в четыре группы:
Таким образом, понятие инсулинорезистентности не сводится только к параметрам, характеризующим метаболизм углеводов, а включает также изменение метаболизма жиров, белков, функции эндотелия, экспрессии генов и др.
Можно выделить целый ряд заболеваний и физиологических состояний, сопровождающихся инсулинорезистентностью. Основные из них следующие (М. И. Балаболкин, 2001):
Термин «инсулинорезистентность» не следует отождествлять с «синдромом инсулинорезистентности» или «метаболическим синдромом», описанным G. Reaven (1988) и включающим в себя: нарушение толерантности к глюкозе (или СД 2 типа), артериальную гипертензию, гиперурикемию, гиперкоагуляцию, микроальбуминурию и некоторые другие системные нарушения.
Свое биологическое действие на уровне клетки инсулин осуществляет через соответствующий рецептор. Инсулиновый рецептор представляет собой белок, состоящий из двух α- и двух β-субъединиц. α-субъединица располагается на наружной поверхности клеточной мембраны, именно с ней связывается инсулин. β-субъединица является трансмембранным белком и обладает тирозинкиназной активностью, которая не проявляется при отсутствии инсулина. Присоединение инсулина к центру связывания на α-субъединицах активирует фермент, причем субстратом служит сам этот фермент, т. е. происходит аутофосфорилирование β-субъединицы рецептора инсулина по нескольким тирозиновым остаткам. Фосфорилирование β-субъединицы, в свою очередь, приводит к изменению субстратной специфичности фермента: теперь он способен фосфорилировать другие внутриклеточные белки — субстраты инсулинового рецептора (СИР). Известны СИР-1, СИР-2, а также некоторые белки семейства STAT (signal transducer and activator of transcription — переносчики сигнала и активаторы транскрипции). Фосфорилирование СИР ведет к плейотропной реакции клетки на инсулиновый сигнал. Мыши лабораторной линии, лишенные гена СИР-1, проявляют резистентность к инсулину и сниженную толерантность при нагрузке глюкозой. Инсулин при посредничестве СИР-1 активирует фосфатидилинозитол-3-киназу (ФИ-3-киназу). Активация ФИ-3-киназы является центральным звеном сигнального пути, стимулирующего транслокацию глюкозного транспортера ГЛЮТ-4 из цитозоля в плазматическую мембрану, а следовательно, и трансмембранный перенос глюкозы в мышечные и жировые клетки. Ингибиторы ФИ-3-киназы подавляют и базальное, и стимулированное инсулином потребление глюкозы; в последнем случае ингибируется транслокация ГЛЮТ-4 к мембране (M. Reaven Gerald, 1999).
Согласно современным представлениям резистентность периферических тканей (мышечной, жировой и ткани печени) к действию инсулина лежит в основе патогенеза СД 2 типа. Нарушения обменных процессов, наблюдаемые вследствие инсулинорезистентности при СД 2 типа, представлены в таблице 1.
Инсулинорезистентность мышечной ткани является наиболее ранним и, возможно, генетически определяемым дефектом, который намного опережает клиническую манифестацию СД 2 типа. Результаты исследований с применением ядерной магнитно-резонансной спектроскопии (NMR) показали (G. I. Shulman, D. L. Rothman, 1990), что синтез гликогена в мышцах играет принципиальную роль в инсулинобусловленном усвоении глюкозы как в норме, так и при СД 2 типа, вместе с тем нарушение синтеза гликогена является вторичным по отношению к дефектам транспорта и фосфорилирования глюкозы.
Снижение концентрации инсулина в печени характеризуется отсутствием его ингибирующего влияния на процессы глюконеогенеза, снижением синтеза гликогена, активацией процессов гликогенолиза, что в конечном итоге приводит к повышению продукции глюкозы печенью (R. A. DeFronzo, 1990).
Другим звеном, играющим значительную роль в развитии гипергликемии, является резистентность жировой ткани к действию инсулина, а именно резистентность к антилиполитическому действию инсулина. В результате неконтролируемого окисления липидов освобождается большое количество свободных жирных кислот (СЖК). Повышение их уровня ведет к ингибированию процессов транспорта и фосфорилирования глюкозы и, как следствие, к снижению окисления глюкозы и синтеза гликогена в мышцах (M. M. Hennes, E. Shrago, 1990). Таким образом, изменения жирового обмена, а именно метаболизма СЖК, способствуют нарушению утилизации глюкозы тканями.
Избыток СЖК активизирует процессы глюконеогенеза, влияет на синтез липопротеидов в печени, приводя к повышенному образованию липопротеинов очень низкой плотности (ЛПОНП) и триглицеридов, что сопровождается снижением уровня липопротеинов высокой плотности (ЛПВП) (R. H.Unger, 1995).
Длительное повышение уровня СЖК оказывает прямое повреждающее действие на β-клетки поджелудочной железы, что описано как эффект липотоксичности, результатом которого является снижение секреторной способности β-клеток панкреатических островков.
Состояние инсулинорезистентности и высокий риск развития СД 2 типа характерен для лиц с висцеральным, а не с периферическим характером распределения жировой клетчатки. Возможно, это связано с биохимическими особенностями висцеральной жировой ткани: она слабо реагирует на антилиполитический эффект инсулина. В висцеральной жировой ткани отмечено усиление синтеза фактора некроза опухолей, который снижает активность тирозинкиназы инсулинового рецептора и фосфорилирование СИР-белков. Гипертрофия адипоцитов при абдоминальном типе ожирения приводит к изменению конформации молекулы инсулинового рецептора и нарушению процессов связывания его с инсулином.
Пока β-клетки поджелудочной железы способны вырабатывать достаточное количество инсулина для компенсации перечисленных дефектов и поддерживать состояние гиперинсулинемии, гипергликемия будет отсутствовать. Однако при истощении резервов β-клеток возникает состояние относительной недостаточности инсулина, что проявляется повышением уровня сахара крови и манифестацией диабета. Как показали результаты исследований (Levy et al., 1998), у больных СД 2 типа находящихся только на диете, через 5–7 лет от начала заболевания происходит значительное снижение функции β-клеток, в то время как чувствительность тканей к инсулину практически не меняется. Существует немало клинических доказательств тому, что гиперинсулинемия является независимым фактором риска развития ишемической болезни сердца как у лиц, не имеющих СД 2 типа, так и у больных с СД 2 типа (S. Lebto et al., 2000).
Тактика лечения СД 2 типа должна быть направлена на нормализацию патогенетических процессов, лежащих в основе заболевания, т. е. на уменьшение инсулинорезистентности и улучшение функции β-клеток.
В настоящее время существуют нефармакологические и фармакологические методы коррекции инсулинорезистентности. К нефармакологическим методам относятся низкокалорийная диета, направленная на снижение массы тела, и физические нагрузки — фундамент на котором базируется лечение всех больных СД 2 типа с инсулинорезистентностью. Снижение веса может быть достигнуто при соблюдении низкокалорийной диеты, содержащей менее 30% жиров, менее 10% насыщенных жиров и более 15 г/ккал клетчатки, а также при регулярном режиме физических нагрузок.
Больным могут быть рекомендованы регулярные аэробные физические нагрузки средней интенсивности (пешие прогулки, плавание, равнинные лыжи, велосипед) продолжительностью 30–45 мин от 3 до 5 раз в неделю, а также любой посильный комплекс физических упражнений (J. Eriksson, S. Taimela, 1997). Физические нагрузки стимулируют инсулиннезависимое поглощение глюкозы, при этом индуцированное упражнениями увеличение потребления глюкозы не зависит от действия инсулина. Более того, во время физических нагрузок происходит парадоксальное снижение уровня инсулина в крови. Потребление глюкозы мышцами увеличивается, несмотря на падение уровня инсулина, при этом физическая нагрузка сопровождается перемещением ГЛЮТ-4 из другого пула, нежели под действием инсулина (N. S. Peirce, 1999).
В период дебюта заболевания, до формирования стойкого снижения секреторной функции β-клеток поджелудочной железы, особенно при избыточной массе тела или ожирении, препаратами выбора являются средства, снижающие инсулинорезистентность периферических тканей. К этой группе препаратов относятся бигуаниды и тиазолидиндионы (глитазоны).
В России, как и во всех странах мира, из группы бигуанидов применяется только метформин (сиофор, глюкофаж, глиформин).
Основной механизм действия метформина направлен на устранение продукции глюкозы печенью, а также на снижение инсулинорезистентности мышечной и жировой ткани. Препарат обладает способностью подавлять глюконеогенез, блокируя ферменты данного процесса в печени. В присутствии инсулина бигуаниды увеличивают периферическую утилизацию глюкозы мышцами, активируя тирозинкиназу инсулинового рецептора и транслокацию ГЛЮТ-4 и ГЛЮТ-1 в мышечных клетках. Бигуаниды повышают утилизацию глюкозы кишечником (усиливая анаэробный гликолиз), что проявляется в снижении уровня глюкозы в крови, оттекающей от кишечника. Длительное применение метформина положительно влияет на липидный обмен: приводит к снижению уровня холестерина и триглицеридов в крови. Механизм действия метформина — антигипергликемический, а не гипогликемический. Препарат не снижает содержание глюкозы в крови ниже ее нормального уровня — вот почему при монотерапии метформином отсутствуют гипогликемические состояния. По данным ряда авторов, метформин обладает аноректическим действием. У больных, получающих метформин, наблюдается снижение массы тела, преимущественно за счет уменьшения жировой ткани. Доказано положительное влияние препарата и на фибринолитические свойства крови за счет подавления ингибитора активатора плазминогена-1.
Результаты проспективного исследования, проведенного в Великобритании (UKPDS), показали, что применение метформина с момента установления диагноза снижает смертность от причин, связанных с СД, на 42%, общую смертность — на 36%, а частоту диабетических осложнений — на 32% (Lancet, 1998). Полученные данные свидетельствует о том, что прием метформина достоверно улучшает выживаемость и снижает риск развития осложнений СД 2 типа. При этом в исследовании UKPDS средняя суточная доза метформина (глюкофаж) составляла для большинства пациентов 2000 мг и выше. Именно доза 2000 мг/сут является оптимальной суточной дозой, при которой наблюдается лучший контроль сахара крови.
Показанием к назначению метформина является СД 2 типа на фоне избыточной массы тела или ожирения, при неудовлетворительной компенсации углеводного обмена на фоне диеты и физической нагрузки.
Начальная суточная доза метформина — 500 мг. Через 1 нед от начала терапии при отсутствии побочных эффектов дозу препарата увеличивают. Максимальная суточная доза препарата составляет 3000 мг. Принимают препарат 2–3 раза в день во время еды, что чрезвычайно важно для максимальной эффективности применения. Длительность действия препарата составляет 8–12 ч.
Среди побочных эффектов действия метформина следует отметить диарею, диспепсические расстройства, металлический вкус во рту. Побочные эффекты обычно исчезают при снижении дозы препарата. Упорная диарея является противопоказанием для отмены препарата.
Угнетая глюконеогенез, бигуаниды способствуют увеличению содержания лактата, пирувата, аланина (веществ, являющихся предшественниками глюкозы в процессе глюконеогенеза), что в крайне редких случаях может привести к развитию лактацидоза. Риск развития лактацидоза увеличивается при приеме чрезмерно больших доз препарата, у больных с почечной и печеночной недостаточностью, а также при наличии состояний, сопровождающихся гипоксией тканей.
Противопоказаниями к назначению метформина являются нарушения функций почек (снижение клиренса креатинина ниже 50 мл/мин или повышение креатинина в крови выше 1,5 ммоль/л), злоупотребление алкоголем, беременность, лактация, а также гипоксические состояния любой природы: недостаточность кровообращения, дыхательная недостаточность, анемия, острые инфекции, острый инфаркт миокарда, шок, внутривенное введение йодсодержащих контрастных веществ.
Исследования последних лет показали, что частота летального повышения в крови уровня молочной кислоты на фоне длительного лечения метформином составляет лишь 0,084 случая на 1000 больных в год. Соблюдение противопоказаний к назначению метформина исключает риск развития данного осложнения.
Метформин может применяться как монотерапия или в сочетании с препаратами сульфонилмочевины у больных СД 2 типа. Комбинация бигуанидов и производных сульфонилмочевины является рациональной, поскольку влияет на оба звена патогенеза СД 2 типа: стимулирует секрецию инсулина и улучшает чувствительность тканей к инсулину. В настоящее время разработаны и активно используются комбинированные препараты с фиксированной дозой метформина и производных сульфонилмочевины:
Комбинированные препараты имеют ряд преимуществ. За счет более низких терапевтических доз комбинируемых препаратов отмечается лучшая их переносимость, а также наблюдается меньшее количество побочных эффектов, чем при монотерапии или при раздельном назначении комбинируемых препаратов. При приеме комбинированных препаратов отмечается более высокая комплаентность, поскольку уменьшается количество и кратность приема таблетированных препаратов. Использование комбинированных препаратов дает возможность назначения трехкомпонентной терапии. Наличие различных дозировок препаратов, входящих в состав комбинированного препарата (как для препарата глюкованс), делает возможным более гибкий подбор именно оптимального, нужного соотношения комбинируемых препаратов. Однако строго фиксированная доза препаратов вызывает вместе с тем и ряд трудностей при необходимости изменения дозы только одного из комбинируемых препаратов.
Также у больных СД 2 типа метформин может применяться в комбинации с инсулином в случае выраженной инсулинорезистентности, что позволяет улучшить компенсацию углеводного обмена.
Активация PPARγ изменяет экспрессию генов, вовлеченных в такие метаболические процессы, как адипогенез, передача инсулинового сигнала, транспорт глюкозы (Y. Miyazaki еt al., 2001), что приводит к снижению резистентности тканей к действию инсулина в клетках-мишенях. В жировой ткани действие глитазонов приводит к торможению процессов липолиза, к накоплению триглицеридов, результатом чего является снижение уровня СЖК в крови. В свою очередь, снижение уровня СЖК в плазме способствует усилению процессов поглощения глюкозы мышцами и уменьшает глюконеогенез. Поскольку СЖК оказывают липотоксическое действие на β-клетки, их снижение улучшает функцию последних.
Глитазоны способны увеличивать экспрессию и транслокацию глюкозного транспортера GLUT4 на поверхности адипоцита в ответ на действие инсулина, что усиливает утилизацию глюкозы жировой тканью. Глитазоны оказывают влияние на дифференцировку преадипоцитов, что приводит к увеличению доли более мелких, но более чувствительных к действию инсулина клеток. In vivo и in vitro глитазоны уменьшают экспрессию лептина, влияя таким образом опосредованно на массу жировой ткани (B. M. Spiegelman, 1998), а также способствуют дифференцировке бурой жировой ткани.
Глитазоны улучшают утилизацию глюкозы в мышцах. Как известно, у больных СД 2 типа наблюдается нарушение инсулинстимулированной активности ФИ-3-киназы инсулинового рецептора в мышцах. В сравнительном исследовании было показано, что на фоне терапии троглитазоном инсулинстимулированная активность ФИ-3-киназы возросла почти в 3 раза. На фоне же терапии метформином изменения активности данного фермента не наблюдалось (Yoshinori Miyazaki et al., 2003).
Результаты лабораторных исследований позволили предположить, что глитазоны (росиглитазон) обладают защитным эффектом в отношении β-клеток, препятствуют гибели β-клеток путем усиления их пролиферации (P. Beales еt al., 2000).
Действие глитазонов, направленное на преодоление инсулинорезистентности и улучшение функции β-клеток, приводит не только к поддержанию удовлетворительного гликемического контроля, но и предотвращает прогрессирование заболевания, дальнейшее снижение функции β-клеток и прогрессирование макрососудистых осложнений. Оказывая воздействие практически на все компоненты метаболического синдрома, глитазоны потенциально снижают риск развития сердечно-сосудистых заболеваний.
Рецепторы PPARγ присутствуют во всех клетках сосудистой стенки и участвующих в развитии атеросклероза: в эндотелиальных клетках, в гладкомышечных клетках сосудов (VSM), моноцитах и макрофагах. PPARγ лиганды ингибируют дифференцировку, пролиферацию и миграцию всех видов клеток. PPARγ лиганды ингибируют рост и миграцию VSM-клеток путем остановки клеточного цикла в фазу G1. Они также ингибируют два процесса, необходимые для движения VSM-клеток: миграцию, индуцированную хемоатрактантами и продукцию матриксной металопротеиназы. Помимо ингибирования миграции моноцитов, индуцированной белком хемотаксиса моноцитов (MCP)-1, PPARγ лиганды ингибируют экспрессию молекул адгезии в эндотелиальных клетках, что приводит к снижению адгезии моноцитов на эндотелиальных клетках и уменьшению воспалительного действия макрофагов (A. Greenberg et al., 2001).
В настоящее время зарегистрированы и разрешены к применению два препарата из группы тиазолидиндионов: пиоглитазон (актос) и росиглитазон (авандия).
Показанием к применению глитазонов в качестве монотерапии является впервые выявленный СД 2 типа с признаками инсулинорезистентности при неэффективности диеты и режима физических нагрузок. Глитазоны показаны в качестве комбинированной терапии в случае отсутствия адекватного гликемического контроля при приеме метформина или производных сульфонилмочевины. Для улучшения гликемического контроля может использоваться и тройная комбинация (глитазоны, метформин и производные сульфонилмочевины).
Рекомендуемые дозы тиазолидиндионов представлены в таблице 2. Препараты могут приниматься как вместе с едой, так и между приемами пищи 1 или 2 раза в день. Уровень глюкозы понижается постепенно, максимальный эффект развивается через 6–8 нед. Препараты являются эффективными и хорошо переносимыми также у пожилых больных СД 2 типа (старше 65 лет).
Противопоказаниями к применению тиазолидиндионов являются: СД 1 типа, беременность и лактация, кетоацидоз, повышение печеночных трансаминаз более чем в 2,5 раза, сердечная недостаточность III–IV класса.
Ни пиоглитазон, ни росиглитазон не обладают гепатотоксичностью.
Вместе с тем при назначении препаратов из группы глитазонов необходимо мониторировать функцию печени до начала лечения. Повышение уровня аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (АСТ) более чем в 2,5 раза является противопоказанием для назначения глитазонов. Регулярный контроль ферментов АЛТ, АСТ в ходе лечения не показан, однако может проводиться по рекомендации врача при индивидуальных показаниях. Увеличение активности АЛТ на фоне лечения более чем в 3 раза требует прекращения дальнейшего приема препаратов.
Прием глитазонов сопровождался умеренной прибавкой массы тела, однако при этом отмечалось улучшение гликемического контроля и улучшение утилизации глюкозы тканями. В среднем при приеме росиглитазона отмечается увеличение массы тела на 1–4 кг в течение первого года. При приеме росиглитазона в комбинации с метформином прибавка массы тела была, как правило, меньше. Важно отметить, что увеличение массы тела происходит за счет увеличения подкожной жировой клетчатки, при этом масса абдоминального жира снижается.
У небольшого числа больных прием глитазонов может сопровождаться развитием анемии и отеками.
Представителем нового поколения глитазонов является росиглитазон (авандия). В отличие от пиоглитазона росиглитазон является более селективным в отношении PPARγ-рецепторов, обладает несравненно более высоким связующим сродством с PPARγ-рецепторами (в 40–100 раз выше, чем пиоглитазон) при меньшей концентрации препарата в крови. Различны и механизмы метаболизма этих двух препаратов. Росиглитазон метаболизируется изоферментными системами цитохрома P450, в основном CYP3С8, в меньшей степени — CYP2C9, в то время как пиоглитазон метаболизируется CYP3A. При терапевтических концентрациях росиглитазона в крови другие изоферменты цитохрома P450, включая CYP3A4, не угнетаются. Это означает, что вероятность взаимодействия росиглитазона с другими препаратами низка. В отличие от пиоглитазона росиглитазон не влияет на формакокинетику дигоксина, нифедипина, ранитидина, этинилэстрадиола, норэтиндрона.
Гипогликемическое действие глитазонов проявляется только в присутствии инсулина. При приеме глитазонов в качестве монотерапии наблюдается достоверное снижение не только базальной гликемии, но и постпрандиальной, при этом, что является несомненно важным, не отмечалось увеличения постпрандиальной гиперинсулинемии (G. Grunberger, W. M. Weston, 1999). Интересны данные, указывающие на более стойкий гипогликемический контроль, достигаемый при приеме росиглитазона, в сравнении с монотерапией глибенкламидом. Было показано, что при монотерапии росиглитазоном уровень НвА1с сохранялся неизменным в течение 30 мес без изменения терапии (B. Charbonnel, F. Lonnqvist, 1999). В проведенных исследованиях было показано, что росиглитазон улучшает функцию β-клеток и тем самым способен замедлять прогрессирование заболевания. Росиглитазон благоприятно влияет на функцию эндотелия и обладает способностью предупреждать развитие рестеноза после оперативных вмешательств на сосудах (T. Yoshimoto et al., 1999).
Сегодня получено много данных, указывающих на то, что применение глитазонов не только компенсирует углеводный обмен для больных диабетом, но и создает условия для блокирования механизмов, приводящих к развитию макро- и микроангиопатий, а значит, расширяются показания для применения этого препарата в клинических целях.
Эффективной и целесообразной является комбинация глитазонов и метформина. Оба препарата обладают сахароснижающим и гиполипидемическим действием, однако механизм действия росиглитазона и метформина различен (V. A. Fonseca et al., 1999). Глитазоны прежде всего усиливают инсулинобусловленное усвоение глюкозы в скелетных мышцах. Действие же метформина направлено на подавление синтеза глюкозы в печени. Как было показано в исследованиях, именно глитазоны, а не метформин способны увеличивать более чем в 3 раза активность ФИ-3-киназы, одного из основных ферментов передачи инсулинового сигнала. Помимо этого добавление глитазонов к терапии метформином приводит к значительному улучшению функции β-клеток в сравнении с терапией метформином.
Фирмой ГлаксоСмитКляйн разработан новый комбинированный препарат — авандамет. Предполагается две формы данного препарата с различной фиксированной дозой росиглитазона и метформина: росиглитазон 2 мг и 500 мг метформина и росиглитазон 1 мг в комбинации с 500 мг метформина. Рекомендуемый режим приема — 1–2 таблетки 2 раза в сутки. Препарат обладает не только более выраженным сахароснижающим действием по сравнению с действием каждого компонента в отдельности, но и уменьшает объем подкожной жировой клетчатки. В 2002 г. авандомет зарегистрирован в США, в 2003 г. — в странах Европы. В ближайшее время ожидается появление этого препарата в России.
Комбинация глитазонов с производными сульфонилмочевины позволяет воздействовать на два основных звена в патогенезе СД 2 типа: усиливать секрецию инсулина (производные сульфонилмочевины) и повышать чувствительность тканей к действию инсулина (глитазоны). В ближайшее время ожидается появление комбинированного препарата компании ГлаксоСмитКляйн — авандарила (росиглитазон и глимепирид).
Комбинация глитазонов и инсулина на сегодняшний день одобрена и рекомендована к применению во многих странах, в том числе и в России (P. Raskin, J. F. Dole, 1999). Вместе с тем результаты ряда исследований свидетельствуют об усилении проявления хронической сердечной недостаточности у больных СД 2 типа, получавших инсулин при добавлении к терапии росиглитазона, что требовало более частых обращений к врачу и коррекции проводимой терапии. Наиболее часто наблюдалось появление отеков нижних конечностей. Поэтому необходим более тщательный контроль состояния сердечно-сосудистой системы у больных с хронической сердечной недостаточностью при добавлении росиглитазона к инсулинотерапии. Глитазоны противопоказаны больным с хронической сердечной недостаточностью III и IV класса.
Воздействуя практически на все компоненты метаболического синдрома, глитазоны способствуют снижению риска развития и прогрессирования сердечно-сосудистых заболеваний.
Успешно разрабатываются препараты новой группы — глитазары. В отличие от глитазонов эти соединения являются двойными агонистами, т. е. стимулируют не только PPARγ-, но и PPARα-рецепторы. Препараты активно влияют на восстановление углеводного и жирового обмена у больных СД 2 типа, оказывают благоприятное воздействие на профилактику и течение сосудистых осложнений. Проведенные клинические исследования по применению тезаглитазара и мураглитазара показали их хорошую эффективность.
И. В. Кононенко, кандидат медицинских наук
О. М. Смирнова, доктор медицинских наук, профессор
ЭНЦ РАМН, Москва