Фоллитропин альфа что это
Фоллитроп (Follitrop)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Фоллитроп
| Лиофилизат для приготовления раствора для в/м и п/к введения | 1 фл. |
| фоллитропин альфа | 75 МЕ |
Фармакологическое действие
Фармакокинетика
Показания активных веществ препарата Фоллитроп
Ановуляция (включая синдром поликистозных яичников (СПКЯ)) у женщин в случае неэффективности предшествующей терапии кломифеном.
Контролируемая овариальная гиперстимуляция в программах вспомогательных репродуктивных технологий.
Овариальная стимуляция у женщин с тяжелым дефицитом ФСГ и ЛГ (в комбинации с препаратом ЛГ, в соответствующей лекарственной форме).
Стимуляция сперматогенеза при гипогонадотропном гипогонадизме у мужчин (в комбинации с ХГЧ, в соответствующей лекарственной форме).
Режим дозирования
Побочное действие
Прочие: лихорадка, артралгия.
Прочие: лихорадка, артралгия.
Противопоказания к применению
Повышенная чувствительность к фоллитропину альфа; опухоли гипофиза или гипоталамуса.
Не применяют у девочек-подростков в возрасте до 18 лет.
Применение не показано после наступления менопаузы.
У мужчин: при первичном гипогонадизме (первичной тестикулярной недостаточности).
У пациентов с порфирией, а также при наличии порфирии у родственников. У женщин с наличием тромбоэмболического заболевания в анамнезе или в настоящее время или у женщин с высоким риском развития тромбоэмболических осложнений (наличие тромбозов или тромбоэмболий у ближайших родственников).
Применение при беременности и кормлении грудью
Применение у детей
Применение у пожилых пациентов
Безопасность и эффективность фоллитропина альфа у пожилых пациентов не установлена.
Особые указания
До проведения лечения следует установить факт наличия супружеского бесплодия и возможные противопоказания к беременности. Необходимо исключить сопутствующие эндокринные заболевания (гипотиреоз, надпочечниковая недостаточность, гиперпролактинемия, опухоль гипоталамуса и гипофиза).
Необходимо оценить проходимость маточных труб с целью выбора метода ВРТ. Следует исключить непроходимость маточных труб, если пациентка не участвует в программе экстракорпорального оплодотворения.
У пациентов с порфирией, а также при наличии порфирии у родственников, во время терапии фоллитропином альфа требуется проводить тщательный мониторинг. При ухудшении состояния или появлении первых признаков этого заболевания может потребоваться прекращение терапии.
Реакция на введение ФСГ может отличаться у различных пациентов, поэтому следует использовать минимальные эффективные дозы как у женщин, так и у мужчин.
При назначении чХГ возрастает возможность возникновения синдрома гиперстимуляции яичников, поэтому при возникновении чрезмерной эстрогенной реакции чХГ не назначают, а пациенткам рекомендуют воздержаться от коитуса не менее 4 дней. Вероятность возникновения гиперстимуляции можно снизить путем аспирации всех фолликулов перед овуляцией.
Частота многоплодной беременности и родов при индукции овуляции выше, по сравнению с естественным зачатием, наиболее частым вариантом при многоплодии является двойня. Многоплодная беременность, особенно в случае большого количества эмбрионов, повышает риск неблагоприятного исхода для матери и плода. Для минимизации риска многоплодной беременности необходим тщательный мониторинг овариального ответа. При ВРТ риск многоплодной беременности связан, главным образом, с количеством перенесенных эмбрионов, их жизнеспособностью и возрастом пациентки.
Частота врожденных аномалий развития плода после применения программ ВРТ может быть несколько выше, чем при естественной беременности и родах. Тем не менее, неизвестно, связано ли это с особенностью родителей (например, возраст матери, качество спермы) и многоплодной беременностью или же непосредственно с процедурами ВРТ.
Повышенная концентрация фолликулостимулирующего гормона в сыворотке крови мужчин может свидетельствовать о первичной тестикулярной недостаточности. В этом случае терапия фоллитропином альфа не эффективна, применение его противопоказано.
Лекарственное взаимодействие
При одновременном применении с другими средствами для стимуляции овуляции возможно повышение реакции образования фолликулов, тогда как одновременная десенсибилизация гипофиза агонистом ГнРГ может привести к необходимости увеличения дозы фоллитропина альфа, вызывающей адекватную реакцию яичников.
КОРИФОЛЛИТРОПИН АЛЬФА (CORIFOLLITROPIN ALFA) ОПИСАНИЕ
Фармакологическое действие
Корифоллитропин альфа вызывает и поддерживает рост фолликулов в течение недели. Увеличение длительности фолликулостимулирующей активности было достигнуто за счет присоединения карбокситерминального пептида бета-субъединицы хорионического гонадотропина человека (ХГЧ) к бета-цепи человеческого ФСГ. Корифоллитропин альфа не обладает активностью ХГЧ и ЛГ.
Фармакокинетика
Показатели фармакокинетики корифоллитропина альфа не зависели от дозы в широком диапазоне доз (7.5-240 мкг). Распределение, метаболизм и выведение корифоллитропина альфа сходны с таковыми других гонадотропинов, таких как ФСГ, ХГЧ и ЛГ.
После однократного п/к введения корифоллитропина альфа C max в плазме достигалась через 44 ч (34-57 ч). Абсолютная биодоступность составила 58% (48-70%). Экспозиция корифоллитропина альфа зависит от массы тела. В клинических исследованиях концентрации корифоллитропина альфа в плазме были сходными после введения корифоллитропина альфа в дозах 100 мкг и 150 мкг женщинам с массой тела ≤60 кг и >60 кг соответственно.
После всасывания в кровь корифоллитропин альфа распределяется в основном в яичники и почки. В равновесном состоянии V d и клиренс составляют 9.2 л (6.5-13.1 л) и 0.13 л/ч (0.10-0.18 л/ч) соответственно.
В метаболизме корифоллитропина альфа, преимущественно, участвуют почки. В результате метаболизма образуются фармакологически неактивные альфа и бета субъединицы (включая карбокси-терминальный пептид), которые, преимущественно, выводятся почками.
T 1/2 корифоллитропина альфа составляет 69 ч (59-79 ч). Корифоллитропин альфа выводится, преимущественно, почками.
Показания активного вещества КОРИФОЛЛИТРОПИН АЛЬФА
Режим дозирования
Вводят п/к (предпочтительно под кожу живота) в соответствии со специальными схемами.
Рекомендуемые дозы были установлены только при комбинированном использовании с антагонистом ГнРГ.
Женщинам с массой тела 60 кг однократно вводят 150 мкг.
Побочное действие
Противопоказания к применению
Опухоли яичников, молочной железы, матки, гипофиза или гипоталамуса; кровотечения и кровянистые выделения из половых путей (не связанные с менструацией) неустановленной причины; первичная недостаточность яичников; кисты яичников или увеличение яичников; СГЯ в анамнезе; в случае, если предыдущий цикл контролируемой стимуляции яичников привел к росту более чем 30 фолликулов до размера не менее 11 мм, выявленных при ультразвуковом исследовании; количество базальных антральных фолликулов более 20, выявленных при ультразвуковом исследовании; фиброидные опухоли матки, при которых наступление и дальнейшее вынашивание беременности затруднено; пороки развития репродуктивных органов, при которых беременность невозможна; беременность; период лактации (грудного вскармливания); повышенная чувствительность к корифоллитропину альфа.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период лактации (грудного вскармливания).
После контролируемой стимуляции яичников гонадотропинами в клинической практике тератогенного эффекта не выявлено. Клинические данные не позволяют исключить тератогенный эффект корифоллитропина альфа, в случае его непреднамеренного введения при беременности.
В доклинических исследованиях не наблюдалось тератогенного эффекта корифоллитропина альфа.
Особые указания
Перед началом лечения, пара должна быть обследована должным образом, поставлен диагноз бесплодия и учтены возможные противопоказания. В частности, следует обследовать пациентку на наличие гипотиреоза, надпочечниковой недостаточности, гиперпролактинемии и опухолей гипофиза или гипоталамуса, в случае выявления назначить соответствующее лечение.
Не рекомендуется применять корифоллитропин альфа в сочетании с агонистом ГнРГ, а также у женщин с синдромом поликистоза яичников.
Корифоллитропин альфа предназначен только для однократного п/к введения. Во время того же цикла не следует назначать дополнительные инъекции данного лекарственного средства.
В течение первых 7 дней после введения корифоллитропина альфа не следует вводить рФСГ.
У пациентов с почечной недостаточностью возможно нарушение выведения корифоллитропина альфа, поэтому применение у таких пациентов не рекомендуется.
Рекомендуется тщательный контроль возможной гиперстимуляции яичников в первом цикле стимуляции у пациенток с неуточненными факторами риска СГЯ.
При применении всех препаратов гонадотропинов наблюдались случаи наступления многоплодной беременности и рождения близнецов. Перед началом лечения следует информировать женщину и ее партнера о возможном риске для матери (осложнения беременности и родов) и новорожденных (низкая масса тела). При лечении методами вспомогательных репродуктивных технологий риск многоплодной беременности, в основном, зависит от числа перенесенных эмбрионов.
У женщин с бесплодием, которым предложено лечение методами вспомогательных репродуктивных технологий, особенно, экстракорпоральное оплодотворение (ЭКО), часто встречается патология маточных труб, что может привести к повышению риска эктопической беременности. В связи с этим, на ранних сроках беременности следует провести ультразвуковое исследование, чтобы подтвердить наличие маточной или внематочной беременности.
Частота врожденных пороков развития после вспомогательных репродуктивных технологий несколько выше, чем после естественного оплодотворения. Это связывают с индивидуальными особенностями родителей (например, возраст женщины, показатели спермы) и повышенной частотой многоплодной беременности.
У женщин с факторами риска тромбоэмболических осложнений (тромбоэмболия в анамнезе, отягощенный семейный анамнез, ожирение (индекс массы тела >30 кг/м 2 ) или тромбофилия) лечение гонадотропинами может способствовать дальнейшему увеличению этого риска. В таких случаях необходимо оценить риск и пользу применения гонадотропинов. Следует отметить, что сама беременность повышает риск развития тромбоза.
Влияние на способность к управлению транспортными средствами и механизмами
Корфоллитропин альфа может вызвать головокружение. Пациенток следует предупредить, что при головокружении не следует заниматься вождением транспортных средств или пользоваться сложной техникой.
Фоллитропин-бета в лечении бесплодия методами вспомогательной репродукции.
| Препараты ФСГ в лечении бесплодия |
Все схемы лечения бесплодия с применением вспомогательных репродуктивных технологий (ВРТ) включают в себя применение лекарственных препаратов, содержащих ФСГ. Стойкий подъем уровня ФСГ в сыворотке крови при введении этих препаратов, изменяя процесс селекции доминантных фолликулов, стимулирует развитие большего их числа. В результате, преовуляторного состояния достигают несколько фолликулов, что дает возможность получить большее число зрелых ооцитов. Это создает условия для отбора эмбрионов высокого качества для последующего переноса, что повышает вероятность наступления беременности на каждый цикл стимуляции.
В настоящее время считается, что индукция суперовуляции гонадотропными препаратами представляет собой наиболее эффективный способ получения достаточного количества зрелых ооцитов для оплодотворения in vitro. Предложены различные схемы использования как препаратов, содержащих смесь ФСГ и ЛГ, так и только ФСГ. В проведенном недавно мета-анализе результатов ВРТ с применением мочевых гонадотропинов показано, что при использовании препаратов, содержащих только ФСГ, достигается большая частота наступления беременности, чем при использовании комбинации ФСГ и ЛГ [1].
Фоллитропин-бета (Пурегон) – рекомбинантный ФСГ
Дальнейшие перспективы в лечении бесплодия с помощью ВРТ открыла генно-инженерная (рекомбинантная) технология. Получение человеческого ФСГ in vitro стало возможным после длительных исследований, в результате которых были идентифицированы гены субъединиц ФСГ человека, осуществлено их выделение, перенос и внедрение в ядра клеток млекопитающих (яичника китайского хомячка), с последующим отбором тех из них, которые устойчиво синтезируют молекулы ФСГ с наиболее высокой биологической активностью.
Производство гонадотропинов с использованием культуры (клона) клеток с рекомбинантным наследственным материалом имеет ряд преимуществ перед получением препаратов ФСГ из мочи. Эта технология не требует сбора мочи; рекомбинантный продукт не содержит вирусных, белковых, углеводных и стероидных примесей. Очень важно, что в препарате отсутствует даже следовая ЛГ-активность.
Важным преимуществом генно-инженерной технологии является высокая биохимическая однородность различных серий препарата. Так, по сравнению с мочевыми гонадотропинами, изогормональный профиль фоллитропина-бета (Пурегона) – рекомбинантного ФСГ – состоит из наиболее активных фракций гормона, что позволило разработать специальные лекарственные формы (по 50, 100 и 150 МЕ), позволяющие снизить лекарственную нагрузку при высокой эффективности лечения. Однако наиболее достоверным критерием большей эффективности препарата являются результаты клинических исследований.
Клинический опыт применения фоллитропина-бета (Пурегона): результаты многоцентровых «слепых», рандомизированных исследований
Представленные ниже результаты отражают клинический опыт использования фоллитропина-бета – рекомбинантного ФСГ, получившего название – Пурегон. Название отражает высокую чистоту препарата (от английского pure – чистый). В анализ данных не включили результаты испытаний другого рекомбинантного ФСГ – фоллитропина-альфа (Гонал-Ф; «Арес-Сероно», Швейцария). Это объясняется тем, что различия, затрагивающие генетическое происхождение ФСГ-продуцирующих клеток, условия выращивания клеточных культур, методики очистки и технологии изготовления препаратов могут привести к существенным расхождениям в результатах терапии альфа- и бета-фоллитропинами [6]. В то же время, наиболее обширные клинические исследования выполнены с фоллитропином-бета (Пурегоном).
Появлению Пурегона на лекарственном рынке Европейского Сообщества предшествовало предрегистрационное проспективное исследование в 18 центрах ЭКО 11 европейских стран. Оно включало 981 пару с бесплодием [4]. Необходимо отметить, что это исследование было рандомизированным (случайным), т.е. исключался фактор подбора более легких или тяжелых пациенток в группу Пурегона или мочевого ФСГ, и слепым, т.е. исключался субъективный фактор при оценке результатов лечения. Это самое большое из когда-либо проводившихся проспективных рандомизированных исследований в области лечения бесплодия. Таким образом, результаты, полученные в этом исследовании, имели высокую степень объективности и достоверности.
В последующем, после регистрации Пурегона в странах Европейского Сообщества и США, были выполнены дополнительные клинические исследования с этим препаратом. В настоящее время опубликованные результаты применения Пурегона в программах ВРТ включают более 1000 супружеских пар в 25 центрах ЭКО 13 стран [2, 4, 5]. Для оценки клинической эффективности и безопасности Пурегона особого внимания заслуживают совокупные данные многоцентровых проспективных рандомизированных слепых исследований, обобщенные путем выполнения процедуры мета-анализа [3].
В анализируемых исследованиях участвовали соматически здоровые женщины с бесплодием в возрасте от 18 до 39 лет с нормальными регулярными менструальными циклами. В исследования не были включены пары с мужским фактором бесплодия. Бесплодие в основном (более, чем у половины пациенток) было вызвано непроходимостью маточных труб воспалительного характера или их отсутствием после тубэктомии. В остальных случаях бесплодие было обусловлено наружным генитальным эндометриозом или его сочетанием с трубной патологией. Средний возраст пациенток составил 31,6 лет. Число пациентов, охваченных исследованием, варьировало в разных центрах от 3 до 146 и в среднем составляло 46,4.
В целях рандомизации использовали компьютерную программу, с помощью которой случайным образом пациенток распределили по группам и присвоили номер, соответствующий номеру определенной упаковки с лекарственным средством.
В двух исследованиях индукция суперовуляции либо Пурегоном, либо ФСГ из мочи (Метродин, «Арес-Сероно», Швейцария) проводилась на фоне назначения агонистов гонадолиберина. В качестве агониста гонадолиберина использовали трипторелин для подкожного введения (Декапептил, «Ипсен», Франция) и бусерелин в виде интраназального спрея (Супрекур, «Хехст», Германия). В третьем исследовании Пурегон сравнивали с чМГ (Хумегон, «Органон», Нидерланды) в циклах без применения агониста гонадолиберина. Пурегон назначали 697 пациентам, тогда как 463 женщины получили Метродин или Хумегон. Во всех случаях гонадотропины вводили внутримышечно. После процедуры рандомизации клинические группы, получавшие разные препараты, существенно не отличались между собой по причинам бесплодия, возрасту, а в последующем и по числу эмбрионов на один перенос.
Согласно протоколу исследования, в течение первых четырех дней стимуляции гонадотропинами, пациентки ежесуточно получали одинаковые стартовые дозы препаратов, после чего их назначали индивидуально с учетом реакции яичников. При наличии, как минимум, трех преовуляторных фолликулов, однократно вводили 10 000 МЕ чХГ (Прегнил, «Органон», Нидерланды). Извлечение ооцитов, процедуру ЭКО и поддержку лютеиновой фазы выполняли согласно установленным в каждом центре стандартам. В матку переносили не более трех эмбрионов. В большинстве центров избыток эмбрионов подвергали криоконсервации.
Результаты исследований показали, что назначение Пурегона при лечении бесплодия с помощью ВРТ сопровождается получением существенно большего, чем при применении мочевых гонадотропинов числа зрелых ооцитов (рис. 1). По-видимому, этим объясняется и тот факт, что применение Пурегона приводит к получению существенно большего числа эмбрионов высокого качества (рис. 2). Как известно, высокое качество эмбрионов существенно влияет на успех их имплантации и развитие беременности [7]. Причины получения большего числа ооцитов и эмбрионов высокого качества при использовании Пурегона остаются не совсем ясными. По-видимому, значение имеют такие особенности фоллитропина-бета, отличающие его от мочевых гонадотропинов, как относительно щелочной изогормональный профиль, высокая удельная активность (»10 000 МЕ/мг белка!), очень высокая чистота самого препарата (больше 99% ФСГ), исключающая наличие в нем цитокинов, способных негативно влиять на созревание ооцитов.
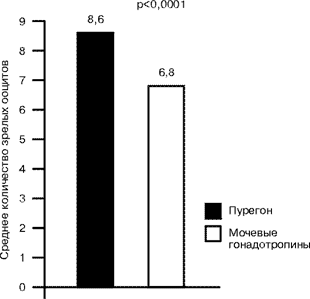 |
Рис. 1. Среднее количество зрелых ооцитов (результаты лечения 981 пары с бесплодием в 18 центрах ЭКО 11 стран: проспективное рандомизированное «слепое» исследование).
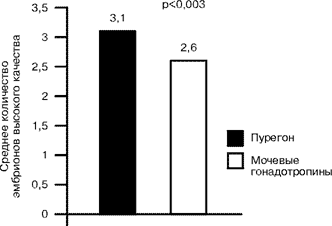 |
Рис. 2. Среднее количество эмбрионов высокого качества (результаты лечения 981 пары с бесплодием в 18 центрах ЭКО 11 стран: проспективное рандомизированное «слепое» исследование).
Важно отметить, что более успешные результаты индукции суперовуляции Пурегоном сопровождаются достоверным снижением расхода ФСГ и, следовательно, лекарственной нагрузки (рис. 3). Это объясняется более высокой биологической активностью Пурегона как за счет содержания более активных изогормональных фракций, так и специальной фармацевтической формы – лиосфер, обеспечивающих более высокую биодоступность ФСГ.
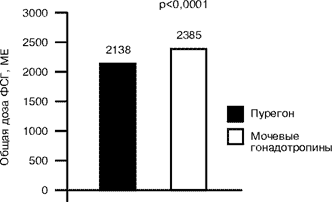 |
Рис. 3. Количество ФСГ, затраченного на цикл индукции суперовуляции (результаты лечения 981 пары с бесплодием в 18 центрах ЭКО 11 стран: проспективное рандомизированное «слепое» исследование).
Одним из наиболее важных критериев эффективности лечения бесплодия ВРТ является частота прогрессирующей беременности, которая фиксируется при ультразвуковом исследовании после 12 нед от момента переноса эмбрионов. Этот показатель особенно важен, поскольку известно, что после применения программ ВРТ значительная часть беременностей прерывается в первом ее триместре. Данные соответствующих исследований показывают, что назначение Пурегона позволяет достичь большего числа прогрессирующих беременностей по сравнению с мочевыми гонадотропинами (рис. 4). Этот факт может объясняться более высоким качеством ооцитов и эмбрионов при использовании этого препарата, о чем уже было сказано выше. Попытки обосновать различия в частоте прогрессирующей беременности особенностями развития эндометрия при индукции суперовуляции разными гонадотропинами кажутся нам не убедительными, поскольку частота наступления беременности в нестимулированных циклах при переносе замороженных эмбрионов выше после использования Пурегона, чем при применении ФСГ, полученного из мочи.
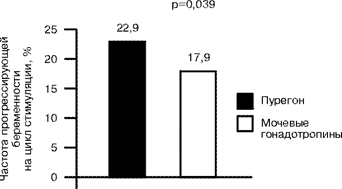 |
Рис. 4. Частота прогрессирующей беременности после переноса незамороженных эмбрионов в расчете на цикл индукции суперовуляции (результаты лечения 1160 пар с бесплодием в 25 центрах ЭКО 13 стран: три проспективных рандомизированных «слепых» исследования).
Наиболее выраженные различия в частоте наступления беременности после применения Пурегона и мочевых гонадотропинов были отмечены в протоколах индукции суперовуляции при использовании агонистов гонадолиберина и, прежде всего, трипторелина (Декапептила). Так, на фоне десенситизации гипофиза этим агонистом при назначении Пурегона частота прогрессирующей беременности составила 30,3% на цикл стимуляции, а при назначении Метродина только – 17,4% [2]. В протоколах с интраназальным введением бусерелина (Супрекур) частота прогрессирующей беременности составила 22,2% – в группе Пурегона и 18,2% – в группе Метродина [4]. При сравнении Пурегона с Хумегоном в протоколах без использования агонистов гонадолиберина этот показатель составил 23,6% и 14,7% соответственно [5]. Таким образом, сводные результаты частоты прогрессирующей беременности показывают существенное преимущество Пурегона перед мочевыми гонадотропинами (рис. 4).
В настоящее время большинство центров ЭКО внедряет программы криоконсервации эмбрионов, которые способствуют увеличению частоты наступления беременности на цикл стимуляции суперовуляции и, тем самым, снижают стоимость рождения одного ребенка при применении ВРТ. В этой связи особый интерес вызывают данные о результатах лечения бесплодия с помощью ВРТ с учетом переноса замороженных/оттаянных эмбрионов при использовании разных гонадотропинов.
Согласно сводным данным указанных выше многоцентровых исследований, частота прогрессирующей беременности с включением случаев переноса замороженных/оттаянных эмбрионов составила 26,3% в группе, получавшей Пурегон, и 19,9% в группе, получавшей мочевые гонадотропины (р = 0,011). Таким образом, при применении Пурегона в циклах ЭКО с последующим применением программы криоконсервации частота прогрессирующей (после 12 нед) беременности на один цикл индукции суперовуляции была почти на треть выше, чем при использовании мочевых гонадотропинов. Эти данные могут быть объяснены более высоким качеством эмбрионов после лечения Пурегоном, в том числе достаточным числом эмбрионов высокого качества, пригодных для переноса в полость матки [4]. В свою очередь, морфологическая оценка эмбриона хорошо коррелирует с вероятностью успешной имплантации и, следовательно, последующей беременности [7]. Это, в конечном счете, приводит к большему числу беременностей после их переноса в матку в нестимулированных циклах. Вследствие этого повышается частота наступления беременности в каждом из стимулированных циклов, снижаются затраты на те циклы ЭКО, в которых используются замороженные эмбрионы.
При анализе осложнений лечения бесплодия с помощью ВРТ с использованием разных гонадотропинов не обнаружено существенного увеличения частоты синдрома гиперстимуляции, внематочной и многоплодной беременности. Это объясняется тщательным мониторингом индукции суперовуляции, а также ограничением числа эмбрионов на перенос.
Лекарственный препарат рФСГ – Пурегон (фоллитропин-бета, «Органон», Нидерланды) в полной мере обладает всеми преимуществами продукта, полученного генно-инженерной технологией. Он имеет высокую биохимическую чистоту и высокую удельную биологическую активность ФСГ.
Результаты различных исследований показывают, что применение фоллитропина-бета (Пурегона) в ВРТ, по сравнению с мочевыми гонадотропинами, сопровождается существенно большей частотой наступления беременности.
Полученные к настоящему времени данные имеют высокую степень объективности и достоверности, благодаря исследованию Пурегона в строгих по дизайну многоцентровых, рандомизированных, «слепых» исследованиях, а также большому числу наблюдений.
Б.В. Леонов, Е.Я. Финогенова, А.Ю. Козлова
Научный центр акушерства, гинекологии и перинатологии РАМН