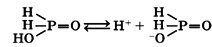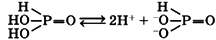Фосфорная и ортофосфорная кислота чем отличаются
Ортофосфорная кислота (Е338)

Способы получения добавки Е338 и химические свойства
Ортофосфорная кислота представляет собой неорганическое соединение и относится к слабым кислотам. Она имеет вид бесцветного порошка, состоящего из мелких гранул, обладает свойствами гигроскопичности.
Температура плавления – от 42 градусов Цельсия, при этом кристаллы превращаются в бесцветную, однородную и вязкую жидкость. Вещество имеет характерный кислый вкус, а запах у него отсутствует. В воде и органических растворителях обладает хорошей растворимостью. Распространённый способ использования в промышленности – в виде 85-процентного водного раствора. В процессе реакции с сильными кислотами образует соли, а с нитратом серебра выделяет жёлтый осадок.
Существует несколько способов получения добавки Е338, поэтому различают непосредственно кислоту ортофосфатную и кислоту ортофосфорную термическую. В первом случае вещество добывают путём обработки фосфатов серной, азотной или соляной кислотой.
Полученное вещество подвергается очистке. Этот метод является более экономически выгодным, так как подразумевает меньшие затраты труда, времени и электроэнергии. Получение термической разновидности добавки подразумевает более чистое вещество на выходе. Этот процесс включает в себя 4 этапа. Сначала элементный фосфор подвергают сжиганию, пока он не перейдёт в фосфорный ангидрид.
Результат термической реакции абсорбируют с участием кислоты, конденсируют и охлаждают. Ещё одна технология получения – гидролиз пентахлорида фосфора.
Добавка, в основном, используется как антиоксидант, замедляющий окисление элементов. В пищевой промышленности ценится как компонент, способный продлить срок хранения пищи, и призванный добавить кислинку вкусу продукта.
Требования к упаковке и правила обращения с веществом

Хранить и транспортировать добавку разрешено в такой упаковке:
Сами емкости для удобства помещают в полиэтиленовые барабаны или дощатые ящики, внутри которых должен быть мягкий наполнитель во избежание повреждения упаковки.
Попадание вещества на кожу или слизистые, в глаза или в дыхательные пути может вызывать ожоги, тошноту, рвоту, головокружение и нарушение целостности тканей. В таком случае необходимо незамедлительно обратиться за врачебной помощью.
Кислота является опасной в обращении, поэтому работать с ней можно только вдали от открытых источников огня, в хорошо вентилируемом помещении.
Обязательно наличие защитной спецодежды: перчаток, респиратора, очков, ботинок и костюма для работы с опасными веществами.
Применение кислоты в промышленности
На сегодняшний день существует как минимум семь отраслей производства, в которых используется ортофосфатная или ортофосфорная кислота.
Как антиоксидант, разрыхлитель и регулятор кислотности, кислота повсеместно применяется в приготовлении таких пищевых продуктов:
Добавка придаёт пище кислинку или слегка горьковатое послевкусие.

Как элемент гидрожидкостей, кислота применяется в авиационной промышленности.
Отрасль сельского хозяйства использует добавку как составляющую минеральных удобрений.
Кроме того, Е338 – элемент производства лакокрасочных изделий, стекла и керамики, моющей продукции, активированного угля, невоспламеняющихся красок.
Медицинская сфера, особенно стоматология, ортофосфорную кислоту применяет в своих целях: для борьбы с мочекаменной болезнью, как реактив для обработки внутренней поверхностей зубных коронок перед их установкой.
Косметологическая отрасль пользуется стабилизирующим свойством кислоты: компонент упрочняет химические связи между составляющими элементами продуктов.
В домашних условиях вещество популярно как средство для удаления ржавчины с металлов.
Влияние на здоровье человека
Пищевая добавка Е338 не является полностью безопасной и безвредной. Тем не менее применение её разрешено в странах Европейского союза, в России, Украине и США. Согласно международным нормам, содержание вещества в пищевой продукции не может превышать 9 г на 1 килограмм готового продукта.
Постоянное употребление кислоты плохо сказывается на костной ткани организма: так как она способствует повышению уровня кислотности в организме, последний пытается его нейтрализовать за счёт кальция.
Макроэлемент он “забирает” из костей и зубов, поэтому может развиваться остеопороз и кариес.
Среди других негативных последствий употребления продуктов с этим компонентом в составе медики отмечают появление заболеваний органов пищеварительного тракта, в том числе, гастрита и язвы желудка и кишечника, тошноту, диарею и рвоту.
Никакой информации по поводу возможной пользы добавки у учёных на сегодняшний день нет. Также не подтверждены данные о возможной связи между употреблением кислоты в пище и появлением онкологических заболеваний, бесплодия или генных мутаций.
Ортофосфорная кислота – синтетический антиоксидант и стабилизатор, регулятор кислотности и компонент многих популярных продуктов и напитков. Несмотря на то, что продукту присвоен средний уровень опасности, он является ингредиентом газировок “Coca-cola” и “Pepsi”, которые очень любят пить и взрослые, и дети. В последнее время учёные всё чаще обращают внимание мировой общественности на тот факт, что пищевая добавка Е338 – одна из распространённых причин появления кариеса, нарушений в работе желудочно-кишечного тракта, вымывания из организма кальция. Пока единственное, чего им удалось достичь – установление максимально разрешённого количества вещества в качестве добавки к пищевым продуктам. И сегодня продолжается изучение свойств и результатов употребления добавки в пищу, а также поиск аналогичной по цене и простоте получения альтернативы. Пока она не найдена, и в составе пищи по-прежнему можно встретить ингредиент под кодом “Е338”. Потребителю остаётся только внимательно изучать этикетки и решать для себя, стоит ли покупать продукты с этим регулятором кислотности.
Фосфорная кислота: получение и свойства
Строение молекулы и физические свойства
Фосфор в степени окисления +5 образует несколько кислот: орто-фосфорную H3PO4, мета-фосфорную HPO3, пиро-фосфорную H4P2O7.
Фосфорная кислота H3PO4 – это кислота средней силы, трехосновная, прочная и нелетучая. При обычных условиях фосфорная кислота – твердое вещество, хорошо растворимое в воде и гигроскопичное.
Валентность фосфора в фосфорной кислоте равна V.
При температуре выше +213 °C орто-фосфорная кислота переходит в пирофосфорную H4P2O7.
При взаимодействии высшего оксида фосфора с водой на холоде образуется метафосфорная кислота HPO3, представляющая собой прозрачную стекловидную массу.
Способы получения
Наибольшее практическое значение из фосфорных кислот имеет ортофосфорная кислота.
1. Получить орто-фосфорную кислоту можно взаимодействием оксида фосфора (V) с водой:
Промышленный способ получения фосфорной кислоты обработка фосфорита концентрированной серной кислотой:
3. Фосфорную кислоту также можно получить жестким окислением соединений фосфора в водном растворе в присутствии кислот.
Химические свойства
1. Фосфорная кислота частично и ступенчато диссоциирует в водном растворе.
HPO4 2– ⇄ H + + PO4 3–
2. Фосфорная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Еще пример : при взаимодействии фосфорной кислоты с гидроксидом калия образуются фосфаты, гидрофосфаты или дигидрофосфаты:
3. Фосфорная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов и др.). Также фосфорная кислота вступает в обменные реакции с солями.
4. При нагревании H3PO4 до 200°С происходит отщепление от нее молекулы воды с образованием пирофосфорной кислоты H2P2O7:
5. Фосфорная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Фосфорная кислота взаимодействует также с аммиаком с образованием солей аммония:
7. Качественная реакция на фосфат-ионы и фосфорную кислоту — взаимодействие с нитратом серебра. При этом образуется ярко-желтый осадок фосфата серебра:
Видеоопыт взаимодействия фосфата натрия и нитрата серебра в растворе (качественная реакция на фосфат-ион) можно посмотреть здесь.
Фосфорные кислоты
Разновидности фосфорных кислот:
Метафосфорная кислота
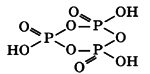
Триметафосфорная кислота (HPO3)3 построена из трех остатков метафосфорной кислоты, которые составляют замкнутый цикл:
Соответственно, тетраметафосфорная кислота (HPO3)4 построена из 4 остатков метафосфорной кислоты, и получается воздействием фосфорного ангидрида P2O5(V) на воду при низких температурах:
P4O10+2H2O = (HPO3)4
Ортофосфорная кислота H3PO4
H3PO4 диссоциирует в три ступени:
Несмотря на тот факт, что фосфорная к-та обладает всеми свойствами общих кислот, она намного слабее, например, азотной или серной кислоты, и не обладает, в отличие от сильных кислот, сколь-нибудь значительными окислительными свойствами, что объясняется устойчивой степенью окисления фосфора (+5).
В промышленности ортофосфорную кислоту получают воздействием серной кислоты на фосфориты и апатиты (экстракционный метод):
Ca3(PO4)2+3H2SO4 = 2H3PO4+3CaSO4
Более чистая кислота получается сжиганием фосфора с последующим растворением в воде образующегося оксида P2O5.
Фосфорную кислоту применяют в производстве:
Полифосфорная кислота
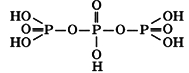
Эти кислоты состоят из открытых цепей, в состав которых входят 2..10 атомов фосфора. На рисунке ниже изображена структура молекулы трифосфорной кислоты H5P3O10:
Фосфорноватистая кислота H3PO2
Бесцветные кристаллы, хорошо растворимые в воде.
Водный раствор фосфорноватистой кислоты является сильной одноосновной кислотой:
Фосфорноватистая кислота и ее соли (гипофосфиты) являются сильными восстановителями:
H3PO2+2I2+2H2O = H3PO4+4HI
Фосфористая кислота H3PO3
Твердое бесцветное вещество, обладающее гигроскопическими свойствами, хорошо растворимо в воде.
Водный раствор фосфористой кислоты является двухосновной кислотой средней силы:
Соли фосфористой кислоты, называемые фосфитами, плохо растворимы в воде за исключением фосфитов щелочных металлов.
Фосфористая кислота и ее соли являются сильными восстановителями, восстанавливая неактивные металлы из их соединений:
2AgNO3+H3PO3+H2O = H3PO4+2Ag↓+2HNO3
Получение фосфористой кислоты:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Фосфорная кислота [H3PO4]: Структура | Свойства | Применение
В чистом виде фосфорная кислота представляет собой бесцветное твердое вещество. В менее концентрированном виде это вязкая жидкость без запаха с плотностью 1,885 г/мл. Обычно она нелетучая и нетоксична, но 85-процентный раствор по-прежнему может повредить глаза и вызвать сильное раздражение кожи.
Давайте копнем глубже и выясним, как образуется фосфорная кислота, как она выглядит на молекулярном уровне, каковы ее физические и химические свойства и где она используется.
Профиль фосфорной кислоты
Молярная масса: 97,994 г/моль
Внешний вид: густая бесцветная жидкость.
Точка кипения: 212 °C
Точка плавления: 42,35 °C (кристаллического твердого вещества)
Динамическая вязкость: от 2,4 до 9,4 сантипуаз (85% водный раствор).
Плотность: 1,83 г / см 3 (твердое вещество); 1,68 г / см 3 (85% водный раствор при 25 °C)
Структура
Соединение H3PO4 имеет в общей сложности 32 валентных электрона. Поскольку фосфор является наименее электроотрицательным, он помещается в центре. Атомы водорода присоединяются к внешней стороне атомов кислорода, образуя он-Группы.
В этой структуре каждый атом имеет полную внешнюю оболочку: атомы фосфора и кислорода имеют восемь валентных электронов, а атомы водорода имеют вокруг себя два валентных электрона.
В структуре все еще есть 32 валентных электрона, и каждый атом имеет формальный заряд, равный нулю. Таким образом, это наиболее вероятная или вероятная структура Льюиса для H3PO4.
Соединение содержит 3 одинарные связи ОН, 3 одинарные связи PO и 1 двойную связь P = O. Каждая одинарная связь является сигма-связью, а двойная связь состоит из сигма-связи и пи-связи.
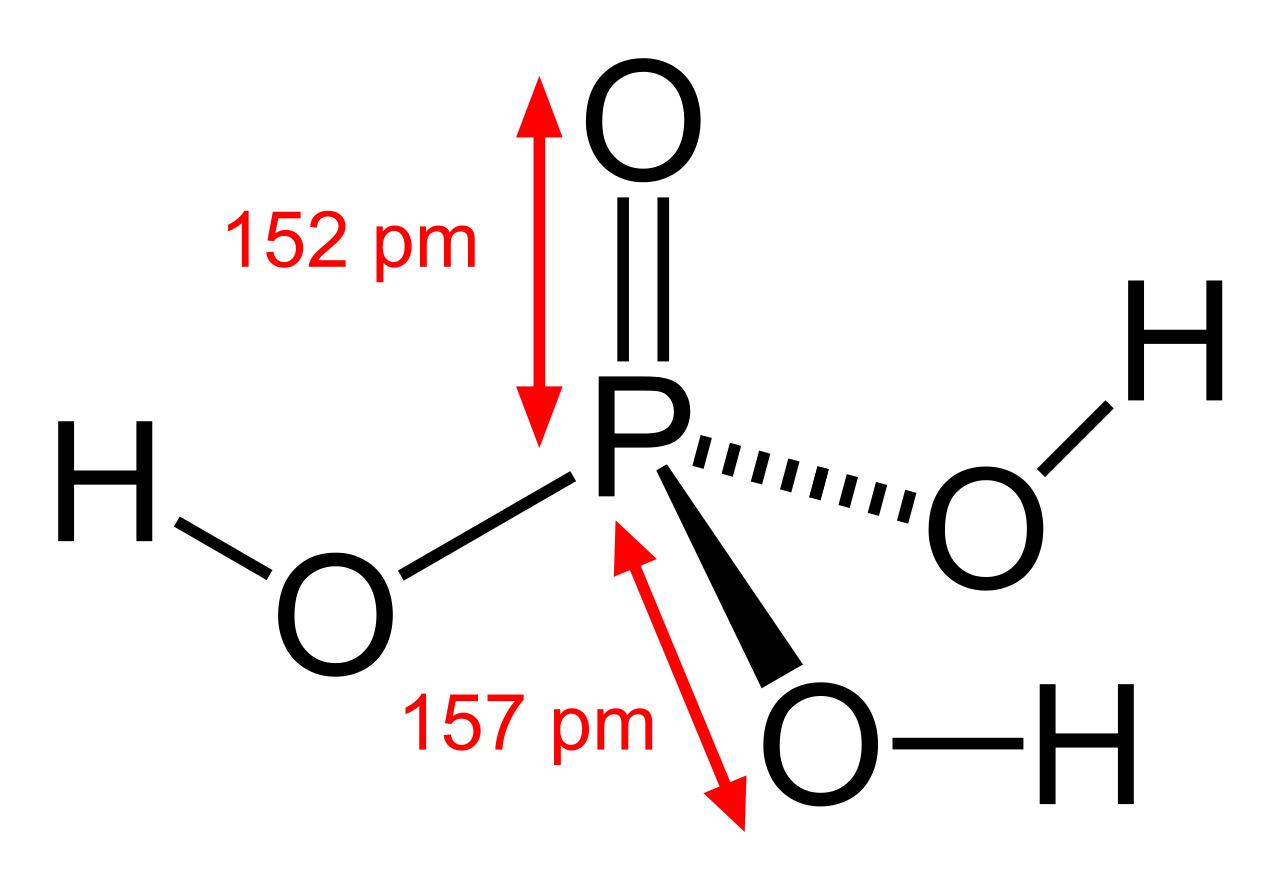
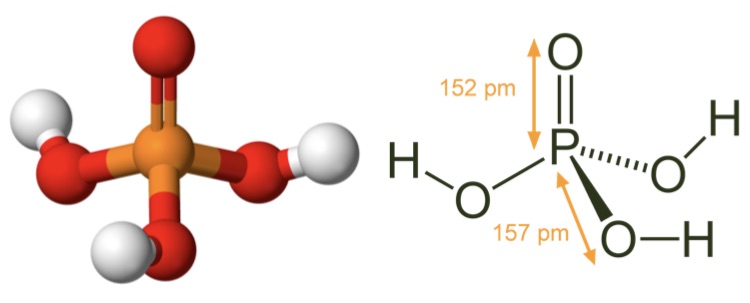
Фосфорная кислота: шарообразная модель и размеры структурной формулы
Молекулярная геометрия PO (OH)3 является тетраэдрической, а кристаллическая структура-моноклинной. А поскольку распределение зарядов на центральных атомах асимметрично, то молекула считается полярной.
Последние достижения в области нанотехнологий, включая методы поглощения рентгеновских лучей вблизи краев и методы рассеяния рентгеновских лучей под большим углом, позволили ученым точно определить структуру фосфорной кислоты. Расстояние связи P=O в структуре близко к 152 пикометрам, и расстояния P=O-O были уточнены до 309 пикометров, с углом связи близким к тетраэдрическому.
Как она производится?
Фосфорная кислота может быть синтезирована либо мокрым способом, либо термическим способом.
В последнем в качестве сырья используются воздух, вода и элементарный фосфор. Он включает в себя три важных этапа: сгорание, увлажнение и запотевание. Вот как это происходит:
Во-первых, жидкий элементарный фосфор сжигается в камере сгорания при высоких температурах в диапазоне от 1650 до 2760 °C. Эта реакция окисления происходит в окружающем воздухе и производит пятиокись фосфора.
Затем продукт гидратируют водой с образованием сильной фосфорной кислоты (в жидком состоянии).
На последнем этапе для удаления фосфорно-кислотного тумана из потока дымовых газов используются высоконапорные каплеуловители.
Концентрация фосфорной кислоты, синтезированной в этом процессе, обычно составляет от 75 до 85 процентов. Такие уровни концентрации необходимы для производства высококачественной химической продукции. Несколько эффективных установок извлекают чрезвычайно концентрированную фосфорную кислоту (до 99,9%), используя тот же тепловой процесс.
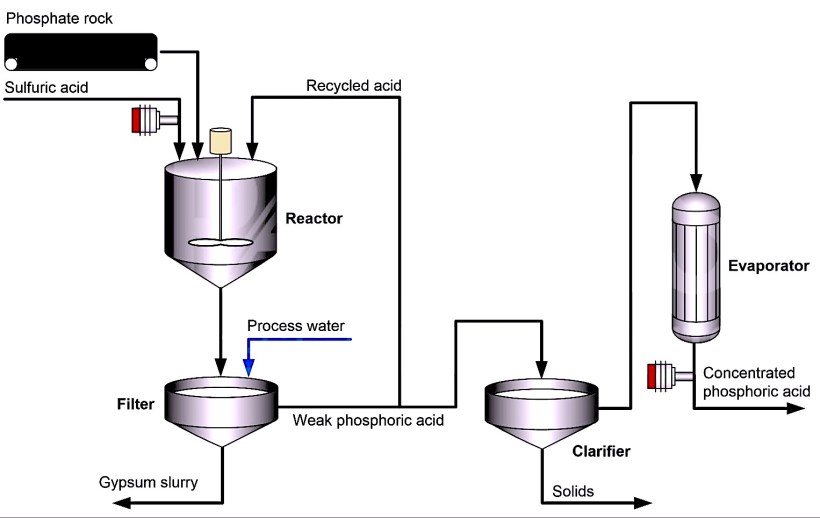
Однако почти 80% фосфорной кислоты производится мокрым способом. В этом методе серная кислота обрабатывается природным фосфатсодержащим минералом, таким как гидроксиапатит.
Минерал высушивают, крошат, а затем подают в реактор вместе с серной кислотой. В результате реакции сульфат сливается с кальцием (из минерала), образуя сульфат кальция (гипс).
Затем добавляется обработанная вода, и гипс вместе с другими нерастворимыми примесями удаляется через фильтр. Фосфорная кислота, полученная этим мокрым способом, содержит 25-30% пятиокиси фосфора.
Обычно эта кислота дополнительно концентрируется, чтобы соответствовать требованиям, предъявляемым к производству удобрений. В большинстве случаев фосфорная кислота концентрируется до 40-55% пятиокиси фосфора с помощью двух / трех вакуумных испарителей.
Свойства
Чистая фосфорная кислота в лаборатории выглядит как плотное, бесцветное, бесформенное кристаллическое твердое вещество, которое плавится при температуре 42,35 °C. Ее физические свойства зависят от чистоты, концентрации кислоты, а также от температуры, при которой вы ее видите.
Фосфорная кислота менее агрессивна и менее опасна по сравнению с азотной и серной кислотами. Это негорючее вещество как в жидкой, так и в твердой форме.
Когда кислота подвергается воздействию тепла, а затем охлаждается до комнатной температуры, она образует прозрачное, хрупкое стекло. После такого воздействия тепла состав кислоты остается прежним.
Обычно фосфорная кислота выпускается в виде бесцветного сиропа с концентрацией в воде 85 процентов и плотностью 1,885 граммов на миллилитр.
В водном растворе фосфорная кислота действует как трипротовая кислота, имеющая три ионизируемых атома водорода. Соединение может потерять эти атомы в виде протонов (ионов H + ).
Кислота растворима как в воде, так и в этаноле. Однако большинство ее солей не растворимы в воде, если нет сильной минеральной кислоты.
Области применения
Фосфорная кислота имеет несколько важных применений. Ее соли, такие как фосфаты аммония и кальция, широко используются в качестве удобрений. Кислота используется для производства электролитов, средств для удаления ржавчины, модификаторов рН, травителей, бытовых чистящих средств и дезинфицирующих средств.
Поскольку это вещество нетоксично и имеет умеренно кислую природу, оно также используется в напитках, пищевых ароматизаторах, косметике, средствах для ухода за зубами и кожей. Давайте подробнее рассмотрим, чем полезна фосфорная кислота.
В менее концентрированной форме она используется для производства различных видов безопасных фосфорных удобрений, которые помогают растениям расти. Фактически, почти 90% синтезированной фосфорной кислоты используется в качестве удобрений.
Многие безалкогольные напитки, в том числе Coca-Cola, содержат фосфорную кислоту. Это придает напитку слегка кисловатый вкус. Несмотря на то, что его концентрация достаточно низкая, экстремальный прием таких напитков может вызвать эрозию зубов и даже привести к образованию почечных камней.
Фосфорная кислота в качестве электролита имеет полезные характеристики, такие как хорошая ионная проводимость, низкая летучесть, стабильность при относительно высоких температурах и устойчивость к диоксиду углерода и монооксиду углерода.
Поскольку чистая фосфорная кислота обладает высокой протонной проводимостью и превосходной термостабильностью, полибензимидазол (PBI), допированный фосфорной кислотой, является наиболее многообещающим среди мембран на основе PBI, которые могут обеспечить хорошую производительность топливных элементов даже при низком уровне увлажнения и температуре 200 °С.
Специфическое применение фосфорной кислоты:
Глобальный рынок
Многие развивающиеся страны начали сосредотачиваться на увеличении добычи фосфатов и производства фосфатов. Правительства некоторых стран уже сотрудничали с различными поставщиками по всему миру для создания заводов по добыче минералов для производства фосфорной кислоты.
В 2019 году объем мирового рынка фосфорной кислоты оценивался в 45,85 миллиарда долларов. Ожидается, что к 2027 году он достигнет более 61 миллиарда долларов, а совокупный годовой темп роста составит 3,7%.
Рынок подразделяется на Азиатско-Тихоокеанский регион, Европу, Северную Америку, Латинскую Америку, Ближний Восток и Африку. Ожидается, что в ближайшем будущем Азиатско-Тихоокеанский регион будет доминировать на мировом рынке. Рост рынка фосфорной кислоты в этих регионах будет дополнительно подпитываться развитым сельскохозяйственным сектором Индии и Китая.