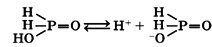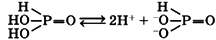Фосфорная кислота и ортофосфорная кислота в чем разница
Фосфорная кислота: получение и свойства
Строение молекулы и физические свойства
Фосфор в степени окисления +5 образует несколько кислот: орто-фосфорную H3PO4, мета-фосфорную HPO3, пиро-фосфорную H4P2O7.
Фосфорная кислота H3PO4 – это кислота средней силы, трехосновная, прочная и нелетучая. При обычных условиях фосфорная кислота – твердое вещество, хорошо растворимое в воде и гигроскопичное.
Валентность фосфора в фосфорной кислоте равна V.
При температуре выше +213 °C орто-фосфорная кислота переходит в пирофосфорную H4P2O7.
При взаимодействии высшего оксида фосфора с водой на холоде образуется метафосфорная кислота HPO3, представляющая собой прозрачную стекловидную массу.
Способы получения
Наибольшее практическое значение из фосфорных кислот имеет ортофосфорная кислота.
1. Получить орто-фосфорную кислоту можно взаимодействием оксида фосфора (V) с водой:
Промышленный способ получения фосфорной кислоты обработка фосфорита концентрированной серной кислотой:
3. Фосфорную кислоту также можно получить жестким окислением соединений фосфора в водном растворе в присутствии кислот.
Химические свойства
1. Фосфорная кислота частично и ступенчато диссоциирует в водном растворе.
HPO4 2– ⇄ H + + PO4 3–
2. Фосфорная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Еще пример : при взаимодействии фосфорной кислоты с гидроксидом калия образуются фосфаты, гидрофосфаты или дигидрофосфаты:
3. Фосфорная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов и др.). Также фосфорная кислота вступает в обменные реакции с солями.
4. При нагревании H3PO4 до 200°С происходит отщепление от нее молекулы воды с образованием пирофосфорной кислоты H2P2O7:
5. Фосфорная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Фосфорная кислота взаимодействует также с аммиаком с образованием солей аммония:
7. Качественная реакция на фосфат-ионы и фосфорную кислоту — взаимодействие с нитратом серебра. При этом образуется ярко-желтый осадок фосфата серебра:
Видеоопыт взаимодействия фосфата натрия и нитрата серебра в растворе (качественная реакция на фосфат-ион) можно посмотреть здесь.
Оксиды фосфора. Фосфорная кислота
Фосфор образует очень большое число различных оксидов и кислот. Среди них наиболее устойчивыми являются оксид фосфора (V) и соответствующая ему ортофосфорная, или фосфорная, кислота Н3РО4.
Оксид фосфора (V), или фосфорный ангидрид Р2О5 – белый порошок, без запаха. По своему характеру является типичным кислотным оксидом. При растворении в воде гидратируется с образованием следующих кислот:
Как кислотный оксид Р2О5 взаимодействует с основаниями и основными оксидами, например:
При взаимодействии Р2О5 со щелочами в зависимости от соотношения реагентов могут образовываться не только средние, но и кислые соли:
Хотя в Р2О5 фосфор имеет высшую степень окисления +5, оксид фосфора (V) не проявляет сколько-нибудь выраженных окислительных свойств, так как эта степень окисления для фосфора очень устойчива.
Оксид фосфора (V) является прекрасным водопоглощающим и водоотнимающим средством. На этом основано его использование в эксикаторах (сосудах для высушивания веществ), при проведении реакций дегидратации и т.д.

Фосфорная (ортофосфорная) кислота Н3РО4 – бесцветное кристаллическое вещество, плавящееся при температуре 42 о С, очень хорошо растворимое в воде. Фосфорная кислота является трёхосновной кислотой средней силы.
В лаборатории её получают окислением фосфора разбавленной азотной кислотой.
В промышленности Н3РО4 получают экстракционным методом, обрабатывая природные фосфаты серной кислотой:
а также термическим методом, восстанавливая природные фосфаты до свободного фосфора, который затем сжигают и образующийся при этом Р2О5 растворяют в воде.
Фосфорная кислота обладает всеми общими свойствами кислот, но она значительно слабее таких кислородсодержащих кислот, как серная и азотная. В отличие от этих кислот фосфорная кислота не обладает даже значительными окислительными свойствами, несмотря на устойчивость степени окисления +5.
Применение фосфорной кислоты
Помимо производства удобрений, фосфорную кислоту используют при изготовлении реактивов, многих органических веществ, для получения катализаторов, для создания защитных покрытий на металлах, в фармацевтической промышленности и т.д.
Соли фосфорной кислоты
Как трёхосновная кислота Н3РО4 образует три ряда солей: средние (нормальные) соли – фосфаты; кислые соли – гидрофосфаты и дигидрофосфаты.
Например, при нейтрализации фосфорной кислоты гидроксидом натрия в зависимости от молярного соотношения кислоты и щёлочи могут идти следующие реакции:
Большинство средних солей – фосфатов – нерастворимо в воде. Исключением являются лишь фосфаты щелочных металлов и аммония. Многие же кислые соли фосфорной кислоты, хорошо растворяются в воде, причем наиболее растворимыми являются дигидрофосфаты.
Фосфорные удобрения
Фосфор, как и азот, является одним из тех элементов, который необходим для питания растений. Поэтому наряду с азотными в сельском хозяйстве широко используются фосфорные удобрения. В качестве удобрения можно использовать только водорастворимые соединения. В связи с этим основная задача при производстве фосфорных удобрений — превращение нерастворимого фосфата кальция (основа фосфоритов и апатитов) в растворимые кислые фосфаты.
Важнейшее фосфорное минеральное удобрение – суперфосфат (или простой суперфосфат), который получают обработкой природных фосфоритов серной кислотой:
Образующаяся смесь содержит дигидрофосфат кальция, который хорошо растворим в воде, и сульфат кальция, который не имеет практического значения.
Для получения двойного суперфосфата из природного фосфорита выделяют сначала фосфорную кислоту по реакции:
Затем полученной кислотой обрабатывают новую порцию фосфорита:
Иногда фосфорную кислоту нейтрализуют гидроксидом кальция, при этом получается так называемый преципитат, который тоже является хорошим удобрением:
СаНРО4 плохо растворяется в воде, но достаточно хорошо растворим при внесении его в кислые почвы.

В последнее время широкое распространение получили сложные удобрения, содержащие несколько необходимых растениям элементов.
Важнейшим из них является аммофос, который содержит азот и фосфор и образуется при взаимодействии аммиака и фосфорной кислоты:
Смесь аммофоса с калийной селитрой KNO3 называется аммофоской. Это удобрение содержит все наиболее необходимые растениям питательные элементы – азот, фосфор и калий.
*на изображении записи минерал апатит
Похожее
Добавить комментарий Отменить ответ
Репетитор по химии. Занятия проходят онлайн по Скайпу. По всем вопросам пишите в Ватсапп: +7 928 285 70 42
Фосфорные кислоты
Разновидности фосфорных кислот:
Метафосфорная кислота
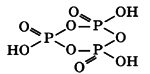
Триметафосфорная кислота (HPO3)3 построена из трех остатков метафосфорной кислоты, которые составляют замкнутый цикл:
Соответственно, тетраметафосфорная кислота (HPO3)4 построена из 4 остатков метафосфорной кислоты, и получается воздействием фосфорного ангидрида P2O5(V) на воду при низких температурах:
P4O10+2H2O = (HPO3)4
Ортофосфорная кислота H3PO4
H3PO4 диссоциирует в три ступени:
Несмотря на тот факт, что фосфорная к-та обладает всеми свойствами общих кислот, она намного слабее, например, азотной или серной кислоты, и не обладает, в отличие от сильных кислот, сколь-нибудь значительными окислительными свойствами, что объясняется устойчивой степенью окисления фосфора (+5).
В промышленности ортофосфорную кислоту получают воздействием серной кислоты на фосфориты и апатиты (экстракционный метод):
Ca3(PO4)2+3H2SO4 = 2H3PO4+3CaSO4
Более чистая кислота получается сжиганием фосфора с последующим растворением в воде образующегося оксида P2O5.
Фосфорную кислоту применяют в производстве:
Полифосфорная кислота
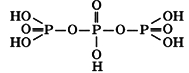
Эти кислоты состоят из открытых цепей, в состав которых входят 2..10 атомов фосфора. На рисунке ниже изображена структура молекулы трифосфорной кислоты H5P3O10:
Фосфорноватистая кислота H3PO2
Бесцветные кристаллы, хорошо растворимые в воде.
Водный раствор фосфорноватистой кислоты является сильной одноосновной кислотой:
Фосфорноватистая кислота и ее соли (гипофосфиты) являются сильными восстановителями:
H3PO2+2I2+2H2O = H3PO4+4HI
Фосфористая кислота H3PO3
Твердое бесцветное вещество, обладающее гигроскопическими свойствами, хорошо растворимо в воде.
Водный раствор фосфористой кислоты является двухосновной кислотой средней силы:
Соли фосфористой кислоты, называемые фосфитами, плохо растворимы в воде за исключением фосфитов щелочных металлов.
Фосфористая кислота и ее соли являются сильными восстановителями, восстанавливая неактивные металлы из их соединений:
2AgNO3+H3PO3+H2O = H3PO4+2Ag↓+2HNO3
Получение фосфористой кислоты:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Фосфорная кислота [H3PO4]: Структура | Свойства | Применение
В чистом виде фосфорная кислота представляет собой бесцветное твердое вещество. В менее концентрированном виде это вязкая жидкость без запаха с плотностью 1,885 г/мл. Обычно она нелетучая и нетоксична, но 85-процентный раствор по-прежнему может повредить глаза и вызвать сильное раздражение кожи.
Давайте копнем глубже и выясним, как образуется фосфорная кислота, как она выглядит на молекулярном уровне, каковы ее физические и химические свойства и где она используется.
Профиль фосфорной кислоты
Молярная масса: 97,994 г/моль
Внешний вид: густая бесцветная жидкость.
Точка кипения: 212 °C
Точка плавления: 42,35 °C (кристаллического твердого вещества)
Динамическая вязкость: от 2,4 до 9,4 сантипуаз (85% водный раствор).
Плотность: 1,83 г / см 3 (твердое вещество); 1,68 г / см 3 (85% водный раствор при 25 °C)
Структура
Соединение H3PO4 имеет в общей сложности 32 валентных электрона. Поскольку фосфор является наименее электроотрицательным, он помещается в центре. Атомы водорода присоединяются к внешней стороне атомов кислорода, образуя он-Группы.
В этой структуре каждый атом имеет полную внешнюю оболочку: атомы фосфора и кислорода имеют восемь валентных электронов, а атомы водорода имеют вокруг себя два валентных электрона.
В структуре все еще есть 32 валентных электрона, и каждый атом имеет формальный заряд, равный нулю. Таким образом, это наиболее вероятная или вероятная структура Льюиса для H3PO4.
Соединение содержит 3 одинарные связи ОН, 3 одинарные связи PO и 1 двойную связь P = O. Каждая одинарная связь является сигма-связью, а двойная связь состоит из сигма-связи и пи-связи.
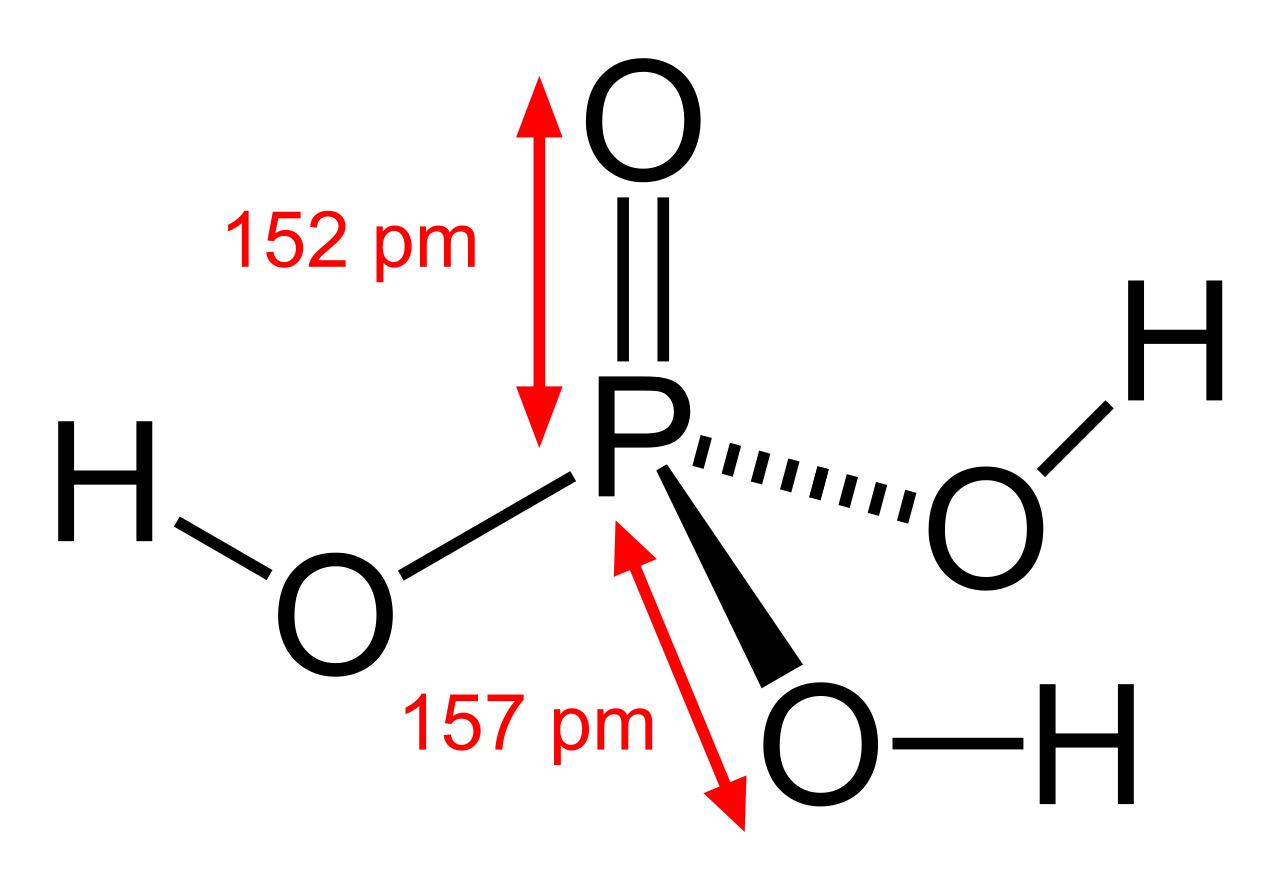
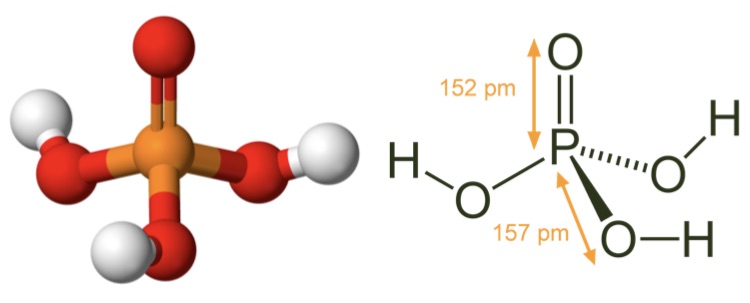
Фосфорная кислота: шарообразная модель и размеры структурной формулы
Молекулярная геометрия PO (OH)3 является тетраэдрической, а кристаллическая структура-моноклинной. А поскольку распределение зарядов на центральных атомах асимметрично, то молекула считается полярной.
Последние достижения в области нанотехнологий, включая методы поглощения рентгеновских лучей вблизи краев и методы рассеяния рентгеновских лучей под большим углом, позволили ученым точно определить структуру фосфорной кислоты. Расстояние связи P=O в структуре близко к 152 пикометрам, и расстояния P=O-O были уточнены до 309 пикометров, с углом связи близким к тетраэдрическому.
Как она производится?
Фосфорная кислота может быть синтезирована либо мокрым способом, либо термическим способом.
В последнем в качестве сырья используются воздух, вода и элементарный фосфор. Он включает в себя три важных этапа: сгорание, увлажнение и запотевание. Вот как это происходит:
Во-первых, жидкий элементарный фосфор сжигается в камере сгорания при высоких температурах в диапазоне от 1650 до 2760 °C. Эта реакция окисления происходит в окружающем воздухе и производит пятиокись фосфора.
Затем продукт гидратируют водой с образованием сильной фосфорной кислоты (в жидком состоянии).
На последнем этапе для удаления фосфорно-кислотного тумана из потока дымовых газов используются высоконапорные каплеуловители.
Концентрация фосфорной кислоты, синтезированной в этом процессе, обычно составляет от 75 до 85 процентов. Такие уровни концентрации необходимы для производства высококачественной химической продукции. Несколько эффективных установок извлекают чрезвычайно концентрированную фосфорную кислоту (до 99,9%), используя тот же тепловой процесс.
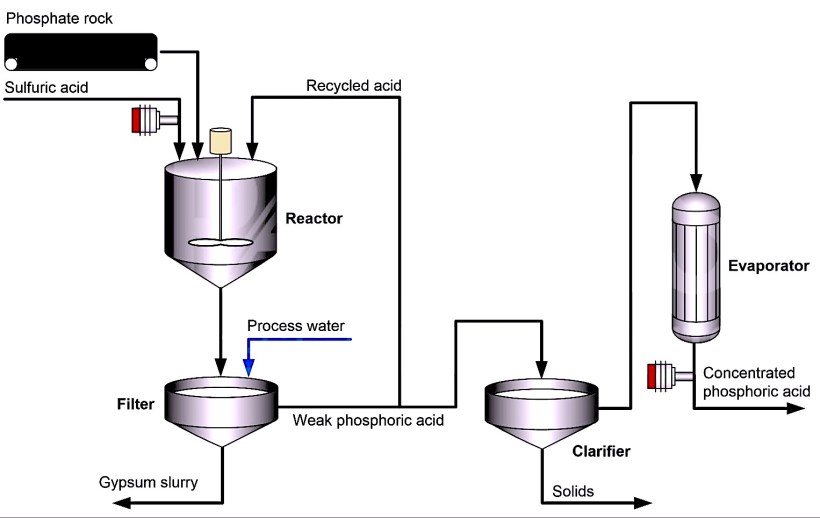
Однако почти 80% фосфорной кислоты производится мокрым способом. В этом методе серная кислота обрабатывается природным фосфатсодержащим минералом, таким как гидроксиапатит.
Минерал высушивают, крошат, а затем подают в реактор вместе с серной кислотой. В результате реакции сульфат сливается с кальцием (из минерала), образуя сульфат кальция (гипс).
Затем добавляется обработанная вода, и гипс вместе с другими нерастворимыми примесями удаляется через фильтр. Фосфорная кислота, полученная этим мокрым способом, содержит 25-30% пятиокиси фосфора.
Обычно эта кислота дополнительно концентрируется, чтобы соответствовать требованиям, предъявляемым к производству удобрений. В большинстве случаев фосфорная кислота концентрируется до 40-55% пятиокиси фосфора с помощью двух / трех вакуумных испарителей.
Свойства
Чистая фосфорная кислота в лаборатории выглядит как плотное, бесцветное, бесформенное кристаллическое твердое вещество, которое плавится при температуре 42,35 °C. Ее физические свойства зависят от чистоты, концентрации кислоты, а также от температуры, при которой вы ее видите.
Фосфорная кислота менее агрессивна и менее опасна по сравнению с азотной и серной кислотами. Это негорючее вещество как в жидкой, так и в твердой форме.
Когда кислота подвергается воздействию тепла, а затем охлаждается до комнатной температуры, она образует прозрачное, хрупкое стекло. После такого воздействия тепла состав кислоты остается прежним.
Обычно фосфорная кислота выпускается в виде бесцветного сиропа с концентрацией в воде 85 процентов и плотностью 1,885 граммов на миллилитр.
В водном растворе фосфорная кислота действует как трипротовая кислота, имеющая три ионизируемых атома водорода. Соединение может потерять эти атомы в виде протонов (ионов H + ).
Кислота растворима как в воде, так и в этаноле. Однако большинство ее солей не растворимы в воде, если нет сильной минеральной кислоты.
Области применения
Фосфорная кислота имеет несколько важных применений. Ее соли, такие как фосфаты аммония и кальция, широко используются в качестве удобрений. Кислота используется для производства электролитов, средств для удаления ржавчины, модификаторов рН, травителей, бытовых чистящих средств и дезинфицирующих средств.
Поскольку это вещество нетоксично и имеет умеренно кислую природу, оно также используется в напитках, пищевых ароматизаторах, косметике, средствах для ухода за зубами и кожей. Давайте подробнее рассмотрим, чем полезна фосфорная кислота.
В менее концентрированной форме она используется для производства различных видов безопасных фосфорных удобрений, которые помогают растениям расти. Фактически, почти 90% синтезированной фосфорной кислоты используется в качестве удобрений.
Многие безалкогольные напитки, в том числе Coca-Cola, содержат фосфорную кислоту. Это придает напитку слегка кисловатый вкус. Несмотря на то, что его концентрация достаточно низкая, экстремальный прием таких напитков может вызвать эрозию зубов и даже привести к образованию почечных камней.
Фосфорная кислота в качестве электролита имеет полезные характеристики, такие как хорошая ионная проводимость, низкая летучесть, стабильность при относительно высоких температурах и устойчивость к диоксиду углерода и монооксиду углерода.
Поскольку чистая фосфорная кислота обладает высокой протонной проводимостью и превосходной термостабильностью, полибензимидазол (PBI), допированный фосфорной кислотой, является наиболее многообещающим среди мембран на основе PBI, которые могут обеспечить хорошую производительность топливных элементов даже при низком уровне увлажнения и температуре 200 °С.
Специфическое применение фосфорной кислоты:
Глобальный рынок
Многие развивающиеся страны начали сосредотачиваться на увеличении добычи фосфатов и производства фосфатов. Правительства некоторых стран уже сотрудничали с различными поставщиками по всему миру для создания заводов по добыче минералов для производства фосфорной кислоты.
В 2019 году объем мирового рынка фосфорной кислоты оценивался в 45,85 миллиарда долларов. Ожидается, что к 2027 году он достигнет более 61 миллиарда долларов, а совокупный годовой темп роста составит 3,7%.
Рынок подразделяется на Азиатско-Тихоокеанский регион, Европу, Северную Америку, Латинскую Америку, Ближний Восток и Африку. Ожидается, что в ближайшем будущем Азиатско-Тихоокеанский регион будет доминировать на мировом рынке. Рост рынка фосфорной кислоты в этих регионах будет дополнительно подпитываться развитым сельскохозяйственным сектором Индии и Китая.
Ортофосфорная кислота
ХимЭксперт осуществляет продажи ортофосфорной кислоты с возможностью доставки заказываемого химического сырья в различные регионы России. Область применения ортофосфорной кислоты разнообразна, но самая большая ценность — это удаление ржавчины на металлических поверхностях, данный метод используется как крупными компаниями при восстановлении свойств поверхности металла, также физическими лицами в бытовых и хозяйственных целях.
Ортофосфорная кислота (фосфорная кислота) — неорганическая кислота средней силы с химической формулой H3PO4, которая при стандартных условиях представляет собой бесцветные гигроскопичные кристаллы. Обычно ортофосфорной (или просто фосфорной) кислотой называют 85 %-й водный раствор (бесцветная сиропообразная жидкость без запаха). Растворима в этаноле, спирте, воде и других растворителях. Ортофосфорная кислота (синоним: кислота фосфорная) представляет собой бесцветную жидкость, плотностью от 1,56г/см3 (для кислоты концентрацией 73%) до 1,71г/см3 (для кислоты концентрацией 87%), не имеющую запаха.
Виды ортофосфорной кислоты и отличия
ГОСТ 10678-76 Кислота ортофосфорная термическая. Марка А, марка Б — 1 и 2 сортов. В зависимости от области применения термическая ортофосфорная кислота выпускается следующих марок:
Б – техническая ( 1-й сорт и 2-й сорт). Применение ортофосфорной кислоты марки Б: применяется для производства реактивных и пищевых фосфорных кислот, технических фосфорных солей, кормовых фосфорных удобрений, синтетических моющих средств, металлообрабатывающей, текстильной, нефтяной, стекольной и керамической промышленности. Широко используется также для фосфатирования металлов, в качестве катализатора в органическом синтезе.
ГОСТ 6552-80 Кислота ортофосфорная. Реактив. Ч (ортофосфорная кислота чистая), ХЧ (химически чистая) и ЧДА (чистая для анализа). Отличия ортофосфорной кислоты по видам и ГОСТам указаны в самих ГОСТах, и это касаемо, прежде всего, норм и содержания, концентрации определенных веществ в растворе.
УСЛОВИЯ ТРАНСПОРТИРОВКИ И ХРАНЕНИЯ
Термическую ортофосфорную кислоту транспортируют железнодорожным и автомобильным транспортом в соответствии с правилами перевозки опасных грузов, действующими на транспорте данного вида. Ортофосфорную термическую кислоту по железным дорогам транспортируют также в вагонах-цистернах. Степень (уровень) заполнения цистерн следует рассчитывать с учетом полного использования вместимости (грузоподъемности) цистерн и объемного расширения продукта при возможном перепаде температур в пути следования.
Термическую ортофосфорную кислоту хранят в стальных футерованных закрытых емкостях, а также в бутылях, канистрах и контейнерах, в которых она транспортировалась.
Применение ортофосфорной кислоты
Ортофосфорная кислота применяется в самых различных сферах и промышленных отраслях:
Требования безопасности. Класс опасности ортофосфорной кислоты
Основной класс опасности — 2, дополнительный — 8. Ортофосфорная кислота по степени воздействия на организм человека относится к веществам 2-го класса опасности по ГОСТ 12.1.007. Предельно допустимая концентрация продукта (по фосфорному ангидриду) в воздухе рабочей зоны производственных помещений составляет 1 мг/м3. При увеличении концентрации пары ортофосфорной кислоты вызывают атрофические процессы слизистых оболочек и крошение зубов, а также воспалительные заболевания кожи. По ГОСТу 19433-88 ортофосфорная кислота относится к 8 классу опасности, стандарт определяет классификацию перевозки опасных грузов (ADR), и распространяется на опасные грузы и устанавливает: классификацию; номенклатуру показателей и критерии для отнесения грузов к опасным и их классификации; методы определения показателей для классификации опасных грузов; маркировку и правила ее нанесения на грузовые единицы с опасными грузами, в том числе поставляемыми на экспорт.