Фоспренил или ронколейкин что лучше
Иммуномодуляторы в ветеринарной практике: применение и противоречия (Продолжение 1)
Автор: А.В. Санин, А.Н. Наровлянский, С.В. Ожерелков, А.В. Пронин, В.Ю. Санина ГУ НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи РАМН, г. Москва.
Опубликовано: 29 ноября 2015
Применение ИМД при вирусных инфекциях.
Поскольку вирусные инфекции практически всегда сопровождаются иммуносупрессией, актуальны поиск и применение тех ИМД, которые способны не только повышать естественную резистентность организма (стимулируя фагоцитоз и выработку антител, усиливая цитотоксическую активность лимфоцитов, индуцируя синтез ИФ и других цитокинов), но и оказывать прямой противовирусный эффект. В наибольшей степени этим требованиям удовлетворяют Фоспренил и Гамапрен. Такие препараты, сочетающие в себе свойства ИМД и антивирусного средства, можно рекомендовать для лечения и профилактики вирусных инфекций, сопровождающихся иммунодефицитным состоянием.
Таким образом, в инкубационном периоде и в первые 1 – 2 дня клинической стадии вирусного заболевания целесообразно назначать ИМД, стимулирующие продукцию ИФН, а также других факторов естественной резистентности организма (например: ИЛ-12, ФНО, ИЛ-1). Объективным критерием эффективности указанных ИМД может служить восстановление выработки ранних цитокинов, синтез которых подавлен вирусами (6). Так, Фоспренил после введения в организм при вирусной инфекции стимулирует раннюю продукцию ИФ-γ, ФНОα и ИЛ-6 и ИЛ-12 в сыворотке (12, 13), что, по-видимому, является одним из ключевых механизмов противовирусной активности препарата при его использовании в качестве профилактического средства или на самых ранних стадиях инфекционного процесса. Вирусы обладают способностью нарушать сбалансированное развитие Th1/Th 2 иммунного ответа, необходимое для формирования эффективного противовирусного иммунитета, а Фоспренил, судя по всему, способен восстанавливать этот необходимый баланс, в частности, благодаря стимуляции продукции ключевых цитокинов, обеспечивающих сбалансированное формирование Th1 (ИЛ-12, ИФ-γ,) и Th2 (ИЛ-4, ИЛ-5, ИЛ-6) иммунного ответа при вирусном инфекционном процессе (13, 15). Это свойство Фоспренила в сочетании с прямым противовирусным действием, по-видимому, и обеспечивает защиту животных от вирусной инфекции.
При лечении тяжелых инфекций следует отдавать предпочтение ИМД природного происхождения (из тимуса, дрожжей, бактериальных клеток, растений), которые, как правило, не оказывают побочных эффектов. В настоящее время чаще рекомендуют применять индукторы ИФН — интерфероногены, а не препараты самих ИФН, в том числе рекомбинантные (сейчас из препаратов на основе ИФН при лечении вирусных инфекций еще применяют разве что Кинорон, более эффективный на ранних стадиях заболевания). Это связано, в частности, с тем, что, во-первых, экзогенный ИФН после введения в организм способен подавить синтез эндогенного ИФН по принципу механизма обратной связи и вызвать дисбаланс в системе ИФН. Во-вторых, рекомбинантные ИФН быстро инактивируются. Напротив, индукторы ИФН (Максидин, Фоспренил, Достим, Риботан, Камедон, Сальмозан и др.) стимулируют синтез эндогенного ИФН (что физиологично, да и активность эндогенного ИФН сохраняется дольше), а также, в большинстве случаев, запускают синтез и продукцию других цитокинов, прежде всего, именно Th1 ряда. Кроме того, в раннем противовирусном процессе активно участвуют неспецифические естественные киллеры (ЕКК). Эти клетки после активации и пролиферации синтезируют и секретируют противовоспалительные цитокины, которые запускают каскад сигналов, способствующих прерыванию цикла репродукции вируса в инфицированной клетке. Ввиду этого, при лечении вирусных инфекций целесообразно применение ИМД, стимулирующих ЕКК, а именно Фоспренила, Максидина, Ронколейкин (его активность закономерно возрастает в сочетании с Фоспренилом). К сожалению, из ветеринарной практики изъят очень эффективный ИМД — циклоферон, который способен индуцировать секрецию ИФН всех типов. Напротив, следует приветствовать, что ветеринарные специалисты практически перестали использовать в качестве ИМД Левамизол (Декарис), который не только довольно токсичен, но также (при применении в малых дозах) избирательно стимулирует супрессорные (регуляторные) Т-клетки (4). ИМД на основе цитокинов (в том числе рекомбинантных) при введении в организм способны восполнить дефицит растворимых иммунорегуляторных факторов, что особенно важно при тяжелых поражениях иммунной системы, когда ее компенсаторные возможности нарушены. С другой стороны, необоснованное назначение подобных препаратов (при отсутствии серьезных показаний) может привести к дисбалансу в иммунной системе за счет блокирования синтеза гомологичных эндогенных молекул по принципу механизма обратной связи. Большое значение имеет сочетание ИМД на основе рекомбинантных цитокинов с другими препаратами. Очевидно, например, что эффективность Ронколейкина (рекомбинантного ИЛ-2) возрастает, если перед его введением в организм повысить уровень экспрессии соответствующих рецепторов с помощью препаратов, усиливающих секрецию ИЛ-1. Это подтверждено на практике в экспериментах по комплексному применению Ронколейкина с Фоспренилом или с Гамавитом (в состав последнего входит нуклеинат натрия — эффективный индуктор ИЛ-1 и ИФН) — эти ИМД существенно повышают активность самого Ронколейкина.
Следует остановиться на возможности сочетанного применения ИМД, различающихся между собой по спектру воздействия на лимфоидные клетки-мишени. В частности, сочетание Достима или Сальмозана (более активно воздействующих на В-клетки, чем на Т-клетки) с противовирусными ИМД (например: с Фоспренилом или Гамапреном) может, при своевременно начатом лечении, предотвратить развитие вторичных инфекций и, следовательно, снизить потребность в антибиотикотерапии. В серии экспериментальных исследований на модели острой клинически выраженной инфекции, вызываемой вирусом клещевого энцефалита (ВКЭ) у мышей, был выявлен эффект взаимного усиления активности Фоспренила и Максидина (12). В результате одновременного совместного введения мышам этих двух ИМД протективный эффект возрастал в 2 – 2,5 раза, по сравнению с эффектом от введения какого-либо одного препарата. Эти данные легли в основу клинических испытаний при лечении собак с диагнозом чума плотоядных и кошек с диагнозом панлейкопения. В результате оказалось, что при тяжелом течении чумы плотоядных, а также при вирусных инфекциях кошек сочетанное применение Фоспренила и Максидина дает положительный эффект: оба препарата, обладая различными механизмами противовирусного действия, дополняют друг друга. Их совместное применение ускоряет сроки лечения и предотвращает рецидивы заболевания, а также позволяет значительно (более чем вдвое) снизить разовые дозы препаратов, уменьшая тем самым стоимость лечения животных (21).
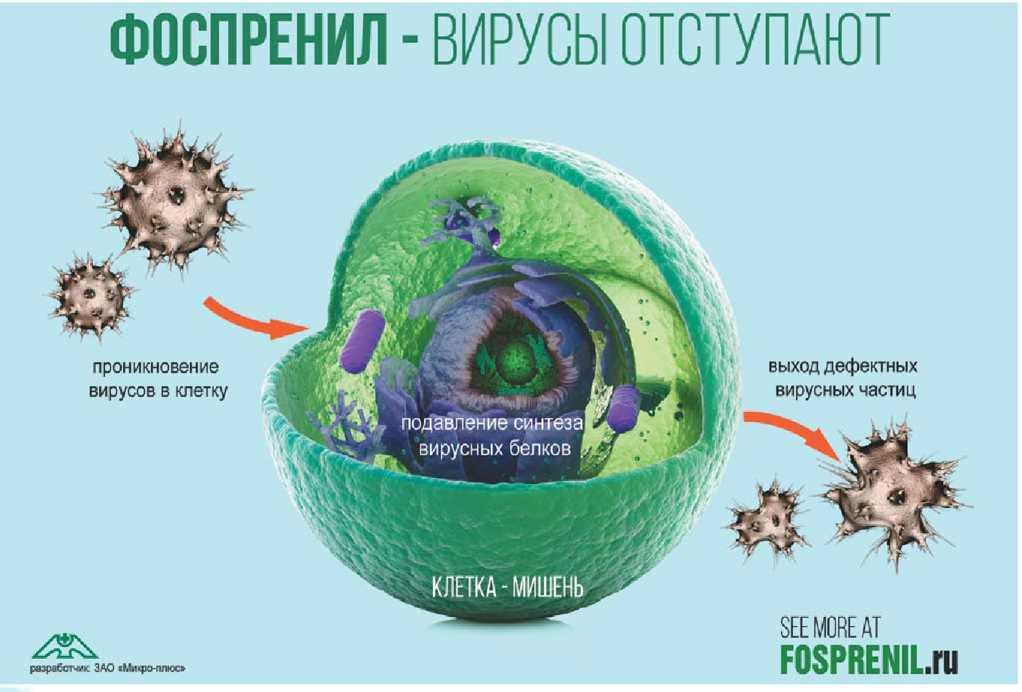
Полученные экспериментальные данные научно обосновывают применение ИМД на различных стадиях инфекционного вирусного процесса. При этом показано, что Фоспренил как ИМД комплексного действия, может использоваться не только на ранних, но и на более поздних клинически выраженных этапах вирусной инфекции, так как он обладает прямым противовирусным действием и способностью нарушать жизненный цикл вирионов в клетках. Причем, в отличие от большинства других противовирусных препаратов, нарушающих определенные этапы репликации вирусов (и, следовательно, имеющих ограниченный спектр применения), механизм действия Фоспренила более многообразен и включает как непосредственное воздействие на вирусы, например — торможение синтеза ключевых белков, приводящее к изменению структуры вириона, так и нарушение репликации вирусов опосредованно, через изменение метаболизма инфицированной клетки, а также системное действие.
Применение ИМД при бактериальных инфекциях.
В литературе давно утвердилось мнение о том, что инфекционные болезни являются моноэтиологичными заболеваниями. В свое время такие представления, несомненно, оказали положительное влияние и способствовали изучению проблем патогенеза, иммунитета, диагностики, профилактики и этиотропного лечения вирусных или бактериальных инфекций. Однако на практике вирусные заболевания у мелких домашних животных редко протекают в виде моноинфекции. Как правило, на фоне уже имеющегося иммунодефицита, сопровождающего вирусную инфекцию, развиваются вторичные (секундарные) инфекции, которые тоже нередко полиэтиологичны. Помимо состояния иммунной системы хозяина, большое значение в развитии секундарных инфекций отводят биологическим свойствам и активности возбудителей, а также внешним стрессорным факторам. Так, респираторные вирусы повышают восприимчивость слизистых оболочек дыхательных путей к стафилококкам, стрептококкам и другим микроорганизмам; энтеровирусы оказывают аналогичное действие на чувствительность кишечного тракта к сальмонеллам и шигеллам. Впрочем, у мелких домашних животных встречаются и чисто бактериальные инфекции. При последних, хорошо зарекомендовало себя подключение к комплексной схеме лечения Сальмозана — ИМД бактериального происхождения. Сальмозан, полученный и всесторонне исследованный в НИИЭМ им. Гамалеи РАМН, представляет собой очищенный полисахарид из О-антигена брюшнотифозных бактерий. Препарат повышает образование антител, фагоцитарную активность лейкоцитов и макрофагов, титр лизоцима в крови, стимулирует неспецифическую резистентность к инфекциям, вызванным сальмонеллами, листериями, клебсиеллами, эшерихиями, стафилококками, бруцеллами, риккетсиями, возбудителями туляремии и некоторых других заболеваний (23). Согласно данным клинических испытаний, проведенных специалистами в 10 различных клиниках РФ, при бактериальных инфекциях (сальмонеллез, колибактериоз и стафилококкоз, подтвержденные лабораторной диагностикой), респираторных заболеваниях (бронхит, пневмония), энтеритах различной этиологии и энтероколитах собак и кошек применение Сальмозана позволило значительно сократить сроки лечения и повысить эффективность терапии. Сделано заключение о целесообразности применения Сальмозана как препарата первого выбора, стимулирующего иммунитет и неспецифическую резистентность. При лечении гнойных и рваных ран применение Сальмозана позволило существенно сократить срок лечения, отмечено снижение отечности, уменьшение гнойного экссудата в первые 2 – 3 дня, выздоровление наступало в полтора раза быстрее. Способность Сальмозана активировать макрофаги и стимулировать продукцию специфических антител В-лимфоцитами и обусловливает то, что сочетание Сальмозана с ИМД, обладающими противовирусной активностью, может, при своевременно начатом лечении, предотвратить развитие вторичных инфекций. Показано, что применение Сальмозана в сочетании с такими ИМД как Фоспренил, Максидин, Гамапрен, Гамавит, Иммунофан, Кинорон и др., не только существенно повышает эффективность лечения панлейкопении, герпесвирусных инфекций и калицивироза кошек, чумы плотоядных и парвовирусного энтерита собак, а также кожных, респираторных, гнойных и некоторых иных заболеваний, но и позволяет снижать дозы антибиотиков и сократить курс антибиотикотерапии (21). При этом отмечено, что Ампиокс, Бензилпенициллин и другие антибиотики при применении Сальмозана действуют гораздо эффективнее, что позволяет, при необходимости снижения стоимости лечения, отказаться от применения дорогих антибиотиков последнего поколения.
При выборе препаратов для лечения бактериальных, вирусных и смешанных инфекций важны и другие, вспомогательные функции ИМД. В частности, при инфекциях, сопровождающихся поражением желудочно-кишечного тракта (сальмонеллез, энтериты различной этиологии, инфекционный гепатит, панлейкопения и др.) большое значение имеет обезвреживание токсинов, обильно поступающих в организм в связи с дисфункцией кишечника. Очевидно, что при таких заболеваниях показаны такие ИМД препараты, как Фоспренил, Достим, а также нуклеинат натрия или Гамавит.
При лечении хламидиоза хорошие результаты получены при использовании совместно с антибиотиками таких ИМД как Максидин, Фоспренил или Иммунофан в сочетании с Гамавитом (9). По-видимому, это объясняется описанными выше механизмами действия данных ИМД, поскольку решающая роль в выздоровлении от хламидийной инфекции принадлежит Th1- иммунному ответу, продуктами активации которого являются IL-2, ФНОβ и вырабатываемый Th1 — ИФНγ, который не только ингибирует размножение хламидий, но и стимулирует выработку IL-1 и IL-2.
Видео
Сравнительная эффективность иммуностимуляторов при лечении вирусного ринотрахеита у кошек
В последние время одной из важнейших проблем ветеринарии является рост заболеваний, торпидных к адекватной этиотропной терапии и связанных с нарушениями в системе иммунитета [3;10]. Иммунная система любого животного выполняет важную функцию по сохранению постоянства внутренней среды организма, осуществляемую путем распознавания и элиминации из организма чужеродных веществ антигенной природы, как эндогенно возникающих, так и экзогенно проникающих в организм. Эта функция иммунной системы осуществляется с помощью факторов врожденного и приобретенного (или адаптивного) иммунитета [12].
В последние годы было проделана большая работа по изучению иммунного ответа кошек на различные эндогенные факторы. В частности, авторы фундаментального учебника «Ветеринарная иммунология» Манько В.М., Девришов Д.А. (2011 г.) отмечали, что при заражении острыми вирусными инфекциями обычно развивается стойкая иммуносупрессия [10]. В работе Орловой С.Т., Сидорчук А.А. (2015; 2016 г.) по поствакцинальному иммунитету кошек и собак указывается, что иммунитет после естественного переболевания кошек FCV кратковременный и неполный [11]. Вирус может сохраняться в организме кошки пожизненно латентно, реактивируясь при стрессах, нарушениях условий содержания и неполноценном кормлении [12]. Henzel. A с соавторами в работе, посвященной выделению и идентификации калици- и герпесвируса из организма кошек доказали, что «вакцинация предупреждает тяжелые проявления болезни, но не инфицирование с местной репликацией и распространением вируса» [21]. Кроме того, на фоне фармакотерапии острых вирусных инфекций, при наличии идеосинкразии или сенсибилизации к ряду ветеринарных препаратов, у кошки могут развиться вторичные иммунологические нарушения: иммунодефициты, аллергические, аутоиммунные и пролиферативные процессы. Нарушение иммунных механизмов защиты организма приводит к появлению инфекционных осложнений, аутоиммунной патологии, развитию злокачественных опухолей и аллергических заболеваний [1].
Вторичная иммунная недостаточность часто наблюдается при вирусных, паразитарных и некоторых бактериальных инфекциях, истощении организма, длительном стрессе, тяжелых травмах, интоксикациях, лечении онкологических больных химиотерапевтическими средствами при длительном воздействии вредных факторов, в число которых в последнее время относят и корма эконом-класса, или в неблагоприятных экологических условиях [2;3].
В связи с резко возросшим интересом практикующих врачей к противовирусной терапии особенно важно выявить область применения и степень адекватного ответа животных на иммунную фармакотерапию различными препаратами.
Рынок предлагает большое количество лекарственных средств, биологически-активных добавок и даже кормов для ослабленных животных со сниженным иммунитетом. Практикующему врачу зачастую трудно разобраться в этом громадном потоке информации и предложений и выбрать нужное средство. Исходя из этого, мы поставили целью провести серию экспериментов по действию наиболее часто применяемых в нашем регионе препаратов, предназначенных для этиотропной терапии герпесвирусной инфекции кошек I типа (FHV-1). Для сравнения нами были выбраны наиболее часто применяемый Форвет, Фоспренил и рекомбинантный интерферон кошки Фелиферон.
Фоспренил – динатриевая соль фосфата полипренолов, получаемых из хвои сосны. Позиционирован в инструкции производителя как противовирусный лекарственный препарат с иммуномодулирующими свойствами. Наиболее подробно его действие при заболевании кошек описано в работе Гуровой Ю.Н., Бакулина Е.А. (2002 г.), «Применение препарата Фоспренил при подострой форме вирусных респираторных инфекций кошек». В экспериментах, проведенных А.В. Саниным и соавт., показано, что Фоспренил, зарегистрированный в РФ как противовирусный препарат (А.В. Санин и др., 1991 г.), является эффективным иммунокорректором вторичных иммунодефицитов, индуцированных различными внешними факторами: вирусной инфекцией, стрессом, радиацией [18].
Форвет – иммуномодулирующий препарат на основе полисахаридного комплекса, относящегося к классу высокомолекулярных гексозных гликозидов сложного строения, выделенного из побегов картофеля. Аналог оригинального медицинского препарата Панавир, обладающего цитопротекторным действием, индуцирующего синтез интерферона, тормозящего репликацию вирусов в клетках. Были проведены исследования, доказавшие эффективность применения этого препарата в терапии дерматитов кошек и собак [8], а также для профилактики коронавирусной инфекции кошек [13].
Фелиферон – рекомбинантный интерферон кошки, обладающий противовирусным и иммуностимулирующим действием, появившийся на рынке ветеринарных препаратов более 3 лет назад зарекомендовал себя в ведущих ветеринарных клиниках. Ранее этот препарат был исследован при терапии острых вирусных инфекций у кошек [4;6;7;14;15], медленнотекущих вирусных инфекций [16;17].
Данная серия экспериментов была заложена нами для проверки сравнительной эффективности 3 препаратов, назначаемых в комплексной терапии острого течения герпесвирусной инфекции кошек, наиболее часто используемых ветеринарными врачами городов Дзержинска и Нижнего Новгорода и прилегающей местности. Эксперимент проводился с января по апрель 2018 г. В эксперименте участвовало 24 кошки в возрасте 6-12 месяцев, отобранных методом аналогов. Основным критерием отбора были результаты общеклинического исследования крови на первичном приеме. При этом внешний вид животных мог сильно отличатся: при похожих гематологических данных одни животные могли тяжело переносить заболевание, а другие – легко с сохранением аппетита и субфебрильной температурой тела. Первичное клиническое обследование проводилось непосредственно в «Центре ветеринарной помощи», далее животные находились на амбулаторном наблюдении и приносились на прием на 5-й и 10-й дни терапии. В дни приема врач фиксировал в амбулаторном журнале и индивидуальной электронной карточке состояние пациентов и результаты лабораторный исследований. Гематологическое сопровождение эксперимента выполняла ветеринарная лабораторная служба «Веттест» Нижнего Новгорода. Диагностика проводилась по следующим позициям: общий анализ крови базовый, СОЭ, и ПЦР-профиль респираторный базовый.
После первичного обследования и подтверждения диагноза лабораторией «Веттест» животным назначалась следующая терапия:
в контрольной группе для пассивной иммунизации применяли препарат Глобфел, согласно инструкции предприятия-производителя 3 раза с интервалам 24 часа подкожно, в качестве средства профилактики развития секундарной инфекции однократно использовали антибиотик пролонгированного действия амоксициллин 15% ЛА (Amoxycillin L.A.), фирмы «Биовета» (Чехия), для стимуляции процессов репарации эпителия, стимуляции гемопоэза и оптимизации нарушенного обмена веществ мы применяли препарат Гемобаланс в дозе и кратности, рекомендованной производителем. Первая опытная группа получала аналогичную терапию и дополнительно Фоспренил, согласно рекомендациям организации-производителя – ЗАО «Микро-плюс» (Москва).
Вторая опытная группа в дополнение к контрольной терапии получала препарат Форвет производства ООО «Национальная Исследовательская Компания» (Москва), в дозах, предложенных производителем. Кошкам третьей опытной группы в дополнение к контрольной терапии применяли рекомбинантный интерферон кошки Фелиферон производства Научно-технологического центра «БиоИнвест» (Москва).
Таблица 1 Схема эксперимента по сравнительной эффективности препаратов при этиотропной терапии вирусного ринотрахеита у кошек
Публикации
Иммуномодуляторы при лечении и профилактике гельминтозов
ПРИМЕНЕНИЕ ИММУНОМОДУЛЯТОРОВ СОВМЕСТНО С АНТИГЕЛЬМИНТИКАМИ ЯВЛЯЕТСЯ НОВЫМ НАПРАВЛЕНИЕМ В ВЕТЕРИНАРНОЙ МЕДИЦИНЕ. ГЛАВНАЯ ЦЕЛЬ ИХ ИСПОЛЬЗОВАНИЯ — ВОССТАНОВЛЕНИЕ ИММУННОГО СТАТУСА ЖИВОТНЫХ
Городские собаки и кошки проживают в стрессовых условиях, из-за чего у них нередко развиваются вторичные иммунодефициты. Дополнительным фактором риска является достижение питомцем возраста 7 лет, когда его иммунитет начинает давать сбои. Это требует применения дополнительных мер по защите иммунитета домашних питомцев.
Организм здорового животного способен частично уничтожать яйца гельминтов. Такой способностью обладают макрофаги, нейтрофилы, эозинофилы и тромбоциты. Они секретируют цитотоксические соединения и функционируют более эффективно при активации цитокинами, которые выделяют Т-клетки. Однако молодые животные, чей иммунитет еще только формируется, а также ослабленные и старые животные становятся легкой добычей паразитов.
Гельминты наносят организму ослабленных домашних питомцев ощутимый урон. В результате эволюции паразиты приспособились потреблять питательные вещества из организма хозяина. Кишечные гельминты поглощают значительное количество витаминов и минералов из химуса, в частности витамины группы В, что приводит к развитию анемии. Под влиянием паразитов снижается активность органов секреции (щитовидной железы и гипофиза), нарушаются обменные, а также иммунные процессы, что ведет к снижению общей сопротивляемости организма.
Обсемененность почв яйцами гельминтов в мегаполисах крайне высокая, поэтому собаки и кошки нуждаются в ежеквартальной обработке антигельминтиками. В случае заболевания или в целях профилактики четвероногому пациенту чаще всего назначают комплексный препарат на основе 2-3 активных компонентов. Хотя современные ан- тигельминтики в большинстве случаев относятся к малоопасным веществам, ослабленный организм животного нуждается в дополнительной поддержке, в том числе в витаминно-минеральных препаратах, а также в средствах, стимулирующих клеточный иммунитет.
Воздействие химиотерапевтических препаратов на иммунную систему животных сегодня активно изучается. Экспериментальными исследованиями установлено, что некоторые действующие вещества антигельминтиков способны вызвать иммуносупрессию, что также оправдывает применение иммуномодулирующих препаратов. Например, мебендазол угнетает Т- и В-лимфоциты у спонтанно зараженных трихинеллезом мышей. Отдельныеантигельминтики в определенных дозах обладают, напротив, иммуномодулирующим эффектом. Однако их действие также может наносить вред. Например левамизол, стимулирующий клеточный иммунитет млекопитающих и применяющийся в основном для продуктивных животных, в малых дозах подавляет иммунитет за счет активации супрессорных клеток.
Поданным некоторых исследований, иммуномодуляторы способны подавлять развитие паразитов и за счет резервов организма вызывать частичную гибель паразитов. Например, в экспериментальных условиях иммуномодулятор Ронколейкин оказывает защитный эффект в пределах40% при эхинокок- козе собак. Таким образом, включение отдельных иммуномодуляторов в схему дегельминтизации полезно для профилактики гельминтозов в загрязненных паразитами мегаполисах. Применение данных средств способствует противодействию клеток кишечника тканевым антигенам и токсинам паразита.
Современные иммуномодуляторы характеризуются разнообразным составом и механизмами действия.
Иммуномодуляторы могут усиливать или подавлять действие антигельминтиков. В частности, выявлено синергитическое действие альбендазола и препарата Ронколейкин. Однако при превышении рекомендованной дозы последний может нейтра- лизовывать действие альбендазола.
По мнению О. Мамыковой, для научно-обоснованного выбора фармакологических средств важно знать не только характер иммунотропной активности препаратов, входящих в комбинацию, но и комбинированное действие, поскольку очевидна возможность изменения иммунотропных эффектов под влиянием дополнительных средств. Результаты наблюдений показывают, что препараты, примененные изолированно и обладающие однонаправленным иммунобиологическим действием, проявляют противоположное влияние на иммунокомпетентные клетки при совместном назначении.
Некоторые иммуномодуляторы способствуют защите клеток печени, что является положительным моментом при дегельминтизации. Например, азок- симера бромид, действующее вещество препарата Азоксивет, оказывает активирующее действие на неспецифическую резистентность организма, фагоцитоз, гуморальный и клеточный иммунитет, кроме этого, он обладает свойствами гепатопро- тектора. Эффективными гепатопротекторами являются также фосфорилированные полипренолы (Фоспренил) и Гамавит. Последний также является эффективным детоксикантом.
Совместное применение антигельминтиков и иммуномодуляторов, стимулирующих клеточный иммунитет, увеличивает эффективность лечения и снижает риск возникновения резистентности паразитов к препаратам. На сегодняшней день продолжаются исследования по выявлению наилучших сочетаний этих препаратов. В частности, уже установлено, что для лечения и профилактики гельминтозов возможно применять такие препараты, как Азоксивет (Полиоксидоний-Вет), Гамавит, Иммунофан, Ронколейкин и Риботан.
МНЕНИЕ ЭКСПЕРТА
А.В. САНИН, д-р биол. наук, профессор ФГБУ ФНИЦЭМ им. Н Ф. Гамалеи Минздрава России
Современные антигельминтики характеризуются селективной токсичностью для паразитов и низкой токсичностью для хозяина. Такая избирательность в их воздействии основана на существенных физиологических и биохимических различиях между организмами паразитов и теплокровных животных. Так, в отличие от млекопитающих, гельминты получают энергию в результате анаэробной ферментации углеводов в восстановленные конечные продукты. Ключевую роль в этом отводят ферменту НАД.Н-зависимой фумаратредуктазе (Т.С. Носик, В.Б. Ястреб, 2000). Тем не менее время от времени ветврачи продолжат регистрировать у животных нежелательные последствия после приема даже «мягких» антигельминтиков. Одной из причин подобных явлений служит повышенная индивидуальная чувствительность либо генетическая восприимчивость (например повышенная чувствительность собак породы колли к макроциклическим лактонам). Большинство же негативных последствий, часто возникающих после приема современных антигельминтных препаратов (тошнота, рвота, слабость, неустойчивый стул и др.), вызваны, по-видимому, не токсическим воздействием самих препаратов (за исключением случаев передозировки), а действием всасывающихся из кишечника продуктов раощда гельминтов. Дело в том, что современные противогельминтные средства при правильном применении (соблюдение схем, дозировок, предписанных ветврачом) не изгоняют глистов, а убивают их непосредственно в кишечнике животного или ином месте обитания. Вследствие массивного распада и разложения гельминтов их токсины всасываются в кровь и становятся причиной усиления интоксикации и сенсибилизации организма.
Последнее можно, пожалуй, считать оборотной стороной высокой эффективности современных антигельминтных средств. Когда антигельминтик, образно говоря, одерживает победу над противником и глисты погибают, Янус и оборачивается своим третьим, незримым ликом: токсические продукты распада глистов могут погубить организм. Отсюда следует парадоксальный вывод: чем антигельминтный препарат лучше (т.е. чем эффективнее он уничтожает паразитов), тем он хуже (с точки зрения вредного д ействия на организм продуктов их распад а). Описан случай гибели из-за интоксикации, вызванной продуктами разрушения аскарид, пятинедельного щенка бультерьера, которому дали полтаблетки вермокса (А.В. Святковский, 1994). Продукты распада гельминтов вызывают общую интоксикацию организма, снижают иммунитет, вызывают аллергические реакции, проявляющиеся в виде эозинофилии, астматического компонента, кожного зуда, крапивницы и т.д. Накопление продуктов распада паразитов в кишечнике способствует изменению pH внутренней среды и развитию дисбактериоза. При массовой гибели гельминтов и интенсивном всасывании продуктов их распада могут развиться и более тяжелые проявления аллергии по типу реакции немедленного типа. При разрушении трематод (описторхи и др.) собаки теряют аппетит, на коже возможны высыпания, отмечается зуд, слабость, рвота. При массовой гибели дирофилярий может возникнуть угроза последующей закупорки легочной артерии и других сосудов. Особенно ярко негативные последствия проявляются на фоне высокой интенсивности инвазии.
Именно поэтому чаще всего для снижения токсической нагрузки на организм антигельминтного средства и продуктов распада гельминтов ветеринарные врачи назначают Гамавит. Этот препарат превосходно зарекомендовал себя как мощное детоксикационное средство при паразитарных инвазиях и незаменим при использовании так называемых «тяжелых» антигельминтиков.
Таблица 1. АКТИВНОСТЬ И СОСТАВ НЕКОТОРЫХ ИММУНОМОДУЛЯТОРОВ ДЛЯ СОБАК И КОШЕК