Фтористый алюминий что это
Алюминий фтористый — важное для алюминиевой промышленности соединение
Алюминий фтористый — неорганическое соединение с формулой AIF3, соль фтороводородной (плавиковой) кислоты, фторид (трифторид) алюминия.
В природе фторид алюминия не встречается, только производится искусственно. Получают его различными способами, а также он образуется как сопутствующий продукт при переработке фторсодержащего сырья на заводах минеральных удобрений.
Свойства
По внешнему виду это порошок с бесцветными, белыми, сероватыми 
Как химическое вещество фтористый алюминий отличается низкой активностью. Он не реагирует с водными щелочами и кислотами, кроме концентрированной серной кислоты, да и с ней реагирует очень медленно. Вступает в реакции с расплавами щелочей. Взаимодействие с водой при высоких температурах приводит к образованию гидроксида алюминия. В результате реакции с фторидами металлов получаются комплексные соединения — фтороалюминаты, востребованные в разных областях промышленности. Самый известный из фтороалюминатов — криолит.
Меры предосторожности

Работы с фтористым алюминием должны проводиться в помещениях с хорошей вентиляцией. В местах, где возможно образование пыли реактива, должна работать локальная вытяжная система. Следует обращать особое внимание на герметизацию производственных установок и систем коммуникации. Работники должны использовать респираторы, герметичные защитные очки и защитные перчатки или рукавицы.
Хим.реактив не горит и не взрывается. Хранится и перевозится в бумажных или полиэтиленовых мешках, контейнерах. Перевозить его можно любым видом транспорта. Хранят трифторид алюминия в крытых сухих складских помещениях с хорошей вентиляцией.
Применение
— Львиная доля получаемого фтористого алюминия используется для производства металлического алюминия. Его добавляют в расплав при электролитическом методе получения алюминия. Добавки AIF3 и некоторых других компонентов делают процесс энергоэффективнее.
— Для производства криолита, который является основой электролита для получения алюминия.
— Для очистки алюминия, перекиси водорода.
— В качестве катализатора в органических синтезах.
— В стекольной индустрии и керамике для получения стекол, 
— Как один из компонентов смеси в производстве покрытий электродов для сварочных аппаратов, а также для изготовления флюсов.
— Как антисептик в процессах брожения (останавливает брожение).
— При изготовлении кинопленки, оптических деталей.
— В кожевенной промышленности.
Трифторид алюминия
| Трифторид алюминия | |||
|---|---|---|---|
| |||
| Традиционные названия | трифторид алюминия, фторид алюминия, алюминия трифторид | ||
| Хим. формула | AlF3 | ||
| Состояние | белое твердое кристаллическое вещество без запаха | ||
| Молярная масса | (тригидрат) 138.023 г/моль | ||
| Плотность | 2,88 г/см³ | ||
| Температура | |||
| • плавления | 1291 °C | ||
| Мол. теплоёмк. | 75,10 Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | −1510 кДж/моль | ||
| Удельная теплота испарения | (возгонка) 272 Дж/кг | ||
| Растворимость | |||
| • в воде | (при 0 °C) 0.56 (при 100 °C) 1.72 г/100 мл | ||
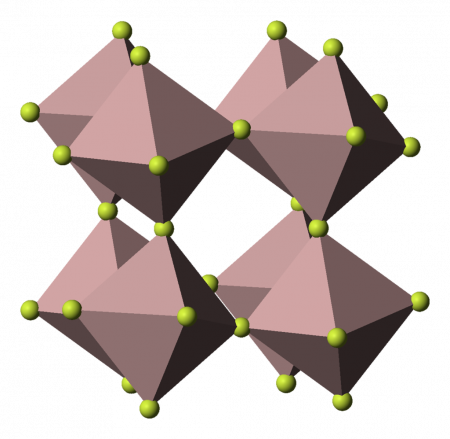
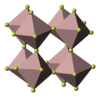
| Кристаллическая структура | ромбоэдрическая | ||
| Рег. номер CAS | |||
| RTECS | BD0725000 | ||
| ChEBI | 49464 | ||
| ChemSpider | 2039 | ||
| Предельная концентрация | 2 мг/м3 | ||
| ЛД50 | 100 мг/кг (крысы, орально) | ||
| Пиктограммы ECB |    | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Фторид алюминия — неорганическое бинарное соединение алюминия и фтора. Химическая формула AlF3.
Содержание
Физические свойства
Фторид алюминия представляет собой бесцветное или белое кристаллическое вещество. При сильном нагревании возгоняется без разложения. При обычных условиях устойчива α-модификация с тригональной решеткой (а = 0,5039 нм, α = 58,50°, z = 2, пространственная группа R32), плотность 2,882 г/см³. При нагревании до
700 °C переходит в γ-модификацию с тетрагональной решеткой (а = 0,354 нм, с = 0,600 нм).
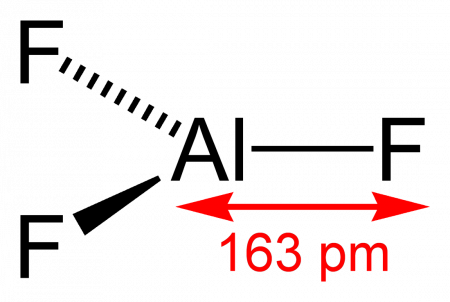
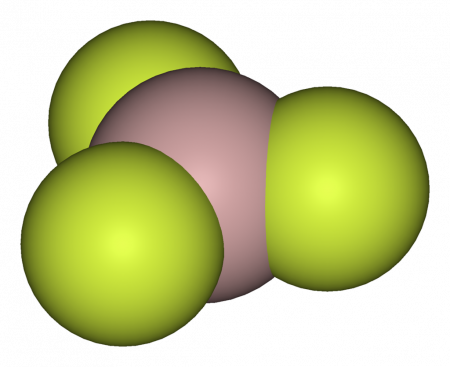
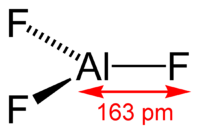
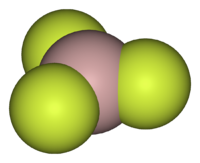
Длина связи Al—F составляет 0,163 нм. В газовой фазе, при температуре около 1000 °C, трифторид алюминия существует в виде молекул тригональной симметрии D3h.
Фторид алюминия плохо растворим в воде (0,41 % по массе при 25 °C), лучше — в растворах HF, не растворим в органических растворителях.
Получение
Взаимодействием Аl2O3 или Аl(ОН)3 с раствором HF с последующим выделением, сушкой и прокаливанием при 500-600 °C образовавшегося кристаллогидрата AlF3·3H2O:
Действием на Аl2O3 газообразного HF при 450-600 °C:
с последующем выделением, сушкой и прокаливанием гидрата.
При температуре в 700 °C гексафторсиликат натрия с алюминием дают на выходе чистый кремний, гексафторалюминат натрия и трифторид алюминия:
Самым легким путём получения трифторида алюминия является прямой контакт фтора с алюминием при температуре 600 °C:
2 Al + 3 F2 → 600oC 2 AlF3
Нагрев до температуры примерно 175 °C моногидрат трифторида алюминия получим воду и трифторид алюминия:
Для получения чистого безводного трифторида алюминия нужно гексафторалюминат аммония нагреть и получится трифторид алюминия с фторидом аммония:
В основном трифторид алюминия получают при обработке оксида алюминия гексафторсиликоновой кислотой, где на выходе получается оксид кремния IV, трифторид алюминия и вода:
Кроме того, он изготавливается путём термического разложения аммония гексафторалюмината.
Химические свойства
Образует кристаллогидраты с 1, 3 и 9 молекулами воды, которые легко разрушаются при нагревании:
При нагревании гидролизуется парами воды:
Медленно взаимодействует с концентрированной серной кислотой H2SO4:
Разлагается растворами и расплавами щелочей.
С фторидами щелочных металлов AlF3 образует фтороалюминаты, например, гексафтороалюминат натрия Na3[AlF6]:
Трифторид алюминия
| Трифторид алюминия | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Традиционные названия | трифторид алюминия, фторид алюминия, алюминия трифторид |
| Химическая формула | AlF3 |
| Физические свойства | |
| Состояние (ст. усл.) | белое твердое кристаллическое вещество без запаха |
| Молярная масса | (ангидрид) 83.9767 |
(тригидрат) 138.023 г/моль
(при 100 °C) 1.72 г/100 мл
Фторид алюминия — неорганическое бинарное соединение алюминия и фтора. Химическая формула AlF3.
Содержание
Физические свойства
Фторид алюминия представляет из себя бесцветное или белое кристаллическое вещество. При сильном нагревании возгоняется без разложения. При обычных условиях устойчива α-модификация с тригональной решеткой (а = 0,5039 нм, α = 58,50°, z = 2, пространственная группа R32), плотность 2,882 г/см³. При нагревании до
700 °C переходит в γ-модификацию с тетрагональной решеткой (а = 0,354 нм, с = 0,600 нм).
Длина связи Al—F составляет 0,163 нм. В газовой фазе, при температуре около 1000 °C, трифторид алюминия существует в виде молекул тригональной симметрии D3h.
Фторид алюминия плохо растворим в воде (0,41 % по массе при 25 °C), лучше — в растворах HF, не растворим в органических растворителях.
Получение
Взаимодействием Аl2О3 или Аl(ОН)3 с раствором HF с последующим выделением, сушкой и прокаливанием при 500-600 °C образовавшегося кристаллогидрата AlF3·3H2O:
Действием на Аl2О3 газообразного HF при 450-600 °C:
с последующем выделением, сушкой и прокаливанием гидрата.
При температуре в 700 °C гексафторсиликат натрия с алюминием дают на выходе чистый кремний, гексафторалюминат натрия и трифторид алюминия:
Самым легким путем получения трифторида алюминия является прямой контакт фтора с алюминием при температуре 600 °C:
Нагрев до температуры примерно 175 °C моногидрат трифторида алюминия получим воду и трифторид алюминия:
Для получения чистого безводного трифторида алюминия нужно гексафторалюминат аммония нагреть и получится трифторид алюминия с фторидом аммония:
В основном трифторид алюминия получают при обработке оксида алюминия гексафторсиликоновой кислотой, где на выходе получается оксид кремния(IV), трифторид алюминия и вода:
Кроме того, он изготавливается путем термического разложения аммония гексафторалюмината.
Химические свойства
Образует кристаллогидраты с 1, 3 и 9 молекулами воды, которые легко разрушаются при нагревании:
При нагревании гидролизуется парами воды:
Разлагается растворами и расплавами щелочей.
Алюминия фторид
Смотреть что такое «Алюминия фторид» в других словарях:
АЛЮМИНИЯ ФТОРИД — AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для получения и очистки алюминия … Большой Энциклопедический словарь
алюминия фторид — AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для получения и очистки алюминия. * * * АЛЮМИНИЯ ФТОРИД АЛЮМИНИЯ ФТОРИД, AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для… … Энциклопедический словарь
алюминия фторид — aliuminio fluoridas statusas T sritis chemija formulė AlF₃ atitikmenys: angl. aluminium fluoride; aluminium trifluoride rus. алюминий трехфтористый; алюминий фтористый; алюминия фторид ryšiai: sinonimas – aliuminio trifluoridas … Chemijos terminų aiškinamasis žodynas
АЛЮМИНИЯ ФТОРИД — A1F3, бесцв. кристаллы. При обычных условиях устойчива модификация с тригон. решеткой ( а =0,5039 нм, 58,50 … Химическая энциклопедия
Фторид брома(I) — Фторид брома(I) … Википедия
Фторид брома(V) — (пентафторид брома) BrF5 соединение брома с фтором, представляющее собой при комнатной температуре легкоиспаряющуюся жидкость светло жёлтого цвета, с сильным раздражающим запахом, и чрезвычайно высокой химической активностью и… … Википедия
Фторид магния — Общие Систематическое наименование Фторид магния Традиционные названия Фтористый магний Химическая формула MgF2 Физические свойства Состояние ( … Википедия
Фторид кислорода(II) — Фторид кислорода(II) … Википедия
Фторид лития — Общие … Википедия
Фторид иода(I) — (монофторид иода) IF соединение иода с фтором, представляющее собой при комнатной температуре жидкость жёлтого цвета с сильным раздражающим, запахом похожим на запах трифторида иода. Содержание 1 Физические свойства 2 Химические свойства … Википедия
АЛЮМИНИЯ ФТОРИД
A1F3, бесцв. кристаллы. При обычных условиях устойчива 

Смотреть что такое «АЛЮМИНИЯ ФТОРИД» в других словарях:
АЛЮМИНИЯ ФТОРИД — AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для получения и очистки алюминия … Большой Энциклопедический словарь
алюминия фторид — AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для получения и очистки алюминия. * * * АЛЮМИНИЯ ФТОРИД АЛЮМИНИЯ ФТОРИД, AlF3, бесцветные кристаллы. Плохо растворяется в воде. Входит в состав электролита для… … Энциклопедический словарь
алюминия фторид — aliuminio fluoridas statusas T sritis chemija formulė AlF₃ atitikmenys: angl. aluminium fluoride; aluminium trifluoride rus. алюминий трехфтористый; алюминий фтористый; алюминия фторид ryšiai: sinonimas – aliuminio trifluoridas … Chemijos terminų aiškinamasis žodynas
Алюминия фторид — фтористый алюминий, AIF3, соль, бесцветные кристаллы, плотность 3100 кг/м2. При нагревании возгоняется без плавления. В воде очень мало растворим (0,559 г в 100 г H2O при 25°С), со щелочами и кислотами (кроме кипящей серной) не реагирует … Большая советская энциклопедия
Фторид брома(I) — Фторид брома(I) … Википедия
Фторид брома(V) — (пентафторид брома) BrF5 соединение брома с фтором, представляющее собой при комнатной температуре легкоиспаряющуюся жидкость светло жёлтого цвета, с сильным раздражающим запахом, и чрезвычайно высокой химической активностью и… … Википедия
Фторид магния — Общие Систематическое наименование Фторид магния Традиционные названия Фтористый магний Химическая формула MgF2 Физические свойства Состояние ( … Википедия
Фторид кислорода(II) — Фторид кислорода(II) … Википедия
Фторид лития — Общие … Википедия
Фторид иода(I) — (монофторид иода) IF соединение иода с фтором, представляющее собой при комнатной температуре жидкость жёлтого цвета с сильным раздражающим, запахом похожим на запах трифторида иода. Содержание 1 Физические свойства 2 Химические свойства … Википедия