Genetic code жидкость
Genetic code жидкость
| Крепость | 45 мг/мл, Salt |
| Объем | 30 мл |
| Бренд | GENETIC CODE от Glitch Sauce |
| VG/PG | 50/50 |
| Качество | 100 % оригинал |
| Возрастное ограничение | 18+ |
| Состав | Пищевой глицерин, пищевой пропиленгликоль, пищевой ароматизатор. Никотин (в безникотиновых нет) |
| Срок годности | 24 месяца |
| Импортер в РБ | Частное предприятие «ВипМаг». 223610, Минская обл., г. Слуцк, ул. Социалистическая, д.176, кв.22 |
| Предостережение | Не употреблять несовершеннолетним, женщинам во время беременности и в период лактации, внутрь. |
| Условия хранения | Хранить в темном прохладном месте, при температуре до +25°С, недоступном для детей и животных. |
| Производство: | Россия |
| Изготовитель | GLITCH SAUCE |
| Контроль качества | Нет информации |
| Сервисный центр | Частное предприятие «ВипМаг». УНП 690765092. Юр. адрес: 223610, Минская обл., г. Слуцк, ул. Социалистическая, д.176, кв.22. Фактический адрес: г. Минск, ул. Суражская, 4. |
| Гарантия | 2 месяца |
Отзывы на жидкость GENETIC CODE SALT Mulberry-Kiwi-Guava
Характеристики
Характеристики
| Крепость | 45 мг/мл, Salt |
| Объем | 30 мл |
| Бренд | GENETIC CODE от Glitch Sauce |
| VG/PG | 50/50 |
| Качество | 100 % оригинал |
Официальная информация
| Возрастное ограничение | 18+ |
| Состав | Пищевой глицерин, пищевой пропиленгликоль, пищевой ароматизатор. Никотин (в безникотиновых нет) |
| Срок годности | 24 месяца |
| Импортер в РБ | Частное предприятие «ВипМаг». 223610, Минская обл., г. Слуцк, ул. Социалистическая, д.176, кв.22 |
| Предостережение | Не употреблять несовершеннолетним, женщинам во время беременности и в период лактации, внутрь. |
| Условия хранения | Хранить в темном прохладном месте, при температуре до +25°С, недоступном для детей и животных. |
| Производство: | Россия |
| Изготовитель | GLITCH SAUCE |
| Контроль качества | Нет информации |
В наличии
Указанные на данном сайте контакты также являются контактами для связи по вопросам обращения покупателей о нарушении их прав.
Номер телефона работников местных исполнительных и распорядительных органов по месту государственной регистрации ЧП»ВипМаг»,
уполномоченных рассматривать обращения покупателей: +375 17 95 75055.
В интернет-магазине присутствует продукция с возрастным ограничением «18+». Смотрите отметку в характеристиках товара.
Указанные на данном сайте контакты также являются контактами для связи по вопросам обращения покупателей о нарушении их прав.
Номер телефона работников местных исполнительных и распорядительных органов по месту государственной регистрации ЧП»ВипМаг»,
уполномоченных рассматривать обращения покупателей: +375 17 95 75055.
В интернет-магазине присутствует продукция с возрастным ограничением «18+». Смотрите отметку в характеристиках товара.
AZF фактор и мужское бесплодие
Мужское бесплодие может быть спровоцировано самыми разными факторами, в том числе неполадками с Y-хромосомой. Давайте выясним, почему они возникают, как влияют на репродуктивную функцию и можно ли в этом случае добиться успешного зачатия.
Что такое половые хромосомы?
У каждого человека есть 46 хромосом, составляющих 23 пары. И если в 22-х парах они практически идентичны, то в последней имеются серьезные различия. Речь идет о хромосомах, которые регулируют пол человека.
У женщин присутствуют 2 хромосомы X (XX), у мужчин – одна X-хромосома и одна Y-хромосома (XY). Собственно, именно наличие Y-хромосомы и обусловливает развитие организма по мужскому типу.
Сперматогенез и дефекты Y-хромосомы
Сперматогенезом называют процесс образования и созревания мужских половых клеток. Процесс этот, как и все остальные, происходящие в организме, регулируется генами, которые расположены на хромосомах. Если гены имеют дефекты, качество эякулята ухудшается.
Особенно сильно снижается оплодотворяющая способность спермы при наличии делеций, то есть при утрате участков хромосом и, как следствие, некоторых генов, играющих большую роль в регуляции сперматогенеза. Тяжесть нарушений может различной: от олигозооспермии (значительного сокращения числа половых клеток) до азооспермии (полного их отсутствия в семенной жидкости).
Что такое AZF?
Участок мужской хромосомы, где содержатся гены, ответственные за сперматогенез, называют регионом (локусом) AZF.
AZF-регион включает 3 субрегиона (AZFa, AZFb и AZFс), содержащие гены, мутации в которых приводят либо к значительному снижению концентрации, либо к полному отсутствию сперматозоидов в эякуляте.
На изображении, размещенном ниже, представлена Y-хромосома, имеющая дефекты в локусе AZF.
Микроделеции (потери мелких фрагментов хромосомы) локуса AZF становятся причиной:
Впервые догадку о том, что мужское бесплодие может иметь генетические причины, высказали еще в середине 70-х годов прошлого века. Сделали это итальянские специалисты, которые в ходе исследований обнаружили, что у пациентов с диагностированной азооспермией отсутствует определенный участок Y-хромосомы. Ученые предположили, что именно там располагаются гены, ответственные за сперматогенез, и назвали этот регион AZF (azoospermia factor). Впоследствии, когда были разработаны молекулярные методы диагностики, эта гипотеза подтвердилась.
Часто ли диагностируют AZF-делеции?
Согласно представленным в медицинской литературе данным, нарушения в локусе AZF могут быть обнаружены более чем у 7% пациентов с репродуктивной дисфункцией. У мужчин с диагностированной азооспермией и олигозооспермией тяжелой степени наличие делеций выявляется в среднем в 10-15% случаев. Таким образом, значительное снижение концентрации сперматозоидов всегда должно служить поводом для генетического обследования.
Почему появляются такие нарушения?
Мужская хромосома имеет тенденцию к появлению случайных мутаций, поэтому в большинстве случаев такие дефекты имеют спонтанный характер.
Как проводится диагностика?
Чтобы обнаружить поломки в Y-хромосоме, нужно сдать кровь из вены. Специалисты исследуют структуру AZF-региона, используя метод полимеразной цепной реакции (ПЦР).
Почему важно обнаружить генетические нарушения?
Во-первых, генетическую причину снижения фертильности важно сразу выявить потому, что ее нельзя скорректировать. Как следствие, пациенту не придется тратить время, силы и средства на лечение.
Во-вторых, выявление делеций в том или ином субрегионе позволяет разработать оптимальную тактику. Так, при делеции AZFa получить сперматозоиды невозможно в принципе, в то время как при делеции AZFc шанс обнаружить половые клетки остается.
Кроме того, в случае успешного преодоления бесплодия диагностика дает возможность определить риск передачи делеции от отца к сыну.
Что делать, если обнаружена мутация AZF?
Использование вспомогательных репродуктивных технологий (метода ЭКО-ИКСИ) в ряде случаев позволяет добиться зачатия и рождения ребенка. Однако, как мы отметили выше, есть вероятность, что у сына могут быть такие же генетические нарушения и, как следствие, снижение фертильности.
На этапе подготовки к программе ЭКО всем пациентам с олигозооспермией тяжелой степени (менее 5 миллионов сперматозоидов в 1 миллилитре эякулята) или азооспермией показаны исследование на наличие микроделеций в Y-хромосоме и консультация генетика.
Если в результате обследования выявлена делеция AZFc, шансы на получение половых клеток, пригодных для использования в программе ЭКО-ИКСИ, составляют порядка 70%. При этом успех во многом зависит от квалификации и практического опыта эмбриолога и хирурга. Полученные клетки криоконсервируют (замораживают и хранят при сверхнизких температурах). Шансы на успешное оплодотворение и имплантацию эмбрионов у пациентов с делециями или без них примерно равны.
Если выявлены делеции AZFa или AZFb, обнаружить сперматозоиды не получится.
Специалисты Нова Клиник на протяжении многих лет занимаются диагностикой и лечением различных форм бесплодия, в том числе при наличии генетического фактора. Наши врачи обязательно сделают все возможное для того, чтобы вы смогли стать родителями.
Генетические тесты: как это работает и когда они нужны
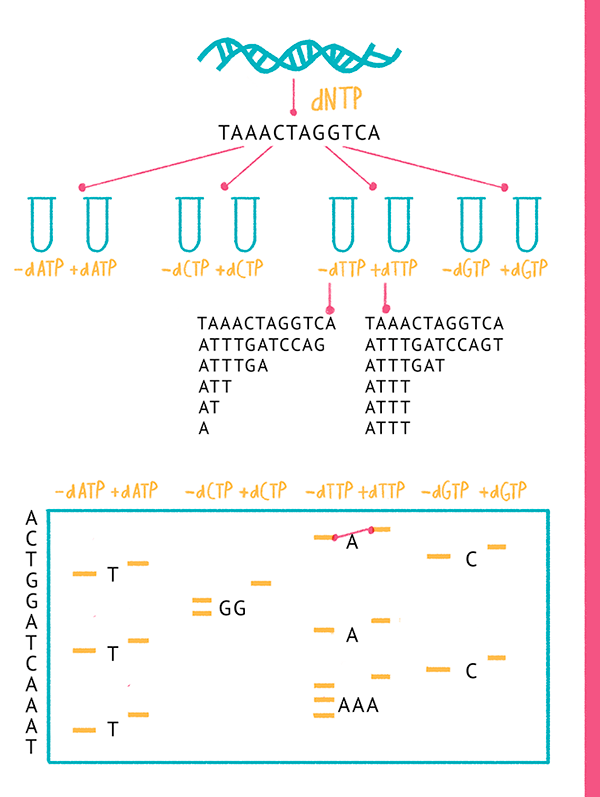
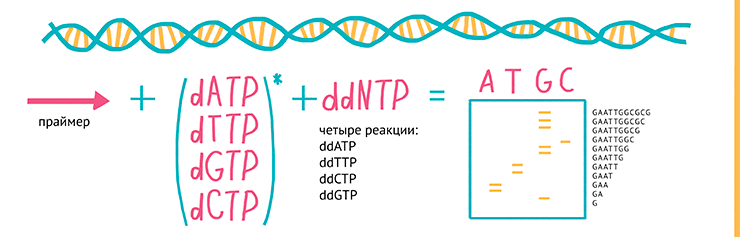
Любой генетический анализ — расшифровка ДНК человека и интерпретация результатов — состоит из нескольких этапов. Генетический материал берут из клеток: раньше работали с кровью, теперь лаборатории все больше переходят на неинвазивные методы и выделяют ДНК из слюны.
Выделенный материал секвенируют — с помощью химических реакций и анализаторов определяют то, в какой последовательности в нем расположены мономеры: это и есть генетический код. Полученную последовательность сравнивают с эталонными и ищут определенные участки, соответствующие тем или иным генам. На основании наличия или отсутствия генов или их изменения и делают заключение о результате теста.
Запуск секвенатора — прибора, который расшифровывает последовательность ДНК, — стоит очень дорого из-за большого количества необходимых химических реактивов. За один запуск можно расшифровать много образцов ДНК, но чем их будет больше, тем менее достоверным получится результат для каждого образца и тем ниже окажется точность генетического теста. Поэтому следует обращаться в проверенную лабораторию, которая не станет экономить на качестве анализа путем увеличения количества образцов.
Важный момент, который стоит учитывать при получении результатов генетического анализа: генетика определяет далеко не все, что происходит с нашим организмом. Не менее существенную роль играют образ жизни и факторы окружающей среды — экологическая обстановка, климат, количество солнечного света и другие.
К сожалению, российские компании редко упоминают об этом и ограничиваются перечислением преимуществ генетического теста. Многие также играют на необразованности пациентов и навязывают дорогостоящие лишние анализы.
Вот основные случаи, для которых применяются современные генетические анализы.
В первую очередь генетика призвана помочь в лечении и профилактике болезней. Есть три основных группы случаев, когда генетический анализ поможет уточнить диагноз или предотвратить возможное заболевание.
Диагностика вирусов и бактерий по наличию их ДНК в крови
Для кого тест. Для тех, кто подозревает у себя вирусную или бактериальную инфекцию. Так, например, могут диагностировать боррелиоз при укусе клеща — болезнь с широким спектром симптомов.
Как это работает. ДНК организмов, вызывающих болезни, отличается от человеческой. У пациента берут анализ крови и определяют, есть ли там чужеродный генетический материал.
Что важно учитывать. Это относительно недорогие анализы, ведь здесь не требуется расшифровка самой ДНК, нужно определить просто ее наличие или отсутствие. Такой тест будет более точным, чем, например, поиск антител (они появляются в крови только после инкубационного периода), но возможен он лишь при подозрении на конкретное заболевание.
Диагностика уже имеющихся заболеваний
Для кого тест. Как правило, это сложные случаи или хронические недуги, причина которых неочевидна. Тогда врачи ищут возможные причины болезни в генах и на основе результатов могут точнее поставить диагноз и скорректировать лечение.
Как это работает. Генетический материал могут получать из любых клеток пациента, в том числе из материала, взятого для других анализов. После расшифровки ДНК в последовательности ищут поврежденные гены. Как правило, это не поиск «вслепую» по всей длине, а исследование заранее известных участков.
Что важно учитывать. Генных болезней — тех, которые происходят по вине мутаций всего одного гена, — довольно мало. Около 92% заболеваний, причину которых можно найти в ДНК, являются многофакторными. Это значит, что мутация не единственная причина болезни, и корректировка других факторов, например питания или климата, может облегчить ее течение.
Профилактика заболеваний, к которым есть предрасположенность
Для кого тест. Такой анализ врачи могут посоветовать здоровым людям, у которых среди родственников были неоднократные случаи различных болезней, таких как, например, большинство видов рака, сахарный диабет и ишемическая болезнь сердца. То есть тех самых многофакторных наследственных заболеваний, которые также называют «полигенными с пороговым эффектом». Еще подобный анализ может выявить вероятность развития аллергии, помочь скорректировать диету в зависимости от генетической основы обмена веществ и подобрать оптимальные физические нагрузки.
Как это работает. Помимо мутаций врачи также могут обращать внимание на вариации гена — аллели. При проверке предрасположенностей к определенным заболеваниям анализируют конкретный участок ДНК. Комплексное обследование на ряд потенциальных наследственных болезней может задействовать весь геном.
Что важно учитывать. Указанные болезни не зря называют «с пороговым эффектом». Это значит, что болезнь разовьется только после достижения организмом «порога». Задача профилактики как раз в том, чтобы этого не допустить. То есть положительный тест на предрасположенность к раку груди вовсе не означает, что это стопроцентно произойдет. Такой результат скорее служит рекомендацией относиться к себе внимательнее, избегать факторов риска и не пренебрегать регулярными обследованиями у маммолога.
Когда люди хотят завести ребенка, они волей-неволей задумываются о его будущем здоровье. Генетические анализы могут помочь на двух этапах — при планировании беременности и в ходе ее течения.
Для кого тест. Такой тест поможет выяснить, не унаследует ли ребенок «спящие мутации» и риски врожденных патологий. Это важно при частых случаях каких-то заболеваний в семейном анамнезе отца и/или матери либо при фактическом наличии у кого-то из родителей болезни.
Как это работает. По своей сути такие тесты не отличаются от выявления предрасположенностей к болезням у взрослых, но анализируют одновременно два родительских генома.
Что важно учитывать. Сложность анализа заключается в том, что нельзя заранее выяснить, какие именно гены родителей достанутся ребенку, это некая лотерея. Гены всегда работают не сами по себе, а в комплексе, что делает число вариаций генома будущего ребенка бесконечным. То есть тест на наследственность планируемого потомства всегда вероятностный, и даже наличие у родителей «плохих» мутаций не делает рождение здорового малыша невозможным.
Для кого тест. Этот анализ проводится во время беременности и нужен при подозрении на врожденные патологии. Также пренатальная генетическая диагностика может определить пол будущего ребенка на ранней стадии беременности и установить отцовство.
Как это работает. Для пренатальной диагностики есть несколько методов взятия образца генетического материала, главными из которых являются биопсия хориона (взятие кусочка ткани зародыша) и амниоцентез (взятие образца околоплодных вод). В последнее время также практикуется выделение ДНК эмбриона из крови матери — неинвазивный пренатальный ДНК-тест (НИПТ). При экстракорпоральном оплодотворении возможна также преимплантационная диагностика — ДНК выделяют из клетки зародыша до его внедрения в матку.
Что важно учитывать. Инвазивные методы — это всегда риск. Так, вероятность самопроизвольного прерывания беременности после биопсии доходит до 15%, а амниоцентез может привести к заражению или отслоению оболочек плода. Оба этих метода становятся возможными на относительно позднем сроке беременности, когда формируется плодный пузырь и хорошо различимый на УЗИ зародыш, поэтому прибегать к ним стоит только при серьезных подозрениях на генные или хромосомные дефекты. Неинвазивная диагностика не имеет таких последствий, и ее можно проводить начиная с девятой недели беременности.
Определение талантов и склонностей
Для кого тест. Нередко компании, проводящие генетические тесты, также предлагают родителям выявить предрасположенность детей к определенным видам спорта или другим занятиям. Такой тест может быть полезен для юных спортсменов перед началом серьезной карьеры: по мнению исследователей, спортивная успешность на 60% определяется генами.
Как это работает. Сам анализ проводится так же, как и для определения наследственных болезней, только исследуются другие участки ДНК. К настоящему времени известно около 50 генов, которые связывают с предрасположенностью к занятиям различными видами спорта. С другими талантами человека сложнее: например, установлена частичная генетическая природа абсолютного слуха, но по большей части это направление находится на стадии изучения.
Что важно учитывать. Несмотря на широко распространенное мнение, что наши гены предписывают нам определенные таланты и черты характера, генные основы психики — самая малоисследованная область в генетике человека. Не только болезни могут быть полигенными — таково большинство признаков в организме (например, цвет глаз определяется 15 генами). Вырванная из контекста информация может оказаться не только неполной, но и в принципе ложной: по одному гену нельзя определить, станет ребенок выдающимся спортсменом или нет. То, что касается интеллектуальных способностей и особенностей характера, до сих пор лежит в области предположений. Наконец, если результат генетического теста «предсказывает» ребенку успех в какой-то стезе, это может оказать психологическое давление на родителей и помешать ребенку самому определиться с планами на будущее. Гены — рекомендация, а не прямое указание.
Для кого тест. Генеалогические исследования выросли из криминалистики и популярной задачи установления отцовства. Сегодня при помощи генетики доступно как определение ближайших родственников, так и выяснение предковой группы — из какой части света произошел род много поколений назад. Такой анализ служит для решения прикладных задач установления родства (это важно для таких юридических моментов, как претензии на наследство) и может заинтересовать просто любознательных людей, изучающих семейную историю.
Как это работает. В ходе жизни у каждого человека накапливаются маленькие изменения в ДНК — не только в генах, но и в «нерабочей» части (а доля такой в наших клетках — больше 90%). При генеалогическом генетическом анализе исследователи сравнивают полученную ДНК на предмет сходства с другими — либо с ДНК потенциальных родственников, либо с большой базой данных. В такие базы могут входить как древние ДНК, так и генетический материал жителей страны. В зависимости от страны и доступа генетической лаборатории к базам данных картина анализа может различаться по полноте и подробности.
Что важно учитывать. В отличие от предыдущих анализов, когда ДНК пациента сравнивалась с эталоном, здесь речь идет о сравнении с генетическим материалом других людей. Такая процедура затрагивает вопросы конфиденциальности и нуждается в сложной законодательной регуляции. В Исландии собрана генетическая база данных, в которую занесены расшифрованные ДНК всех граждан и постоянных жителей (соответствующий закон был принят 1997 году). В России подобная практика только начинает появляться, для экспертизы на родство требуется согласие всех участников и сложная юридическая процедура. Впрочем, «древние» базы данных по всему миру находятся в открытом доступе, и любой желающий может узнать о своих корнях. Например, здесь, здесь и здесь.
Экспресс-тест на коронавирус SARS-CoV-2-антиген : инструкция по применению
Назначение
Характеристика и принцип работы
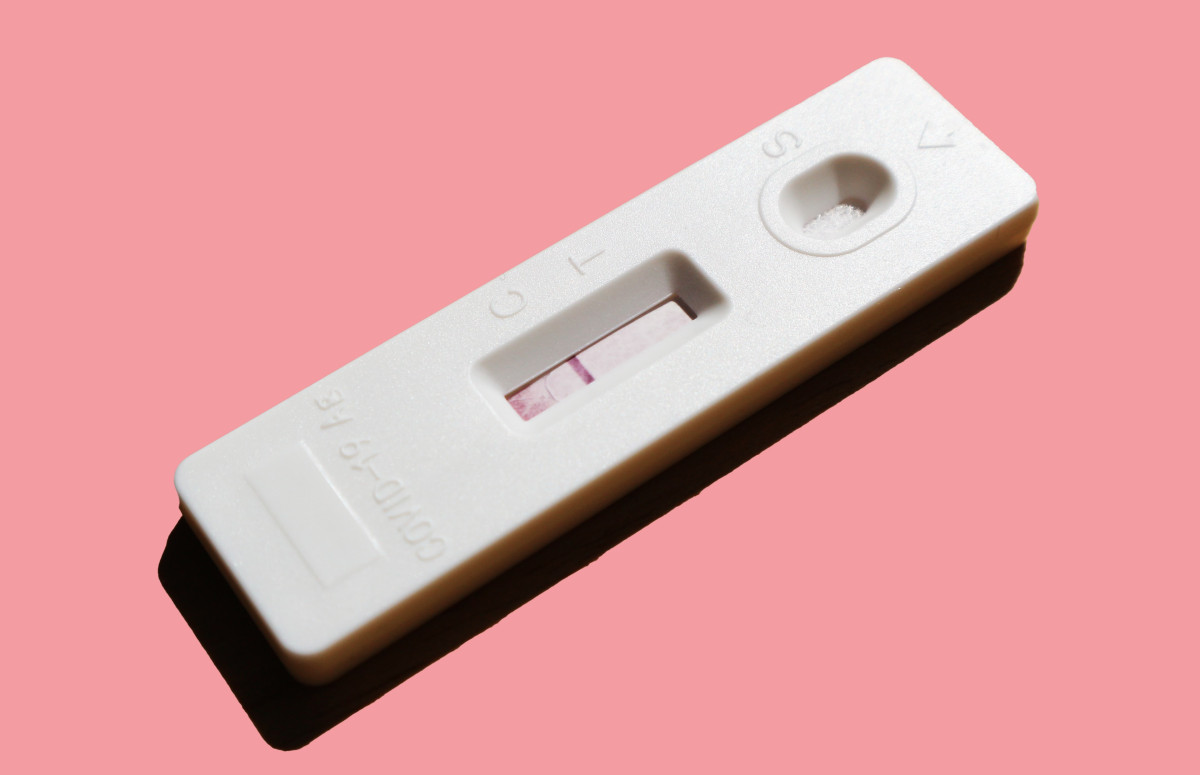
2.1 Высокая скорость и простота использования иммунохроматографического анализа обеспечивается благодаря предварительному нанесению аналитических реагентов на мембрану тестовой кассеты. Контакт с пробой запускает иммунохимические реакции, приводящие к окрашиванию определенных участков мембранной полоски, по которому можно через 10 мин визуально регистрировать результат анализа.
2.2 Экспресс-тест предназначен для обнаружения присутствия или отсутствия нуклеокапсидного белка вируса SARS-CoV-2 в образцах мазков, взятых из носоглотки пациентов, подозреваемых на COVID-19, при наличии соответствующих признаков и симптомов. Когда образцы обрабатываются и добавляются в тестовое устройство, антигены вируса SARS-CoV-2, присутствующие в образце, связываются с антителами, меченными коллоидным золотом на тест-полоске. Комплексы антиген-антитело перемещаются по тест- полоске в зону реакции и захватываются линией антител, связанных на мембране.
2.3 Результат считается положительным, когда комплексы антиген-антитело, осажденные в позиции теста «Т», и контрольная позиция «С» на тестовом устройстве образуют цветные линии.
Результат считается отрицательным, когда цветная линия образуется только в позиции контроля «C», но не появляется видимая цветная линия в позиции теста «T».
2.4 Для контроля качества, чтобы гарантировать достоверность результата теста, цветная линия всегда должна появляться в позиции контроля «C», независимо от того, появляется ли результат (положительный или отрицательный) в позиции теста «T». Если в контрольной позиции «C» нет видимой линии, результат экспресс-теста считается недействительным, и необходимо провести новый тест.
Состав
Меры предосторожности при работе с экспресс-тестом
3.1 Использовать экспресс-тест необходимо в строгом соответствии с инструкцией.
3.2 Этот экспресс-тест предназначен только для диагностики in vitro.
3.3 Со всеми образцами следует обращаться как с биомедицинскими отходами, содержащими потенциально инфекционные вещества. Процесс утилизации использованного экспресс-теста и материалов для образцов должен соответствовать местным законам об утилизации инфекционных веществ или лабораторным нормам.
3.4 Надевайте соответствующие средства индивидуальной защиты (например, халат, перчатки, очки, маску) при использовании экспресс-теста. Работы проводить с соблюдением мер предосторожности в соответствии с требованиями.
3.5 Правильный сбор, хранение и транспортировка образцов имеют решающее значение для выполнения этого теста.
3.6 После использования тестовую кассету необходимо утилизировать. Тест нельзя использовать более одного раза.
3.7 Не прикасайтесь к реакционной зоне тестовой кассеты.
3.8 Не используйте экспресс-тест после истечения срока годности.
3.9 Не используйте тестовую кассету, если пакет проколот или если его герметичность нарушена.
3.10 Тестирование должно проводиться специально обученным медицинским персоналом. Образцы также берутся квалифицированным медицинским персоналом.
3.11 Результат теста должен интерпретироваться врачом или обученным медицинским специалистом вместе с клиническими данными и результатами других лабораторных тестов.
3.12 Со всеми образцами и использованными экспресс-тестами следует обращаться как с биомедицинскими отходами, содержащими потенциально инфекционные вещества.
3.13 Результаты должны быть прочитаны сразу же по истечению 10 минут после введения образца в отверстие для образцов тест-кассеты. Результаты теста станут недействительными через 20 минут.
3.14 При взятии мазка из носоглотки используйте тампоны, входящие в комплект. Использование других тампонов может привести к ложноотрицательным результатам.
3.15 Перед использованием проверьте срок годности и целостность упаковки тестовой кассеты. Если упаковка тестовой кассеты повреждена и срок годности истек, его нельзя использовать.
3.16 Необходимо соблюдать время тестирования и считывания результатов.
3.17 После вскрытия пакета с тестовой кассетой, анализ следует провести в течение 60 мин. Тестовую кассету можно использовать только один раз.
3.18 Экспресс-тест должен храниться при температуре (2-30) °С. Беречь от влаги, прямых солнечных лучей, тепла и холода.
3.19 Результаты анализа предназначены для предварительной клинической оценки. Клинический диагноз заболевания следует рассматривать в сочетании с симптомами и признаками заболевания, историей болезни пациента, другими лабораторными тестами и ответом на лечение.
Сбор и подготовка образцов
4.1 Настройка теста
Перед использованием экспресс-теста пакет с тестовой кассетой и буферный раствор должны быть доведены до комнатной температуры (18-25) °С.
Извлеките из пакета тестовую кассету непосредственно перед тестированием.
Пометьте тестовую кассету и экстракционную пробирку для каждого исследуемого образца. Поместите промаркированные экстракционные пробирки в штатив.
Снимите крышку с флакона с буфером для экстракции образца, держите флакон вверх дном. Сожмите флакон и добавьте 7 капель (
210 мкл) буферного раствора в пробирку для экстракции. При индивидуальном использовании экспресс-теста отобрать пипеткой Пастера буферный раствор из пробирки и добавить 9 капель (
210 мкл) в пробирку для экстракции.
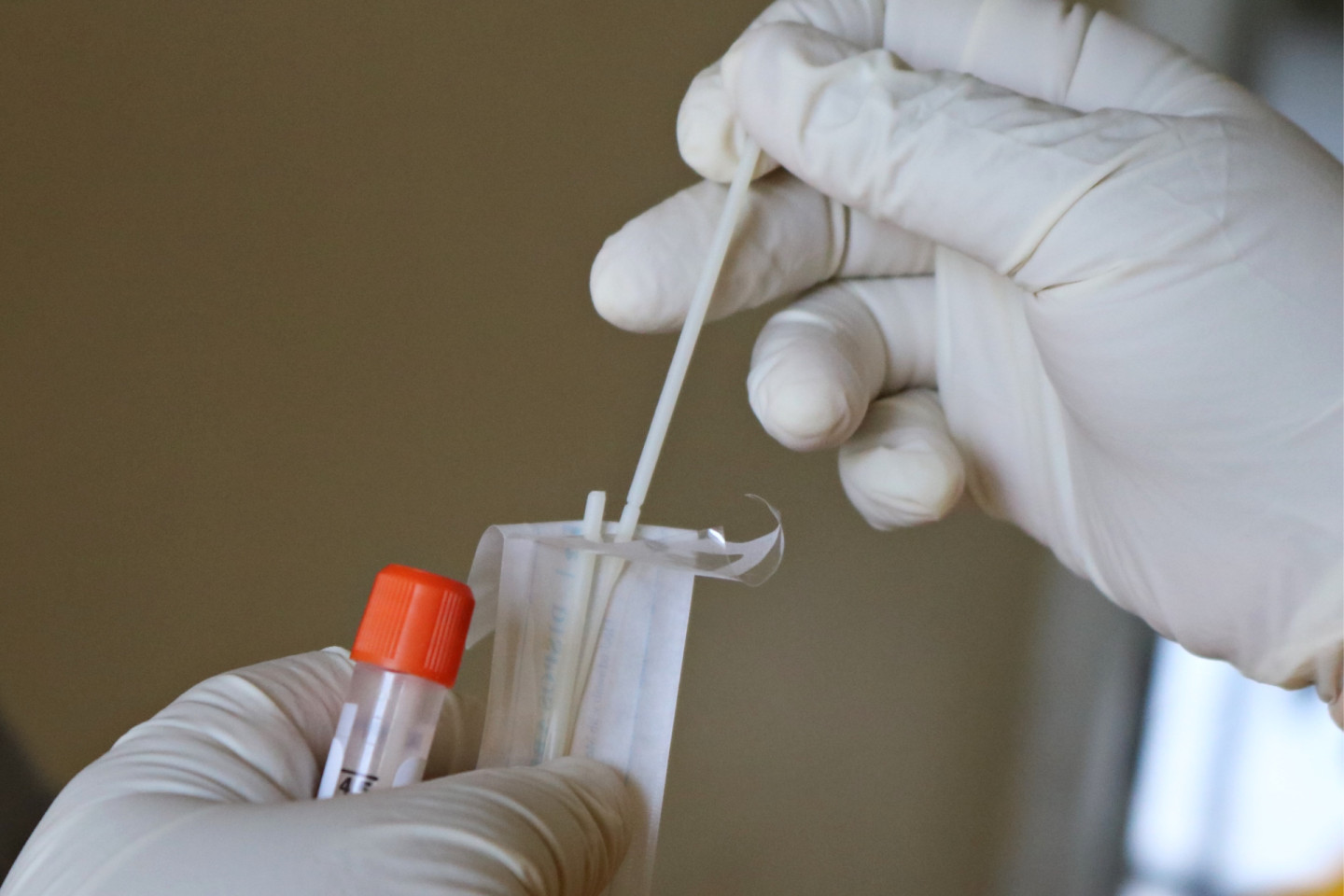
4.2 Сбор образцов мазков из носа
Чтобы взять мазок из носа, осторожно вставьте тампон для взятия образцов в ноздрю с наибольшей секрецией при визуальном осмотре. Плавным вращением проталкивайте тампон до сопротивления на уровне носовых раковин (около 2,0-2,5 см вглубь ноздри). Прокрутите тампон 5 раз по стенке носа, затем выньте его из ноздри.
4.3 Подготовка образца
После взятия пробы немедленно погрузите тампон в буфер. Чтобы образец, извлеченный из тампона, полностью проник в буфер, 6 раз поверните тампон по стенке пробирки в течение 20 секунд, оставьте тампон в пробирке на 1 минуту, а затем пальцами, удерживая пробирку (стенка пробирки не твердая), несколько раз сожмите тампон, при этом медленно удаляйте его из пробирки. Прижатие тампона к стенке пробирки очень важно, так как при этом образца, содержащего жидкость, остается в пробирке как можно больше. Вынув тампон и выбросив его в контейнер для биологически опасных отходов, плотно наденьте насадку (входит в комплект) на верхнюю часть экстракционной пробирки и осторожно встряхните ее, чтобы качественно перемешать находящуюся внутри жидкость.
Процедура анализа
5.1 Удерживая экстракционную пробирку вертикально вверх дном. Сожмите ее и через насадку для экстракционной пробирки добавьте 3 капли (около 70-90 мкл) подготовленной ранее жидкости с образцом в центр лунки для образца (S-лунка), убедившись, что в ней нет пузырьков воздуха.
5.2 Запустите таймер. Считайте результат через 10 минут. Не более чем через 20 минут.
Учет и интерпретация результатов
6.1 Положительный результат: как в позиции теста «T», так и в контрольной позиции «C» появляются видимые цветные линии. Если тестовая позиция «Т» имеет бледный цвет, результат также считается положительным (рисунок 2).
6.2 Отрицательный результат: цвет отображается только в контрольной позиции «C», а в позиции теста «T» окраски нет.
6.3 Недействительный результат: если контрольная позиция «C» остается без появления цвета, результат теста считается недействительным, поскольку контрольное обнаружение не сработало. В таком случае требуется повторное исследование образца.
6.4 Ограничения исследования
6.4.1 Этот экспресс-тест предназначен для обнаружения наличия или отсутствия антигенов к SARS-CoV-2 в респираторных образцах, взятых у лиц, имеющих контакт с COVID-19, или у лиц при наличии соответствующих признаков и симптомов заболевания в первые 7 дней.
6.4.2 Этот экспресс-тест представляет собой качественный анализ.
6.4.3 Точность анализа зависит от качества взятия пробы. Неправильный сбор образцов, их неправильное хранение повлияют на результат теста.
6.4.4 Результаты этого экспресс-теста предназначены для предварительной клинической оценки. Подтвержденный диагноз может быть установлен только после оценки всех клинических и лабораторных данных.
6.4.5 Из-за ограничений, которые имеет экспресс-тест для обнаружения антигенов, при отрицательных результатах тестирования рекомендуется использовать тест амплификации нуклеиновых кислот или методы идентификации вирусных культур для проверки и подтверждения результатов.
6.4.6 Положительные результаты анализов не исключают коинфицирование другими вирусами. Отрицательный результат этого экспресс-теста может быть вызван:
1) неправильным сбором образцов, неправильной передачей или использованием образцов;
2) уровень вируса SARS-CoV-2 ниже предела обнаружения теста;
3) вариации вирусных генов, которые могли вызвать изменения в детерминантах антигена.
Аналитические характеристики экспресс-теста
7.1 Чувствительность экспресс-теста SARS-CoV-2-Антиген: 97,8%, в сравнении с тестом на нуклеиновую кислоту, были подтверждены положительные случаи.
7.2 Специфичность набора: 100 %, отрицательные случаи были также подтверждены тестом на нуклеиновую кислоту.
7.3 Воспроизводимость экспресс-теста SARS-CoV-2-Антиген: межсерийная 97%, внутрисерийная 99%.
7.4 Перекрёстная специфичность: перекрестная специфичность с вирусом гриппа A, вирусом гриппа B, аденовирусом, вирусом Коксаки, вирусом ECHO и энтеровирусом отсутствует; отсутствует перекрестная специфичность с Chlamydia pneumoniae, Mycoplasma pneumoniae, Chlamydia psittaci и Chlamydia trachomatis; отсутствует перекрестная специфичность с Acinetobacter baumannii, Bordetella pertussis, Candida albicans, Escherichia coli, Haemophilus influenzae и Neisseria gonorrhoeae.
Условия хранения и применения экспресс-теста
ДНК-тест на состояние здоровья организма MyWellness
Общие рекомендации не работают?
Не пить кофе, отказаться от сладкого и соленого, вместо бокала вина в компании друзей — прогулки с эспандером. И еще тысяча ограничений?
Давайте уточним у ваших генов, что именно позволит вам чувствовать себя «как раньше» и жить насыщенной жизнью.
В отличие от традиционных советов, рекомендации анализа на генетические заболевания учитывают:
Следование традиционным советам
Путь по рекомендациям ДНК-теста
Когда полезно сделать ДНК-тест на болезни MyWellness?
Мнение эксперта
Мы изучаем ДНК методами молекулярной биологии.
С помощью данных нутригенетики — взаимосвязей между генами человека и потребностями в питании — понимаем, что необходимо вашему организму.
В зависимости от ваших целей, мы изучаем от 8 до 34 генов, чтобы выявить нужные закономерности. По результатам анализа специалисты по питанию и нутрициологи MyGenetics составляют ДНК-отчёт с подробными рекомендациями.
Технологии ДНК-анализа MyGenetics научно-обоснованы и проводятся на основе международных исследований Stanford University, данных NCBI (США) и Европейского научно-исследовательского консорциума Food4Me.
Для получения точных результатов, анализы проводятся методом Real Time PCR (полимеразной цепной реакцией в режиме реального времени). В ходе реакции создаются миллионы копий определённых частей одной молекулы, позволяя многократно увеличить необходимый участок ДНК для детального изучения. Преимущества такого метода: быстрый процесс выделения ДНК и наиболее точный результат.
Все исследования проводятся в собственной клинико-диагностической лаборатории MyGenetics. Лаборатория имеет лицензию на проведение генетических анализов и оснащена высокотехнологичным современным оборудованием от мировых лидеров отрасли — проводятся на амплификаторах C1000 Touch, CFX от компании BioRad. Работа на базе собственной лаборатории позволяет быстрее получать результаты ДНК-анализов и самостоятельно контролировать качество результатов.
Молекулярно-генетические исследования
Термин “молекулярно-генетическое исследование” (МГИ) объединяет ряд медицинских тестов для выявления изменений в генах, хромосомах, белках.
Выделяют следующие виды тестов:
Виды исследований
ИГХ, ПЦР, FISH применяются для поиска самых частых генетических нарушений.
NGS может выполняться для поиска более редких мутаций. Более подробно читайте здесь.
Для чего проводится МГИ?
Молекулярно-генетическое исследование выполняют при скрининге новорожденных для выявления генетических нарушений, для подтверждения генетического или хромосомного заболевания в любом возрасте, для определения риска пары иметь ребенка с генетическим заболеванием, для установления родства между людьми и многих других целей.
МГИ в онкологии необходимы для определения:
Какие параметры оцениваются?
Рак молочной железы
Для выбора терапии при раке молочной железы обязательно определение:
Опухоли с рецепторами к эстрогену или прогестерону называются гормонозависимыми. В их лечении используют гормональную терапию для подавления стимулирующего влияния гормонов на опухоль.
Если же опухоль HER2-положительна, то используется таргетная терапия препаратами, блокирующими HER2-рецепторы.
Рак предстательной железы
Риск возникновения рака простаты увеличивают мутации в генах:
Более подробно читайте здесь.
Рак легкого
В зависимости от гистологического подтипа опухоли легкого используются разные методы исследования.
Более подробная информация здесь и здесь.
Меланома
При меланоме кожи для подбора таргетной терапии проводят МГИ на наличие мутации в гене BRAF. При отсутствии мутации проводят тест на мутацию в гене KIT, NRAS и более редко на ALK и ROS1.
Где и кто проводят МГИ?
Исследование проводят врачи-генетики в специализированных лабораториях. Онколог может направить пациента в лабораторию напрямую (форма 057/у-04) или через программу Российского общества клинической онкологии.
В Москве в рамках ОМС МГИ доступно в лабораториях:
В других городах МГИ доступно в лабораториях:
Лучше всего выполнять МГИ на образцах опухолевой ткани, полученных в течение года до исследования. Позже исследование может дать ложно-отрицательные результаты.
Как понять, что МГИ необходимо, и к кому обращаться?
При наличии онкологического заболевания для определения показаний к генетическому тестированию, необходимо обратиться к онкологу. ИГХ, ПЦР, FISH доступны в России по ОМС. Исследование NGS в рамках ОМС проводится после получения отрицательного результата ПЦР-теста, во всех остальных случаях исследование проводится платно (цена более 100 тысяч рублей). Направление 057/у-04 на их выполнение дает врач-онколог.
Если нет установленного онкологического заболевания, но в семье были случаи рака молочной железы, кишечника, яичников, предстательной железы, поджелудочной железы или другие, то для оценки показаний к генетическому тестированию нужна консультация врача-генетика.
Как долго ждать результат?
Средний срок ожидания результата молекулярно-генетического исследования составляет около двух недель. Длительность выполнения NGS составляет около 1 месяца.
Результатом МГИ может быть отсутствие мутации (возможно, необходимо провести тестирование другим способом), наличие мутации или выявление мутации с неизвестной клинической значимостью.
ДНК-тест на продуктивность MyNeuro
Общие рекомендации не работают?
Тайм-менеджмент, метод «помидорок», мантра «цель-действие» — всё это стандартные рецепты продуктивности. Но иногда они только сильнее загоняют нас в рамки.
Секрет личной продуктивности в ваших генах. ДНК-тест на серотонин, дофамин и нейромедиаторы MyNeuro описывает тенденции психики, которые дадут научное понимание сильных и слабых сторон вашей продуктивности.
В отличие от унифицированных методик, рекомендации на основе ДНК включают в себя:
Когда полезно сдать ДНК-тест MyNeuro?
Персональный отчёт MyNeuro
Мы изучаем ДНК методами молекулярной биологии.
С помощью данных нутригенетики — взаимосвязей между генами человека и потребностями в питании — понимаем, что необходимо вашему организму.
В зависимости от ваших целей, мы изучаем от 8 до 34 генов, чтобы выявить нужные закономерности. По результатам анализа специалисты по питанию и нутрициологи MyGenetics составляют ДНК-отчёт с подробными рекомендациями.
Технологии ДНК-анализа MyGenetics научно-обоснованы и проводятся на основе международных исследований Stanford University, данных NCBI (США) и Европейского научно-исследовательского консорциума Food4Me.
Для получения точных результатов, анализы проводятся методом Real Time PCR (полимеразной цепной реакцией в режиме реального времени). В ходе реакции создаются миллионы копий определённых частей одной молекулы, позволяя многократно увеличить необходимый участок ДНК для детального изучения. Преимущества такого метода: быстрый процесс выделения ДНК и наиболее точный результат.
Все исследования проводятся в собственной клинико-диагностической лаборатории MyGenetics. Лаборатория имеет лицензию на проведение генетических анализов и оснащена высокотехнологичным современным оборудованием от мировых лидеров отрасли — проводятся на амплификаторах C1000 Touch, CFX от компании BioRad. Работа на базе собственной лаборатории позволяет быстрее получать результаты ДНК-анализов и самостоятельно контролировать качество результатов.
Правда и вымысел вокруг иммунотерапии. Интервью с онкологом Михаилом Ласковым
В октябре Нобелевку вручили исследователям иммуотерапии. Если и раньше вокруг этого метода ходило много слухов, то после решения Нобелевского комитета ажиотаж возрос еще больше. Мы поговорили с онкологом Михаилом Ласковым о том, что такое иммунотерапия и что выдают за иммунотерапию, при лечении каких видов рака она наиболее эффективна, и почему во многих случаях ее нельзя использовать.
Что такое иммунотерапия?
Иммунотерапия – это относительно новый метод лечения онкологических заболеваний. Иммунотерапия не действует напрямую на опухоль, но заставляет иммунитет убивать раковые клетки. Это и есть принципиальное ее отличие от химиотерапии и таргетной терапии.
По большому счету, иммунотерапия заставляет иммунитет делать то, что он и так должен, но не делает по каким-либо причинам. Например, иногда раковые клетки маскируются под здоровые, тогда иммунная система перестает воспринимать их как инородные и не уничтожает. Иммунотерапия может “снимать маску” с опухолевых клеток и помогать иммунитету распознавать их.
Справедливости ради нужно сказать, что сейчас поднялся очень большой хайп по поводу иммунотерапии, потому что вышли действительно эффективные препараты: авелумаб, атезолизумаб, дурвалумаб, пембролизумаб, ниволумаб и ипилимумаб. Но иммунотерапия началась, конечно же, не сейчас и даже не три года назад. Она очень давно применялась с переменным успехом. Как правило, с не очень большим.
Что же произошло сейчас? Появился новый класс препаратов, которые действуют на рецепторы PD1 и PD-L1. Именно эти рецепторы позволяют опухолевой клетке повлиять на иммунитет так, чтобы он перестал распознавать ее, и, следовательно, убивать раковые клетки.
Для лечения каких видов рака используется иммунотерапия?
Сначала эти препараты начали применяться при меланоме и имели большой успех. Почему именно при меланоме? Как мы понимаем, есть опухоли, которые лечатся относительно легко, а есть те, что лечатся очень плохо, рак поджелудочной, например.
Новые препараты стараются разрабатывать именно для труднолечимых раков. Меланома – это как раз один из таких труднолечимых раков, в лечении которого двадцать лет не происходило ничего хорошего, никаких новых высокоэффективных препаратов не появлялось.
Иммунотерапия показала себя очень эффективно при меланоме, все воодушевились и начали применять этот метод лечения на все раки, которые только могли. Тут, конечно же, очень быстро выяснилось, что где-то он работает, где-то не работает совсем, а где-то работает только в конкретных ситуациях.
Иммунотерапия сейчас успешно применяется при лечении рака легких. Как мы знаем, есть разные мутации и разные виды этого рака. И при некоторых из них иммунотерапия быстро заменила химию, оказалась и лучше, и безопаснее. Это очень большой успех. Но стоит помнить, что далеко не весь рак легких успешно лечится иммунотерапией.
В России иммунотерапию также используют при лечении рака почек, а на Западе – в случаях рака головы и шеи, лимфомы Ходжкина, рака мочевого пузыря и некоторых случаях рака печени.
Как объяснить, что иммунотерапия подходит только по показаниям и небольшому проценту больных?
Как и все, что есть в онкологии, иммунотерапия – это не панацея от всего рака. Это просто еще один способ воздействовать на опухоль, далеко не всегда эффективный и ни разу не безопасный
Использовать иммунотерапию можно лишь в ограниченном количестве случаев. На данный момент ее эффективность доказана только для следующих видов рака:
— немелкоклеточный рак легких;
— мелкоклеточный рак легких;
— рак мочевого пузыря.
*** Иммунотерапия может быть эффективной в строго определенных ситуациях даже при вышеуказанных видах рака.
К тому же есть ряд побочных эффектов. И довольно серьезных. В некоторых случаях иммунная система начинает атаковать здоровые ткани и органы, что может вызвать такие осложнения, как:
— проблемы с желудочно-кишечным трактом,
— нефрит и нарушение функции почек,
— мышечные боли, боли в костях и суставах,
— ощущение усталости, слабость,
— тошнота, диарея, нарушения аппетита и др.
Впрочем, серьезные осложнения появляются в среднем только в одном случае из шести.
В октябре вы назвали Нобелевскую премию за иммунотерапию премией для маркетологов. Почему вы отреагировали именно так?
Вспомним историю прекрасного препарата бевацизумаб. Когда он вышел, маркетологи подняли хайп по поводу этого средства, которое останавливает рост сосудов в опухоли. Начали из каждого утюга говорить о том, какое это чудо-чудо-чудо. В итоге, конечно, никакого чуда не было, и этот препарат нашел свое довольно ограниченное применение. И по соотношению цена-польза он, вежливо говоря, далеко не идеален.
И вот уже на этой неделе ко мне толпами приходят люди, которые пытаются спастись при помощи иммунотерапии. И только максимум у 10 % из них этот метод можно пробовать с неизвестным результатом.
Вот про такую ситуацию как раз и было предостережение в этом посте. Потому что на этом сейчас можно быстро срубить много денег в России, именно срубить, а не заработать. Ведь у людей есть все подтверждения: 1) не могли просто так дать Нобелевку; 2) все журналисты написали, что это чудо и панацея; 3) препарат стоит от 200 тысяч в месяц. Все сходится – Нобелевка, цена. Отлично, квартиру продаем.
И тут еще какой-нибудь радостный доктор из частной клиники предлагает его назначить и прямо сейчас, ведь завтра может быть уже поздно.
И главное – очень хочется верить, что это спасет. Это ведь не гомеопатия, а высокая наука.
Как пациенту понять, назначают ему фейковые препараты или нормальные?
Это сделать можно, но необходимо, конечно, включать голову. Нужно много читать и стараться уметь разбираться в источниках.
Еще можно посмотреть русскоязычные рекомендации, но только профессиональные.
А какие препараты иммунотерапии используются сейчас в России?
Их всего четыре, и они довольно дорогие. Это атезолизумаб «Тецентрик», пембролизумаб «Кейтруда», ипилимумаб «Ервой» и ниволумаб «Опдиво». И все, больше пока ничего нет, но много всего на предрегистрационной стадии.
Какие “методики” на рынке выдают за фальшивую иммунотерапию? Например, назначают профилактические капельницы с иммуномодуляторами против рака.
Инарон, рефнот, вакцины всякие, фракция АСД, всего и не упомнишь.
Как пациенту понять, что ему нужна и может помочь иммунотерапия и как ее можно попробовать получить в рамках ОМС?
Поговорить с врачом, почитать надежные источники (об этом выше). По ОМС пойти к химиотерапевту по месту жительства. Все, больше никак.
За счет чего иммунотерапия такая дорогая? Из чего складывается стоимость лекарства?
Разработка нового лекарства, действительно нового, как эти ингибиторы, стоит миллиард долларов. И семь лет после разработки формула защищена патентом. После этого срока буквально на следующий же день заранее скопированный препарат начинают продавать дешевле.
Появляется большая конкуренция. Соответственно, за эти семь лет люди, работающие над созданием лекарства, должны вернуть себе “ярд” и заработать. Один “ярд” что в себя включает? Что из 10 лекарств, которые на ранней стадии компания начинает разрабатывать, до клиник доходит только одно, и это занимает лет двадцать.
Соответственно, вот и вся экономика, за 7 лет нужно всю стоимость отбить и немного заработать для акционеров. Очень сложно разрабатывать и очень просто копировать.
Как пациенту понять, что он наткнулся на мошенников?
Сигнальный значок – это, прежде всего, давление. Когда начинается – давайте скорее, уже вчера надо было начать применять препарат, думать вам некогда, по другим местам ходить нечего. То есть такие довольно простые элементы давления.
В онкологии, на самом деле, крайне редко бывает так, что необходимо вот прямо сейчас, сию минуту начать лечение.
Понятно, что если требуют много денег и есть давление по времени, чтобы человек не успел одуматься, то, скорее всего, что-то не так.
Как они работают: сервис генетических исследований «Генотек»
Один из самых футуристических стартапов в России — компания «Генотек». С ее помощью любой желающий может пройти генетическое тестирование. Для этого нужно заказать тест на сайте, дождаться курьера, плюнуть в привезенную им пробирку, а через несколько недель получить анализ ДНК и его расшифровку. Мы поговорили с основателями компании и узнали, как им удалось превратить науку в бизнес.
Как возникла идея
В 2010 году три студента МГУ — двое с мехмата и один с биофака — познакомились на образовательной программе Московского государственного университета для молодых предпринимателей «Формула успеха». Там они запустили свой первый бизнес-проект. Он был посвящен медицинской тематике, поскольку идея принадлежала студенту биофака Валерию Ильинскому. Суть проекта была в разработке новых технологий для ДНК-диагностики.
На момент запуска «Генотека» в США уже было несколько таких проектов, самый известный из которых — 23andMe, основанный Энн Войжитски, теперь уже бывшей женой основателя Google Сергея Брина. Компания расшифровывает геном клиента, затем проводит интерпретацию анализа и выдает результат, в котором говорится о предрасположенности к наследственным заболеваниям и способах избежать их развития.
«Мы столкнулись с тем, что нам было интересно сделать свои ДНК-паспорта, но в России такие услуги почти никто не предоставлял. А те, кто был, предоставляли очень запутанные или наоборот слишком общие отчеты о полученных данных, — говорит исполнительный директор «Генотека» и выпускник мехмата МГУ Кир Петренко. — Изучив рынок, мы узнали, что в США жена Сергея Брина запустила стартап, который существует уже 7 лет. Мы подумали, что это очень классная идея. По сути, мы запускали копипаст американского стартапа».
Развитию «Генотека» в России, несмотря на существование подобных западных компаний, способствовали особенности российского законодательства. Чтобы переслать слюну, то есть биологический материал, из России за границу, необходимо заключать с каждым отправителем специальный договор, соответствующий российским таможенным правилам. Это не очень просто и занимает много времени, поэтому таким компаниям логичнее открывать здесь фирму-посредника. Это значительно затрудняет их выход на российский рынок и создает конкурентные преимущества для местных компаний.
Откуда деньги
Когда проект выиграл в «Формуле успеха», создателям стало ясно, что для его развития необходима достаточно крупная сумма, а на самоокупаемость он сможет выйти только через несколько лет. «Мы поняли, что не способны пять лет жить на 20 тысяч рублей в месяц, или на минус 20 тысяч рублей, а возраст не позволял нам уже брать деньги у родителей. Нужно было быстро запустить бизнес, который позволил бы нам оперативно выйти на самоокупаемость. Чтобы получать кэш уже сейчас», — рассказывает Кир. Ребята вложили в создание системы генетической интерпретации около пяти миллионов рублей (гранты и собственные средства). На самоокупаемость проект вышел уже через два года.
В чем конкурентное преимущество
«Копипастом» назвать компанию «Генотек» можно только условно, поскольку саму технологию интерпретации генетического кода Валерий Ильинский вместе со своей командой придумывал самостоятельно.
«В каждой компании, подобной нашей, есть своя система интерпретации генетического кода, она разрабатывается самостоятельно, в каждом случае это ноу-хау. Она основывается на известных публикациях, научных статьях и базе данных. В зависимости от базы данных можно делать более или менее точные интерпретации генетических тестов, — рассказывает Валерий. — Мы долго разрабатывали нашу систему, над ней трудились несколько действительно классных математиков, потому что это все основано на математической логике. Мы очень гордимся нашей системой интерпретации, она у нас одна из лучших в мире».
Благодаря качественным научным разработкам «Генотеку» удалось создать не просто подобие американское компании, а проект, которые способен конкурировать с западными, считает Кир. «За три года работы получилось так, что мы начали думать о конкуренции с американскими компаниями. Многие продукты, которые у нас появились, у них отсутствуют», — говорит он.
В России, в свою очередь, стали появляться аналоги «Генотека». По словам Кира, три года назад существовало 2–3 компании, которые проводили генетические исследования, а сейчас их стало в десять раз больше.
Как собиралась команда
Компания была создана на деньги ее основателей. До запуска «Генотека» ее нынешний генеральный директор Артем Елмуратов работал в консалтинговой компании Accenture, Кир Петренко занимался разработками для оборонной промышленности, а Валерий Ильинский заканчивал обучение на биофаке после стажировки в Цюрихе и Вашингтоне. Так как сначала в средствах ребята были ограничены, это сказывалось и на составе команды.
«К концу второго года нас было 6–7 человек — друзья и друзья друзей. Где искать команду, когда тебя никто не знает? «Family, fools and friends». На рынке труда, конечно, нет смысла искать, так как денег нет. Никакие профессиональные звезды к тебе не пойдут, потому что платить нечем», — говорит Кир.
С тех пор, как компания вышла на чистую прибыль, коллектив вырос до 25 человек. Но в основном это все равно друзья и друзья друзей, и большинство из них — выпускники МГУ. «Обнаружилось, что через HeadHunter искать в 10 раз менее эффективно, чем через ВКонтакте и на LinkedIn. Потому что это твой социальный слой, это люди, которые тебя окружают, это друзья друзей друзей, у вас общая картина мира, вы вместе закончили МГУ, это круто. А на HeadHunter у большинства людей бэкграунд гораздо хуже, чем у выпускников МГУ», — объясняет Кир.
Сейчас в компании есть отдел по работе с клиентами, научный и IT-отделы. Сам Кир отвечает за найм сотрудников, производство и логистику, Артем — за продажи, продвижение, бухгалтерию и финансы, а Валерий — за все научные разработки.
Что продает компания
Компания не предлагает парам, которые являются носителями одинаковых заболеваний, разойтись или отказаться от рождения детей. На данный момент существует ряд компаний, которые совместно с партнерскими ЭКО-клиниками могут предотвратить появление на свет больного ребенка. Для этого берется сперматозоид и яйцеклетка пары, производится зачатие в пробирке, и на определенной стадии компания проверяет, есть ли в ДНК эмбриона ген того или иного заболевания. Если нет, то происходит искусственное оплодотворение.
Кому это нужно
У «Генотека» есть два основных типа клиентов. Первые — это люди от 25 до 40 лет, которые думают о своем здоровье, знают, что такое превентивная медицина, и следят за последними достижениями науки и техники. «Не скажу, что они ипохондрики, они живут не по принципу «меньше знаешь — крепче спишь», а по принципу «предупрежден — значит вооружен»», — говорит Кир.
Пока что услугами «Генотека» могут воспользоваться только достаточно обеспеченные люди, поскольку цена самого популярного продукта «Мой геном», включающего в себя все основные исследования, составляет 25 тысяч рублей. По словам Кира, пока что у «Генотека» нет возможности сделать цену ниже, поскольку себестоимость исследований очень высокая. «Но эта возможность появится, потому что я вижу, как растет поток заказов. Тут работает эффект масштаба напрямую», — говорит Кир.
Какие перспективы
Основные планы «Генотека» связаны с развитием в России. Но компания подумывает и о работе на зарубежных рынках. Через пару дней после интервью Кир должен был улететь в Соединенные Штаты, чтобы начать выстраивать там сеть контактов. В любом случае выход на иностранные рынки состоится не скоро, потому что во всех странах разная сертификация, и для ее оформления необходимо время.
Также «Генотек» не исключает возможности заключения сделки с крупной компанией. Кир приводит в пример американский стартап 454 Life Sciences, который был куплен международной фармацевтической корпорацией Roche за 140 миллионов долларов. Основатели «Генотека» не отрицают, что через несколько лет они могли бы пойти на подобную сделку, но пока что планируют развиваться самостоятельно.
Genetic code жидкость
Сегодня много пациентов страдает от неверного диагноза или несвоевременно обнаруженного заболевания, связанного с нарушениями в структуре ДНК.
Распространенные генетические тесты, такие как анализ одного гена, панели из нескольких генов или микроматричный анализ, часто не могут до конца выявить точную причину болезни из-за своих ограниченных возможностей.
Недавние достижения молекулярной генетики позволили сделать доступным по цене и скорости выполнения новый метод генетического тестирования — полногеномное секвенирование.
Полное секвенирование генома способно обнаружить почти все изменения в ДНК пациента, расшифровывая последовательность всех кодирующих и некодирующих областей. Результат такого исследования — информация о тысячах генов, участвующих в нормальном росте и развитии организма.
Этот метод с успехом заменяет все ранее известные способы генетического тестирования, соединяя в себе их возможности. С каждым годом он позволяет установить точный диагноз все большего числа заболеваний.
Используя полногеномное секвенирование, лечащий врач получает помощь не только в диагностике, но и более точно принимает решения по лечению, может наблюдать за течением заболевания, делать прогноз развития болезни и выздоровления. Точные рекомендации о прогрессировании заболевания также возможны в некоторых случаях.
По результатам тестирования может быть проведена оценка риска наследственных заболеваний для других членов семьи.
Полное секвенирование может быть проведено по направлению лечащего врача, а также по желанию пациента без наличия срочных медицинских показаний.
Структура генома не изменяется в течение всей жизни. Сделав анализ однократно, его результатами можно пользоваться всю жизнь. К ним можно повторно обращаться при появлении очередных открытий в генетике и с учетом новых знаний более точно интерпретировать данные.
Имея на руках готовую расшифровку своего генотипа, человек подготовит себя к возможным экстренным ситуациям, когда подробная генетическая информация может спасти жизнь — травмы, операции, тяжелые заболевания, пересадка органов и другие.
Полногеномное секвенирование — лучший на сегодня метод продолжать исследование структуры ДНК, функций генов, их влияния друг на друга и на проявления фенотипа.
Хотя крупные исследовательские центры в мире ведут эту работу, ее результаты не всегда широко доступны.
Поэтому многие исследователи делают это самостоятельно для своих узкоспециализированных целей — подбор и разработка препаратов, спортивные достижения, селекция растений и животных, диагностика и лечение болезней.
Лаборатория «Геномед», обладая современным оборудованием, проверенными технологиями и квалифицированными специалистами-генетиками, готова предоставлять эти ресурсы для целого ряда научных разработок.
Фундаментальные исследования
Изучение структуры и функции генома
Исследование генома человека не завершено до сих пор. Полногеномное сенквенирование дает новые возможности поиска нераскрытых функций генов, изучения некодирующих областей и регуляторных участков ДНК.
Структурные изменения и CNV
В отличие от большинства других генетических методов полногеномное секвенирование позволяет точно определять любые изменения структуры ДНК.
Часто достигается точность определения до уровня единичного нуклеотида. Поэтому, если требуется достоверно определить транслокации, инверсии, вставки или делеции участков, стоит использовать тест Genome UNI.
Эпигенетика
После создания технологии полногеномного секвенирования появилась возможность изучать закономерности наследования, не связанные с генетической последовательностью. В первую очередь речь идет о механизмах регуляции экспрессии генов.
В вопросах эпигенетики важную роль играют методики исследования метилирования ДНК (MeDIP-Seq, WGBS), взаимодействия и модификации гистонов (ChlP-Seq), метилирования РНК (TRM).
Полногеномные ассоциативные исследования
Исследование связи между структурой генома и фенотипическими признаками позволяет выявить, как проявляются различные сочетания генов.
Результат такой работы — более четкое понимание механизмов развития полигенных и многофакторных заболеваний, выявление влияния гетерозиготности на развитие признаков и оценка влияния средовых факторов.
Митохондриальный геном
В отличие от других генетических тестов полногеномное секвенирование исследует одновременно весь генетический материал клетки — ДНК ядра и ДНК митохондрий. Это особенно важно при изучении наследственности по материнской линии и обнаружении наследственных митохондриальных заболеваний.
Транскриптом
Полногеномное секвенирование позволяет оценивать не только геном клетки, но и ее транскриптом — совокупность всех типов РНК.
Важность транскриптома в том, что он показывает активность экспрессии определенных генов на текущий момент. Эта активность сильно зависит от состояния окружающей среды и самого организма и может говорить о наличии неблагоприятных процессов.
Биоинформатический анализ
Расширенный пайплайн
Многопотоковое секвенирование позволяет одновременно проводить расшифровку множества участков одной ДНК. Это значительно ускоряет процесс чтения, позволяет снизить стоимость и добиться высокой точности.
В настоящее время полногеномный анализ покрывает больше 96% генов с глубиной прочтения >20х, а время исследования одного генома сократилось до 1 суток.
Платформа управления данными
Результаты анализов представлены в виде удобного пользовательского интерфейса в личном кабинете. Там же доступны данные интерпретации, если она проводилась, и полученные рекомендации.
Владелец доступа может в любое время обратиться к своим результатам или загрузить их для off-line использования.
Пользовательский биоинформационный сервис
Кроме оборудования и передовых технологий «Геномед» рад предоставить консультационные услуги опытных врачей-генетиков.
Направляя пациента на анализ, вы получите не только расшифровку нуклеотидной последовательности, но и, при необходимости, ее клиническую интерпретацию и рекомендации по использованию результатов.
Собственное хранилище данных
Данные о проведенных исследованиях хранятся на собственных серверах лаборатории.
Все данные шифруются и доступ к ним предоставляется исключительно заказчику с индивидуальным логином и паролем.
Прикладные исследования
Диагностика генетических заболеваний
Сегодня насчитывают около 6000 различных генетических заболеваний и нарушений. Многие из них обладают схожими симптомами, но вызваны патологией разных генов. Если искать эти заболевания по отдельности, потребуется огромное количество исследований.
Полногеномное секвенирование позволяет заменить все виды генетических и многих лабораторных исследований единственным точным и высокоинформативным тестом.
Геном опухоли
Полногеномное секвенирование опухоли дает ключ к пониманию канцерогенеза. Это не только определение основных мутаций, приводящих к развитию рака.
Получив полную расшифровку генома, онколог может оценить уровень сопротивляемости организма росту опухоли, следить за изменением опухоли под воздействием терапии, подбирать наиболее эффективные и безопасные сочетания препаратов.
Профилактическое здоровье
Данные об индивидуальных предрасположенностях к заболеваниям могут изменить образ жизни человека.
На этом основании проще подобрать диету, нагрузки, препятствовать или способствовать воздействию различных факторов внешней среды.
Это позволит не просто увеличить продолжительность жизни, но и улучшить ее качество.
Создание лекарств
Данные об индивидуальных предрасположенностях к заболеваниям могут изменить образ жизни человека.
В зависимости от своего генетического статуса человек по разному реагирует на лекарственную терапию. Гены влияют как на эффективность, так и на переносимость препаратов. Полногеномное тестирование позволяет решать две важные задачи фармакотерапии.
Первая задача — поиск биомаркеров заболеваний. Наглядный пример — простатоспецифический антиген, используемый для диагностики опухолей предстательной железы.
Вторая задача — персонализация лекарственной терапии. В идеале препарат должен разрабатываться для генотипически близких групп пациентов или даже индивидуально с учетом конкретного набора генов.
Судебная медицина / Судебная патология
Генетические данные сегодня широко используются в криминалистической и судебной практике. Ниже перечислены некоторые примеры такого применения. Определение родства\материнства\отцовства.
Антропология и этнос
Изучение ДНК предков или представителей различных этнических групп позволяет понимать историю происхождения и развития человека и законы передачи наследственной информации.
Для отдельного человека появляется возможность разобраться в своих корнях и родословной. Для общества и науки — это источник изучения этнических особенностей здоровья, заболеваемости, долголетия и возможностей развития.
Диагностика наследственных заболеваний
Анализ всего генома в одном исследовании чаще всего приводит к более быстрой постановке диагноза генетического состояния по сравнению с многочисленными сериями одиночных генетических тестов. Особенно это справедливо, если клиническая картина не дает генетику четких указаний, в каких локализациях следует искать патологию, либо тогда, когда клиника может быть обусловлена патологией разных или нескольких генов.
Репродуктивное здоровье
Четко определена связь ряда генов с репродуктивной функцией. Мужское и женское бесплодие, невынашивание, хромосомные болезни новорожденных — все эти состояния можно обнаружить, а впоследствии и успешно лечить, если знать состояние генов, ответственных за процессы зачатия и развития плода.
Онкология
Молекулярно-генетические исследования — мощный инструмент в борьбе с онкологическими заболеваниями.
Во-первых, расшифровав полный геном, можно оценить не только гены, напрямую связанные с развитием рака. Одновременно врач получает полную картину состояния антиоксидантной защиты, противоопухолевого иммунитета, антитоксической функции и других систем, которые косвенно влияют на появление и течение онкопроцесса.
Во-вторых, генетические методы позволяют более эффективно подобрать препарат, контролировать процесс лечения и склонность к рецидивированию.
Важно, что полногеномное исследование (WGS) экономически намного выгоднее, чем исследование отдельных генов или серии генетических панелей (наборов анализов генов, связанных с определенной патологией).
Сегодня с помощью полногеномного тестирования можно оценить 649 опухолевых генов и еще 28 генов, способных нести хромосомные транслокации (перенос участков ДНК между хромосомами), связанные с развитием рака.
Планирование семьи
Известно, что предрасположенность к заболеваниям передается по наследству. Существует группа заболеваний, которые зависят от состояния генов и носят название аутосомно-рецессивных.
Полногеномное секвенирование способно показать людям, вступающим в брак, риски рождения у них детей с аутосомно-рецессивными болезнями.
Предрасположенность к заболеваниям
Почему одни люди заболевают раком, а другие нет? Кто-то живет до 100 лет, многие же умирают в молодости. Как узнать причину?
Сегодня уже четко установлена связь многих генов с развитием заболеваний. Причем, состояние одних генов улучшает прогноз, других — ухудшает. Примеры таких болезней — атеросклероз, остеопороз, тромбозы.
Если знать сочетание всех генов, можно рассчитывать риск развития заболеваний для человека, даже если он пока абсолютно здоров, а также предотвращать их появление.
Индивидуальные способности
Для многих способностей и склонностей человека показана прямая зависимость от состояния его генотипа. К ним относятся мышечная выносливость и сила, темперамент, наклонность к разного рода зависимостям и многое другое. Если планировать профессию и образ жизни на основании генетического анализа, можно достигать лучших результатов быстрее и с меньшими усилиями.
Почему нужно использовать
секвенирование генома
Полногеномное тестирование обладает целым рядом преимуществперед другими методами
в скорости, широте и точности расшифровки генетической последовательности
и установлении диагноза.
| Секвенирование панелей генов | Клиническое секвенирование экзома | Полное секвенирование экзома | Genome UNI | |
|---|---|---|---|---|
| Покрытие кодирующих участков генома | Равномерное, только в области экзонов исследуемых генов | Неравномерное | Неравномерное | Равномерное по всему геному |
| Поиск вариантов в интронах | — | — | — | + |
| Поиск вариантов мтДНК | — | — | — | + |
| Определение CNVs с высокой точностью | — | — | — | + |
| Определение экспансии тринуклеотидных повторов | — | — | — | + |
| Вероятность выявления причины заболевания при повторном анализе данных | Низкая | Низкая | Средняя | Высокая |
| Показания к исследованию | Заболевания с преимущественным поражением одной системы органов или одним ведущим симптомом, когда определены гены ассоциированные с фенотипом | Подозрение на определенную генетическую патологию, когда другие методы (анализ отдельного гена или панели) недоступны | Секвенирование пробанда или родителей (трио) для поиска генов кандидатов (GUS) при отсутствии патогенных вариантов в клинически значимых генах | «В качестве теста первой линии у пациентов с признаками наследственного заболевания или при отсутствии специфического фенотипа.» |
| Другие особенности | Повышенное покрытие таргетных участков генома позволяет лучше выявить однонуклиотидные и in/del варианты | Нет рекомендованного перечня клинически значимых генов | Не обладает преимуществами при секвенировании только пробанда | Большой объем данных требует использования дополнительных вычислительных ресурсов |
Информация для исследователей
Фундаментальные исследования
Секвенирование и ресеквенирование генома, анализ метагенома, экспрессии и метилирования генов.
Прикладные исследования
Поиск биомаркеров, рекрутинг пациентов, решения для селекции.
Медицинские исследования
Секвенирование генома и экзома, анализ на микрочипах.
Биоинформатический анализ
Расширенный пайплайн, биоинформационный сервис, платформа управления данными, хранилище данных.
Genome UNI рекомендован:
Врачам на заметку!
Genome UNI выявит:
Обладает ли тест Genome UNI
доказанной эффективностью?
Для анализа данных используется проприетарный алгоритм и пайплайн, разработанный одной из ведущих компаний США, которая специализируется на анализе данных полного секвенирования генома.
Пайплайн разработан в соответствии с требованиями профессиональной ассоциации медицинских генетиков (ACMG) и ассоциации клинических патологов (CAP) США и включает возможность анализа данных с учетом формализованного описания фенотипа в терминах HPO.
Строгий подход к оценке качества лабораторных данных при использовании профессионального пайплайна позволяет не только повысить выявляемость вариантов, но и избежать ошибок которые могут возникнуть на стадии сиквенса и снизить вероятность ложноположительных результатов.
WGS выявляет больше инсерцционно-
делеционных вариантов при 30х чем WES
при средней глубине 100х
WGS охватывает больше генов на при 30х,
чем WES при 100х
Секвенирование экзома
Cеквенирование экзома – это тест для определения генетических повреждений (мутаций) в ДНК, которые являются причиной наследственных болезней.
Несмотря на то, что существует более 2000 генетических или менделевских болезней (их наследование подчиняется закону Менделя), вызываемых известными отклонениями в ДНК, многие пациенты, у которых на основании клинических данных предполагается наличие редких генетических заболеваний, часто не проходят молекулярную диагностику.
Общепринятой является точка зрения, согласно которой примерно 85% известных отклонений, вызывающих заболевания, происходят в 1% генома, содержащем экзоны и сплайс-зоны, поэтому исследование этой части генома является эффективным и мощным инструментом клинической диагностики для отдельных пациентов.
Тест предназначен для использования в совокупности с клиническими данными и другими лабораторными исследованиями с целью диагностики редких генетических заболеваний.
Путем исследования в одном тесте практически всех областей генома, кодирующих белки, можно не только заменить потенциальную необходимость во многих дорогостоящих анализах каждого гена, но также резко увеличить шансы на обнаружение вариантов с высоким риском, которые могут в дальнейшем быть подтверждены другими методами как у пациента, так и у его родственников.
Используя разработанный компанией Иллюмина тестовый набор TruSight и секвенатор нового поколения Illumina HiSeq2500, стандартные процедуры, проверенные и реализованные в прошедшем CLIA сертификацию Центре клинической геномики при Калифорнийском университете в Лос-Анджелесе (UCLA), можно в одном тесте получить информацию о 95% кодирующих белковых последовательностях генома из числа всех генов, которые отвечают за появление болезней.
Предназначение этого теста в том, чтобы предоставить полногеномную и исчерпывающую геномную экспертизу, с небольшими затратами и значительно более эффективную, чем последовательный анализ при помощи специальных целевых панелей.
В среднем, для каждого пациента определяется примерно 20 000 вариантов ДНК в экзоме. Однако значительная часть этих ДНК вариантов является доброкачественными полиморфизмами. Чтобы определить потенциально болезнетворные варианты, к данным применяется серия фильтров, специфичных для каждого пациента. В их число входит семейная история, любые дифференциальные диагнозы и все соответствующие компоненты родительских заболеваний. При помощи этого можно провести эффективный поиск всех генов, встречающихся в медицинской литературе или мутационных базах данных, которые по данным врачей отвечают за проявление фенотипов и включают известные варианты ДНК, вызывающие нарушения в белках.
На практике у примерно 50% пациентов обнаруживаются однозначные варианты ДНК, которые являются причиной заболевания. Если однозначных причинных вариантов ДНК не обнаружено, то прочие потенциально вызывающие болезни варианты ДНК сохраняются для возможных будущих перепроверок в будущем, когда будут опубликованы результаты новых исследований.
Также иногда рекомендуется провести дополнительный анализ обнаруженных изменений в ДНК для членов семьи пациента, что может помочь с их дальнейшим анализом и интерпретацией.
Клиническое секвенирование экзома.
Этот тест включает глубокий анализ 4800 клинически значимых генов, которые связаны с известными наследственными заболеваниями. Наличие обнаруженных мутаций подтвержданется классическим секвенированием по Сэнгеру. При необходимости проводится поиск аналогичных мутаций у родителей. Метод клинического секвенирования экзома подходит для обнаружения точечных мутаций, вставок, делеций, инверсий и перестановок в экзоме. Пациент получает заключение об изменениях, связанных с его заболеванием. В то же время лечащий врач может дополнительно запросить более подробную информацию, включая данные о потенциально патогенных вариантах, локализованных в хорошо изученных областях экзома.
Цель теста – полное исследование экзома конкретного пациента. При этом результаты изысканий анализируются и проверяются целой командой специалистов медиков. Кроме того, отчет об обнаруженных изменениях сопровождается подробными комментариями.
Перед проведением тестирования рекомендуется дополнительная консультация врача-генетика. В таком случае пациент может убедиться в необходимости прохождения того или иного набора тестов. Также в ходе консультации рассказывается о возможных преимуществах и рисках генетического тестирования. Дело в том, что потенциальную опасность может представлять не само тестирование (оно совершенно безвредно для пациента), а информация об обнаруженных в генетическом материале отклонениях. В частности, сведения о врожденной предрасположенности к тому или иному заболеванию обычно не сообщаются лицам, не достигшим совершеннолетия. Каждая лаборатория вырабатывает свою политику поведения в подобных случаях.
В качестве исходного материала для тестирования берется свежая кровь. Заморозка или нагрев образцов перед тестированием не допускается, поскольку эти воздействия приводят к разрушению ДНК, что в свою очередь делает результаты исследования недостоверными. Образцы должны поступить в лабораторию течение 48 часов с момента взятия.
Стоит отметить, что полное секвенирование экзома может включать или не включать анализ митохондриальной ДНК. Уточнять возможность данного анализа нужно непосредственно в лаборатории, выполняющей секвенирование. В том случае, если лаборатория проводит митохондриальный анализ, данные по гетероплазмии материнского образца могут не сообщаться.
Вопросы и ответы
Что включает клиническое секвенирование экзома?
Клиническое секвенирование экзома разделяется на несколько этапов.
Секвенирование: Диагностическое секвенирование экзома (DES) включает секвенирование примерно 20 000 генов. Это отличает его от секвенирования всего генома, поскольку метода нацелен на исследование 1-2% областей генома, кодирующих синтез белков, которые предположительно ответственны за появление примерно 85% от числа известных заболеваний. Целью DES является выявление изменений, которые определяют фенотип пациента.
Анализ и проверка: после завершения секвенирования все полученные данные пропускаются через биоинформационный конвейер и последовательно анализируются коллективом медиков. Для каждой обнаруженной альтерации проводится проверка, является ли она связанной с исследуемыми особенностями фенотипа. Потенциально связанные альтерации отправляются на ко-сегрегационный анализ.
Формирование отчета: каждый отдельный случай проходит несколько уровней медицинской проверки, и только после последней из них формируется отчет. Каждый отчет является специфическим для пробанда (человека, генетика которого исследуется) и включает проверку и анализ в том числе литературных данных. Подготовка отчета может длиться от нескольких дней до нескольких недель в зависимости от сложности исследования.
Доступные варианты секвенирования экзома:
Первый уровень (Клиническое секвенирования): Анализ примерно 4 800 клинически охарактеризованных генов. Полное секвенирование экзома пробанда. Проведение ко-сегрегационного анализа семьи для всех положительных или неоднозначных результатов.
Второй уровень (Полное секвенирование экзома): Анализ всех предоставленных генов с целью проведения поиска новых генов (порядка 20 000 генов по всей базе NCBI RefSeq). Полное секвенирование экзома семейного трио. Семейный ко-сегрегационный анализ для обнаруженных позитивных или неоднозначных результатов. Обязательное требование: минимум три образца от членов семьи. Тестирование на образцах эмбрионов не проводится.
Какие данные входят в отчет?
Общие результаты: положительный, предположительно положительный, отрицательный, неоднозначный.
Первичные сведения могут ограничиваться информацией, напрямую связанной с фенотипом. Это помогает выделить наиболее полезную для диагностики болезни информацию. Дополнительные сведения чаще содержат более подробные данные, относящиеся к экзому в целом, безотносительно связи с фенотипом.
Дополнительные сведения: Они варьируются в зависимости от предпочтений и возраста пациента. Данный отчет обсуждается отдельно. В дополнительные сведения попадают только установленные патогенетические или предположительно патогенетические альтерации. О клинически незначимых и доброкачественных альтерациях не сообщается. Дополнительные сведения передаются только пробанду. Прочие члены семьи не получают отчета с дополнительной информацией, однако носительство может быть предположено на основании результатов пробанда.
Когда следует заказывать таргетное секвенирование (целевая панель генов) вместо полного сквенирования экзома?
Перед тем, как начать клиническое секвенирования экзома, важно определить возможность использования таргетных панелей, которые разработаны в отношении некоторой группы заболеваний, например, аутизм, задержка психического развития и пр. К примеру, если в истории семьи обнаруживаются признаки одного или нескольких различных наследственных опухолевых заболеваний, то семья вполне может быть носителем опухолевого наследственного заболевания.
В таком случае более эффективным подходом может оказаться первоначальная проверка при помощи таргетных панелей нового поколения, таких как CancerNext, с целью добиться полного покрытия задействованных генов, поскольку такая проверка позволяет получить в том числе полностью отрицательный результат и исключить наличие мутаций в основных опухолевых генах.
Можно ли комбинировать секвенирование экзома с проведением иных генетических тестов (к примеру, хромосомным микроматричным анализом) в рамках одного заказа?
Мы рекомендуем вначале делать хромосомный микроматричный анализ, а затем выполнять секвенирование экзома.
Что необходимо предоставить для клинического секвенирование экзома?
Для выполнения секвенирования экзома необходимы:
Какова политика сообщения дополнительных результатов тестирования?
В 2013 году Американская общество медицинских генетиков (ACMG) выпустила «Рекомендации по случайным находкам в ходе секвенирования экзома и генома» («Recommendations in Incidental Findings in Clinical Exome and Genome Sequencing»).
В соответствии с рекомендациями ACMG минимальный перечень дополнительных результатов предоставляется по умолчанию для каждого тестирования экзома.
По желанию пациент может отказаться от получения всех дополнительных данных, отметив соответствующий пункт в бланке заявки.
В дополнение к перечисленному, мы можем предостаить возможность получения расширенного отчета о дополнительных результатах. Пациенты, заказавшие клиническую диагностику экзома (DES), могут выбрать один из стандартных вариантов расширенного отчета (получить данные о носительстве рецессивных болезней, предрасположенности к раку, возникающим в детском и зрелом возрасте болезням). Для получения подробной информации требуется заполнить соответствующий бланк заявки на получение дополнительных результатов, детально описывающий подробности заказа.
Информация об обнаруженных альтерациях может не сообщаться в том случае, если для связанного с ними заболевания в настоящее время не существует лечения. К примеру, склонность к раннему возникновению болезни Альцгеймера, в итоговый отчет НЕ включается.
Принимаются ли для тестирования материалы только пробанда, когда образцы родителей или иных родственников первой степени предоставить невозможно (к примеру, для приемных детей)?
Если для тестирования предоставляются только образцы пробанда либо предоставляется менее трех образцов от родственников первой степени, то можно заказать лишь проведение тестирования первого уровня (FTE).
Есть ли у клинического секвенирования экзома технические ограничения?
Да, ограничения существуют.
Можно ли сделать повторный анализ данных, полученных при секвенировании?
Да, мы предоставляем такую возможность.
Можно ли провести полное секвенирование экзома для эмбриональных образцов?
Эмбриональные образцы принимаются только в случае гибели плода. Для эмбриональных образцов доступно тестирование первого уровня (FTE).
Если вариант ДНК был пересмотрен и классифицирован иначе, получит ли врач уведомление об этом, чтобы сообщить обновленную информацию своему пациенту?
Секвенирование экзома в нашей лаборатории предполагает повторную классификацию вариантов. Получение дополнительной информации основанной на больших популяционных исследованиях помогает облегчить интерпретацию и уточнить диагноз. Наша лаборатория, как и все научное сообщество вовлечены в активную работу с целью лучшего понимания человеческого генома. Интерпретации и методы постоянно совершенствуются.
Проверяются ли новые гены?
Новые гены анализируются при условии выбора DES тестирования (клиническая диагностика экзома). Под новыми генами подразумеваются альтерации в генах, которые ранее не связывались с болезнями. В связи со сложностью анализа новых генов, клиническая диагностика экзома (DES) требует больше времени для выполнения заказа по сравнению с тестированием первого уровня экзома (FTE).
Если альтерации в новых генах уже обнаружены и описаны, все усилия направляются на изучение гена, включая координационные исследования и функциональные исследования с группами исследователей, изучающих ген, при наличии таковой возможности.
Предоставляет ли лаборатория полный список вариантов по пациенту?
Да, список предоставляется.
Примечание: не все альтерации из списка вариантов проходят подтверждение другими методами, и потому эти данные должны использоваться лишь в исследовательских целях.
Включает ли проводимое тестирование секвенирование митохондриального генома?
Если было обнаружено, что пациент является носителем мутации (или мутаций), можно ли протестировать членов его семьи?
Да, для членов семьи пациента можно провести односайтовый анализ альтераций, классифицированных как причины болезни.
Родственники первой степени и прочие родственники с тем же фенотипом проверяются в рамках ко-сегрегационного анализа, если соответствующие образцы были получены вместе с образцами пробанда для тестирования.
Тест на здоровье волос и кожи MyBeauty
Уход за кожей по ДНК, в отличие от советов подруг и блогеров, включает:
Уход за кожей по рекомендациям ДНК‑теста
Когда полезно сделать ДНК‑тест MyBeauty?
Персональный отчет MyBeauty
Мы изучаем ДНК методами молекулярной биологии.
С помощью данных нутригенетики — взаимосвязей между генами человека и потребностями в питании — понимаем, что необходимо вашему организму.
В зависимости от ваших целей, мы изучаем от 8 до 34 генов, чтобы выявить нужные закономерности. По результатам анализа специалисты по питанию и нутрициологи MyGenetics составляют ДНК-отчёт с подробными рекомендациями.
Технологии ДНК-анализа MyGenetics научно-обоснованы и проводятся на основе международных исследований Stanford University, данных NCBI (США) и Европейского научно-исследовательского консорциума Food4Me.
Для получения точных результатов, анализы проводятся методом Real Time PCR (полимеразной цепной реакцией в режиме реального времени). В ходе реакции создаются миллионы копий определённых частей одной молекулы, позволяя многократно увеличить необходимый участок ДНК для детального изучения. Преимущества такого метода: быстрый процесс выделения ДНК и наиболее точный результат.
Все исследования проводятся в собственной клинико-диагностической лаборатории MyGenetics. Лаборатория имеет лицензию на проведение генетических анализов и оснащена высокотехнологичным современным оборудованием от мировых лидеров отрасли — проводятся на амплификаторах C1000 Touch, CFX от компании BioRad. Работа на базе собственной лаборатории позволяет быстрее получать результаты ДНК-анализов и самостоятельно контролировать качество результатов.
Генетический фактор невынашивания беременности. Актуальность проблемы
Шансы наступления и сохранения беременности определяются различными генетическими факторами. В статье рассмотрены цитогенетические и молекулярно-генетические методы выявления хромосомных аномалий, повышающих риск самопроизвольного аборта и аномалий плода
Доброхотова Юлия Эдуардовна, д.м.н., профессор, заслуженный врач Российской Федерации, ФГБОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации
Резюме. Бесплодие – это заболевание репродуктивной системы, характеризующееся отсутствием наступления клинической беременности после 12 и более месяцев регулярных незащищенных половых контактов. Для выявления причин и выбора тактики лечения бесплодия и невынашивания беременности парам назначается проведение цитогенетических и молекулярно-генетических исследований. Исследование кариотипа партнеров является важным аспектом в диагностике, поскольку причиной мужского или женского бесплодия могут быть хромосомные аномалии.
В статье рассмотрен клинический случай пациентки 35 лет, обратившейся с невынашиванием беременности. При проведении цитогенетического кариотипирования была выявлена хромосомная транслокация, в связи с чем ей было рекомендовано экстракорпоральное оплодотворение с преимплантационным генетическим тестированием. Беременность завершилась рождением здоровой двойни.
Бесплодие определяют как неспособность к зачатию в течение 12 месяцев регулярной половой жизни без использования контрацепции для женщин в возрасте до 35 лет или в течение шести месяцев для женщин старше 35 лет [1]. Бесплодие широко распространено во всем мире: по оценкам экспертов 1 из 4 пар бесплодны [2], и с годами эта тенденция растет [3]. В России частота бесплодия составляет от 17,2% до 24% [4]. К сожалению, женщины недостаточно информированы о снижении фертильности и откладывают деторождение до критического возраста, когда способность к зачатию значительно снижается [5].
У мужчин фертильность и объем эякулята также снижаются с возрастом, начиная с 35 лет [6]: уменьшается подвижность сперматозоидов, чаще встречается нарушение морфологии [7]. Экспериментальные данные демонстрируют, что от отцов в возрасте от 35 до 39 лет и старше рождается экспоненциально меньше детей по сравнению с более молодыми возрастными группами, даже с учетом возраста женщины [8].
Женщина рождается с примерно 1 миллионом яйцеклеток, и к периоду наступления менархе их количество сокращается до 300 000. В фертильном возрасте происходит потеря около тысячи яйцеклеток в месяц [9]. Шансы наступления и сохранения беременности определяются различными генетическими факторами, в том числе хромосомными аномалиями у матери и плода, которые повышают риск самопроизвольного аборта. Хромосомные аномалии плода как причина невынашивания беременности могут возникать спонтанно, а риск их возникновения повышается с увеличением возраста родителей. Кроме того, хромосомные аномалии могут передаваться по наследству, когда один из родителей является здоровым носителем сбалансированной хромосомной перестройки.
Рисунок 1. Взаимосвязь между снижением фертильности и возникновением хромосомных аномалий в зависимости от возраста женщины. Адаптировано из Cimadomo et al. (2018); doi: 10.3389/fendo.2018.00327
Возраст будущей матери является ключевым фактором, определяющим риск развития эмбриональных анеуплоидий (аутосомные трисомии – 52%, моносомии X – 19%, полиплоидии – 22%, другие формы – 7%), и, как следствие, невынашивания беременности (41-50% в первом триместре) [10], поэтому исследование кариотипа абортивного материала и родителей – один из первых шагов к генетическому консультированию [11].
Хромосомные аберрации, обнаруживаемые в кариотипах, подразделяются на две основные группы: первая группа включает структурные изменения хромосом, вторая – количественные хромосомные аномалии. Наиболее часто встречающимися структурными изменениями являются делеции, дупликации, инверсии и транслокации. В родительских хромосомах чаще встречаются сбалансированная транслокация, инверсия или дупликация в разных частях хромосом. Кроме того, партнеры с хромосомными аберрациями в кариотипе имеют более высокий риск повторных выкидышей, чем с нормальным кариотипом [12]. Сбалансированные транслокации возникают de novo во время оогенеза и сперматогенеза, не зависят от возраста родителей и могут в равной степени проявляться у обоих партнеров [13].
Хромосомные анеуплоидии и полиплоидии плода, как правило, вызваны нарушениями процесса эмбриогенеза. Определение цитогенетического статуса является важным фактором, определяющим жизнеспособность эмбриона. Большинство хромосомных аномалий, возникающих во время эмбриогенеза, приводят к невынашиванию беременности. Хотя хромосомный анализ плода не является рутинной практикой, определение кариотипа является важным этапом диагностики не только для ведения последующих беременностей у женщин с привычным невынашиванием, но и прогноза хромосомных аномалий будущего ребенка [14].
Среди различных методов диагностики хромосомных аномалий наиболее распространенными в клинической практике являются цитогенетическое кариотипирование и хромосомный микроматричный анализ, которые будут рассмотрены в настоящей работе.
Кариотипирование
Кариотипирование – это цитогенетический метод, основанный на визуализации хромосом человека посредством световой микроскопии и выявления аномалий в их количестве или структуре. Для получения препарата хромосом лимфоциты в течение 72 часов культивируют в среде с добавлением митогена – вещества, стимулирующего деление хромосом. После культивирования лимфоциты обрабатывают колхицином, который останавливает деление клеток на стадии метафазы. Далее готовят препараты хромосом на микроскопических стеклах и окрашивают красителем Гимзе для визуализации их структуры и морфологии и выявления неоднородных участков. После этого подсчитывают количество и анализируют строение каждой хромосомы [15]. На базе Лаборатории Гемотест используется мощная система исследования метафаз Metafer, осуществляющая поиск и съемку с высоким разрешением 100 метафаз с одного стекла не более чем за 5 минут, что позволяет получить результаты исследования в самые короткие сроки. Полученные изображения сохраняют в единую базу. Metafer обеспечивает идеальные условия для автоматического и полуавтоматического анализа аберраций в хромосомах и способствует объективной и быстрой диагностике генетических повреждений в клетках.
Наряду с преимуществами у метода кариотипирования имеется ряд недостатков. Во-первых, относительно низкое разрешение микроскопов позволяет обнаружить только крупные хромосомные аномалии, такие как анеуплоидии, робертсоновские и сбалансированные транслокации и инверсии [16]. Во-вторых, цитогенетический анализ проводится в культурах живых клеток [17].
Хромосомный микроматричный анализ
Хромосомный микроматричный анализ (ХМА) – технология молекулярно-генетического исследования, который позволяет с высокой точностью определять количество и характер структурных аномалий хромосомного дисбаланса и выявлять хромосомные нарушения длиной от 50 до 100 тысяч пар нуклеотидов, такие как микроделеции и микродупликации, что в 10 раз превышает разрешение кариотипирования [18]. Таким образом, преимущества ХМА заключаются в высоком разрешении, коротком цикле исследования, более объективных результатах и исключении необходимости культивирования клеток.
Преимуществом использования ХMA по сравнению с классическими цитогенетическими методами диагностики хромосомных аномалий является способность метода обнаруживать и с высокой точностью определять хромосомный дисбаланс. Это важно не только для субмикроскопических аномалий, но и для видимых аберраций неясного происхождения, например, при наличии маркерных хромосом и несбалансированных перестроек. Для этого в Лаборатории Гемотест используются ДНК-микрочипы и зарегистрированный в России анализатор «Геноскан 3000».
Несмотря на ряд преимуществ, данный метод имеет и свои недостатки. Так, при ХMA ДНК пациента анализируются относительно нормы, позволяя выявить дисбаланс только по сравнению с контролем, в то время как сбалансированные перестройки остаются невыявленными. Наличие сбалансированной перестройки у одного из партнеров не имеет клинического значения, однако служит предиктором увеличения риска невынашивания для последующих беременностей, если один из родителей является носителем.
Клиническое наблюдение
Семья обратилась по поводу привычного невынашивания беременности. В анамнезе – 3 случая замершей беременности в первом триместре. При сборе семейных данных стало известно, что у матери обследуемой женщины в анамнезе также были случаи самопроизвольного прерывания беременности. При исследовании кариотипа в Лаборатории Гемотест у женщины выявлена сбалансированная транслокация 16 и 19 хромосомы, унаследованная от матери, которая может приводить к формированию хромосомной патологии плода. Учитывая возраст женщины (35 лет), анамнез и высокий риск повторных самопроизвольных абортов, супружеской паре было рекомендовано экстракорпоральное оплодотворение (ЭКО) с предимплантационной генетической диагностикой хромосомной патологии эмбриона перед его переносом. Были отобраны эмбрионы без хромосомной патологии, перенос эмбрионов в полость матки прошел успешно. Беременность завершилась рождением здоровой двойни.
Рисунок 2. Кариотип пациентки N — 46,ХХ,t(16;19)(p13.3;q12)
Обсуждение и выводы
При генетическом консультировании супружеской пары с бесплодием и привычным невынашиванием беременности перед проведением цитогенетических или других необходимых молекулярных исследований анамнез является важным фактором не только при оценке количества прошлых выкидышей, врожденных дефектов или наследственных заболеваний, но и других потенциальных факторов риска, таких как пожилой возраст, избыточный вес и вредные привычки (преимущественно курение и употребление алкоголя).
Важной частью генетической консультации является проведение кариотипирования у пар с бесплодием и привычным невынашиванием беременности, поскольку в зависимости от результата исследования можно прогнозировать дальнейшее ведение этих пациентов. По литературным данным, если один из партнеров является носителем сбалансированной транслокации, примерно 2/3 пар удается зачать ребенка [19]. После индивидуальной оценки каждого случая возможны дальнейшие молекулярно-генетические исследования, такие как хромосомный микроматричный анализ.
В зависимости от локализации хромосомной аберрации можно оценить вероятность рождения ребенка с генетическим синдромом. Наиболее частым случаем является носительство сбалансированной транслокации по 21 хромосоме, которая передается ребенку и вызывает синдром Дауна (трисомия по 21 хромосоме). По данным литературы, если носитель хромосомной аномалии – женщина, вероятность рождения ребенка с синдромом Дауна составляет около 10%, а в случае мужчины-носителя – 0,5% [20]. В таких случаях пациенткам следует рекомендовать проходить пренатальную диагностику при последующих беременностях.
ТОП-26 Лучших Жидкостей Для Электронных Сигарет На 2022 Год
Чем пар отличается от табачной продукции
Главное отличие – отсутствие канцерогенных смол и других вредных добавок, которые обычно наблюдаются в обычных сигаретах. Самое хорошее, что можно сказать о вейпах, вреда они наносят организму меньше, однако, полностью безопасными все же не считаются.
Внимания заслуживает эксперимент, который был проведен в Бостонском университете. Обзор 15 различных заправок для вейпов лишь доказал, что абсолютной безопасностью вещества не характеризуются. Однако, это дало возможность опровергнуть сделанное ранее заявление производителей, в котором говорилось, что истинный состав таких жидкостей неизвестен. Помимо того, что ученым удалось выявить все без исключения элементы состава, так и проведенные исследования доказали, что такой состав поддается изучению, в отличие от состава обычных сигарет.
Угрозой для здоровья могут стать лишь определенные вещества, которых в составе может и не быть. Однако, следует обратить внимание на то, что в процессе парения горячие пары вдыхаются, что может привести к раздражению слизистой и ожогам разной степени. Процесс сгорания «табака» обладает повышенным уровнем опасности, так как все смолы и дым поступают непосредственно в легкие, откладываясь там и образуя прослойку, которая впоследствии затрудняет дыхание. Вследствие этого у человека появляется отдышка, проблемы с сердцем и дыханием.
Какие бывают жидкости
Эмульсия для электронных сигарет представляет собой сложный раствор, в состав которого входят определенные химические элементы. Нельзя с точностью сказать, какой фирмы товар лучше. Однако, новичкам рекомендуется отдать предпочтение популярным моделям, которые имеют многочисленные положительные отзывы. Также не лишним будет прислушаться к советам и рекомендациям продавцов, которые знакомы с большинством поставляемых на рынок новинок.
| Красители | Придают составу определенный цвет или оттенок. Однако, их наличие может способствовать развитию аллергической реакции. В процессе парения окрашивается не только испаритель, но и вата. Использовать их следует с осторожностью. |
| Ароматизаторы | В зависимости от дозировки этого компонента, жидкость будет иметь классические, десертные, алкогольные или фруктовые нотки. За подобный эффект отвечают эфиры. |
| Синтетический никотин | Главной его функцией считается придание продукту определенной крепости. Показатель варьируется от 0 до 36 мг/мл. |
| Дистиллированная вода «AD» | За счет нее состав приобретает необходимую текучесть. Встречается не в каждом составе. |
| Пропиленгликоль «PG» | Отвечает за растворение других используемых элементов. Усилитель ароматических характеристик. Благодаря ему жидкость становится текучей. На этот показатель следует обратить особое внимание, так как он влияет на крепость и «удар по горлу». Именно от него зависит качество парения. Не добавляется в жидкость только в том случае, если глицерина в составе более 80%. |
| Глицерин «VG» | Делает послевкусие мягким. Способствует образованию пара. Ключевой компонент в любом составе. |
Жижа для вейпа без никотина
Жижа без никотина в основном пользуется популярностью среди тех, кто никогда не курил сигареты и просто хочет побаловаться паром. Это не очень хорошая затея, но всё же лучше, чем губить свое здоровье ещё и никотином.
Mad Fruits Green Chief
Mad Fruits Green Chief – популярный производитель, в линейках которого можно найти как жижи с никотином, так и без него. Жидкость со вкусом кислого яблока пользуется большой популярностью, так как сочетает в себе сладкий и кислый привкусы и не зря занимает лидирующее место в топе. Это отличный объём и вкус за такую незначительную сумму. Не горчит, а наоборот, слегка сладковат. Многие пользователи утверждают, что это один из самых приятных вкусов, что они пробовали. Упаковка очень яркая и привлекает внимание. Закрывается плотно, не протекает.
9.9 /10рейтинг
Плюсы
Vardex Американский табак
Жижа от российского популярного производителя. Удивительно, что, несмотря на вкус табака жижи, она совершенно не содержит никотина. Очень удобно заправлять бак: для этого предусмотрен специальный пластиковый носик, поэтому разлить жидкость очень сложно.
Вкус очень мягкий, не горчит, но при этом насыщенный. Баночка плотно закрывается, и даже если кинуть её в сумку, вероятность того, что она протечет, минимальна. Благодаря этой жидкости можно постепенно бросить курить, так как вкус и запах остаются такими же, а никотиновая зависимость начинает потихоньку исчезать. Многие пользователи отмечают, что после затяжки с непривычки хочется кашлять.
9.8 /10рейтинг
Плюсы
Cuttwood Outrage Orange
В этой жидкости собраны насыщенные ароматы апельсинов. Это очень сбалансированный вкус, максимально приближенный к натуральному. Жижа залита в специальный флакон с дозатором в виде пипетки. Это помогает не только расходовать её более экономично, но и защищает от протеканий. Иногда встречается и флакон с пластиковым носиком, и он не менее надёжен.
Стоимость одного флакончика довольно высокая, но она полностью себя оправдывает. Производством жижи для вейпа занимается американская компания. Несмотря на множество восторженных отзывов, встречаются и те, кому вкус и запах этого апельсина не нравится. Некоторые считают, что он очень химический.
9.5 /10рейтинг
Плюсы
Beard Vape Co The One Blueberry
Это очень популярная за границей жидкость, поэтому чаще всего приходится заказывать её на иностранных сайтах. Но иногда Beard Vape Co The One Blueberry можно найти и в обыкновенных табачных магазинах или лавках. Beard Vape Co The One Blueberry – это смесь аромата пончиков из духовки и свежей черники, залитой охлаждённым молоком. Это идеальный вариант для тех, кто уже перепробовал огромное количество вкусов и хочет небольшого разнообразия.
Стоимость одного флакона выше средней, но за уникальность нужно платить. Вкус не горчит, сладость умеренная, кашлять после затяжки не хочется.
9.3 /10рейтинг
Плюсы
Nasty Juice SLOW BLOW
Nasty Juice SLOW BLOW – необычный летний вкус: смесь лимонада и ананаса с добавлением холодка. У жижи для вейпа очень интересный дизайн: чёрная упаковка и белый флакон внутри, всё это сопровождается яркими принтами. Она пользуется особой популярностью среди молодёжи.
Жижа находится в очень удобном флаконе. Благодаря пипетке раствор легко заливается в вейп или электронную сигарету, расходуется экономично, не разливается. Линейка представлена двумя размерами, точно такую же жижку можно купить и с никотином.
9.0 /10рейтинг
Плюсы
Какие Жидкости Для Электронных Сигарет Лучше Выбрать? — Рейтинг ТОП-10 на 2022 год
Здесь представлены лучшие жижи для заправки вейпа. Но не забывайте, что вкусы у всех разные, важно пробовать самостоятельно и сделать свой выбор.
Список наилучших жидкостей для парения:
Рассмотрим каждый бренд более подробно.
Bad Drip
Купить жидкость для электронных сигарет этого бренда можно за 1100 руб. Но оно того стоит. Ведь средство отличается высочайшим качеством и считается одним из лучших. Выглядит емкость как упаковка из-под американских таблеток. Оснащается салфеткой, выполненной в виде смайлика, а также пипеткой для заправки. Такую жидкость для вейпа не стыдно подарить. Выглядит она очень привлекательно. Предлагается в разных объемах. Есть флакончики на 60, 15 и 30 мл. Выбор вкусов очень большой. Есть жидкость с ароматом спелой дыни, персика, груши. Вкусы мягкие и приятные, с различными оттенками.
Это качественная российская жижа для электронных сигарет. Марка является любимой для многих курящих. Появилась она на отечественном рынке достаточно давно. Жидкость (кисель) данного бренда продается за 390 руб. Предлагается с разными вкусами. В том числе есть очень необычные ароматы: пышка, ириска, кисель. Есть серия с солевым никотином Made in USSR Salt. Продукт имеет яркую упаковку.
The Ohm Fantasi
Жидкость данного бренда продается в специализированных магазинах за 990 руб. за емкость объемом 120 мл. Есть разные вкусы: апельсин, манго, яблоко и т.п. Очень многим курящим женщинам и мужчинам нравится жидкость с вишневым ароматом. Она продается с низким содержанием солевого никотина. Но можно сделать ее более крепкой. Для этого нужно добавить немного никотина. Продается он отдельно.
Жидкость для вейпинга данной марки характеризуется высоким качеством и разнообразием вкусов. Есть серии с ароматом гуавы, манго, груши и т.п. Жидкость мягкая и приятная. Во время парения не возникает раздражения в горле. Продается средство для курения марки NKTR за 1290 руб. Относится к премиальным. И считается одним из самых лучших. Жидкость данного бренда создавалась с учетом мнения экспертов в области вейпинга. Для разработки и оценки ароматов были задействованы профессиональные сомелье. Жидкость содержит чистый никотин без вредных химических добавок.
Nasty Juice
Жидкость этого бренда можно приобрести за 850 руб. Цена немаленькая. Но продукт того стоит. Он подарит вейперу очень приятные ощущения. Жидкость для парения предлагается в большом разнообразии ароматов. Все виды сбалансированы по вкусу и отличаются высоким качеством. Ароматы приятные и незабываемые. Многим курильщикам нравится оригинальный сладкий насыщенный вкус с холодком. Жидкость этой марки выбирают обычно на каждый день.
Atmose Dresscode Hipster
Жидкость для парения данной марки пользуется большой популярностью среди вейперов. Предлагается она в четырех интересных вкусах:
Все эти вкусовые сочетания можно назвать необычными и специфическими. Но состав и ароматы продуманы и проработаны очень хорошо. Поэтому каждая серия приятная и интересная. Жидкости данного бренда подойдут мужчинам и женщинам. Подросткам и начинающим вейперам их выбирать не стоит.
Продается жидкость для вейпинга этого бренда по средней цене. Стоимость в магазинах города составляет около 600 руб. Оформлена она достаточно необычно и красиво. На флаконе изображен смокинг. Это подчеркивает солидность бренда. Жидкость можно приобрести в качестве подарка другу или знакомому. На бутылочке отмечена дата разлива. Есть защита от детей.
Zenith
Жидкость для парения этого бренда выпускает компания Zenith E-Juice. Ее ценят за высокое качество. Но по вкусу ее можно назвать «на любителя». При курении может показаться, что средство содержит много химических компонентов. Но это совсем не так. В жидкости нет лишних вредных примесей. Она подходит на каждый день. Является классической по вкусу. Многим курильщикам нравятся варианты с ароматом лимонада. Интересными являются серии с холодными вкусами. Купить жижу для сигарет этого бренда можно за 850 руб. за емкость.
Жидкость для заправки этой марки можно приобрести в городском магазине за 690 руб. Не всем она приходится по вкусу. Все из-за выраженного холодка в аромате. Тем, кому нравится, чтобы во время вейпинга охлаждало рот, марка XEO точно придется по вкусу. Под данным брендом выпускаются жидкости с разными ароматами. Интересной является линейка с апельсиновым соком. При ее парении возникают фантастические ощущения. Холодок с апельсиновыми нотками хорошо ощущается и является очень интересным.
Vardex
Жидкость для парения этой марки входит в категорию бюджетных. Ее можно приобрести за 370 руб. Производитель предлагает большой выбор вкусов. Многим вейперам особенно нравится малиновый лед. При парении такой жидкости хорошо ощущается аромат малины с мятными нотками. Сочетание очень интересное и приятное. Также часто покупают аромат под названием песчаная буря. В нем ощущаются ореховые нотки и вкус печенья.
В составе всех жидкостей этой марки присутствует пропиленгликоль. Это вещество отвечает за вкус. Глицерина содержится мало. За счет этого пар становится более мягким. Все вкусы отличаются яркостью и оригинальностью. У флакончиков тонкий носик. Емкости удобные в использовании. Плотно закрываются, поэтому можно не переживать о том, что жидкость с солевым никотином случайно прольется. Крышка имеет защиту от вскрытия. Что важно для семей с детьми.
FlavourArt
Под данной маркой выпускается хорошая и при этом недорогая жидкость для заправки электронок. Принадлежит она итальянской компании. Продается за 140 руб. за емкость. FlavourArt переводится как «фруктовый аромат». Производитель предлагает большой и разнообразный ассортимент вкусов. Все они приятные и интересные, не приедаются. Во вкусе не ощущается приторности, которая характерна для жидкостей других брендов. В составе качественные компоненты. Каждая емкость оснащается крышечкой с защитой от детей. Что очень важно для семей с малышами. После применения жидкости данной марки испарители не забиваются.
Лучшие жидкости для вейпа со средней концентрацией никотина
Five Pawns Sixty-Four
Новый микс от известной американской компании получил необычное сочетание грейпфрутового ликера с огурцом и лаймом. Товар изготавливают вручную маленькими партиями. Каждая бутылочка имеет эффектный дизайн с оригинальной маркировкой. Главная особенность — выдержка в специально подготовленных для этих целей бочках. Бодрит буквально после первого вдоха.
Joyetech Сигара
Подарит наслаждение от курения настоящей сигары, она на протяжении десятка лет считалась признаком роскоши и достатка. Для всех ценителей классики.
Лучшие жидкости для вейпа с концентрацией никотина выше среднего
Joyetech Дыня
Ароматная медовая дыня — настоящая редкость. Ее найти удается далеко не всегда. Новый продукт дарит возможность насладиться фруктом всем желающим.
Atmose Tobacco Pinkerton
Сочная клубника со спелым бананом, приправленные отборными сортами табака. Легкая и ненавязчивая композиция постепенно раскрывает себя во время парения. Рекомендован всем любителям легким табачных вкусов.
NASTY JUICE VANILLA TOBACCO (SILVER)
Изысканный дуэт ванильного крема и высушенного листа табака. Баланс терпкости и бархатного послевкусия понравится новичкам и бывалым вейперам.
Лучшие жидкости для вейпа с высокой концентрацией никотина
INTRUE Lab Черный чай с бергамотом
Всеми любимый и хорошо знакомый аромат свежезаваренного чая с примесью бергамота. Взбодрит ранним утром и настроит на позитив в течении всего дня.
Sweet Salt — Coffee Break
Капуччино подарит необходимый заряд бодрости. Опознается молочная пенка и свеже обжаренные зерна кофе, бодрит буквального с первого вдоха. Первая затяжка наполняет запахом пережаренных зерен, со второй приходит сладость, а уже к 4 композиция складывается.
Лучшие солевые жидкости для вейпа
Солевые жидкости популярны вследствие того, что обладают некоторыми преимуществами, среди которых стоит выделить возможность утолить голод курильщика за 7-8 затяжек. Кроме этого, эти вещества относительно экономно расходуются, лучшее усваиваются организмом, а во рту нет неприятного привкуса. Последнее обусловлено дополнительной очисткой никотина, в результате чего он становится нейтральным. Среди лучших солевых жидкостей было отобрано 4 варианта, обладающих наибольшим количеством положительных отзывов покупателей.
Bad Salt Bad Apple
Солевая жидкость для вейпа обладает достаточно ярким яблочным вкусом. Заправка в электронную сигарету осуществляется пипеточным способом. Флакон выполнен из стекла, отличается небольшим весом и компактными габаритными размерами. Производство жидкости для вейпов налажено на территории Соединенных Штатов Америки. Дополнительно разработчики предусмотрели крышку с функцией защиты от детей.
Несмотря на наличие недостатков у этой жидкости, все же она обладает соответствующей популярностью у покупателей.
The Clown Laffy Salt
Жидкость для вейпа с солевым никотином для электронных сигарет обладает вкусным чернично-виноградным ароматом, который не может не понравиться настоящий вейперам. Основным ингредиентом вещества есть солевой никотин, поэтому его можно использовать в электронных сигаретах небольшой мощности. Кроме всего прочего, имеет не только фруктовый, но и конфетный аромат. Производитель предусмотрел пипеточный способ заправки вейпа. Флакон выполнен из стекла. Он отличается небольшими размерами и соответствующим весом. Производство налажено на заводах в США. Дизайнеры оснастили флакон вещества специальной крышкой с защитой от детей.
Эта жидкость для электронных сигарет основана на солевом никотине. Отличается своей повышенной безопасностью для здоровья. Многие предпочитают именно этот бренд.
Joyetech Salt Ментол
Популярность этой необычной жидкости связана с тем, что она представляет собой не классический микс разных веществ, а специально продуманное химическое соединение, не имеющее больше аналогов на рынке. Оно отличается вкусом бодрящего ментола, вызывающем небольшое покалывание слизистой рта. При этом совершенно не переходит в ощущение жвачки. Заправка электронной сигарет осуществляется благодаря носику. Производство вещества налажено на территории Китайской народной республики. Вследствие этого товар имеет очень низкую цену, доступную большинству покупателей.
Большинство покупателей отмечает небольшую емкость флакона. Именно поэтому лучше всего приобретать сразу несколько упаковок.
XEO Virginia Honey
Отличием данной версии заправки электронных сигарет считают приятный медовый аромат, который появляется при послевкусии. Это вещество хорошо подходит для тех, кто любит ощущать знакомую терпкость табачного листа. Жидкость хорошо подходит для современных картриджных систем. Их мощность не должна превышать 20 Ватт. Производитель не рекомендует использовать это вещество на мощных атомайзерах и дрипках. Заправка электронных сигарет этим веществом осуществляется через удобный носик. Флакон выполнен из пластика, поэтому легкий и практичный, такую упаковку довольно просто хранить, транспортировать, плюс крышка флакона защищена от детей. Производство товара налажено на фабриках Германии.
Vape рассчитан только на устройства, обладающие небольшой мощностью. В противном случае объема вещества хватит всего на несколько затяжек. Для любителей вейпа этого будет совершенно недостаточно, чтобы утолить голод курильщика.
Какую жидкость для вейпа лучше купить?
Выбор жидкости представляет собой сложную задачу. Нужно учитывать такие факторы: вкусовые характеристики вещества, способность образовывать пар. Кроме этого, стоит обратить внимание также на безопасность состава и наличие в нем никотина. Также надо осуществлять выбор на эргономичность дизайна, удобство использования и качество применяемых при производстве материалов. После отбора интересующих вариантов выбор нужно отдать номинанту с ценой ниже, чем у конкурентов.
Подведя итоги, отметим, что выбрать лучшие жидкости для вейпа не сложно. Для этого нужно проанализировать конкурентов в номинациях: солевые жидкости, без никотина, с никотином. Сравнив выбранные позиции и оценив плюсы и минусы каждой модели, можно сделать выбор в пользу лучшего производителя и самого вкусного аромата.
Что делать, если жидкость закончилась
В такой ситуации экспериментировать не рекомендуется. Нужно отказаться от навязчивой идеи заправить электронную сигарету спиртными напитками, соком, кофе, чаем или иной жидкостью. Подобными вариантами можно безвозвратно испортить любимое курительное устройство.
Предлагается два способа решения вопроса:
Стоит заметить, что второй вариант отличается выгодой, так как позволяет экономить денежные средства. Да и появится возможность провести эксперименты с различными вкусовыми добавками, чтобы создать необычный аромат пара.
Тест на антигены COVID-19: преимущества экспресс-метода и инструкция
Экспресс-тест на коронавирус обладает многими преимуществами. Он помогает оперативно выявить наличие вируса и оградить окружающих, особенно из групп риска, от возможного инфицирования. Чтобы сориентироваться в большом числе различных тестов, необходимо определить, для чего он предназначен и когда необходимо сдать анализ.
Какие существуют экспресс-тесты на COVID-19
Сегодня наличие SARS-CoV-2 — вируса, вызывающего COVID-19, определяют при помощи двух методик:
— экспресс-тест на антиген.
ПЦР-тесты
ПЦР или полимеразная цепная реакция — это метод молекулярной диагностики. Он обнаруживают РНК вируса в организме и позволяет узнать, болен ли человек в данный момент или является носителем. Точность этого метода довольно высокая и составляет почти 100%. Но на конечный результат анализа влияет тщательная подготовка материала.
ПЦР-тесты на коронавирус (RT-PCR) нужно обязательно сдавать тем, кто вернулся из-за границы, имел контакты с больными коронавирусом, а также пациентам с диагнозом «внебольничная пневмония», ОРВИ и грипп, сотрудникам медучреждений и людям старше 65 лет — они находятся в группе риска.
Сделать ПЦР-тест можно в государственной поликлинике (при наличии полиса ОМС) и в частных лабораториях. Важное условие — отсутствие явных признаков простуды и контактов с больными в последние несколько дней. Для проведения теста на COVID-19 биологический материал из ротоглотки и полости носа берут амбулаторно либо специалист может выехать на дом. Затем его исследуют в лаборатории с помощью специального оборудования, ждать результатов нужно не менее 24 часов.
Тесты на антиген
Тесты на антигены (RAT) выявляют белки вируса. При помощи небольших одноразовых пластиковых кассет определяют наличие генетического материала вируса аналогично лабораторным методам. Преимущество этого способа в том, что исследование проводится с помощью небольших приборов, которые легко транспортировать и устанавливать вне специализированной лаборатории. В этом случае также исследуют образцы из носа или горла. Анализ основывается на обнаружении антигена вируса и занимает от 5 до 30 минут.
Первые тест-системы давали высокую погрешность, однако современные модели тестов сегодня достаточно точны. При правильном соблюдении порядка сдачи анализов достоверность результатов составляет более 80%.
Сегодня экспресс-тестирование считается удобным и быстрым способом определить наличие вируса в организме. Тест-системы применяются в аэропортах, вокзалах, на крупных предприятиях и в медицинских учреждениях. Анализ требует минимальной подготовки и значительно дешевле ПЦР-тестирования.
Преимущества экспресс-тестов для диагностики COVID-19
Экспресс-тесты в медицинских учреждениях делают с целью подтверждения или исключения инфекции COVID-19 у людей с симптомами или без них. Такие тесты:
Пациенты с подозрением на COVID-19 должны быстро узнать о возможном наличии инфекции, чтобы получить лечение, информировать находившихся в близком контакте. Чаще всего коронавирусную инфекцию подтверждают тестом ПЦР, но, как говорилось выше, для его проведения нужно специальное оборудование, а для получения результата — не менее 24 часов.
Экспресс-тесты на антиген в медицинских пунктах могут протестировать гораздо большее число людей. Кроме того, анализ можно проводить не только в специализированных медицинских пунктах. При условии, что точность результатов будет высокой, более быстрая диагностика позволит пациентам быстрее принять необходимые меры и снизить распространение COVID-19.
Экспресс-тестирование на антиген как альтернатива ПЦР-тестам
Ученые из Института микробиологии в Лозанне провели исследование: они внедрили тестирование на антиген SARS-CoV-2 в отделении неотложной помощи больницы швейцарского университета [1]. Чувствительность тестов и точность результатов эксперимента проверили на 532 пациентах. Ученые сравнили самые популярные и доступные экспресс-тесты на антиген с ПЦР.
В результате они пришли к выводу, что RAT может представлять собой полезный ресурс в отдельных клинических условиях в качестве дополнительного к ПЦР инструмента. Это поможет при быстрой сортировке больных, особенно во время вспышки заболевания. Но необходимо учитывать более низкую чувствительность теста, особенно у бессимптомных пациентов.
В ходе исследования также выяснили, какие тесты на антигены дают самые точные результаты. Ученые проанализировали самые популярные и доступные к продаже образцы [2]. В ходе эксперимента PBCheck Covid 19 Ag показал лучшие результаты в сравнении с аналогами [3]. У этого теста высокая точность — 88,5%. При этом этот показатель у тестов Panbio Covid-19 Ag Rapid Test составил 87%, а у Standard Q и BD Veritor — 87,2%.
Использование экспресс-тестов на антиген в Швейцарии помогло справиться с очередной волной пандемии. Сортировка пациентов с их помощью позволила швейцарским специалистам быстро изолировать пациентов с положительным результатом анализа на COVID-19 и сэкономить ресурсы. Поэтому многие страны Европы сегодня выбирают экспресс-тесты на антиген как залог эпидемиологической безопасности.
В России также были проведены испытания теста PBCheck Covid 19 Ag. Для этого использовали наборы реагентов с использованием 35 положительных и 35 отрицательных клинических образцов биологического материала (мазков из носа и ротовой полости). В ходе эксперимента установлены следующие диагностические характеристики: диагностическая специфичность 100%, диагностическая чувствительность 92,11% [4].
Как сделать тест на антиген
Экспресс-тестирование на антиген — довольно удобная методика диагностики SARS-CoV-2, так как позволяет проверить наличие инфекции у большого количества людей в максимально короткие сроки.
Антигены коронавируса можно обнаружить в содержимом носоглотки путем иммунохроматографического анализа. Для этого необходимо взять мазок. Вот инструкция, как это правильно сделать:
Комментарий эксперта
Сапожкова Жанна Юрьевна, заведующая лаборатории Гемоскрин, кандидат медицинских наук, руководитель Международной Школы Цитологии (МШЦ, Москва); автор более 40 научных публикаций; главный редактор учебных программ МШЦ для аккредитации в НМО; член-корреспондент Международной Академии Цитологии/MIAC
Каков процент точности у современных экспресс-тестов на ковид? Насколько верны результаты?
В диагностике такой серьезной и социально значимой инфекции, как COVID-19, важны точность и высокая специфичность. То есть тесты должны выявлять даже незначительные количества вируса и не должны диагностировать другие инфекции. Практически все современные тесты для диагностики коронавирусной инфекции отвечают требованиям высокой чувствительности и специфичности.
Например, тест PBCheck COVID-19 Ag, с которым работает наша лаборатория, имеет специфичность 100%, то есть никаких других инфекций, кроме коронавирусной, он диагностировать не будет, а чувствительность теста составляет 92,11%, то есть из 100 инфицированных вирус будет определен у 92. Остальные 8 — это могут быть, например, низкокопийные образцы, то есть те образцы, где количество вируса незначительно.
Можно ли равноценно использовать тесты на антиген вместо ПЦР-теста?
Скорее, наравне с ПЦР-тестом. Во многих странах Европы так и происходит. В аптеках можно купить тест, провести его самостоятельно, принести результат и получить справку на выезд в другую страну. Европа валидирует экспресс-тесты и маркирует их знаком СЕ (свидетельствует о том, что продукция отвечает стандартам и обеспечивает свободный допуск товаров на рынки всех стран Евросоюза. — «РБК Стиль»). Наши европейские коллеги считают, что экспресс-тестирование станет одним из возможных факторов, которые помогут пережить очередную волну коронавируса.
В каких ситуациях использование теста на антиген будет предпочтительнее ПЦР?
Это ситуации, когда тест нужен быстро, например, тестирования на мероприятиях или если кто-то из родственников пришел в больницу навестить пациента. В этих случаях экспресс-тесты несравнимо лучше ПЦР, так как дают быстрый ответ с таким же качеством исследования. Еще ситуация, когда, например, есть симптомы, а ПЦР-тест — отрицательный. В этом случае использование экспресс-теста поможет выявить инфекцию.
Если тест на антиген проводится намного проще и быстрее, есть ли вероятность, что в будущем он заменит традиционный ПЦР?
Насколько я могу видеть развитие диагностики в последние десять лет, лабораторные тесты становятся все разнообразнее и быстрее. Экспресс-тестирование относится к POC-тестированию (point of care), это позволяет своевременно, быстро и качественно исключить или подтвердить заболевание, а значит, вовремя принять необходимые меры лечения или профилактики. Так что будущее, безусловно, за экспресс-тестами.
Регистрационное удостоверение на экспресс-тест PBCheck COVID-19 Ag № 2021/14179 действительно до 01.01.2022. Товар предназначен для профессионального использования (медицинскими работниками).
ДНК-тест на продукты питания MyWellness
Общие рекомендации не работают?
Больше клетчатки, пять порций овощей и фруктов в день, на ужин — кефир, про сливочное масло и сладости забыть. Знакомо, но не очень эффективно?
Пора вместе с MyGenetics разобраться, что именно мешает удерживать вес и почему скромные результаты даются таким трудом.
В отличие от популярных диет, питание по ДНК определяет:
Когда полезно сделать ДНК-тест на диетологию MyWellness?
Мы изучаем ДНК методами молекулярной биологии.
С помощью данных нутригенетики — взаимосвязей между генами человека и потребностями в питании — понимаем, что необходимо вашему организму.
В зависимости от ваших целей, мы изучаем от 8 до 34 генов, чтобы выявить нужные закономерности. По результатам анализа специалисты по питанию и нутрициологи MyGenetics составляют ДНК-отчёт с подробными рекомендациями.
Технологии ДНК-анализа MyGenetics научно-обоснованы и проводятся на основе международных исследований Stanford University, данных NCBI (США) и Европейского научно-исследовательского консорциума Food4Me.
Для получения точных результатов, анализы проводятся методом Real Time PCR (полимеразной цепной реакцией в режиме реального времени). В ходе реакции создаются миллионы копий определённых частей одной молекулы, позволяя многократно увеличить необходимый участок ДНК для детального изучения. Преимущества такого метода: быстрый процесс выделения ДНК и наиболее точный результат.
Все исследования проводятся в собственной клинико-диагностической лаборатории MyGenetics. Лаборатория имеет лицензию на проведение генетических анализов и оснащена высокотехнологичным современным оборудованием от мировых лидеров отрасли — проводятся на амплификаторах C1000 Touch, CFX от компании BioRad. Работа на базе собственной лаборатории позволяет быстрее получать результаты ДНК-анализов и самостоятельно контролировать качество результатов.
Что такое НИПТ и почему об этом исследовании столько говорят в последнее время? Какие преимущества у данных тестов? Кому они показаны и существуют ли ограничения? Сегодня мы найдём ответы на эти и другие актуальные вопросы.
Биохимические скрининговые программы не обладают высокой точностью, они основаны на cовокупности данных статистики, уровня гормонов и размеров плода по УЗИ. Амниоцентез – самый точный метод, но он инвазивный (нужно сделать прокол плодного пузыря, чтобы получить для исследования клетки, принадлежащие плоду) и угрожает развитием осложнений и прерыванием беременности.
Медицинская наука не прекращала поиски новых тестов для скрининга, которые были бы более точны и не зависели от расчётных показателей. В качестве скрининговых тестов в последнее время хорошо себя зарекомендовали НИПТ (неинвазивные пренатальные тесты) как надёжные, удобные и не мешающие нормальному протеканию беременности. Точность метода достигает 99,9%, так как исследуется генетический материал плода (его ДНК) в венозной крови будущей матери.
Как это возможно? Учёные выяснили, что начиная примерно с 10 недели беременности в крови женщины свободно циркулирует ДНК плода. Благодаря современным технологиям врачи научились выделять её и исследовать, выявляя самые распространенные изменения хромосом.
Таким образом, почти каждая женщина может сдать венозную кровь, дождавшись срока 10 недель беременности, и определить генетическое здоровье будущего малыша.
В каких случаях исследование с применением НИПТ будет наиболее полезно?
В спектре лаборатории KDL представлено несколько комплексов НИПТ. Они отличаются объёмом исследования, показаниями и ограничениями. Важно чтобы понять, какой тест подходит именно Вам.
В каких случаях выполнение НИПТ невозможно?
Итак, выполнение неинвазивных пренатальных тестов возможно при одноплодной и двуплодной беременности. Если беременность одноплодная естественная или наступила после ЭКО с использованием собственной яйцеклетки, то доступны все исследования НИПТ. В остальных случаях существуют ограничения.
В чем отличия разных тестов линейки НИПТ?
НИПС Т21 (Геномед)- диагностика только синдрома Дауна. В исследовании выявляется дополнительная 21 хромосома, если она есть у плода. Синдром Дауна считается одной из самых частых хромосомных аномалий и его частота растёт с увеличением возраста женщины. Выполняется при беременности вследствие естественного зачатия, при ЭКО с собственной яйцеклеткой или при использовании донорской яйцеклетки; при беременности одним плодом и двойней, а также при суррогатном материнстве и если произошла редукция одного эмбриона в двойне.
НИПС 5 – ДНК тест на 5 синдромов (Геномед) – неинвазивный тест на 5 синдромов, можно определить аномалии 13, 18, 21 и в большинстве исследований выявить аномалии половых хромосом X и Y.
НИПС 5 универсальный, его выполнение возможно как при одноплодной естественной беременности, так и при беременности двойней, при носительстве донорской яйцеклетки, суррогатным матерям и в том случае, когда один плод в двойне редуцирован.
3 тестовые базовые панели:
Базовые панели позволяют выявить хромосомные аномалии 13,18, 21, Х и Y хромосом плода, а также триплоидии.
НИПС (Геномед) – включает определение вышеперечисленных синдромов (скрининг 13, 18, 21, Х, Y хромосом плода) и определение носительства у матери частых мутаций, которые могут привести к наследственным болезням, если ребенок унаследует два дефектных рецессивных гена от обоих родителей или один доминантный ген. Данные мутации выявляются в крови без выделения ДНК плода, т.е. оценивается не хромосомная мутация плода, а наличие аномальных вариантов генов у матери.
Генетические заболевания, связанные в тестируемыми в этом исследовании вариантами генов:
НИПС уникален не только клинической значимостью, но и доступностью. Одноплодная беременность, беременность двойней (с определением зиготности), в том числе при редукции одного из эмбрионов в двойне. При ЭКО с донорской яйцеклеткой и суррогатном материнстве этот тест нецелесообразен, так как определять мутации, связанные с генетическими заболеваниями нужно по крови той женщины, чья яйцеклетка дала начало эмбриону.
Следующие 2 панели включают микроделеционные синдромы:
Микроделеции – это поломки сегмента хромосом, которые являются менее распространенными, но не менее опасными, и их невозможно заподозрить на УЗИ.
НИПТ Panorama, расширенная панель (Natera) – исследуются и стандартные аномалии хромосом (13,18,21, Х, Y, триплоидии) и микроделеционные синдромы. Если у Вас беременность одноплодная естественная или в результате ЭКО с собственной яйцеклеткой, то выполнение данных панелей возможно.
При наличии двух плодов, ЭКО с донорской яйцеклеткой и суррогатном материнстве определить сегментарные нарушения технически невозможно.
Можно ли определить пол плода и в каких случаях?
Да, по желанию женщины любой НИПТ определяет пол плода и это доступно как при одноплодной, так и при двуплодной беременности.
Обращаем Ваше внимание, что получение результатов, указывающих на риски развития патологических синдромов, требует консультации генетика и дополнительной инвазивной диагностики.
Молекулярно-генетическая служба ФГБУ «НМИЦ Радиологии» Минздрава России
Молекулярно-генетическая служба ФГБУ «НМИЦ Радиологии» Минздрава России имеет подразделения во всех 3-х филиалах Центра (МНИОИ имени П.А. Герцена, МРНЦ имени А.Ф. Цыба, НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина) и проводит уникальные молекулярно-генетические исследования (в том числе методов NGS) и медико-генетическое консультирование онкологических пациентов и их родственников.
Узнать о риске онкозаболевания
Вовремя начать профилактику рака
Выбрать оптимальную схему лечения
ОМС, ДМС, платные медицинские услуги
Руководитель молекулярно-генетической службы, д.м.н. Людмила Николаевна Любченко
Записаться к врачу
Оставьте заявку и ожидайте консультацию нашего специалиста
Что нужно знать о молекулярно-генетической диагностике?
Молекулярно-генетическая диагностика онкологических заболеваний
Совершенствование диагностических методик и развитие онкогенетики требуют внедрения более персонифицированного подхода к выявлению генетической предрасположенности к наследственным онкологическим заболеваниям (индивидуализированная оценка риска). По этой причине сегодня пациентам предлагается широкий спектр генетических тестов: от выявления наиболее частых мутаций до полного секвенирования генома. Подбор соответствующей методики проводится онкологом, совместно с врачом генетиком.
Принимая во внимание доказанный и хорошо охарактеризованный вклад различных мутаций определенных генов в риск развития рака, проведение генетического тестирования, позволяет предсказывать наследственные формы рака, а также разрабатывать программу его профилактики и контроля.
Вторым направлением в молекулярно-генетической диагностике рака является проведение молекулярно-генетического тестирования, которое помогает выбрать наиболее эффективное лечение на основе индивидуальных характеристик опухолевых тканей, таких как соматические мутации или другие уникальные биологические параметры злокачественных опухолей.
Кому и чем полезны генетические исследования?
По результатам молекулярно-генетической диагностики врач-онколог:
● подбирает эффективную лекарственную терапию пациентам с установленным онкологическим диагнозом;
● определяет наличие онкологической предрасположенности и корректирует лечение пациентам моложе 50 лет с диагнозом рак молочной железы, рак яичников, рак желудка и рак поджелудочной железы;
● определяет наличие онкологической предрасположенности и заблаговременно проводит профилактические мероприятия по раннему выявлению опухоли здоровым людям с неблагоприятной наследственностью в генах, вовлеченных в канцерогенез.
Лаборатория молекулярной генетики и методы диагностики
Лаборатория молекулярной генетики является профильным высокоспециализированным подразделением ФГБУ “НМИЦ Радиологии” Минздрава РФ, выполняющим молекулярно-генетическую диагностику при наследственных и спорадических формах злокачественных новообразований с целью индивидуализации диагностики, лечения и профилактики онкологических заболеваний у пациентов и членов их семей, а также с целью проведения научно-исследовательской работы. На базе Лаборатории молекулярной генетики выполняются молекулярно-генетические исследования, в том числе молекулярное профилирование, индивидуального и опухолевого геномов с целью определения герминальных, соматических мутаций и других геномных перестроек у пациентов и членов их семей.
Проектирование и комплектация Лаборатории регламентированы Методическими указаниями (МУ 1.3.2569–09) «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности».
Оснащение Лаборатории молекулярной генетики
Оборудование для проведения молекулярной диагностики
● Роботизированная станция для автоматической экстракции нуклеиновых кислот из различных биологических материалов методом сорбции на магнитных частицах.
● Детектирующие амплификаторы в режиме реального времени.
● Система генетического анализа (капиллярный секвенатор) для секвенирования по Сэнгеру.
● Фрагментный анализатор на основе капиллярного гель- электрофореза.
● Высокопроизводительные NGS секвенаторы.
● Гель-детектирующая станция.
● Низкотемпературные холодильные камеры хранения биологического материала.
● ПЦР-боксы, дозаторы, центрифуги и др.
Рабочие зоны лаборатории молекулярной генетики
Лаборатория оснащена современным диагностическим оборудованием для проведения широкого спектра молекулярно-генетической диагностики: выделения нуклеиновых кислот из любого биологического материала (опухолевая и/или нормальная ткань, плазма, лимфоциты, клеточные культуры и др.), полимеразная цепная реакция (ПЦР), ПЦР в реальном времени (высокоспецифичный и чувствительный метод, использующийся в качестве инструмента для выявления соматических мутаций при различных видах рака), фрагментный анализ (позволяет обнаружить изменения в ДНК для идентификации наличия или отсутствия определенной геномной последовательности), секвенирование методом Сэнгера и методы секвенирования нового поколения (позволяют идентифицировать мутации при анализе длинных участков ДНК или всего генома).
Список рабочих зон лаборатории:
* прием, регистрация, разбор и первичная обработка материала;
* выделение ДНК/РНК;
* приготовление реакционных смесей и проведения ПЦР;
* детекции продуктов амплификации методом электрофореза и др;
*секвенирование.
Применение методов молекулярной диагностики
Молекулярно-диагностические исследования
ФГБУ «НМИЦ радиологии» Минздрава России располагает необходимой материально-технической базой и квалифицированным персоналом для применения комбинированных методов исследований из тканей ДНК пациента:
● позволяют обнаружить и исследовать соматические мутации в генах, имеющих ключевое значение в развитии онкологических заболеваний (EGFR, KRAS, NRAS, BRAF, PIK3Ca, PDGFRA, ERBB2, c-KIT и др.);
● идентифицировать герминальные мутации в генах, вовлеченных в наследственную предрасположенность к раку (BRCA1/2, CHEK2, MSH6, CDH1, VHL, RET и др);
Молекулярно-диагностические исследования
Какие анализы сдаются для молекулярно-генетического тестирования?
Что необходимо сдать для исследования
Для проведения молекулярно-генетических исследований в качестве образцов биологического материала используются:
● периферическая кровь, буккальный эпителий и нормальная ткань (постоперационный материал) для диагностики герминальных мутаций, определения чувствительности и токсичности лекарственных препаратов, HLA-типирования, определения вирусной нагрузки, определения MSI-статуса и др;
● все патоморфологические материалы: опухолевая ткань в парафиновых блоках и стеклах. При низком качестве срезов или для выявления важных деталей могут понадобиться дополнительные срезы. Культуры опухолевых клеток, асцитическая, плевральная и др. жидкости для диагностики соматических мутаций и молекулярных маркеров с целью подбора таргетной терапии.
Перечень анализов по ОМС
ПЦР диагностика: что это такое
Как расшифровывается ПЦР, насколько эта методика эффективна и стоит ли доверять её результатам? Где и в каких случая она применяется? Поговорим о тестах, ставших повседневными, и о тестах не столь известных. А также о том, что показывает ПЦР анализ, далее в этой статье.
ПЦР тестирование
Полимеразная цепная реакция — это технология, позволяющая выделить из двойной спирали ДНК участок с конкретным геном, размножить его и изучить. Открытие ПЦР в биологии и генетике по своей значимости можно сравнить с изобретением микропроцессора в сфере компьютерных технологий. Новые возможности, которые дало исследование, взбудоражили научный мир.
Методика вдохнула новую жизнь в молекулярно-генетические исследования и сделала возможными многие тестирования, которые по разными причинам были невыгодны или недоступны широким массам.
Из плюсов:
Как и у большинства сложных и высоких технологий, у полимеразного метода присутствуют и достоинства, и недостатки. В двух словах ситуация выглядит так.
Кому нужен анализ на ПЦР
Поскольку ПЦР позволяет выявить даже мигрирующие из поколения в поколение наследственные заболевания в их скрытой фазе, провести такое исследование будет полезно каждому. Конечно, не всем такие знания кажутся насущными и необходимыми здесь и сейчас. Но, думается, по мере развития цивилизации будут расти и успехи медицины и генетики. А новые открытия позволят далеко продвинуться в достижении долголетия и здоровья. К тому моменту тест на наследственность вполне может стать обыденным и обязательным для всех анализом.
Пока же этого не случилось, чаще всего тест необходим в таких случаях:
Остальные цели тестирования больше относятся к сферам индивидуальных интересов. Кому-то интересно узнать, что показывает расшифровка всех народностей в его роду. Кто-то пытается планировать будущего ребенка и тестируется на совместимость. Кто-то решил заменить ДНК-тестом диетолога и получить индивидуальные инструкции, советы по правильному питанию. К примеру, такой цели можно достичь с помощью ДНК-теста MyWellness.
Специфика
Специфика всех тестов на основе метода обследования ПЦР в том, что его результаты не могут быть ложноположительными. То есть, если анализ фиксирует присутствие молекулы ДНК возбудителя болезни, она точно имеется в пробе. Но такая точность требует стерильных условий для всего процесса исследования, иначе есть риск получения недостоверных данных из-за загрязненной пробы или несоблюдения техники забора или проведения анализа. В этом, как уже говорилось, заключается некоторая уязвимость методики.
Поэтому лучше всего обращаться за ДНК-тестированием в специализированную клинику с собственной хорошо оборудованной лабораторией. Создание таких учреждений происходит за счет больших вложений как в оборудование, так и в квалифицированный персонал.
Применение ПЦР
Спектр применения технологии полимеразной цепной реакции столь широк, что позволяет проводить различные исследования молекулярно-генетической направленности. Метод используется как для ДНК-тестов, ставших быстрыми и повседневными, так и для изучения ещё не исследованных структур ДНК.
И всё благодаря тому, что технология позволяет извлечь из любого количества ДНК интересующий исследователя участок, размножить его и провести глубокий анализ его свойств в различных формах посредством изучения химических реакций. Таким образом, ПЦР выявляет, позволяет наблюдать зависимости между генами и изучать их совместные реакции на искусственные экспериментальные раздражители.
Проведение ПЦР
Что значит ПЦР исследование? ПЦР диагностика проводится в специальном аппарате – амплифакторе. Это прибор, в который устанавливаются пробирки с биологическими пробами. В зависимости от исследования амплифактор настраивается на нужное количество циклов и начинает попеременно нагревать и охлаждать пробирки, в которых в это время идут реакции. При этом создаётся однородность температуры по всей внутренней камере, необходимая температура задается буквально в один миг и регулируется с точностью до 0,1 градуса.
Такая точность при нагреве и охлаждении необходима для того, чтобы не превысить пороговые значения и не испортить биоматериал.
Что необходимо для проведения анализа методом ПЦР:
Ход реакции
Один цикл реакции протекает в три стадии:
Обычно одно исследование составляет от 20 до 35 подобных циклов.
Подготовка материала
Главное при подготовке биоматериала для анализа — собрать его в как можно более стерильном виде, без посторонних примесей. Для этого имеются рекомендации к гигиеническому графику, употреблению фармакологических веществ и прочие.
Похожие требования и к транспортировке проб – они должны быть упакованы в подходящие для этого чистые контейнеры, а в некоторых случаях также требуется соблюдение особого теплового режима хранения.
Сдача анализов методом ПЦР
Анализ методом ПЦР требует особой аккуратности. Поскольку главное требование всей процедуры — это идеально чистый образец для пробы, многие анализы сдаются непосредственно в клинике: кровь, другие физиологические жидкости, иногда ткани.
Самый простой метод сбора биоматериала — это сбор слюны с внутренней поверхности полости рта на ватную палочку. Способ прост, выполняется на дому, но подходит не для всех тестов.
Подготовка нестандартных проб требует иного порядка действий, который у каждой клиники индивидуален. Лучше проконсультироваться в выбранной вами медицинской организации.
Как подготовиться к анализу ПЦР мужчине
Для мужчин особых требований при сдаче анализов на различные тесты нет. Но в случае тестирования на наличие половых инфекций рекомендуется повышенная интимная гигиена, не менее пары суток воздержания, а также рекомендовано не справлять естественные малые потребности за три часа до процедуры.
Как подготовиться к анализу ПЦР женщине
Для женщин наставлений, запретов и рекомендаций к сдаче несколько больше:
Расшифровка результатов ПЦР теста
Когда из всего спектра возможностей ПЦР диагностики речь идет всего лишь о выявлении заболевания,сам тест и его расшифровка довольно просты. Высокая точность анализа позволяет выявить самые незначительные следы присутствия чужеродной ДНК, размножить её до необходимых объемов и исследовать.
С непривычки такое точное диагностирование, выявляющее заболевания на сверхранней стадии, может вызвать недоверие к результатам. Симптомов нет, самочувствие хорошее, а результаты теста говорят об обратном. Если в теме о проблемах здоровья вообще уместно говорить о везении, то возможность выявить заболевание так рано и сразу начать его лечение — это своего рода удача.
Тем временем за расшифровкой каждого известного гена стоят десятилетия непрерывных исследований ведущих университетов разных стран мира. Например, один из самых длительных исследовательских проектов — проект «Геном человека» — продолжался без малого 13 лет кряду. За время проведения только этих исследований было изучено около 25 тысяч генов, составляющих человеческую ДНК.
Проверка на ВИЧ
У ДНК-анализа на ВИЧ имеется несколько специфических особенностей и рекомендаций:
Все пороки плода на УЗИ: таблица развития, расшифровка генетических отклонений
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/uzi-beremennoy.jpg?fit=436%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/uzi-beremennoy.jpg?fit=799%2C550&ssl=1″ />
УЗИ плода на выявление генетических патологий — это выявление трисомий (дополнительной третьей хромосомы в генетическом наборе плода), приводящих к рождению малыша с серьёзными наследственными заболеваниями и физическими уродствами. Обнаружить пороки плода на УЗИ можно уже на первых этапах развития беременности.
Зачем нужно делать УЗИ для выявления пороков развития плода
Когда и почему возникают генетические патологии плода: риски по возрастам
Самопроизвольные выкидыши случаются в 50% аномальных оплодотворений. Так природа защищает человечество от полного вырождения.
В целом хромосомные патологии разделяются на 4 группы:
Никто не застрахован от рождения малыша с генетическими отклонениями. Если раньше к группе риска относили матерей старше 35 лет, диабетиков, женщин, имеющих хронические заболевания (почечная недостаточность, проблемы с щитовидкой), то в наши дни больные дети рождаются у молодых матерей в возрасте от 20 до 30 лет.
Данные статистики наводит на мрачные мысли. Так, риск рождения малыша с хромосомными аномалиями у 20-летних женщин составляет 1:1667, а у 35-летних уже 1:192. А на деле это означает, что в 99,5% случаев ребёнок у тридцатипятилетней матери родится здоровым.
Какие генетические заболевания плода можно увидеть на УЗИ, когда проходить
В 1 семестре на сроке от 10 до 14 недель (до 10 недели УЗИ неинформативно) беременная проходит исследование, именуемое скринингом. Он состоит из биохимического анализа крови и УЗИ исследования эмбриона. Результатом скрининга является выявление следующих патологий:
На 20-24 неделе делается ещё одно УЗИ. Среди генетических заболеваний плода, видимых на ультразвуковом исследовании во 2 семестре, можно отметить:
На 3 семестре проводится допплерометрия — УЗИ исследование с определением сосудистой системы плода, плаценты и матери. Начиная с 23 недели беременности проверяются артерия пуповины, маточная артерия и средняя мозговая артерия. Исследуется систолический (при сокращении сердечной мышцы) и диастолический (при расслаблении сердечной мышцы) кровоток. У малыша с хромосомными нарушениями кровоток атипичен.
Также в 3 семестре обязательно делают фетометрию плода — измерение размеров с целью выявления аномалий развития.
пороки плода на УЗИ
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?fit=450%2C291&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?fit=851%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda-851×550.jpg?resize=790%2C511″ alt=»пороки плода» width=»790″ height=»511″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?resize=851%2C550&ssl=1 851w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?resize=450%2C291&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?resize=768%2C497&ssl=1 768w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/06/poroki-ploda.jpg?w=982&ssl=1 982w» sizes=»(max-width: 790px) 100vw, 790px» data-recalc-dims=»1″ />
Разновидности УЗИ исследований
Ультразвуковая диагностика представляет широкий спектр исследований. Существует несколько видов УЗИ, которые с предельной точностью определяют внутриутробные пороки развития малыша.
Допплерометрия — э то необычное УЗИ исследование, которое оценивает кровоток плода. Разница между посылаемым и отражаемым сигналом указывает на норму или патологию цепочки «плод-плацента-мать».
Как выглядит УЗИ общих патологий плода: фото и расшифровка результатов УЗИ
Генетические патологии бывают как специфические (синдром Дауна, опухоль Вильмса), так и общие, когда внутренний орган развивается неправильно. Для выявления общих аномалий существует анатомическое исследование плода. Оно проводится на 2 семестре начиная с 20 недели беременности. В этот период можно увидеть личико малыша и определить его пол.
При анатомическом УЗИ все органы плода выводятся на экран в разрезе, и на снимке кости будут иметь белый цвет, а мягкие ткани различные оттенки серого. Специалисту хорошо видно строение головного мозга, он также в состоянии увидеть аномалии в развитии. Становится заметной расщепление верхнего нёба, именуемая заячьей губой.
Продольная и поперечная проекция позвоночника подтверждает или опровергает правильное расположение костей, можно убедиться в целостности брюшной стенки. Отсутствие патологий сердца подтверждают одинаковые размеры предсердий и желудочков. О нормальной работе желудка говорит его наполненность околоплодными водами. Почки должны располагаться на своём месте, а моча из них свободно поступать в мочевой пузырь. Врач чётко видит конечности плода, кроме пальчиков ног.
Генетические патологии плода: как они выглядят на УЗИ и прогноз патологии
Патология
Как и когда выявляют
В чём суть патологии
Характерные черты
Психическое и интеллектуальное развитие
Синдром Дауна
Проводится биопсия хориона, увеличенное воротниковое пространство у плода, недоразвитость костей носа, увеличенный
мочевой пузырь, тахикардия у плода
Хромосомы 21-й пары вместо положенных 2 представлены 3 в цепочке
Раскосый монголоидный разрез глаз независимо от расы ребёнка, неразвитая переносица, неглубоко посаженные глаза, полукруглое плоское ухо, укороченный череп, плоский затылок, укороченный нос
Задержка интеллектуального развития, маленький словарный запас, отсутствует абстрактное мышление, нет концентрации внимания, гиперактивность
Синдром Патау
Маленькая голова на 12 неделе на УЗИ, несимметричные полушарии, лишние пальцы
В 13-й хромосоме присутствует трисомия
Дети рождаются с микроцефалией (неразвитость головного мозга), низкий лоб, скошенные глазные щели, расщелины губы и нёба, помутнение роговицы, дефекты сердца, увеличены почки, аномальные половые органы
Глубокая умственная отсталость, отсутствие мышления и речи
Синдром Эдвардса
Биопсия хориона, внутриутробное взятие крови из пуповины, на УЗИ видна микроцефалия
В 18-й хромосом есть трисомия
Рождаются в основном девочки (3/4), а плод мужского пола погибает ещё в утробе. Низкий скошенный лоб, маленький рот, недоразвитость глазного яблока, расщелины верхней губы и нёба, узкий слуховой проход, врождённые вывихи, косолапость, тяжёлые аномалии сердца и ЖКТ, недоразвитость мозга
Дети страдают олигофренией (органическим поражением головного мозга), умственной отсталостью, имбецильностью (средней умственной отсталостью), идиотией (отсутствием речи и умственной деятельности)
Синдром Шерешевского-Тёрнера
Рентген костных структур плода, МРТ миокарда
Аномалия, встречающаяся в Х-хромосоме
Встречается чаще у девочек. Укороченная шея со складками, отёчны кисти и ступни, тугоухость. Отвисшая нижняя губа, низкая линия роста волос, недоразвитая нижняя челюсть. Рост во взрослом возрасте не превышает 145 см. Дисплазия суставов. Аномальное развитие зубов. Половой инфантилизм (нет фолликул в яичниках), недоразвитость молочных желез
Страдает речь, внимание. Интеллектуальные способности не нарушены
Полисомия по Х-хромосоме
Скрининг на 12 неделе беременности, биопсия хориона, анализ амниотической жидкости. Настораживает увеличение воротниковой зоны
Вместо двух Х-хромосом встречается три и более
Встречается у девочек и редко у мальчиков. Характерен половой инфантилизм (не развиваются вторичные половые признаки), высокий рост, искривление позвоночника, гиперпигментация кожи
Антисоциальное поведение, агрессия, умственная отсталость у мужчин.
Полисомия по Y-хромосоме
Вместо ХY-хромосом есть лишняя Y-хромосома
Встречается у мальчиков. Вырастают высокого роста от 186 см, тяжёлая массивная нижняя челюсть, выпуклые надбровные дуги, узкие плечи, широкий таз, сутулость, жир на животе
Умственная отсталость, агрессия, эмоциональная неустойчивость
Синдром Карнелии де Ланге
При анализе крови беременной женщины в сыворотке не обнаружено протеина-А плазмы (РАРР-А), которого обычно много
мутациями в гене NIPBL или SMC1A
Тонкие сросшиеся брови, укороченный череп, высокое нёбо, аномально прорезавшиеся зубы, недоразвитые конечности, мраморная кожа, врождённые пороки внутренних органов, отставание в росте
Глубокая умственная отсталость,
Синдром Смита-Лемли-Опитца
УЗИ показывает аномалии черепа у плода, не просматриваются рёберные кости
мутация в гене DHCR7, отвечающий за выработку холестерина
Узкий лоб, опущены веки, косоглазие, деформация черепа, короткий нос, низко расположенные уши, недоразвитые челюсти, аномалии половых органов, сращение пальцев
Повышенная возбудимость, агрессия, понижение мышечного тонуса, нарушения сна, отставание в умственном развитии, аутизм
Синдром Прадера-Вилли
Отмечается низкая подвижность плода, неправильное положение,
В 15-й хромосоме отсутствует отцовская часть хромосомы
Ожирение при низком росте, плохая координация, слабый мышечный тонус, косоглазие, густая слюна, плохие зубы, бесплодие
Задержка психического развития, речевое отставание, отсутствие навыков общения, слабая мелкая моторика. Половина больных имеет средний уровень интеллекта, умеют читать
При постоянных занятиях ребёнок может научиться читать, считать,запоминает людей. Следует вести борьбу с перееданием
Синдром Ангельмана
Начиная с 12-й недели наблюдается отставание развития плода в росте и массе
Отсутствуют или мутирует ген UBE3A в 15-й хромосоме
Частый необоснованный смех, мелкий тремор, много ненужных движений, широкий рот, язык вываливается наружу, ходьба на абсолютно прямых ногах
«Синдром счастливой марионетки»: ребёнок часто и беспричинно смеётся. Задержка психического развития, гиперактивность, нарушение координации движения, хаотичное махание руками
Синдром Лангера-Гидеона
На 4D УЗИ заметна челюстно-лицевая аномалия
трихоринофаланговый синдром, заключающийся в нарушении 8-й хромосомы
Длинный нос грушевидной формы, недоразвитость нижней челюсти, очень оттопыренные уши, неравномерность конечностей, искривление позвоночника
Задержка психического развития, умственная отсталость различной степени, отсутствие речи
Синдром Миллера-Диккера
На УЗИ заметно аномальное строение черепа, лицевые диспропорции
Патология в 17-й хромосоме, вызывающая разглаживание мозговых извилин. Вызывается интоксикацией плода альдегидами при злоупотреблении матерью алкоголя
Дизморфия (алкогольный синдром), пороки сердца, почек, судороги
Лиссэнцефалия (гладкость извилин больших полушарий), недоразвитость головного мозга, умственная отсталость
Аномалия ДиДжорджи
В некоторых случаях на УЗИ выявляются различные пороки органов у малыша, особенно сердца (тетрада Фалло)
Заболевание иммунной системы, нарушение участка 22-й хромосомы
Гипоплазия тимуса (недоразвитость органа, отвечающего за выработку иммунных клеток), деформация лица и черепа, порок сердца. Отсутствуют паращитовидные железы, отвечающие за обмен кальция и фосфора
Атрофия коры головного мозга и мозжечка, задержка умственного развития, сложности с моторикой и речью
Лечение иммуностимуляторами,пересадка тимус, кальциевосполняемая терапия. Дети редко доживают до 10 лет, умирают от последствий иммунодефицита
Синдром Уильямса
На УЗИ видны диспропорции в развитии скелета, эластичность суставов
Генетическое заболевание, вызванное отсутствием звена в 7-й хромосоме
Нарушен синтез белка эластина, у детей типично «лицо Эльфа»: припухшие веки, низко расположенные глаза, острый подбородок, короткий нос, широкий лоб
Повышенная чувствительность к звуку, импульсивность, навязчивая общительность, эмоциональная неустойчивость, тревожность, экспрессивная речь
Синдром Беквита-Видеманна
На УЗИ заметны аномально непропорциональные конечности, превышение массы тела, патология почек
Генетическое заболевание, вызванное отсутствием звена в 11-й хромосоме
Бурный рост в раннем возрасте, аномально большие внутренние органы, склонность к раковым опухолям. У ребёнка пупочная грыжа, аномально большой язык, микроцефалия (недоразвитость мозга).
Эмоциональное и психическое развитие в некоторых случаях не отстаёт от нормы. Иногда встречается выраженная умственная отсталость
Синдром Тричера Коллинза
На УЗИ видны ярко выраженная асимметрия черт лица
Генетическая мутация в 5-й хромосоме, вызывающая нарушение костных структур
У ребёнка практически нет лица, ярко выраженное физическое уродство
Абсолютно нормальное психо-эмоциональное развитие
ПРОГНОЗ
Причины патологий плода: что влияет на рождение детей с генетическими отклонениями
К фактором, способствующим рождению детей с генетическими аномалиями, относятся:
Как предотвратить пороки плода и где сделать УЗИ плода в СПБ
Предотвратить большинство проблем с вынашиванием и патологиями плода, можно заранее планируя беременность. Проходя обследование при планировании оба партнера сдают анализы, четко показывающие вероятность генетических отклонений. Также проводится спектр тестов на инфекции, способные вызвать уродства у малыша ( ТОРЧ-комплекс ) и другие исследования.
Приглашаем пройти УЗИ на патологии плода в Санкт-Петербурге в клинике Диана. У нас установлен новейший УЗИ аппарат с доплером. Обследование проводится в 3-Д и 4-Д фоматах. На руки выдается диск с записью.
Genetic code жидкость
Известно более 7 тысяч наследственных заболеваний. К счастью, многие из них достаточно редки. Для отдельных заболеваний описаны только единичные случаи, в то время как другие наследственные патологии встречаются достаточно часто. Это муковисцидоз, фенилкетонурия, спинальная мышечная атрофия.
Дети со СМА страдают от прогрессивной нервно-мышечной атрофии. Многие из них умирают в возрасте до двух лет, другие же остаются прикованными к коляске.
Одно заболевание может быть вызвано различными мутациями в одном и том же гене.
Так, например, известно более 100 мутаций в одном гене CFTR, которые вызывают развитие муковисцидоза.
Для каждой мутации, как правило, существует отдельный тест.
Исследования целесообразны для подтверждения заболевания при наличии у пациента его клинических признаков.
Для выявления патологий, которые связаны с наследственными заболеваниями, необходимо проанализировать несколько сотен, а иногда и тысяч различных мутаций.
Универсальный генетический тест позволяет определить от 30 до 3000 мутаций, вызывающих развитие наиболее распространенных наследственных заболеваний, которые нельзя излечить, но возможно предотвратить.
Тест рекомендован женщинам и мужчинам репродуктивного возраста.
Расшифровка ДНК-анализа
Насколько точна расшифровка генома ДНК, и можно ли ей доверять? Какие виды тестирования может предложить современный рынок медицинских услуг? Зачем это обычному человеку, и какая от этого польза? Анализ, ДНК, расшифровка: попробуем подробно ответить на эти и другие вопросы в этой статье.
ДНК экспертиза: определение и описание
ДНК экспертиза это выявление индивидуальных особенностей организма человека путем расшифровки его генетического кода. На сегодняшний день на рынке услуг по ДНК тестированию предлагается несколько основных тестов, которые широко применяются в медицине, спорте и криминалистике:
Как расшифровывают результаты ДНК-теста
ДНК тест, расшифровка и экспертиза генома проходит в несколько основные стадии:
Достоверность теста
ДНК-тестирования это высокоточная методика изучения микромира организма и микропроцессов в нём. Расшифровка теста происходит на основе генетической базы, над пополнением которой работают многие мировые ученые и институты. Более точных методик диагностики по направления, которые предлагают разные варианты тестирования, на сегодняшний день нет.
На отцовство: индекс
ДНК-тестирование на отцовство это одно из самых известных в обществе исследований, вызывающее наибольший общественный резонанс. Результаты такое исследования имеют юридическую силу и являются достаточным основанием для принятия решения в судебном порядке. В чем же заключается суть тестирования?
Несомненно, многие знают, что спираль ДНК человека имеет двойную структуру. Так, часть генотипа ребенок заимствует от матери, а часть от отца. Сравнение аллелей (различных форм одного и того же гена) ребенка и отца (и в некоторых случаях матери) может подтвердить вероятность отцовства с точностью до 99,99%. Считается, что 100% результат не возможен, поскольку всегда есть вероятность наличия у потенциального отца близнеца. Опровергается же отцовство стопроцентно.
Основной показатель, по которым вычисляется родственная связь, называется «индексом отцовства». Не углубляясь в сложные термины, в общих чертах это показатель того, насколько аллели ребенка и потенциального отца схожи в различных областях генокода.
Для стандартизации результатов и исключения возможных ошибок расшифровки теста на отцовство, международная организация идентификации человека установила следующие пороговые значения для определения отцовства:
На родство
В последние году всё большую популярность обретает тестирование на определение национальности. И речь тут не только в стремлении людей к самоидентификации: кому-то это необходимо для переезда в другую страну и получения гражданства, а кто-то хочет восстановить свое родовое древо и имеет представление о своих предках.
Зачастую результаты удивляют и имеют мало общего с тем, что представлял себе клиент до их получения. Порой результаты исследований таковы, что и вовсе могут сильно изменить отношение человека к другим народностям, и расширить понимание глубокой взаимосвязи между всеми людьми.
Так же, тестирование можно провести без согласия тестируемого и предоставить ему результаты в качестве оригинального подарка.
Врожденные заболевания
Избежать многих рисков и продлить свою жизнь может помочь своевременное исследование на врожденные заболевания и предрасположенности к таковым. Предупрежден – значит вооружен. И это полностью характеризует всю пользу подобного анализа. На сегодняшний день специалисты способны выявить до 6000 различных вирусов и инфекций, а так же определить генетическую предрасположенность к самым опасным заболеваниям современности.
Стоимость исследования
Сколько стоит ДНК-анализ? Стоимость тестирования, как и сроки его проведения, зависит от многих факторов: от самого вида теста до объемов расшифровываемых данных (цена расшифровки) и ценовой политики конкретной лаборатории. По сути, цена складывается почти так же, как и сроки проведения исследований, что описано далее в данной статье. В среднем цена может колебаться от нескольких до десятков тысяч рублей.
Кто оплачивает
На сегодняшний день, в РФ нет государственных программ, проектов и благотворительных фондов, которые могут оплатить ДНК-анализ за вас. Единственная такая возможность возникает, если суд сам решает, что необходимо его проведение. В таком случае анализ оплачивается из областного бюджета.
Сроки
Сроки проведения исследований и получения готового результата зависят они нескольких факторов, и оговариваются индивидуально:
В среднем на проведение исследований и оформления их в готовый документ со всеми сопутствующими рекомендациями уходит 3-4 недели. Но, в зависимости от факторов выше, точные сроки оговариваются индивидуально.
Что нужно для анализа
Провести тестирование можно на любом образце тканей человека, но самым простым и распространённым способом получения биоматериала для исследований является забор слюны в ротовой полости клиента. Забор можно произвести самостоятельно в домашних условиях с помощью обычной ватной палочки. Во избежание возможных ошибок при анализе необходимо соблюдать стерильность образца: ватную палочку для сбора слюны лучше всего взять новую из только что распакованной упаковки, конверт для пересылки и хранения образца не должен быть полиэтиленовым или с полиэтиленовыми вставками.
Проведение процедуры
Проведение процедуры анализа, заказанного в нашей клинике, происходит по соответствующей лицензии в стерильной лаборатории, оборудованной новейшей техникой. Открылась наша лаборатория относительно недавно (в 2018 году) и предоставляет самые современные услуги по ДНК-тестирования, доступные на сегодняшний день для мировой практики.
Расшифровка
Наибольший период от всего затраченного на тестирование времени занимает расшифровка результатов. Поскольку речь идет об исследовании микроструктур, что уже осложняет процесс изучения образца, интересующие врачей гены подкрашиваются флуоресцентной краской, а после облучаются направленным лучом лазера – таким образом, добиваются более-менее четкой и различимой картинки. В зависимости от самого теста гены сравниваются с эталонами в базе данных, и, исходя из сходств и различий, делаются итоговые выводы и составляются рекомендации.
Можно ли повлиять на результат
Даже теоретически подделать результаты ДНК анализа очень и очень не просто. Если допустить, что кому-то удалось подкупить сотрудника лаборатории, то совершить такую подмену можно только в сговоре со всему участниками исследования – вся процедура анализа фиксирует документально и на фото, и проходит под надзором уполномоченного лица.
Если, всё-таки возникли подозрения в недостоверности результатов анализа, всегда можно потребовать повторное исследование в той же или в другой лаборатории. В том случае, если подмена результатов будет подтверждена, виновники таковой не только понесут уголовную ответственность, но и должны будут компенсировать все сопутствующие проверке затраты.
По самому невероятному сценарию, учёнными Израиля тестируется методика синтеза искусственной цепочки ДНК, но это еще не готовая и очень дорогая технология. И для её применения необходимо иметь доступ к банку всех исследованных генов, чего нет у обычного медицинского учреждения.
В связи с этим, и по причине высокой точности результатов исследования ДНК, тестирование является единственным способом доказать отцовство, или его отсутствие в суде. На данный момент государство не предоставляет бесплатную возможность провести анализ на отцовство, но в тех случаях, когда в ходе судебных разбирательств суд сам принял решение о необходимости проведения исследования, его оплата входит в судебные издержки и покрывается из областного бюджета.
Можем ли тест быть ошибочным
При соблюдении всех норм сбора и проведения тестирования вероятность ошибки теста исключена. В редких случаях результаты теста на отцовство могут оказаться ошибочными, если у потенциального отца имеются близкий родственник (например, брат) – такие детали необходимо сообщать специалистом до проведения тестирования. В остальных случаях ошибка может возникнуть в связи с загрязнением или подменой биоматериала.
Что такое ДНК человека
ДНК – что это такое простыми словами и как она устроена? Физически это макромолекула, которая не только хранит в себе наследственную информацию, но и является подробной инструкцией по развитию всего организма условно из одной универсальной клетки.
Если сравнить человека с компьютером, а все многообразие биологической жизни – с различными формами роботизированных компьютеров, ДНК в этом сравнении будет биологическим языком программирования. С той лишь разницей, что биологические виды устроены намного сложнее и совершеннее самых передовых компьютеров.
К примеру, все биологические виды обладают уникальной способностью деления и преобразования клетки. Фактически в ходе самовоспроизводства клетки биомасса не только материализуется сама из себя, но и физически преобразовывается под решение множества узкоспециализированных задач. А все многообразие живых видов, их форм, уникальных способностей исходит из деления одной универсальной клетки. Одно это уже уходит далеко за грань всех современных генетических достижений.
История открытия
Фактически открытие дезоксирибонуклеиновой кислоты произошло дважды. Первым открытие молекулы совершил Иоганн Фридрих Мишер в 1869 году. Будучи швейцарским биологом и физиологом, он из клеток, содержащихся в гное, смог выделить большую молекулу с высоким содержанием азота и фосфора. Свое открытие он назвал нуклеин, а позже – нуклеиновой кислотой, когда были открыты ее кислотные свойства.
Первоначально ученые считали, что основная функция нуклеиновой кислоты состоит в хранении фосфора. А предположения, что она может содержать в себе наследственную информацию, вызывали насмешки, поскольку структура молекулы казалась им слишком простой и однообразной для таких функций. Также считалось, что наличие дезоксирибонуклеиновой кислоты свойственно только животным клеткам, а в растениях содержится только РНК. Но в 1934–1935 годах советские ученые-биологи А. Н. Белозерский и А. Р. Кизель это наглядно опровергли и опубликовали результаты своих работ в советских и мировых научных журналах.
Повторное открытие ДНК уже в качестве носителя наследственной информации и не только было совершено в 1944 году. Группа исследователей, состоящая из Освальда Эвери, Колина Маклауда и Маклина Маккарти, проводила эксперименты с трансформацией бактерий и доказала, что основную роль в этом процессе играет дезоксирибонуклеиновая кислота.
Значение ДНК в медицине
Открытие ДНК в медицине, расшифровка этой кислоты – это события, значение которых трудно преувеличить. Большая часть современных прорывных технологий и исследований прямо или косвенно базируется на этом фундаментальном для науки открытии. Не знай мы про гены, не было бы многих современных методов лечения и диагностики, многих технических изобретений. По сути, не было бы и генетики как полноценной самостоятельной науки. Застопорилось бы изучение клетки и того, как она функционирует. А без этих знаний и множество открытий в этой области было бы невозможно.
На сегодняшний день знания о генах помогают многим людям:
Молекула ДНК
ДНК-определение, поиск ее места в уже систематизированном знании не так прост. По существу, к молекулам ДНК отнесли условно, для удобства. Молекула ДНК – это структура, превосходящая размером обычные молекулы. И она имеет уникальную спиральную структуру. В то время как физики и химики считают молекулами электрически нейтральные частицы, состоящие из одного и более атомов, связанных ковалентными связями. Либо же, по результатам международного съезда химиков 1860 года, молекулой считается наименьшая частица вещества, обладающая всеми его химическими свойствами.
Структура ДНК
У всех на слуху, что дезоксирибонуклеиновая кислота имеет двуспиральную структуру. В интернете, в фильмах, в рекламе – всюду можно встретить ее многократно увеличенное изображение. Но что ответить, если попросят объяснить подробнее. Это уже более сложный вопрос. Давайте разберемся лучше, из чего эта структура состоит:
В цепочках нуклеотидов присутствуют и совсем не изученные структуры, которые, на первый взгляд, никак не участвуют в физиологических процессах. Эти довольно обширные участки называют мусорными.
Состав ДНК
Если говорить о составе ДНК более подробно, то нуклеотиды – это базовый структурный элемент, кирпичики, из которых состоят обе цепи спирали. Нуклеотиды подразделяются на 4 разновидности: аденин, тимин, гуанин и цитозин. И всего четыре этих нуклеотида осуществляют запись всей наследственной информации и составляют все известные гены.
Закручиваются в спираль обе цепочки генов тоже не просто так. Из всех четырех различных нуклеотидов находиться напротив друг друга в разных цепочках они могут только двумя парами: аденин-тимин и гуанин-цитозин. В науке эти пары называются комплементарными.
Между парными нуклеотидами возникает крепкая водородная связь. При этом связь аденином и тимином немного слабее, чем между гуанином и цитозином. Но закручиваются цепочки в спираль по иным причинам:
Исследования показали, что скручивание помогает сократить длину цепочки генов в 5-6 раз. А во время суперспирализации (такое тоже бывает) длина цепочки может сократиться в целых 30 раз!
Помимо того, что пара цепочек генов закручена в спираль, существует и суперспирализация. За это явление отвечают гистоновые белки, которые имеют форму катушек для ниток. Уже закрученная двойная спираль наматывается на эти белки, как нитка. Что не оставляет сомнений в том, что спиральность как таковая специально служит тому, чтобы более компактно упаковать наследственную информацию в клетку.
Роль в клетке
Конечно, одна, даже большая двойная спираль не способна вместить в себя весь объем информации, необходимый для такого сложного проекта, как человеческое тело. Возможно, поэтому эти цепочки объединены в пары, что делает их похожими на букву «Х». Хромосомы, в свою очередь, тоже парные, и их у человека 46 пар.
Помимо того, что хромосома содержит в себе подробную инструкцию по функционированию клетки, она же путем активации актуальных моменту генов провоцирует клетку вырабатывать определенные белки с самыми различными свойствами. Например, в борьбе с опухолями активно участвует ген старости, который старит ее недоброкачественные клетки и не дает им бесконечно делиться.
Что такое нуклеотиды
Нуклеотиды – это четыре элемента, которые являются основой биоязыка программирования цепи ДНК, так же, как ноль и единица являются основой ассемблера (первого из языков программирования). Уникальная последовательность нуклеотидов в одной из двух цепочек ДНК является геном. Если хотя бы немного изменить эту последовательность, то ген уже будет поврежден или разрушен.
Синтез белка
Синтез белков – это ключевое таинство всей физиологии человека. Именно белки запускают и контролируют все процессы в организме на клеточном уровне. Если полностью изучить, какие гены и группы генов в каких случаях запускают синтез белков и сами эти белки, то наука научится полностью настраивать и перенастраивать весь человеческий организм.
На сегодняшний день нам известно, что, реагируя на различные раздражители, в двойной спирали дезоксирибонуклеиновой кислоты активируются гены или участки с генами. Информация с этих участков копируется на РНК (рибонуклеиновая кислота), и уже РНК переносит информацию из ядра клетки, в котором находятся хромосомы, в саму клетку. РНК выступает своего рода глашатаем, который читает указ всем работникам. Так РНК заставляет клетку вести себя тем либо иным образом и вырабатывать различные белки.
Что такое РНК
Если ДНК – это кабинет министров, которые всем управляют и принимают все решения, то РНК – это пресс-атташе. Она извещает всех о новых распоряжениях и указах и раздает инструкции на местах.
РНК – это рибонуклеиновая кислота, которая может копировать формы различных участков дезоксирибонуклеиновой кислоты и транспортировать их из ядра клетки в ее внутриклеточное пространство.
Расшифровка ДНК
ДНК-расшифровка стала возможна только благодаря открытию полимеразной цепной реакции, и происходит она следующим образом:
Проба, содержащая образцы дезоксирибонуклеиновой кислоты, быстро нагревается. Это необходимо, чтобы двойная спираль раскрутилась и распалась на две самостоятельные нити.
К интересующему исследователей участку цепи генов прилепляется полимераза. Эта процедура происходит при немного более низких температурах.
Полимераза активирует деление пойманного участка – так происходит синтез необходимых для изучения участков генов.
Участки пропитываются специальной краской, которая светится при воздействии направленного пучка лазера. Так получают картину гена, которую можно изучать и расшифровывать.
Таким образом, изучение ДНК стало доступным инструментом, который позволяет людям узнать о себе много нового и может помочь сохранить здоровье, избавиться от уже имеющихся заболеваний, похудеть, сохранить молодость и улучшить качество своей жизни!
12 методов в картинках: секвенирование нуклеиновых кислот
12 методов в картинках: секвенирование нуклеиновых кислот
Авторы
Редакторы
Секвенирование ДНК и РНК — это рутинный процесс, позволяющий, тем не менее, вникнуть в суть всего живого. Первоначально расшифровка генома была «развлечением» для избранных, а сегодня заказать эту услугу может каждая вторая научно-исследовательская лаборатория. С каждым годом проникнуть в дебри геномной, транскриптомной и эпигеномной информации становится все проще. Этот обзор посвящен основным принципам секвенирования нуклеиновых кислот и может послужить превосходным путеводителем как для любителя, изучающего основы молекулярной биологии, так и для специалиста, который планирует эксперимент и грезит научными прорывами.
12 биологических методов в картинках
Генеральный партнер цикла — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Партнер этой статьи — «СкайДжин»
Пять причин выбрать SkyGen:
Одна из главных миссий «Биомолекулы» — докопаться до самых корней. Мы не просто рассказываем, какие новые факты обнаружили исследователи — мы говорим о том, как они их обнаружили, стараемся объяснить принципы биологических методик. Как вытащить ген из одного организма и вставить в другой? Как проследить в огромной клетке за судьбой нескольких крошечных молекул? Как возбудить одну крохотную группу нейронов в огромном мозге?
И вот мы решили рассказать о лабораторных методах более системно, собрать воедино в одной рубрике самые главные, самые современные биологические методики. Чтоб было интереснее и нагляднее, мы густо проиллюстрировали статьи и даже кое-где добавили анимации. Мы хотим, чтобы статьи новой рубрики были интересны и понятны даже случайному прохожему. И с другой стороны — чтобы они были так подробны, что даже профессионал мог бы обнаружить в них что-то новое. Мы собрали методики в 12 больших групп и собираемся сделать на их основе биометодический календарь. Ждите обновлений!
Появление и развитие технологий секвенирования
С момента открытия нуклеиновых кислот прошло уже почти полторы сотни лет. В далеком 1869 году Иоганн Фридрих Мишер выделил из находившихся в гное клеток неизвестное доселе вещество, содержащее азот и фосфор, которое назвал нуклеином, а затем (из-за его свойств) — нуклеиновой кислотой. Первоначально считалось, что молекулы нуклеиновых кислот — резерв фосфора в клетках, однако уже в первой половине XX века ученые доказали их наследственную природу. Тогда же появилось понятие гена —наименьшей структурной и функциональной единицы наследственности, — и сформировалась новая наука — генетика.
Вплоть до середины прошлого века структура носителей генетической информации и способы ее передачи оставались неясными. Модель двойной спирали ДНК, которая входит во все современные учебники генетики и молекулярной биологии, предложили в 1953 году Френсис Крик и Джеймс Уотсон (за это в 1962 ученые получили Нобелевскую премию). Последовавшие следом открытие генетического кода и разработка центральной догмы молекулярной биологии дали мощный толчок к развитию естественных наук, в первую очередь — генетики. Основные исторические вехи этого процесса показаны на рисунке 1.
Рисунок 1. История геномных исследований и секвенирования нуклеиновых кислот. 8 марта 1865 г. — Грегор Мендель доложил результаты своих опытов, объясняющие механизм наследования. 1869 г. — Иоганн Фридрих Мишер выделил из клеток в гное неизвестное доселе вещество, содержащее азот и фосфор, которое назвал нуклеином. 1905–1909 гг. — появление терминов «ген» и «генетика». 1953 г. — Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК. 1958 г. — Френсис Крик сформулировал центральную догму молекулярной биологии. 1975 г. — Сэнгер с коллегами разработал «плюс-минус» метод секвенирования ДНК. 1977 г. — группа Сэнгера разработала метод «терминаторов». 1977 г. — Максам и Гилберт предложили метод секвенирования ДНК путем химической деградации. 2001 г. — опубликован первый полный геном человека. 2005 г. — коммерциализация технологии пиросеквенирования. 2006 г. — коммерциализация технологии Solexa (Illumina). 2006 г. — коммерциализация технологии лигазного секвенирования. 2010 г. — коммерциализация технологии ионного полупроводникового секвенирования (технология PostLight TM ). 2011 г. — первый коммерческий релиз секвенаторов PacBio, основанных на технологии одномолекулярного SMRT-секвенирования. 2015 г. — начало продаж первых приборов, основанных на секвенировании через нанопору. Чтобы увидеть рисунок в полном размере, нажмите на него.
Осознав основные принципы функционирования нуклеиновых кислот (НК), научное сообщество предприняло грандиозные усилия для того чтобы разработать быстрые и эффективные методы определения их первичной последовательности (рис. 2) — как это принято говорить сегодня, секвенирования. Спустя десятилетия после открытия Уотсона и Крика в биологической науке наступила новая эпоха — эра секвенирования нуклеиновых кислот и геномики.
Рисунок 2. Секвенирование нуклеиновых кислот (другими словами, определение их нуклеотидной последовательности) — это расшифровка первичной структуры линейных молекул ДНК или РНК, состоящих из последовательности «букв» — нуклеозидтрифосфатов: дАТФ, дГТФ, дЦТФ, дТТФ и УТФ. Эти «буквы» зачастую именуют просто по азотистому основанию, входящему в их состав — аденин (А), гуанин (Г), цитозин (Ц), тимин (Т), а также урацил (У) в случае РНК.
Секвенирование белковых молекул
Кстати, секвенировать можно не только нуклеиновые кислоты, но и другие биополимеры — например, пептиды и белки, «сотканные» из аминокислотных остатков. Однако в этом спецпроекте мы предпочли подробно остановиться на секвенировании только нуклеиновых кислот и не затрагиваем отдельно тему белкового секвенирования.
Примечание от «Диаэм»: Белковое секвенирование методом Эдмана проводят на приборах Shimadzu в сочетании с ВЭЖХ.
Словарик
Почти четверть века назад в Соединенных Штатах стартовал грандиозный по своему масштабу научный проект, посвященный определению последовательности генома человека [1]. Основной его целью стала расшифровка генетической информации, заключенной в хромосомах (компактизованная ДНК), которые мы наследуем от своих родителей. В течение тринадцати лет многочисленные исследовательские группы по всему миру работали над определением полной последовательности генома человека. Почти три миллиарда долларов, потраченные на этот проект, открыли перед исследователями замечательные перспективы. Используя полученные данные, появилась возможность искать и находить участки ДНК, связанные с генетически обусловленными заболеваниями. И если природа многих моногенных болезней (вызываемых отказом единственного гена нашего генома) стала понятна уже давно, то некоторые заболевания — сердечно-сосудистые, онкологические, болезни Альцгеймера [2] и Паркинсона — являются многофакторными: вызвать их может широкий спектр изменений генома, многие из которых до сих пор неизвестны. Информация о генетических вариантах, связанных с человеческими недугами, позволяет формировать научно-обоснованный подход при их диагностике и лечении.
Расшифровка и аннотация (маркировка генов и других объектов в последовательности ДНК) генома человека поставили вопрос об использовании генетической информации как для диагностики заболеваний и их долговременного прогнозирования у человека, так и для исследования популяционной структуры сообществ, этногенеза и эволюционных процессов. Применение современных технологий секвенирования и генотипирования предлагает перспективные способы решения задач современной медицинской геномики и эпигеномики.
Такие результаты могут быть использованы при создании систем для проведения дифференциальной диагностики и выявления генетической природы заболеваний, для проведения персональной терапии и подбора методик лечения на основе анализа индивидуальных генетических характеристик. Решение таких задач тесно связано с разработкой эффективных алгоритмов и математических моделей для биоинформатической обработки данных геномного секвенирования и их использованием на базе суперкомпьютерных кластеров.
Геномные исследования позволяют решать массу задач как прикладного, так и фундаментального плана. Благодаря им разрабатываются новые лекарства и продукты, они же позволяют проникнуть в глубокую историю человечества [3] или понять причину массового вымирания видов.
Сейчас разработано несколько способов секвенирования НК. Самый популярный и надежный из них — секвенирование по Сэнгеру — позволяет «считывать» последовательности до 1000 пар оснований (п.о.) и используется для небольших фрагментов генома/генов или для валидации результатов более современного секвенирования нового поколения (next-generation sequencing, NGS), где размер одного прочитанного фрагмента варьирует от 25 до 500 п.о. В отличие от секвенирования по Сэнгеру, методы NGS используют для глубокого (многократного) прочтения генетического материала, которое необходимо, например, для ресеквенирования и сборки новых геномов (de novo), транскриптомных и эпигеномных исследований [4]. Помимо этого, NGS-секвенирование значительно производительнее, позволяя одновременно считывать миллионы и даже миллиарды коротких фрагментов. Такой рост производительности привел к возможности определения последовательности сразу десятков геномов (в зависимости от их размера) за один запуск прибора (рис. 3).
Рисунок 3. Современные технологии делают процесс секвенирования ДНК рутинной процедурой.
Стремительно развивающиеся новые технологии секвенирования ДНК позволяют быстро и эффективно определять особенности организмов на уровне их геномов. Главным итогом развития геномных и постгеномных технологий стало существенное расширение возможностей изучения генетической природы целого спектра заболеваний человека. Масштабные ассоциативные исследования на больших клинических выборках позволяют получать данные о генетических характеристиках, присущих конкретным группам людей (семьям, популяциям), развивая методы персонализированной медицины. В связи с этим, изучение механизмов генетической предрасположенности к многофакторным заболеваниям и выявление специфических генетических маркеров сегодня имеет особенную актуальность. Подобные методы широко применяются за рубежом и в России, где технологии современного секвенирования также постепенно внедряют в медицинские исследования и медицинскую практику с целью персонификации стратегии лечения [1].
Технологической основой для подобных исследовательских и сугубо прикладных проектов служат геномные секвенаторы (приборы, на которых проводят секвенирование), поставляемые различными коммерческими компаниями, такими как Illumina, Thermo Fisher Scientific, Oxford Nanopore Technologies, Pacific Biosciences и другие.
В 2017 году на рынке представлены сразу несколько перспективных разработок в области секвенирования НК. Эти подходы применены в секвенаторах нового поколения:
и некоторых других.
Современные технологии делают процесс секвенирования ДНК рутинной процедурой, особенно в том случае, когда речь идет об организмах с уже известной последовательностью генома — их последующая биоинформатическая обработка не представляет значительного труда, поскольку исследователь уже имеет референсный (ранее отсеквенированный) геном, который позволяет избежать ошибок при анализе полученных данных. При анализе нового, неопубликованного ранее, генома (de novo секвенирование и сборка) перед исследователем стоит ряд более сложных задач, в ходе решения которых он пытается сложить единичные фрагменты в цельную последовательность, задействуя многочисленные математические алгоритмы и суперкомпьютерные мощности [5], [6].
Однако наибольший интерес представляет не сама последовательность генома, а понимание того, как он функционирует: какие гены обеспечивают жизнедеятельность клетки, как происходит регуляция (включение или выключение генов) или какие генные пути начинают работать в ответ на стрессовые факторы.
Все современные секвенирующие платформы отличаются от метода секвенирования по Сэнгеру тем, что не требуют этапа клонирования фрагментов ДНК. Это экономит рабочее время и позволяет избежать ряда проблем с клонированием АТ-богатых участков. Общий принцип пробоподготовки для большинства современных (NGS) секвенаторов включает фрагментирование ДНК, привязку к субстрату, амплификацию фрагментов с помощью ПЦР (в одномолекулярном секвенировании от ПЦР удалось отказаться) и последующее считывании последовательности НК. В отличие от метода секвенирования по Сэнгеру, современные платформы обеспечивают параллельное проведение миллиардов реакций в малых объемах, что позволяет получить намного больший объем информации на выходе.
Рассмотрим основные технологии секвенирования нуклеиновых кислот подробнее.
Секвенирование по Сэнгеру
«Плюс-минус» метод секвенирования ДНК
Один из наиболее популярных методов секвенирования обязан своим появлением английскому биофизику Фредерику Сэнгеру (1918–2013) — единственному ученому в истории мировой науки, получившему сразу две Нобелевские премии по химии (в 1958 и 1980 годах). Первую премию присудили за установление структур белков, особенно инсулина, а вторую награду ему вручили в том числе и за разработку методов определения первичной последовательности нуклеиновых кислот.
Методику секвенирования ДНК с использованием радиоактивно меченых нуклеотидов и ДНК-полимеразы (или фрагмента Кленова ДНК-полимеразы I) предложили Сэнгер и его коллеги в 1977 году, причем с течением времени этот метод прошел несколько модификаций и к настоящему моменту считается золотым стандартом современного секвенирования.
Первоначально Ф. Сэнгер и Алан Коулсон разработали так называемый «плюс-минус» метод секвенирования ДНК [7], который можно подразделить на две основные стадии:
Рисунок 4. «Плюс-минус» метод секвенирования ДНК, предложенный Ф. Сэнгером и А. Коулсоном.
Секвенирование ДНК по Сэнгеру: метод «терминаторов»
Спустя пару лет Сэнгер с коллегами предложил еще один способ секвенирования, получивший название метода «терминаторов» или метода «обрыва цепи» [9]. Суть этого метода заключается в том, что в реакционную смесь добавляют аналоги привычных нуклеотидов (дидезоксинуклеозидтрифосфаты), включение которых в синтезируемую цепь приводит к невозможности ее дальнейшего синтеза (терминации), а по образовавшемуся «обломку» можно установить последнюю букву секвенируемого фрагмента ДНК (рис. 5).
Рисунок 5. Метод «терминаторов»: используют ДНК-полимеразу, олигонуклеотидные праймеры и смесь четырех дезоксинуклеотидов (dNTPs) (А, Т, G и C), один из которых радиоактивно помечен по α-положению фосфата ( 32 P). В каждую из четырех реакций добавляется по одному 2’,3’-дидезоксинуклеозидтрифосфату (ddATP, ddTTP, ddCTP или ddGTP), которые терминируют дальнейшую реакцию (синтез комплементарной молекулы ДНК с матрицы) — таким образом в каждой пробирке образуется набор фрагментов ДНК разной длины, которые заканчиваются одним и тем же нуклеотидом. Затем полученные фрагменты визуализируют с помощью электрофореза и, сравнивая длины фрагментов из четырех реакций с ddATP, ddTTP, ddCTP или ddGTP, восстанавливают последовательность ДНК.
Автоматизированные модификации метода «терминаторов» активно применяют до сих пор в специальных приборах — секвенаторах. Открытие многочисленных флуоресцентных молекул позволило отказаться от использования радиоактивной метки и сделало возможным проведение реакции в одной пробирке. Реакционную смесь разделяют капиллярным электрофорезом, a выстроившиеся в синтезируемую цепочку ДНК меченые нуклеотиды затем регистрируют детекторами флуоресценции, предоставляя возможность считывать последовательность всего секвенируемого ДНК-фрагмента.
Секвенаторы по Сэнгеру: решения от «Диаэм»
Капиллярные секвенаторы ДНК Applied Biosystems (Thermo Fisher Scientific) — золотой стандарт секвенирования по Сэнгеру. Производительность — 4, 8, 24, 48 и 96 образцов. Они предназначены для секвенирования относительно небольших фрагментов ДНК длиной до 1000 нуклеотидов, характеризуются высокой точностью и используются для генотипирования человека, животных и других организмов (в том числе в медицине — трансплантологии, перинатологии, онкологии, фармакогенетике и др.), для выявления точечных мутаций, делеций и инсерций, для валидации мутаций, выявленных NGS-секвенированием, для анализа метилирования ДНК, для идентификации личности в криминалистике и др.
Новейшая разработка в этой области — капиллярный секвенатор SeqStudio (Applied Biosystems):
Первые впечатления пользователей нового капиллярного секвенатора SeqStudio
Материал предоставлен партнёром — компанией «Диаэм»
Другие методы секвенирования «старого поколения»
Кроме методов, предложенных Сэнгером, в конце прошлого века развивались и другие подходы к определению последовательности НК, которые — в частности, метод химической деградации, разработанный Максамом и Гилбертом [10], — не получили дальнейшего распространения из-за быстрого развития энзимологии (раздел биохимии, изучающий ферменты), которая предоставила преимущество методу «терминаторов» Сэнгера.
Использование секвенирования по Сэнгеру
Секвенирование по Сэнгеру позволяет «считывать» последовательности до 1000 пар нуклеотидов и применяется для небольших фрагментов генома/генов. В частности, оно используется для:
Наиболее популярными секвенаторами, использующими технологию секвенирования по Сэнгеру, являются приборы, производимые компанией Thermo Fisher Scientific: 3730xL, 3730, 3500xL, 3500, 3130xL, 3130, 310.
Следует отметить, что все описанные выше типы исследований сейчас можно проводить с помощью секвенирования «нового поколения», речь о котором пойдет в следующей главе, однако главные плюсы секвенирования по Сэнгеру — высокая точность (достоверность) полученных данных и невысокая стоимость работ при анализе небольшого количества ДНК-фрагментов — сохраняют актуальность этого типа определения последовательности НК.
Секвенирование «нового поколения» — next-generation sequencing (NGS)
За последние полтора десятилетия были разработаны, коммерциализированы и продолжают успешно развиваться совершенно новые технологии определения последовательности НК, в основе которых лежит стремление к миниатюризации, автоматизации, увеличению объема получаемых данных, а также удешевлению процесса. Появление NGS впервые позволило значительно ускорить и удешевить определение полной последовательности миллионов геномов организмов, начиная от бактерий и заканчивая человеком. Более того, появилась реальная возможность единовременно оценивать экспрессию (работу) тысяч генов в организмах, тканях и единичных клетках (секвенирование транскриптомов), а также анализировать регуляцию их активности (анализ экспрессии микроРНК и метилирования генома). В настоящее время на рынке представлено сразу несколько разработок, позволяющих определять последовательность полных геномов организмов, проводить анализ экспрессии генов и метилирования генома. Эти подходы реализуются на секвенаторах нового поколения производства коммерческих компаний Illumina, Thermo Fisher Scientific, Pacific Biosciences и Oxford Nanopore Technologies. Часть разработанных платформ уже ушли с рынка (например, GS FLX, 454/Roche или HeliScope/Helicos Bioscience); другие, пройдя несколько реинкарнаций и модификаций, прочно закрепились на нем (Illumina и Thermo Fisher Scientific); третьи только нащупывают почву, намереваясь занять свою нишу и найти своего потребителя (например, Oxford Nanopore Technologies).
Появление высокопроизводительных технологий секвенирования сопровождается прогрессом программного обеспечения — создаются алгоритмы с открытым программным кодом, появляются открытые источники данных и платформы для вычислений. Новые математические и информационные технологии позволяют геномике развиваться быстрее и использовать более сложные алгоритмы. Эти алгоритмы могут включать в себя сразу несколько приложений и программ и позволяют работать с очень большим объемом данных.
Секвенирование «нового поколения» применяется как для анализа геномов организмов, для которых уже доступен референсный геном (ресеквенирование), так и для того, чтобы впервые расшифровать геном организма (секвенирование de novo).
Для ресеквенирования успешно используют платформы, генерирующие большое количество коротких чтений (секвенируемых фрагментов ДНК), поскольку даже относительно короткие фрагменты ДНК успешно картируются (картирование, или выравнивание, — процесс биоинформатического поиска расположения конкретного короткого фрагмента в полной геномной последовательности) на референсный геном (последовательность ДНК в цифровом виде, составленную учеными как общий репрезентативный пример последовательности генома конкретного вида) при биоинформатическом анализе данных. Такие выравненные чтения могут использоваться для поиска однонуклеотидных полиморфизмов (SNPs), малых делеций и инсерций или других структурных изменений в геноме.
Что касается секвенирования de novo и сборки новых, ранее не прочитанных, геномов, то использование коротких чтений сильно усложняет сборку, особенно в случае больших по размеру и сложно устроенных геномов эукариот (например, полиплоидных геномов). В этих случаях используют комбинированный подход — сочетание платформ, генерирующих как короткие, так и длинные чтения. При сборке генома de novo ученые уподобляются ребенку, пытаясь правильно сложить элементы геномного пазла (короткие фрагменты отсеквенированной ДНК) в единую картину, созданную эволюцией за сотни миллионов лет (рис. 6).
Рисунок 6. Cеквенирование de novo и сборка новых, ранее непрочитанных, геномов требует значительных усилий.
В то же время наибольший интерес представляет отнюдь не сама последовательность генома, а понимание того, как он функционирует. Новые методы секвенирования НК позволяют оценивать уровень метилирования ДНК, проводить анализ дифференциальной экспрессии генов, в том числе и генов-регуляторов (например, микроРНК). Возможность анализа экспрессии генов в биологических системах открывает перед исследователем огромные возможности. Например, этот метод можно применять при исследовании функционирования центральной нервной системы человека (для понимания основных молекулярных аспектов работы головного мозга [11], [12]), при оценке защитного ответа клеток на атаки вирусов [13] или ответной реакции на стресс [14]. Не менее интересные данные может дать изучение регуляции экспрессии генов посредством анализа их метилирования [15] или изучение экспрессии некодирующих РНК [16], [17].
Оценка уровня метилирования генома, например, позволяет определить, какие генные пути и сети включаются в ответ на меняющиеся факторы окружающей среды; такие работы зачастую проводят для изучения эволюционных механизмов в живых системах. Изучение экспрессии кодирующих белки и некодирующих РНК в разных тканях и клетках также позволяет понять и описать гены, вовлеченные в жизнедеятельность клеток, органов и организмов.
Пиросеквенирование
Технологию предложил в 1996 году Пол Нирен с коллегами из Королевского технологического института в Стокгольме [19]. Затем ее коммерциализировали (2005 год) и воплотили в приборе GS FLX, 454 производства Roche (2008 год). Этим методом можно определять нуклеотидную последовательность фрагментов геномной ДНК размером 300–500 пар оснований (п.о.). Особо следует отметить тот факт, что подавляющее большинство NGS-методов требуют предварительной фрагментации ДНК для упрощения ферментативных реакций. К обоим концам фрагментированной ДНК «пришивают» ДНК-адаптеры (данная конструкция называется ДНК-библиотекой), необходимые для эмульсионной ПЦР (эПЦР) на магнитных сферах и последующего секвенирования.
Готовые ДНК-библиотеки иммобилизуют на магнитных сферах. Затем магнитные сферы с нанесенной на них клональной библиотекой доставляют на проточную ячейку, где в присутствии праймера, дезоксинуклеотидтрифосфатов и ферментов — ДНК-полимеразы, люциферазы, АТФ-сульфурилазы — происходит циклический синтез новой цепи.
Во время цикла пиросеквенирования при образовании фосфодиэфирной связи между матричной цепочкой ДНК и нуклеотидом синтезируемой цепи выделяется пирофосфат, который запускает каскад химических реакций, приводящих к выделению АТФ, необходимой для реакции окисления люциферина с выделением кванта света, который фиксируют аналоговой интегральной микросхемой (ПЗС-матрицей), состоящей из светочувствительных фотодиодов. Нуклеотиды, не вовлеченные в синтез новой цепи, удаляют из проточной ячейки, и начинается следующий реакционный цикл, в ходе которого добавляют дезоксинуклеотидтрифосфат другого типа (рис. 7).
Рисунок 7. Принцип пиросеквенирования. При включении нуклеотида в синтезируемую цепочку ДНК происходит регистрация высвобождающихся пирофосфатов — побочного продукта реакции полимеризации нуклеотидов в ДНК.
Пиросеквенирование от «Диаэм»
Принцип пиросеквенирования используется в секвенаторе PyroMark Q24, производимом компанией Qiagen. Этот прибор предназначен для одновременного прочтения 24 коротких последовательностей (до 100 нуклеотидов) и широко применяется в научных исследованиях и диагностике для точечного генотипирования и анализа метилирования. Основное достоинство секвенатора PyroMark — высокая точность и возможность анализа практически любого точечного полиморфизма.
Материал предоставлен партнёром — компанией «Диаэм»
Технология секвенирования на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов
Технология секвенирования на молекулярных кластерах, так же как и пиросеквенирование, подразумевает синтез новой молекулы ДНК по матрице. Этот метод начали разрабатывать еще в середине 90-х годов прошлого века химики Шанкар Баласубраманиан и Дэвид Кленерман из Кембриджа, изучавшие работу ДНК-полимеразы на молекулярном уровне, используя флуоресцентно меченые нуклеотиды и ДНК-матрицу, иммобилизованную на поверхности [20]. Творческие семинары в лаборатории и дружеские посиделки в баре привели к коммерциализации этой технологии в 2006 году под брендом Solexa, который спустя год был приобретен компанией Illumina. Сейчас платформа продолжает развиваться, и потребителям предлагают новые линейки приборов.
Суть метода заключается в следующем. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры, необходимые для ПЦР и последующего секвенирования на молекулярных кластерах. Полученные ДНК-библиотеки иммобилизуют на поверхности проточной ячейки, где и проводят циклический процесс секвенирования. Реакционная смесь для синтеза комплементарной ДНК подается на поверхность проточной ячейки и содержит ферменты, олигонуклеотиды, а также четыре типа флуоресцентно меченых дезоксинуклеозидтрифосфатов. После включения в синтезируемую цепь ДНК нуклеотида-терминатора идентифицируют с помощью ПЗС-матрицы как тип включенного нуклеотида, так и его положение. Затем терминирующая группа и флуоресцентная краска отщепляются от нуклеотида, и цикл синтеза повторяется. Эта серия шагов продолжается определенное количество раз, число которых задает пользователь (рис. 8).
Рисунок 8. Принцип секвенирования на молекулярных кластерах: полимеризация (синтез «дочерней» цепочки) ДНК с использованием флуоресцентно меченых нуклеотидов внутри специальной камеры, регистрирующей флуоресценцию.
Размер чтений, получаемых с секвенатора, может достигать 300 п.о. (прибор Illumina MiSeq). Кроме того, серия секвенаторов 2017 года NovaSeq позволяет определять последовательность до 48 геномов человека за один запуск прибора.
Технология циклического лигазного секвенирования
Технология циклического лигазного секвенирования была разработана группой Джорджа Макдональда Черча [21] и, в отличие от представленных выше, использует метод лигирования (формирование химических связей между нуклеотидами при помощи специального фермента — лигазы). Данный подход к секвенированию НК коммерциализировали в 2006 году, и приборы, известные под брендом SOLiD, уже длительное время представлены на рынке (первоначально развитием этой системы секвенирования занималась компания Applied Biosystems, а затем Life Technologies и Thermo Fisher Scientific).
Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером 25–75 п.о. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры, необходимые для эПЦР на магнитных сферах и последующего секвенирования на проточной ячейке.
Магнитные сферы с нанесенной на них клональной библиотекой помещают на проточную ячейку, где и происходит секвенирование с помощью лигирования восьминуклеотидных зондов, несущих четыре различных флуорофора на 5’-конце. Флуоресценция считывается с помощью специальной камеры после каждого цикла секвенирования и, затем переводится в последовательность нуклеотидов (рис. 9).
Рисунок 9. Принцип лигазного секвенирования и последовательность зондов, которые используют при секвенировании. Зонды для секвенирования можно разделить на несколько участков (начиная с 3’-конца): первые два нуклеотида зонда лигируются к комплементарным участкам на секвенируемой ДНК-библиотеке, нуклеотиды с третьего по пятый — вырожденные (т.е. могут гибридизоваться с любыми тремя нуклеотидами секвенируемой ДНК-библиотеки). Нуклеотиды с шестого по восьмой также способны гибридизоваться с любыми тремя нуклеотидами секвенируемой ДНК-библиотеки, однако они отщепляются вместе с флуоресцентным красителем в конце каждого цикла секвенирования.
Технология лигазного секвенирования применялась в приборах, выпускаемых под брендом SOLiD. Спустя несколько поколений приборов пробоподготовку усовершенствовали, и на рынок вышла новая линейка приборов — 5500, 5500xl, а также 5500w, использующий изотермальную ПЦР (WildFire технология) для клонирования ДНК-библиотек [22].
Ионное полупроводниковое секвенирование
Технология, предлагаемая в этой приборной линейке, основана на использовании полупроводниковых микрочипов для секвенирования. Суть этого подхода весьма проста и заключается в регистрации локального изменения рН на микрочипе в момент удлинения синтезируемой цепи ДНК-полимеразой на ДНК-матрице (рис. 10).
Рисунок 10. Принцип полупроводникового секвенирования основан на обнаружении ионов водорода, которые выделяются во время полимеризации ДНК.
Секвенаторы нового поколения от «Диаэм»
Высокопроизводительные секвенаторы нового поколения Ion S5/S5 XL (Thermo Fisher Scientific) работают по технологии полупроводникового секвенирования Ion Torrent, которая обеспечивает простейшую процедуру таргетного секвенирования, высокую скорость и экономичность. Использование микрочипов различной производительности позволяет проводить на одном приборе анализ как отдельных генов, бактериальных геномов, так и экзомов и транскриптомов.
Материал предоставлен партнёром — компанией «Диаэм»
Пробоподготовка (приготовление ДНК-библиотек) напоминает таковую при циклическом лигазном секвенировании. Первоначально ДНК фрагментируют, затем к концам полученных фрагментов лигируют специфические ДНК-адаптеры, необходимые для эмульсионной ПЦР на магнитных сферах и последующего секвенирования.
Подготовка библиотек для NGS: решение от «Диаэм»
Выделение НК и подготовка библиотек для NGS — это довольно трудоемкий процесс, который включает множество шагов, занимает немало времени и требует максимальной сосредоточенности оператора. На помощь ученым-лаборантам приходят автоматизированные технологии на каждом из этапов пробоподготовки:
Материал предоставлен партнёром — компанией «Диаэм»
Одномолекулярное секвенирование
SMRT-секвенирование (single molecule real time sequencing), предложенное сотрудниками компании Pacific Biosciences, не только позволило отказаться от проведения полимеразной цепной реакции при пробоподготовке, но и дало возможность наблюдать за работой ДНК-полимеразы, наращивающей синтезируемую цепь, в реальном времени [23].
Создание платформы Pacific Biosciences не только решило проблему ПЦР-дупликатов, но и значительно увеличило длину чтений, что крайне важно при сборке геномов de novo. Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером до 20 000 п.о. с лигированными к их концам специфическими ДНК-адаптерами, необходимыми для последующего секвенирования.
Сама реакция секвенирования молекул ДНК проходит в специальных ячейках (SMRT-ячейки) на прозрачной (кремниевой) подложке, с напыленным на нее слоем алюминия. В основе метода лежит использование технологии Zero-mode waveguide (ZMW) [24]. Сквозь дно в ячейку подается свет, однако благодаря особенностям ее строения, пучок фотонов не рассеивается, а освещает только конкретную часть (на подложке), где закреплена молекула phi29 ДНК-полимеразы. Эта полимераза была выбрана в качестве «считывающего» фермента благодаря своей высокой точности, скорости синтезирования дочерней цепи и эффективной работе с нуклеотидами, несущими флуоресцентную метку [25].
Смысл SMRT-секвенирования схож с описанными ранее методами NGS — ДНК-полимераза достраивает вторую цепь исследуемой молекулы ДНК, используя нуклеотиды, меченные различными флуоресцентными метками, которые регистрируют при помощи конфокальной микроскопии. В 2016 году анонсировали покупку платформы Pacific Biosciences биотехнологическим гигантом Roche Diagnostics, однако сделка так и не состоялась [26].
Разработка другого способа одномолекулярного секвенирования (коммерциализированного к настоящему времени) началась в конце прошлого века, когда группа американских ученых наглядно продемонстрировала возможность побуждать молекулы ДНК и РНК проходить сквозь ионный канал диаметром 2,6 нм в двуслойной липидной мембране под воздействием электрического поля. Более того, уже тогда исследователи сумели различать ДНК и РНК, а также оценивать длину входящих в нанопору олигонуклеотидов [27]. Спустя 13 лет впервые продемонстрировали возможность определения последовательности НК нанопоровым секвенированием [28], а затем данную технологию коммерциализировала и представила на рынок компания Oxford Nanopore Technologies (рис. 11).
Рисунок 11. Принцип нанопорового секвенирования, коммерциализованный компанией Oxford Nanopore Technologies. Данный тип секвенирования основан на измерении меняющейся силы тока при прохождении молекулы НК сквозь нанопору в двухслойной мембране.
Суть работы нанопоровых систем (MinION, GridION X5, PromethION и SmidgION), предложенных британской компанией, достаточно проста. Реакционная камера, в которой проходит процесс считывания последовательности НК, разделена двухслойной мембраной с единичной порой. К камере прикладывается напряжение, вызывающее движение ионов и молекул ДНК или РНК через пору. При прохождении молекулы НК сечение поры (доступное для миграции ионов) уменьшается, в результате чего сила тока падает. Таким образом, считывая изменение силы тока, можно определять тип нуклеотида, проходящего через пору в конкретный отрезок времени.
Кроме описанных выше двух технологий компания Helicos Biosсiences пыталась продвинуть на биотехнологический рынок свою технологию одномолекулярного секвенирования — true Single Molecule Sequencing (tSMS). Данный подход во многом схож с технологией секвенирования на молекулярных кластерах (Illumina), однако позволяет обходиться без ПЦР при пробоподготовке.
Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером до 50 п.о. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры. Полученные ДНК-библиотеки иммобилизуют на поверхности проточной ячейки, где и проводят циклический процесс секвенирования. Один цикл состоит из удлинения синтезируемой на матрице цепочки за счет одного из четырех флуоресцентно меченых нуклеотидов, присоединение которого детектируется прибором.
Небольшая длина чтения (до 50 п.о., медиана — 30 п.о.) и большое количество ошибок (3–5%) данной платформы привели к оттоку потенциальных покупателей. Технология не получила широкого распространения, несмотря на потенциальную применимость в работе со сложными образцами, например, в палеогеномике [29], где отказ от ПЦР мог бы привести к сокращению процентного соотношение экзогенной (мусорной) ДНК в анализируемых образцах древней ДНК [30]. В итоге, в конце 2012 года компания Helicos Biosciences была признана банкротом и прекратила свое существование [31].
Одномолекулярное секвенирование длинных фрагментов ДНК может найти свое применение в самых разнообразных областях, и, что самое интересное, при работе с единичными клетками позволяет описывать их молекулярный «портрет» [32]. Это особенно важно при анализе транскриптомов клеток, позволяя описывать все возможные изоформы активных генов — благодаря длине чтений, недоступных для технологии Solexa или PostLight [33].
Секвенирование третьего поколения
Технологию одномолекулярного секвенирования можно также назвать технологией третьего поколения, поскольку она работает по принципу, совершенно отличному от того, который применяется в секвенаторах второго поколения. Кроме того, характерной особенностью таких секвенаторов является их сверхкомпактность. Например, самый компактный портативный секвенатор MiniION имеет вес всего 100 граммов и работает от USB 3.0 обычного компьютера или ноутбука. Первые приборы MiniION уже применяют и в России (официальный дистрибьютор Oxford Nanopore — компания «Диаэм»).
MiniION — портативный прибор для прямого секвенирования ДНК/РНК онлайн от Oxford Nanopore.
Для высокопроизводительного секвенирования Oxford Nanopore разработал приборы, в которые можно параллельно установить несколько секвенаторов MiniION:
В настоящее время Oxford Nanopore работает над созданием модели секвенатора SmidgION, который будет работать от обычного смартфона и сможет применяться в полевых условиях, где нет лаборатории и даже компьютера.
Материал предоставлен партнёром — компанией «Диаэм»
Партнер этой публикации — компания SkyGen: молодой игрок на рынке продукции для LifeScience-лабораторий в России и СНГ
У нас есть три основных принципа:
Бóльшая часть производителей в нашем портфолио — это прямые эксклюзивные поставщики. Мы являемся первым звеном в поставках для таких компаний как Agilent Technologies, New England Biolabs, Oxford Nanopore, QIAGEN, Macherey-Nagel, NIMAGEN, EdgeBio, Thermo Scientific, SIGMA-ALDRICH, Santa Cruz Biotechnology, ChemGenes, Bruker, Dornier, Bio Molecular Systems, Gilson, Opentrons, Titertek-Berthold.
В 2017 году компания «СкайДжин» стала официальным дистрибьютором нанопоровых секвенаторов Oxford Nanopore Technologies в России, Белоруссии и Казахстане. Наши специалисты окажут техническую поддержку и проведут обучение на месте. С нами технология нанопорового секвенирования стала доступной для вас!
Мы верим: чтобы быть близкими к вам, недостаточно просто выставлять счета и осуществлять доставку. Нам важно глубоко разобраться в теме и быть поддержкой для вас. Для этого мы публикуем новости, обзоры и высоко ценим любые замечания и критику. Каждый продукт мы «пропускаем» через себя. Анализируем плюсы и минусы, представляем, как и где он будет работать, консультируемся с вами. И, как результат, создаем методички, проводим семинары и презентации.
Сегодня мы предлагаем современные решения для проведения секвенирования на различных платформах — от капиллярного секвенирования и NGS до мономолекулярного анализа с технологией Oxford Nanopore. Выбор за вами!
Ознакомиться с потенциалом применения новой технологии нанопорового секвенирования MinION можно здесь.
Вы всегда можете обратиться к нам, связавшись с менеджерами или написав по адресу info@skygen.com, а также позвонив по телефону +7 (495) 215-02-22 или бесплатной линии 8 (800) 333-12-26.
Мы стараемся угнаться за вами в научном познании мира, мы стараемся учиться и расти вместе с вами!
Материал предоставлен партнёром — компанией «СкайДжин»
Использование секвенирования нового поколения
Производительность и относительная доступность NGS-методов привели к настоящей революции в биологической и медицинской науке. Более того, благодаря новым подходам появилась реальная возможность проводить ранее технически недоступные исследования. Использование секвенирования нового поколения позволяет проводить такие проекты как:
HLA-типирование с помощью NGS-методик
Примером практического применения таргетного секвенирования в медицинских целях может быть HLA-типирование — секвенирование генов главного комплекса гистосовместимости, ответственных за распознавание организмом клеток по типу «свой-чужой». HLA-типирование проводят при трансплантации, при патологиях беременности, при аутоиммунных заболеваниях и др. NGS, в отличие от других методов HLA-типирования (серологический анализ, методы SSP и SSO, секвенирование по Сэнгеру), позволяет получить полную последовательность генов главного комплекса и гистосовместимости и, соответственно, точный генотип.
Набор для HLA-типирования Holotype HLA от компании Omixon позволяет не только секвенировать эти гены, но и правильно интерпретировать результаты секвенирования. Этот продукт включает в себя реагенты для пробоподготовки и программное обеспечение HLA Twin для интерпретации и предназначен для всех современных моделей NGS-секвенаторов.
Материал предоставлен партнёром — компанией «Диаэм»
Решение по анализу транскриптома от «Диаэм»
Большим недостатком метода NGS является высокая стоимость реагентов. Однако на сегодняшний день можно найти на рынке относительно недорогую альтернативу: например, наборы Lexogen для анализа транскриптома. Это хорошее решение для полнотранскриптомного секвенирования, построения экспрессионного профиля, обогащения фракции мРНК и удаления нецелевых фракций РНК. Для интерпретации данных секвенирования хорошим помощником является программное обеспечение RNA-Seq от Lexogen.
Материал предоставлен партнёром — компанией «Диаэм»
Заключение
В наши дни происходит бурное развитие технологий, связанных с исследованием генов, белков и других молекулярных структур живых организмов. Разрабатываются портативные, быстрые, точные и универсальные методы исследований биологических объектов. Появление высокопроизводительных технологий секвенирования НК сопровождается развитием в области программного обеспечения, создаются алгоритмы с открытым программным кодом. Новые математические и информационные технологии позволяют геномике развиваться быстрее и использовать более сложные алгоритмы (например, нейронные сети).
На сегодняшний день объемы получаемой секвенаторами информации значительно обогнали возможности математического анализа получаемых результатов. Но даже несмотря на это, биомедицинская наука вовлечена в круговорот геномной революции, когда новые данные появляются ежедневно, а биотехнологические компании предлагают все новые и новые решения, значительно облегчающие диагностику заболеваний, приближая мир к новому направлению — персонализированной медицине [34].
Календарь
На основе статей спецпроекта мы решили сделать календарь «12 методов биологии» на 2019 год. Эта статья представляет апрель.











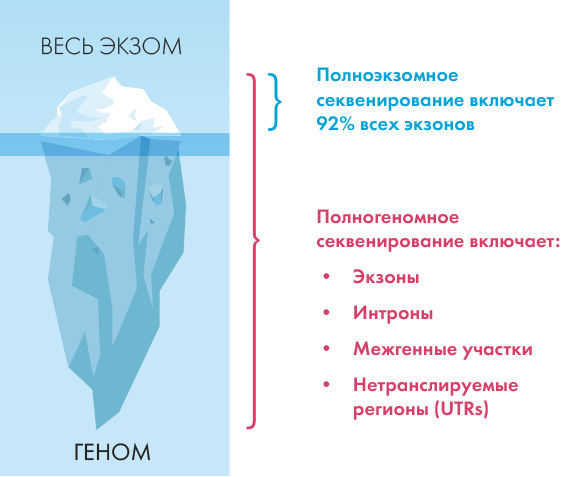
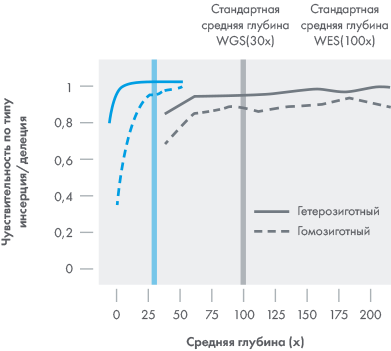
.png)
.png)