Хантер синдром что это такое
Синдром Хантера: две истории о любви
Время чтения: 10 мин.
Синдром Хантера — очень редкое генетическое заболевание. Если его не лечить, оно приводит к тяжелой инвалидности и, как следствие, к преждевременной смерти. До 2007 года лечение синдрома Хантера ограничивалось паллиативной помощью. Сегодня заболевание по-прежнему невозможно вылечить полностью, но благодаря поддерживающей терапии можно замедлить прогрессирование болезни и смягчить некоторые ее проявления.
Рассказываем, что такое синдром Хантера, а еще — истории двух семей, где растут дети с этим заболеванием.
Синдром Хантера относится к группе заболеваний со сложным названием — мукополисахаридозы. Сыну Снежаны Митиной из Москвы диагностировали эту болезнь, когда мальчику было три года. Врачи говорили, что Паша проживет максимум 6-8 лет и все это время будет испытывать постоянную боль. Когда Снежана узнала диагноз, она мысленно «нарисовала» его название: «”Муко” — это очень больно, “поли” — что-то непонятное, но этого непонятного много, “сахаридоз” — это сладкий ребенок. То есть «страдает мой сладкий ребенок, непонятно почему».
Это был 2003 год и никакой информации о мукополисахаридозе на русском языке не было. Снежана рассказывает, что нашла в интернете одну картинку с абзацем текста на английском языке — там говорилось, что дети с синдромом Хантера быстро погибают от этой болезни, лечения нет и не будет. Врачи предложили ей смириться, сын будет тихо угасать. Но никакой тишины не было — Павлик постоянно кричал от боли.
Что такое синдром Хантера
Синдром Хантера — наследственное прогрессирующее мультисистемное заболевание, обусловленное накоплением гликозаминогликан в органах и тканях, что приводит к поражению костно-суставной, сердечно-сосудистой систем, ЦНС, патологии глаз, ЛОР-органов. Внешне это проявляется в огрубении черт лица — гаргоилизме: у детей с этим заболеванием короткая шея, большая голова, крупный нос с широкой плоской переносицей и большими ноздрями, толстый язык, выступающие брови, толстая кожа, жесткие волосы, редкие маленькие зубы, скрюченные, как птичьи лапы, руки. Такие дети больше похожи друг на друга, чем на своих родителей и здоровых братьев и сестер.
Практически все люди с этим заболеванием небольшого роста, со временем крупные и мелкие суставы теряют подвижность, образуются контрактуры. Также страдает нервная система, органы зрения, слуха, сердечно-сосудистая и бронхолегочная системы.
Синдром Хантера относится к группе лизосомных болезней накопления — мукополисахаридозам, или МПС. В результате мутаций в гене IDS в организме больных МПС отсутствует один из ферментов — идуронатсульфатаза, который необходим для расщепления гликозаминогликан — ГАГ.
Гликозаминогликаны — это макромолекулы, которые являются структурным компонентом соединительной ткани. Сами по себе ГАГ нетоксичны, но их накопление в лизосомах из-за дефицита фермента приводит к нарушению функции и гибели клеток.
Обычно в раннем возрасте у детей практически отсутствуют признаки заболевания, но в процессе накопления ГАГ симптомы начинают быстро проявляться.
Заболевание названо в честь канадского врача Чарльза Хантера, который в 1917 году впервые описал подобные нарушения у двух братьев.
У кого бывает синдром Хантера
Если женщина является носителем МПС II типа, то с 50% вероятностью она передаст заболевание своему сыну. Но если ребенок получит здоровую Х-хромосому (женщины имеют две Х хромосомы, одна из которых может быть с геном заболевания), заболевания не возникнет. Также существует 50% вероятность, что дочь женщины-носительницы будет носителем заболевания и в будущем сможет передать болезнь уже своему ребенку.
МПС II типа — очень редкое заболевание, оно встречается у 1 из 132 000 родившихся мальчиков. Сейчас в мире более 2000 людей с синдромом Хантера.
Умственное развитие детей с синдромом Хантера зависит от формы заболевания. У пациентов с легкой формой синдрома Хантера интеллект может быть в пределах нормы. При тяжелом течении у детей в возрасте от двух до четырех лет постепенно нарастает задержка психоречевого развития, а впоследствии они теряют ранее приобретенные навыки. Но даже после утраты речи дети сохраняют способность к эмоциональным переживаниям, способны понимать своих близких, испытывать радость и огорчение.
Вылечить синдром Хантера в настоящее время невозможно, но существует множество вариантов поддерживающей терапии, позволяющих существенно улучшить качество жизни людей с этим заболеванием.
Сейчас используются два препарата для ферментозаместительной терапии (идурсульфаза и идурсульфаза бета), которые позволяют замедлить прогрессирование болезни и смягчить некоторые ее проявления. Но те клинические признаки заболевания, которые есть у ребенка, исправить нельзя, но можно предотвратить прогрессированием заболевания.
Диагностика синдрома Хантера (МПС II типа) осуществляется с помощью биохимических и молекулярно-генетических методов. Сначала ребёнка консультирует генетик, затем у него определяют содержание ГАГ в моче — у людей с МПС он выше, чем у здоровых. Потом измеряют активность фермента идуронат-сульфатазы в лейкоцитах или в плазме крови. Если активность фермента снижена, проводится молекулярно-генетическое обследование — сперва у ребенка, а затем у матери, что выяснить, является ли она носителем заболевания.
Продолжительность жизни людей с синдромом Хантера различна. Люди со слабой формой синдрома доживают до шестидесяти лет, известен случай жизни до 87 лет. Но люди с тяжелой формой синдрома обычно живут лишь до подросткового возраста.
Какой красивый, какой сказочный Хантер!
Снежана Митина рассказывает, что сын родился весом почти 5 кг и плакал басом. Тогда это было забавно, но потом стало ясно, что вес новорожденного более 4 кг, шумное дыхание и низкий голос являются основанием для обращения к генетику. Потом Павлик не особо отличался от сверстников, только казался более ярким. Тревожило, что он чуть чаще простужался, болел отитами, по сравнению с другими детьми говорил чуть меньше слов, но его папа тоже поздно начал разговаривать, а кандидатскую диссертацию защитил. У ребенка были немножко странно согнутые коленки, но ортопед сказал, что мальчик пухленький и ножкам тяжело. На самом деле это было начало контрактур.
После того, как у Паши была странная реакция на наркоз во время операции по грыжесечению (мальчик хохотал как пьяный), его на два с половиной месяца положили в больницу.
Мукополисахаридоз II типа у детей
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Мукополисахаридоз II типа у детей
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 3 года)
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Эпидемиология
Клиническая картина
Cимптомы, течение
Диагностика
Диагноз МПС II устанавливается на основании совокупности клинических данных, результатов лабораторного исследования и молекулярно-генетического анализа 1.
— нарушения со стороны желудочно-кишечного тракта
Основные физикальные проявления в зависимости от возраста дебюта МПСII может варьировать (Приложение Г1).
• Рекомендован контроль общего клинического анализа крови, мочи.
• Рекомендовано проведение компьютерной томографии (КТ) головного мозга.
Лечение
Комментарии: целесообразность обусловлена частыми респираторными инфекциями.
Медицинская реабилитация
Проводится в комплексе реабилитационных мероприятий. Коррекционно-педагогическое воздействие определяется в зависимости от тяжести и длительности течения болезни, структуры нарушений здоровья, степени недоразвития познавательной деятельности, типа эмоционального реагирования, особенностей поведения ребенка. Включение коррекционно-педагогического сопровождения в комплекс восстановительных мероприятий обеспечивает дополнительную оценку динамики психического развития как одного из важных показателей состояния здоровья, повышает эффективность терапевтических вмешательств, снижает экономическое бремя данной патологии за счет социализации пациентов и сохранения психологического потенциала трудоспособных членов семьи.
Прогноз
Продолжительность жизни составляет примерно от 10 до 15 лет. Как правило, причиной смерти являются сердечные и респираторные осложнения. При этом у ряда пациентов описаны случаи более продолжительной жизни: до 50-60 лет.
| Вид медицинской помощи | Специализированная медицинская помощь |
| Условия оказания медицинской помощи | Стационарно / в дневном стационаре |
| Форма оказания медицинской помощи | Плановая |
Профилактика
МУКОПОЛИСАХАРИДОЗ II ТИПА (синдром Хантера): Новые возможности терапии.

Накопление гликозаминогликанов в лизосомах вызывает тяжелые нарушения функций клеток, органов и систем, определяя широкий диапазон клинических проявлений. Клиническая гетерогенность вызвана, в том числе, и многообразием происходящих мутаций патологического гена.
Обычно фенотипический «манифест» наступает в 2-4 года, до этого периода никаких признаков болезни не прослеживается. Первые признаки заболевания проявляются в виде дисморфических черт лица (утолщение губ, ноздрей, широкая переносица, увеличение лобных бугров, густые брови). Затем появляется макроглоссия, аномалии зубов, макроцефалия, скафоцефалия, изменения скелета, короткая шея, низкий рост, толстая кожа с узелками, папулами, гирсутизмом, паховые, пупочные грыжи, тугоподвижность и деформации мелких и средних суставов, увеличенный живот за счёт спленомегалии. Изменения со стороны центральной и периферической нервной систем включают задержку психоречевого развития, нарушение поведения (упрямство, агрессию, гиперактивность), нарушение сна, псевдобульбарный синдром, симптоматическую эпилепсию, спастический тетрапарез, атрофическую гидроцефалию, нейросенсорную тугоухость, поражение зрительных нервов. Со стороны сердечно-сосудистой системы отмечаются аритмии, лёгочная гипертензия, гипертрофическая или рестриктивная кардиомиопатии, поражения клапанного аппарата сердца, вторичная застойная сердечная недостаточность. С раннего возраста отмечается увеличение глоточных и небных миндалин, хроническая ринорея, обструкции верхних дыхательных путей, трахеобронхомаляции, происходит утолщение голосовых связок с изменением тембра голоса. Возможны жизнеугрожающие апноэ. Ребенок часто болеет респираторными инфекциями, отитами, пневмониями.
Поражения глаз представлены атипичным пигментным ретинитом, разрушением сетчатки, атрофией зрительного нерва. Прогрессирующая потеря слуха обуславливает поведенческие нарушения, трудности в обучении. С возрастом эти изменения становятся более выраженными. Молекулярной основой дефекта соединительной ткани является нарушенный обмен гликозамингликанов.
Диагностика СХ основана на совокупности клинических, инструментальных и лабораторных данных. Постановка диагноза СХ базируется на определении активности идуронат-2-сульфотазы в лейкоцитах крови, сыворотке крови, культуре фибробластов кожи, уровня гликозаминогликанов в моче, ДНК-тестировании. Пренатальная диагностика основана на измерении активности фермента I2S в амниотической жидкости, амниоцитах, тканях, ворсинках хориона.
Реальные возможности помощи детям с СХ в нашей стране появились с момента регистрации в РФ в 2008 году рекомбинантной человеческой идуронат-2-сульфатазы, препарата «элапраза» (Idursulfatase), Shire (США), основного патогенетического лекарственного средства в лечении такой категории пациентов. Необходимы еженедельные инфузии препарата в дозе 0,5 мг/кг.
Поскольку в прогрессирующий патологический процесс вовлекаются все органы и системы оказание медицинской помощи пациентам с МПС должно строится с позиций междисциплинарного, комплексного подхода.
Однако, на сегодняшний день, организацию медицинской помощи детям с МПС в целом в РФ нельзя оценивать положительно. Отсутствие опыта и знаний у врачей по данному разделу патологии, стандартов лечения данной болезни диктуют необходимость организации системы мероприятий по информированию «узкопрофильных» специалистов и педиатров общей практики об особенностях дебюта и течения МПС.
Проблемы большинства пациентов с редкими заболеваниями схожи – это поздние сроки диагностики, а следовательно — и начала лечения, трудности в получении дорогостоящих лекарственных препаратов, стоимость которых в год составляет около 400 тысяч евро для одного пациента, В РФ средний возраст начала единственно необходимой ферментозаместительной терапии среди детей с МПС – 6,8 года, когда патологические изменения приобретают уже необратимый характер.
Требуют решения вопросы социальной, юридической, паллиативной помощи, в чём не просто нуждаются, а остро нуждаются эти пациенты и семьи, в которых они воспитываются.
Прогноз: При быстром прогрессировании болезни с вовлечением ЦНС больные обычно погибают в возрасте 10-15 лет, при «мягких» формах МПС 11 типа – продолжительность жизни может составить 50 лет и более при соответствующем лечении [3].
Приводим собственное клиническое наблюдение мальчика П. с синдромом Хантера.
Ребенок родился у молодых здоровых родителей, от 1-ой беременности, протекавшей на фоне анемии легкой степени, гестоза отечной формы. Роды первые, срочные. Масса тела при рождении 3430,0, длина 52 см, окружность груди 34 см. Оценка по шкале Апгар 8/9 баллов, ранняя неонатальная желтуха. Темпы физического и психомоторного развития на первом году жизни соответствовали эпикризным срокам. Профилактические прививки осуществлялись в соответствии с национальным календарём прививок, осложнений не отмечалось. В раннем возрасте переносил частые респираторные инфекции, бронхиты, пневмонию. В 3-х летнем возрасте диагностированы аденоиды III степени. С 3,5 лет появилась тугоподвижность и ограничение объёма движений в суставах, тугоухость, задержка роста, с 5 лет – лицевые дисморфии и другие фенотипические особенности: широкая переносица, толстые губы, редкие зубы, короткие и толстые пальцы, короткая шея, шумное дыхание, увеличение живота за счет гепатоспленомегалии.
В 5 лет выполнена аденотомия, в 5,5 лет — оперативное вмешательство по поводу паховой и пупочной грыжи. При ультразвуковом исследовании выявлена единственная, правая почка.
В 6 лет 4 месяца госпитализирован в кардиоревматологическое отделение ДОКБ г. Орла с жалобами на боли и скованность в лучезапястных, коленных, голеностопных, межфаланговых суставах. По результатам клинико-лабораторно-инструментальных исследований, консультаций специалистов выставлен диагноз: Вторичная артропатия. Двухстворчатый аортальный клапан с недостаточностью 2-3 степени.
Нейросенсорная тугоухость. гиперметропический астигматизм. Мукополисахаридоз VI тип?
При дообследовани в медико-генетическом центре г. Москвы, выявлена повышенная экскреция дерматансульфата и гепарансульфата с мочой, значительное снижение идуронатсульфатазы в плазме, до 3,18 nmol/4h/ml (норма 297-705), что позволило уточнить тип мукополисахаридоза –II тип (синдром Хантера).
В 6 лет 11 месяцев – лечение в психоневротическом отделении НЦЗД г. Москвы с клиническим диагнозом: Мукополисахаридоз II типа (синдром Хантера). Вторичная кардиомиопатия. Темповая задержка психо-речевого развития. Рецидивирующий бронхит. Контрактуры крупных и мелких суставов конечностей 1-2 степени. Гиперметропический астигматизм. Единственная правая почка. Нейросенсорная тугоухость 2 степени.
С сентября 2011 года в возрасте 7 лет 11 месяцев в условиях педиатрического отделения ДОКБ г. Орла ребёнку проводится ферментозаместительная терапии – еженедельные инфузии препаратом «Элапраза» » (Idursulfatase), Shire (США). Пропусков введений не было. Осложнений не отмечалось. На 01.06.2012 года мальчик вырос на 4см (рост 125см), 1,5 кг прибавил в весе (масса 28,5кг), улучшилась переносимость физических нагрузок, сократились размеры печени, селезёнки, увеличился объем движений в суставах.
Таким образом, представленный клинический случай имеет большой практический интерес для врачей-педиатров, генетиков и других специалистов в связи с редкостью данного наследственного заболевания. Заслуживает внимания появление новых возможностей в терапии таких пациентов, а именно, внедрение единственно эффективного патогенетического средства идуронат-2-сульфатазы (элапраза), открывающего новые реалии в прогнозе данного заболевания.
Своевременная диагностика мукополисахаридозов, правильное ведение данного контингента больных, раннее назначение ферментозаместительной терапии, будут способствовать уменьшению тяжести заболевания, снижению инвалидизации детей, более адекватной интеграции их в общество.
Синдром Ханта
При герпетической инфекции, помимо тройничного нерва, также могут поражаться III, IV и/или VI пары ЧН, а при инфекционном поражении коленчатого ганглия и возможно нарушение функции лицевого и/или преддверно-улиткового нерва.
СИМПТОМЫ
• Синдром Ханта-1 (невралгия коленчатого узла, синдром коленчатого узла, Herpes zoster oticus, Zoster oticus) — в остром периоде высыпания локализуются в наружном слуховом проходе, на ушной раковине, мягком нёбе, нёбных миндалинах.
• Синдром Ханта-2 — герпетические высыпания появляются в наружном слуховом проходе, передних 2/з языка, на волосистой части
головы.
ДИАГНОСТИКА
• Синдром Ханта-1. Клиническая картина постгерпетической невралгии коленчатого узла складывается из односторонней постоянной или периодической боли в области уха,в ипсилатеральной половине лица, наружном слуховом проходе, нарушения вкуса на передних 2/з языка, умеренного периферического пареза мимических мышц.
• Синдром Ханта-2. Боли в задней части полости рта иррадиируют в ухо, затылок, шею и сопровождаются расстройством слюноотделения, горизонтальным нистагмом, головокружением.
ПРИЧИНЫ
• Синдром Ханта-2 обусловлен поражением сенсорных узлов нескольких ЧН преддверно-улиткового, языкоглоточного, блуждающего, а также второго и
третьего шейных спинномозговых нервов.
ЛЕЧЕНИЕ
Лечение должно производиться исключительно врачом-неврологом. Самолечение недопустимо.
Мукополисахаридозы – путь к диагнозу
Мукополисахаридозы (МПС) – это группа редких наследственных заболеваний, которые обусловлены дефицитом определенных лизосомных ферментов, участвующих в разрушении гликозаминогликанов (ГАГ), и характеризуются накоплением последних в различных органах и тканях. У части больных наблюдается медленное прогрессирование МПС, а типичные фенотипические признаки появляются в подростковом или зрелом возрасте, что в значительной степени затрудняется диагностику. Одним из типичных симптомов МПС является нарастающая тугоподвижность суставах, поэтому такие больные могут обращаться за помощью к ревматологам. Особенность поражения опорно-двигательного аппарата при МПС – отсутствие локальных и системных признаков воспаления. Важное диагностическое значение имеют системные проявления, такие как пупочная и паховая грыжа, изменение черт лица, помутнение роговицы, низкий рост, увеличение печени и селезенки, рецидивирующие инфекции дыхательных путей и средний отит и др. Для подтверждения диагноза определяют экскрецию ГАГ с мочой и активность лизосомных ферментов, а также проводят молекулярно-генетическое исследование.
Мукополисахаридозы (МПС) – это группа редких лизосомных болезней накопления, характеризующихся нарушением обмена гликозаминогликанов (ГАГ). Причиной каждого МПС является генетически обусловленный дефицит определенного лизосомного фермента, участвующего в разрушении ГАГ. Практически все МПС (за исключением МПС II) наследуются по аутосомно-рецессивному типу и с равной частотой встречаются у мальчиков и девочек. МПС II – это Х-сцепленное рецессивное заболевание, которое развивается у мальчиков, хотя описаны отдельные случаи и у девочек [1].
Накопление ГАГ в лизосомах различных тканей сопровождается разнообразными системными проявлениями, в том числе поражением опорно-двигательного аппарата, сердца, нервной системы, органа зрения и др., и приводит к прогрессирующему ухудшению функции внутренних органов. МПС в целом характеризуются тяжелым течением и неблагоприятным прогнозом, поэтому многие пациенты умирают в детском или подростковом возрасте. Однако возможно и более легкое течение заболевания, в частности МПС I и МПС VI, когда симптомы появляются в подростковом или старшем возрасте и нарастают более постепенно, а пациенты доживают до зрелого возраста [2,3]. В таких случаях диагноз нередко устанавливают с опозданием, а МПС длительно протекает под маской других болезней, прежде всего ревматических. Выделение легкого варианта течения МПС весьма условно, так как при медленном прогрессировании заболевания в конечном итоге развивается тяжелое поражение отдельных органов, которое приводит к инвалидизации пациентов и может потребовать оперативного вмешательства (например, протезирование тазобедренного сустава, имплантация искусственного клапана сердца, декомпрессия спинного мозга) [4]. МПС – это неоднородная группа заболеваний, которые имеют как общие фенотипические признаки, так и существенные различия (табл. 1, 2)
| • МПС I, II и VII – системные заболевания, поражающие различные органы и ткани, включая ЦНС; неврологические нарушения не бывают изолированными. |
| • МПС III характеризуется поражением ЦНС при отсутствии соматических проявлений. |
| • МПС IV поражает в основном опорно-двигательный аппарат и не сопровождается снижением интеллекта. |
| • При МПС VI наблюдается поражение различных органов и систем, интеллект остается нормальным. |
| Тип | Название | Фермент | Ген | Тип наследования | Лечение |
|---|---|---|---|---|---|
| МПС I | Синдромы Гурлера, Шейе или Гурлера-Шейе | α-L-идуронидаза | IDUA 4p16.3 | Аутосомно-рецессивный | Ларонидаза |
| МПС II | Синдром Хантера | Идуронат-2-сульфатаза | IDS Xq28 | X-сцепленный рецессивный | Идурсульфаза |
| МПС IIIA | Синдром Санфилиппо A | Гепаран-N-сульфатаза | SGSH 17q25.3 | Аутосомно-рецессивный | Разрабатывается |
| МПС IIIB | Синдром Санфилиппо В | α-N-ацетилглюкозаминидаза | NAGLU 17q21 | Аутосомно-рецессивный | |
| МПС IIIC | Синдром Санфилиппо С | Ацетил-КоА α-глюкозамин-ацетил-трансфераза | HGSNAT 8p11.1 | Аутосомно-рецессивный | |
| МПС IIID | Синдром Санфилиппо D | N-ацетилглюкозамин-6-сульфатаза | GNS 12q14 | Аутосомно-рецессивный | — |
| MПС IVA | Синдром Моркио А | Галактозамин-6 сульфатсульфатаза | GALNS 16q24.3 | Аутосомно-рецессивный | Элосульфаза |
| MПС IVB | Синдром Моркио В | β-Галактозидаза | GLB1 3p21.33 | Аутосомно-рецессивный | — |
| MПС VI | Синдром Марото-Лами | Арилсульфатаза B | ARSB 5q11.q13 | Аутосомно-рецессивный | Галсульфаза |
| МПС VII | Синдром Слая | β-Глюкуронидаза | GUSB 7q21.11 | Аутосомно-рецессивный | Разрабатыва |
| МПС IX | Синдром Натовича | Гиалуронидаза I | AH 3p21.3-p21.2 | Аутосомно-рецессивный | — |
Своевременная диагностика МПС сегодня приобрела особое значение, учитывая возможность заместительной терапии рекомбинантными ферментами, такими как идурсульфаза (МПС II), ларонидаза (МПС I), галсульфаза (МПС VI) и элосульфаза (МПС IVA), которые позволяют улучшить состояние больных или по крайней мере затормозить прогрессирование заболевания [5]. Ферментозаместительная терапия (ФЗТ) более эффективна, если ее начинают на более раннем этапе, когда еще отсутствуют необратимые проявления болезни.
Трудности диагностики МПС
МПС относятся к очень редким (орфанным) заболеваниям. В разных странах различные МПС регистрировали с частотой 1 на 16000-29000 живых новорожденных [6,7], а в 2007 году в Скандинавских странах распространенность МПС составила всего 4-7 случаев на 1 млн населения [8]. В связи с этим информированность врачей, особенно наблюдающих взрослых пациентов, о МПС низкая. Дополнительные сложности в диагностике возникают при более легком течении МПС, особенно при отсутствии типичных фенотипических проявлений, таких как низкий рост и характерные черты лица. Например, в зависимости от клинических проявлений и течения выделяют три формы МПС I – тяжелую (синдром Гурлера), промежуточную (синдром Гурлера-Шейе) и более легкую (синдром Шейе). Во всех случаях причиной заболевания является мутация гена, кодирующего α-L-идуронидазу. У пациентов с синдромом Гурлера симптомы появляются в раннем детском возрасте и часто наблюдается тяжелое поражение ЦНС, в то время как при синдроме Шейе симптомы менее выражены и возникают значительно позднее, а когнитивные расстройства обычно отсутствуют [9]. Два варианта течения заболевания – тяжелый и более легкий – возможны и при МПС VI (синдроме Марото–Лами), обусловленном мутациями гена, кодирующего арилсульфатазу В.
В клинике им. Е.М. Тареева за последние 3 года были обследованы 5 взрослых пациентов в возрасте от 20 до 33 лет с МПС VI. У трех из них диагноз был установлен в подростковом возрасте (от 7 до 16 лет), а у двух – в возрасте 23 и 30 лет, соответственно. Необ хо димо подчеркнуть, что хотя у двух последних пациенток наблюдалось замедленное прогрессирование заболевания, тем не менее, в обоих случаях на момент госпитализации в клинику имелось тяжелое поражение опорно-двигательного аппарата с резким ограничением подвижности в суставах, пороки клапанов сердца, стеноз шейного отдела позвоночника, нарушение проходимости дыхательных путей, поражение органа зрения и др. Обе пациентки были низкого роста (132 и 146 см) [4].
Замедленное прогрессирование течение иногда на блюдается и при МПС II (синдроме Хантера). Два года назад в нашу клинику был госпитализирован 42-летний пациент с МПС II, который был диагностирован в возрасте 13 лет на основании характерных изменений внешнего вида и наличия синдрома Хантера у старшего брата и подтвержден при энзимологическом (дефицит активности идуронат-2-сульфатазы) и молекулярногенетическом (мутация с.236С>А гена IDS в гемизиготном состоянии) исследованиях [10]. В течение длительного времени состояние пациента оставалось удовлетворительным. Успешно закончил школу, а затем институт. Работал инженером на заводе. С 30-летнего возраста прогрессирующее снижение чувствительности и боли в кистях и стопах, ухудшение зрения и выпадение центральных полей зрения, однако продолжал работать. Резкое ухудшение состояния, связанное с развитием сердечной недостаточности на фоне тяжелого порока аортального клапана, было отмечено только за год до госпитализации, т.е. в возрасте около 40 лет.
При обращении к ревматологу на МПС может указывать поражение суставов, не сопровождающееся признаками воспаления, такими как припухание, повышение СОЭ и/или уровня С-реактивного белка [12]. T. Rocha Siqueira и соавт. измеряли экскрецию ГАГ с мочой у 55 пациентов в возрасте от 3 до 21 года (в среднем 9 лет) с невоспалительной артропатией неясного генеза. У всех больных определялись дискомфорт или боль в суставах, а у 2/3 – скованность [12]. Экскре ция ГАГ была повышена у 1 из 55 больных. При дополнительном обследовании у 15-летней пациентки был установлен диагноз МПС II. Хотя очевидным ограничением этого исследования было небольшое число обследованных пациентов, тем не менее, полученные данные указывают на возможную роль скрининга в диагностике более легких форм МПС.
Как заподозрить МПС?
В настоящее время известно 11 лизосомных ферментов, дефицит которых приводит к развитию 7 типов МПС [13]. Замедленное прогрессирование заболевания и более поздняя диагностика чаще отмечаются у пациентов с МПС I, IV, VI и VII, в то время как другие типы МПС обычно характеризуются тяжелым течением и более короткой продолжительностью жизни. Следует отметить, что в задачи практического врача не входит дифференциальная диагностика различных МПС – вполне достаточно заподозрить этот диагноз и направить пациента на консультацию к генетику и/или провести скрининговое исследование (определение экскреции ГАГ с мочой).
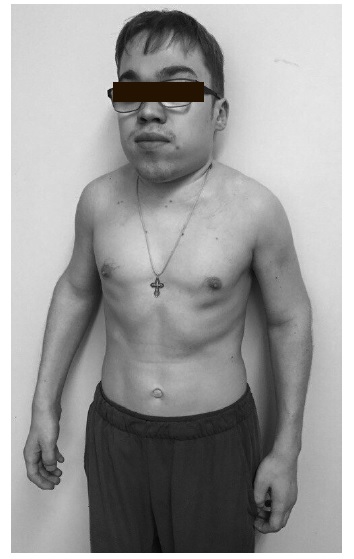
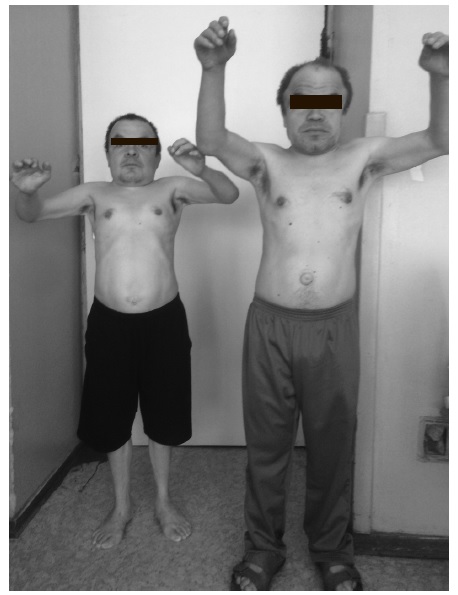
Хотя МПС представляют собой неоднородную группу болезней и отличаются по тяжести течения и частоте поражения центральной нервной системы, тем не менее, в целом клинические проявления некоторых из них достаточно однотипны и позволяют предположить наличие заболевания, особенно у пациентов старшего возраста при наличии типичного фенотипа. При осмотре пациентов с МПС прежде всего обращают на себя внимание низкий рост, непропорциональное строение скелета (короткие туловище и шея, длинные конечности), а также грубые черты лица, толстые губы, увеличение языка, запавшее переносье, увеличение расстояния между глазами (гипертелоризм) (рис. 1, 2). При тяжелом течении МПС рост пациентов не превышает 95-100 см, хотя при медленном развитии заболевания может достигать 140-150 см. Например, в нашей серии наблюдений рост 5 взрослых пациентов с МПС VI варьировался от 132 до 153 см, а рост 42-летнего пациента с МПС II составлял 158 см. В крупном исследовании среди 121 пациента с МПС VI доля взрослых составляла около 25% [14]. Средний рост больных в возрасте 19-24 и 25-56 лет равнялся 142,7±20,1 и 157,0±8,5 см, соответственно. Таким образом, по крайней мере у части больных МПС рост может быть фактически нормальным.
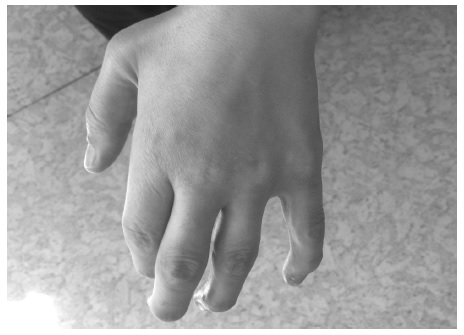
При всех МПС развивается тяжелое поражение опорно-двигательного аппарата (множественный дизостоз), которое проявляется тугоподвижностью и контрактурами суставов (в большей степени ухудшается разгибание), деформацией кистей (“когтистая лапа”) (рис. 3) и позвоночника (кифоз, сколиоз), воронкообразной грудной клеткой. Наблю даются недоразвитие таза, дисплазия головок бедренных костей и вальгусное положение шейки бедренной кости. Ограничение подвижности суставов отмечается уже в детском или подростковом возрасте, постепенно нарастает и в конечном итоге служит причиной инвалидизации больных.
Для МПС IV (синдрома Моркио), в отличие от других типов МПС, типично развитие гипермобильности суставов, обусловленной деформацией метафизов, гипоплазией костей и деградацией соединительной ткани, окружающей суставы [15].
У пациентов с МПС часто наблюдаются обструкция глотки, верхних и нижних дыхательных путей, связанная с увеличением языка и миндалин, сужением трахеи, утолщением надгортанника и голосовых связок, отложением ГАГ в слизистой оболочке бронхов. Обструкция дыхательных путей сопровождается затрудненным дыханием и громким храпом с эпизодами апноэ во время сна. Характерно развитие рецидивирующего среднего отита, вызывающего прогрессирующую тухоугость, которая обусловлена как кондуктивными, так и нейросенсорными механизмами. Причинами нарушения функции дыхания могут быть также небольшие размеры и малоподвижность грудной клетки, растя жение живота в сочетании с кифозом, сколиозом и значительным поясничным лордозом, а также рецидивирующие инфекции нижних дыхательных путей.
Еще одно типичное проявление МПС – поражение клапанов сердца, частота которого достигает 60-90%. С. Wippermann и соавт. обследовали 84 больных в возрасте от 1 до 47 лет с различными типами МПС [16]. Частота недостаточности митрального и/или аортального клапана составила 75,0%, однако тяжелая митральная или аортальная регургитация наблюдалась только в 4,8% и 8,3% случаев, соответственно. Частота пороков клапанов сердца достигала 89-100% у больных МПС I, II и VI, но была ниже у пациентов с МПС III и IV – 3366%. В другом исследовании у 28 больных МПС VI частота поражения митрального клапана составила 96%, трикуспидального – 71% и аортального – 43% [17]. Следует отметить, что, в отличие от некоторых других лизосомных болезней накопления, таких как болезнь Фабри, для МПС не характерно тяжелое поражение миокарда.
У большинства больных МПС I, VI и VII часто отмечается помутнение роговицы, в то время как при других типах МПС оно отсутствует [18].
У пациентов с тяжелыми формами МПС I и II наб лю дается поражение ЦНС (поведенческие расстрои ̆ства, задержка умственного развития, ухудшение интеллекта, тяжелая когнитивная дисфункция) [10]. Выраженные неврологические и когнитивные расстройства характерны также для МПС III. В то же время у большинства пациентов с МПС VI сохраняется нормальный интеллект.
МПС I, II и VI могут привести к развитию синдрома запястного канала, проявляющегося стойкой болью и онемением пальцев кисти в результате сдавления срединного нерва между костями и сухожилиями мышц запястья. Возможно также сдавление спинного мозга вследствие сужения спинно-мозгового канала и нестабильности атлантоаксиального канала. Компрессион ная миелопатия может осложниться слабостью в нижних конечностях и спастической параплегией или квадриплегией.
Диагноз и дифференциальный диагноз
Алгоритм диагностики и дифференциальной диагностики МПС у пациентов с поражением опорно-двигательного аппарата представлен на рис. 4 [19]. Если контрактуры суставов определяются у новорожденного ребенка, то наиболее вероятен диагноз артрогрипоза – заболевания, характеризующегося врожденными контрактурами двух и более суставов несмежных областей в сочетании с мышечной гипо- или атрофией. Различают артрогрипоз с поражением верхних и/или нижних конечностей, генерализованный и дистальный варианты. Артрогрипоз – это не самостоятельная нозологическая форма, а скорее физический симптом, который может быть обусловлен различными причинами, например, ограничением движений плода во время его развития (многоводие, маловодие, пороки развития и опухоли матки, многоплодная беременность), нарушением развития мышц (вирусные инфекции), генетическими факторами и др.
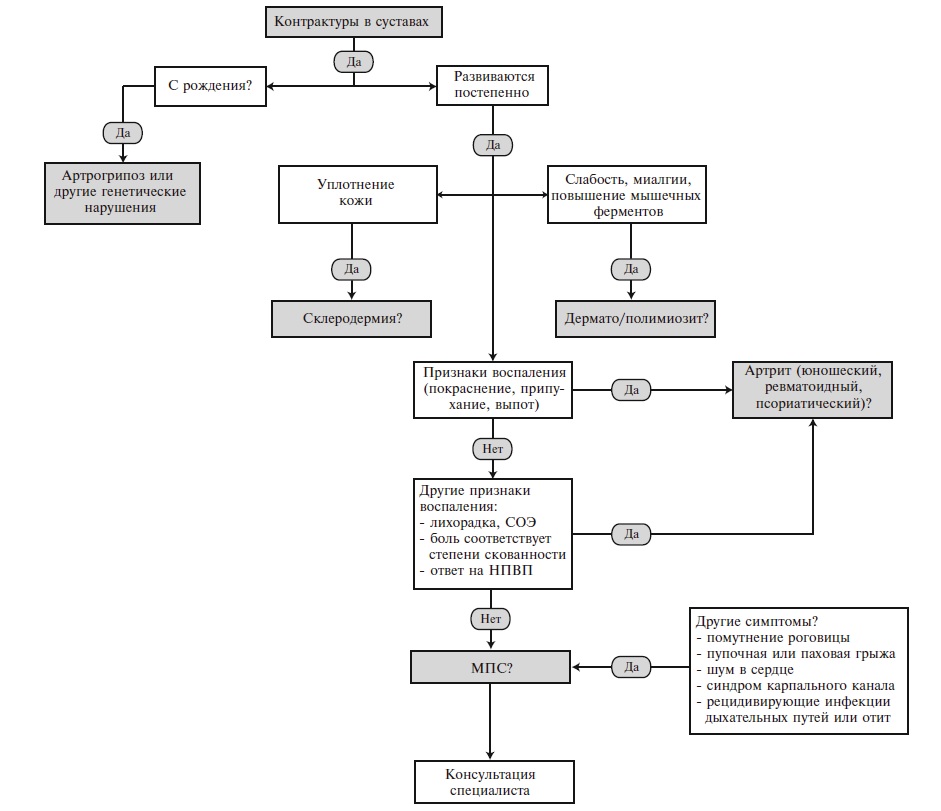
Боли и тугоподвижность суставов, появляющиеся в детском или подростковом возрасте, могут имитировать ревматические заболевания, в частности юношеский идиопатический артрит, ревматоидный или псориатический артрит. Основное значение для дифференциальной диагностики с этими заболеваниями имеют отсутствие воспалительной боли (т.е. боли, возникающей по утрам и сопровождающейся скованностью, которая уменьшается на фоне физической активности), локальных (припухание и болезненность при пальпации суставов) и системных (повышение температуры тела и/или СОЭ и уровня С-реактивного белка) признаков воспаления (рис. 4) [19]. Глюкокортикостероиды неэффективны, хотя нестероидные противовоспалительные препараты могут несколько уменьшить имеющиеся симптомы.
Признаки поражения суставов, появляющиеся в более старшем возрасте, часто расценивают как первичный остеоартроз. Дифференцировать поражение опорно-двигательного аппарата при МПС с этим забо леванием позволяют развитие артропатии в подростковом или молодом возрасте при отсутствии факторов риска первичного остеоартроза и наличие других типичных проявлений генетического заболевания (карликовый рост, измененные черты лица, порок клапана сердца, помутнение роговицы и т.п.) (табл. 3).
| Поражение опорно-двигательного аппарата |
| Контрактуры суставов, развивающиеся в раннем возрасте и не сопровождающиеся признаками воспаления или эрозивными изменениями костей |
| “Когтистая лапа” |
| Деформация позвоночника (сколиоз, кифоз, лордоз) |
| Рентгенологические признаки множественного дизостоза |
| Другие клинические проявления |
| Нарастающая “грубость” черт лица |
| Помутнение роговицы |
| Короткая ригидная шея |
| Частые респираторные инфекции, рецидивирующий средний отит, заложенность носа, шумное дыхание/храп |
| Шум в сердце |
| Пупочные и/или паховые грыжи |
| Низкий рост |
| Нарушение походки |
| Увеличение живота за счет печени и селезенки |
Скрининговым методом диагностики МПС является измерение экскреции ГАГ с мочой. Определение типа ГАГ в моче (дерматансульфат, гепарансульфат, хондороитинсульфат и кератансульфат) с помощью тонкослойной хроматографии или электрофореза имеет определенное значение для дифференциальной диагностики МПС, однако результаты этих исследований все же не позволяют установить окончательный диагноз. Экскреция ГАГ с мочой у детей, подростков и молодых людей с МПС обычно превышает таковую у здоровых людей сопоставимого возраста [13]. Однако у взрослых людей с МПС, особенно с более легкими и медленно прогрессирующими формами заболевания, она может оказаться близкой к норме. Соответственно, следует осторожно интерпретировать результаты этих тестов и продолжать обследование, если диагноз МПС представляется вероятным на основании клинических данных.
Следующий этап диагностики – определение активности лизосомных ферментов в высушенных пятнах крови, лейкоцитах или фибробластах. Анализ высушенных пятен крови обычно проводят в тех случаях, когда образец необходимо отправить в лабораторию, находящуюся в другом городе или стране. Более надежным считают исследование лейкоцитов, выделенных из цельной крови, или культивированных фибробластов.
Для подтверждения диагноза проводят молекулярногенетическое исследование, которое необходимо также для выявления носителей мутантных генов и пренатальной диагностики.
Лечение мукополисахаридозов
Для патогенетической терапии МПС применяют рекомбинантные формы ферментов, дефицит которых лежит в основе развития соответствующего заболевания, в том числе ларонидазу для лечения МПС I, идурсульфазу – МПС II, галсульфазу – МПС VI, элосульфазу альфа – МПС IVa (в Российской Федерации последний препарат не зарегистрирован). Все препараты предназначены для внутривенного введения. Их эффективность и безопасность установлены как в рандомизированных, двойных слепых, плацебо-контролируемых исследованиях, так и длительных наб людательных исследованиях, позволивших изучить отдаленные эффекы ФЗТ [20].
Эффективность и безопасность галсульфазы оценивали в рандомизированном, двойном слепом, плацебоконтролируемом, 24-недельном исследовании 3 фазы у 39 больных МПС VI [21]. Критериями эффективности были толерантность к физической нагрузке и экскреция ГАГ с мочой. Лечение галсульфазой в течение 24 недель по сравнению с плацебо привело к значительному увеличению пройденной за 12 минут дистанции (р=0,025) и скорости подъема по лестнице (р=0,053) и достоверному снижению экскреции ГАГ с мочой (p
Заключение
МПС – это группа редких заболеваний, которые обычно диагностируют поздно вследствие низкой информированности врачей о лизосомных болезнях накопления. Наибольшие диагностические трудности возникают при более легких формах МПС, которые характеризуются медленным развитием соматических проявлений и стертостью типичных внешних признаков. Выделение легких, или ослабленных (attenuated), форм МПС весьма условно, так как в конечном итоге у таких больных развиваются инвалидизирующие осложения, часто требующие оперативного лечения. Одним из типичных симптомов МПС I, II и VI является нарастающая тугоподвижность в суставах, поэтому такие больные могут обращаться за помощью к ревматологам. Особенность поражения опорно-двигательного аппарата при МПС – отсутствие локальных (припухания суставов и болезненности при их пальпации) и системных (повышения температуры тела и/или СОЭ и уровня С-реактивного белка) признаков воспаления. Исключить остеоартроз позволяют молодой возраст пациента и отсутствие типичных факторов риска дегенеративных заболеваний суставов. Важное диагностическое значение имеют системные проявления, такие как пупочная и паховая грыжа, изменение черт лица, помутнение роговицы, низкий рост, увеличение печени и селезенки, рецидивирующие инфекции дыхательных путей и средний отит и др. Если заподозрен диагноз МПС, то необходимо определить экскрецию ГАГ с мочой, а также измерить активность лизосомных ферментов и провести молекулярно-генетическое исследование для подтверждения диагноза.


