Хелаты что это в химии
Удобрения в хелатной форме – что это такое и чем они полезны для растений
Добавление статьи в новую подборку
«Продвинутые» садоводы сегодня все чаще отдают предпочтение удобрениям в хелатной форме. Они отлично усваиваются растениями, безопасны для окружающей среды и весьма эффективны. Знакомьтесь – хелаты, комплексные минеральные удобрения нового поколения.
В данном материале мы расскажем вам, чем хелатные микроудобрения отличаются от обычных, для чего они нужны растениям, в каких дозах вносятся и как приготовить хелатные удобрения своими руками.
Микроэлементы в жизни растений
Микроэлементы – элементы питания растений, столь же необходимые для их нормальной жизнедеятельности, как и основные компоненты (калий, магний, фосфор и др.). Их отличие от последних состоит лишь в том, что требуются они организму в микроскопических количествах, отсюда и название. Соответственно и удобрения, содержащие микроэлементы, именуются микроудобрениями.

Для растений выделяют семь важнейших микроэлементов:
Они принимают самое непосредственное участие в биохимических процессах в растениях – влияя на обмен и транспорт макроэлементов, участвуя в синтезе хлорофилла, активизируя ферменты… Кроме этого, микроэлементы играют важную роль в нормальном росте и развитии растения, его устойчивости к заболеваниям и неблагоприятным факторам окружающей среды, урожайности в конечном итоге.
Недостаток того или иного микроэлемента можно обнаружить даже визуально, если нет возможности сделать анализ почв:
Разумеется, в идеальном случае все микроэлементы должны содержаться прямо в почве и оттуда самостоятельно добываться растениями. Однако это – в идеале, который мы редко можем наблюдать на среднестатистическом дачном участке. К тому же в условиях интенсивного огородничества со временем истощаются даже самые богатые почвы – истощаются и требуют для получения качественного урожая внесения всех полезных веществ (в том числе и микроудобрений) извне.

Итак, микроудобрения растениям необходимы на протяжении всего периода роста – начиная с этапа прорастания семян и вплоть до сбора урожая. Какие же микроудобрения выбрать из множества существующих?
Ранее в состав большинства удобрений микроэлементы входили в виде растворимых неорганических солей. Увы, в таком виде усваивались они растениями весьма слабо – не более чем на 20-35%! Соли эти могли вступать в перекрестные реакции в почве с образованием неусвояемых соединений. К тому же некоторые из них даже токсичны, а еще – требуют дополнительной переработки почвенными микроорганизмами. А из-за низкой усвояемости приходится регулярно вносить достаточно большие дозы таких удобрений, неотвратимо засоляя почвы. Это сложно и неэффективно.

Но, к счастью, прогресс не стоит на месте. И сегодня производителю есть что предложить садоводам-огородникам в этом плане. Например, удобрения в форме хелатов.
Хелатные минеральные удобрения
Хелаты для растений – неоценимые помощники, они позволяют усваивать микроэлементы практически на 90%, что позволяет в несколько раз снизить химическую нагрузку на почву! За счет чего?
Комплексы эти биологически активны и близки по своей структуре к природным веществам (например, хлорофилл или витамин В12 по своей природе являются хелатами), поэтому безвредны и эффективны для растения, особенно молодого. Они не связываются в почве и не вступают в сторонние реакции. Именно на основе хелатов созданы препараты нового поколения для предпосевной обработки семян, последующих внекорневых подкормок растений и капельного орошения.

В различных удобрениях используются разные хелатирующие агенты, которые могут различаться по силе связывания ионов и по стабильности в среде той или иной кислотности. Поэтому при выборе хелатного удобрения нужно учитывать, для каких именно растений и в каких почвах предстоит его использовать:
Когда использовать хелатные удобрения?
Хелатные удобрения могут быть «одиночными», включая лишь один микроэлемент (например, Fe-ЭДТА или Fe-ДТПА), а могут быть и комплексными (например, водный раствор хелатов микроэлементов Mn, Zn, Cu, Mo на основе ОЭДФ). Выбирать те или иные нужно, учитывая состояние растений и почвы именно на вашем участке.

Как правильно использовать хелатные удобрения? Общие рекомендации сводятся к тому, чтобы вносить хелаты в особенно важные для растения периоды жизни, чтобы действенно помочь им:
Разумеется, используются хелаты не только для огородных растений. Комнатные и садовые цветы также будут вам благодарны за такую подкормку. Например, большой популярностью у опытных садоводов пользуются хелатные удобрения для роз, которые заметно улучшают их качество и товарный вид цветов.
Как использовать удобрения-хелаты?
Наибольший эффект дает применение хелатных микроудобрений для обработки семян с последующей внекорневой и корневой подкормкой (в течение всего вегетационного периода, как мы упоминали выше). К тому же микроудобрения в хелатной форме можно вносить одновременно с другими макроудобрениями и ядохимикатами, если нет противопоказаний по совместимости веществ.
Обязательно читайте инструкцию по применению хелатов – производитель указывает на упаковке важные данные по особенностям состава и применения препарата!
В какой же форме и как употребляют хелатные микроудобрения.
Хелатные удобрения своими руками
В продаже чаще всего вы увидите жидкие хелатные удобрения. Преимущество таких водных растворов микроэлементов заключается в удобстве их применения – легко отмерять готовый рабочий раствор хелатов, легко его использовать (тогда как хелаты в сыпучей форме придется еще растворять согласно инструкции, ведь в сухом виде они неэффективны).
При желании вы можете изготовить хелатные моноудобрения и в домашних условиях. Расскажем технологию на примере наиболее востребованных железосодержащих хелатных удобрений:
Точно так же готовится хелат меди – в качестве исходных веществ используются 20 г медного купороса и 40 г аскорбиновой кислоты.
Напомним лишь, что домашние удобрения за счет большого количества балластных веществ подойдут скорее для профилактических обработок, чем для принятия срочных мер по лечению, к примеру, того же хлороза. К тому же они не хранятся (обработку растений нужно провести в тот же день) и не допускают дальнейшего разведения.
Итак, хелатные удобрения безопасны, высокоэффективны и удобны в применении. Они улучшают усвояемость основных питательных элементов и заметно помогают растениям. Единственным их недостатком можно назвать лишь повышенную цену – производство стоит достаточно дорого. Однако достоинства удобрений в хелатной форме с избытком покрывают этот изъян, надеемся, мы вам это доказали.
Хелатные соединения
Хелат, Хелаты, Хелатные соединения (от лат. chelate — клешня) или внутрикомплексные соединения — клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными (то есть имеющими несколько донорных центров) лигандами. Хелаты содержат центральный ион (частицу) — комплексообразователь и координированные вокруг него лиганды. Хелаты используют в химии для разделения, концентрирования и аналитического определения различных элементов.
См. также
Хелаты, или циклические комплексные соединения. Хелатами называют комплексные соединения, внутрення сфера которых состоит из циклических группировок, включающих комплексообразователь. Например, a-аминоуксусная кислота (глицин) может реагировать с гидроксидом меди с образованием сине-фиолетового прочного комплекса, растворимого в воде:
Cu(OH)2 + 2 NH2CH2COOH = [Cu(NH2CH2COO)2] + 2 H2O
Функции лиганда в этом комплексном соединении выполняет диметилглиоксимат-анион
образующий две химические связи с комплексообразователем, вследствие чего получаются два пятичленных циклических фрагмента, упрочняющих комплекс.
Строение получаемого хелата плоское; благодаря внутримолекулярным водородным связям (между лигандами) образуются еще две шестичленные циклические группировки, включающие атомы никеля и стабилизирующие частицу комплекса.
Реакция Чугаева очень чувствительна и селективна по отношению к катионам никеля(II) и позволяют уверенно определить его присутствие в любых химических объектах, а получаемый хелатный комплекс используется как пигмент.
Полезное
Смотреть что такое «Хелатные соединения» в других словарях:
ХЕЛАТНЫЕ СОЕДИНЕНИЯ — (хелаты внутрикомплексные соединения, клешневидные соединения) (от греч. chele клешня), комплексные соединения, в которых лиганд присоединен к центральному атому металла посредством двух или большего числа связей. Характерная особенность хелатных … Большой Энциклопедический словарь
хелатные соединения — (хелаты, внутрикомплексные соединения, клешневидные соединения) (от греч. chēlē клешня), комплексные соединения, в которых лиганд присоединён к центральному атому металла посредством двух или большего числа связей. Характерная особенность… … Энциклопедический словарь
ХЕЛАТНЫЕ СОЕДИНЕНИЯ — (хелаты, внутрикомплексные соединения, клешневидные соединения) (от греч. chele клешня), комплексные соединения, в к рых лиганд присоединён к центр. атому металла посредством двух или большего числа связей. Характерная особенность X. с. наличие… … Естествознание. Энциклопедический словарь
Хелатные соединения — (от греч. chele клешня) клешневидные соединения, один из классов химических комплексных соединений; то же, что Внутрикомплексные соединения … Большая советская энциклопедия
Соединения внутрикомплексные — комплексные циклические (хелатные, клешневидные) соединения, содержащие внутрисферные поликоординационные заместители, присоединенные к центральному атому металла как за счет главной валентности (замещение водорода), так и за счет побочной (через … Толковый словарь по почвоведению
Клешневидные соединения — хелатные соединения, один из классов химических комплексных соединений; то же, что Внутрикомплексные соединения … Большая советская энциклопедия
внутрикомплексные соединения — то же, что хелатные соединения. * * * ВНУТРИКОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ВНУТРИКОМПЛЕКСНЫЕ СОЕДИНЕНИЯ, то же, что хелатные соединения (см. ХЕЛАТНЫЕ СОЕДИНЕНИЯ) … Энциклопедический словарь
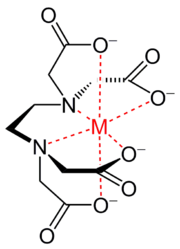
Внутрикомплексные соединения — Хелат иона металла и этилендиаминтетрауксусной кислоты Хелат, Хелаты, Хелатные соединения (от лат. chelate клешня) или внутрикомплексные соединения клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными … Википедия
Внутрикомплексные соединения — клешневидные соединения, хелатные соединения, один из классов комплексных соединений (См. Комплексные соединения). Классический пример В. с. гликоколят меди Адденд (радикал гликокола строения NH2CH2COO ) присоединяется к … Большая советская энциклопедия
ВНУТРИКОМПЛЕКСНЫЕ СОЕДИНЕНИЯ — то же, что хелатные соединения … Большой Энциклопедический словарь
Хелаты
Хелаты, хелатные соединения (от лат. chelate — клешня), также внутрикомплексные или циклические комплексные соединения — клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными (то есть имеющими несколько донорных центров) лигандами. Хелаты содержат центральный ион (частицу) — комплексообразователь и координированные вокруг него лиганды. Внутренняя сфера хелата состоит из циклических группировок, включающих комплексообразователь.
Иногда разделяют понятия хелатного и внутрикомплексного соединения. Второе определение применяют в случае, когда атом-комплексообразователь замещает протон лиганда в соединении.
Содержание
Пример
Аминоуксусная кислота (глицин) может реагировать с гидроксидом меди с образованием сине-фиолетового прочного комплекса, растворимого в воде:
Лиганд NH2CH2COO − (глицинат-ион) относят к категории бидентатных лигандов, образующих две химические связи с комплексообразователем — через атом кислорода карбоксильной группы и через атом азота аминогруппы.
Реакция Чугаева
Важное значение в химико-аналитической практике имеет открытая Л. А. Чугаевым реакция взаимодействия диметилглиоксима с катионами никеля(II) в аммиачной среде, приводящая к образованию малорастворимого ярко-красного комплексного соединения — бис(диметилглиоксимато)никеля(II).
Функции лиганда в этом комплексном соединении выполняет диметилглиоксимат-анион, образующий две химические связи с комплексообразователем, вследствие чего получаются два пятичленных циклических фрагмента, упрочняющих комплекс.
Строение получаемого хелата плоское; благодаря внутримолекулярным водородным связям (между лигандами) образуются еще две шестичленные циклические группировки, включающие атомы никеля и стабилизирующие частицу комплекса.
Реакция Чугаева очень чувствительна и селективна по отношению к катионам никеля(II) и позволяют уверенно определить его присутствие в любых химических объектах. Получаемый хелатный комплекс используется как пигмент.
Литература
См. также
Полезное
Смотреть что такое «Хелаты» в других словарях:
хелаты — сущ., кол во синонимов: 1 • микроудобрения (3) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
хелаты — Термин хелаты Термин на английском chelate Синонимы хелатные соединения, клешневидные соединения Аббревиатуры Связанные термины супрамолекулярная химия, хлорофилл Определение Кооординационные соединения, образуемые при взаимодействии ионов… … Энциклопедический словарь нанотехнологий
хелаты — хел аты, ов … Русский орфографический словарь
ХЕЛАТЫ — вещества, образующие с металлом комплексную соль, в которой металл закреплен по всем валентностям и пространственно находится внутри молекулы, так что его возможности вступления в реакцию снижаются. X. являются многие биополимеры, сложные… … Словарь ботанических терминов
Хелаты — (син.: комплексоны) соединения органических веществ с металлами, в которых атом металла связан с двумя или с большим числом атомов органического соединения (комплексообразователя) … Толковый словарь по почвоведению
ХЕЛАТНЫЕ СОЕДИНЕНИЯ — (хелаты, внутрикомплексные соединения, клешневидные соединения) (от греч. chele клешня), комплексные соединения, в к рых лиганд присоединён к центр. атому металла посредством двух или большего числа связей. Характерная особенность X. с. наличие… … Естествознание. Энциклопедический словарь
Внутрикомплексные соединения — Хелат иона металла и этилендиаминтетрауксусной кислоты Хелат, Хелаты, Хелатные соединения (от лат. chelate клешня) или внутрикомплексные соединения клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными … Википедия
Хелатные соединения — Хелат иона металла и этилендиаминтетрауксусной кислоты Хелат, Хелаты, Хелатные соединения (от лат. chelate клешня) или внутрикомплексные соединения клешневидные комплексные соединения, образуются при взаимодействии ионов металлов с полидентатными … Википедия
Микроудобрения — удобрения, содержащие Микроэлементы (В, Cu, Mn, Zn, Со и др.), т. е. вещества, потребляемые растениями в небольших количествах. Подразделяются на борные, медные, марганцевые, цинковые и др., а также полимикроудобрения, в составе которых 2 … Большая советская энциклопедия
Хелаты: как в них разобраться?
На рынке присутствуют разнообразные формы комплексных соединений металлов, используемых в кормлении животных. Все эти разнообразные формы называют «органическими микроэлементами», поскольку входящие в их состав микроэлементы образуют комплексы, или другие типы химических соединений, с органическими молекулами.
Химические процессы комплексообразования, или образования хелатов, понимаются по-разному различными специалистами отрасли кормопроизводства, что приводит к возникновению путаницы в терминах и интерпретации свойств продуктов. Часто встречаются такие термины, как «комплекс металла и аминокислот», «хелат металла и аминокислот», «комплекс металла с полисахаридом», «протеинат металла», однако официальные определения этих терминов расплывчаты и не проясняют ситуацию. В качестве примера в Таблице 1 приведены различные определения органических микроэлементов, используемых в сельском хозяйстве, в формулировках Ассоциации американских контролёров качества кормов (AAFCO, 1998).
Таблица 1. Органические комплексы минералов – определения терминов в формулировках AAFCO.
Комплекс металла и аминокислоты – продукт, образующийся при формировании комплекса между растворимой солью металла и аминокислотой.
Чтобы разобраться в запутанных определениях, характеризующих химические и физические свойства микроэлементов, прежде всего, необходимо выявить отличия между терминами «комплекс» и «хелат».
Комплексы или хелаты
Термин «комплекс» может использоваться при описании соединений, образующихся при взаимодействии иона металла с молекулой или ионом (лигандом), которые обладают свободной парой электронов. Такие ионы металлов связываются с лигандом посредством атомов-доноров, например, кислорода, азота или серы. Лиганды, обладающие только одним атомом-донором, называются монодентатными, а лиганды, обладающие двумя и более атомами-донорами, называеются би-, три- или тетрадентатными, также их иногда называют полидентатными.
Аминокислоты являются бидентатными лигандами, образующими связи с ионами металла посредством кислорода карбоксильной группы и азота аминогруппы.
Этилендиаминтетрауксусная кислота (ЭДТА) является примером гексадентатного лиганда, который содержит шесть атомов-доноров. ЭДТА образует очень прочные комплексы с большинством ионов металлов, и не очень подходит для образования хелатов минералов, поскольку биологическая доступность таких комплексов невысока.
Хотя могут образовываться хелаты, содержащие четыре, пять, шесть или семь колец, установлено, что наиболее стабильными являются хелаты, содержащие пять колец.
Также необходимо помнить о том, что хотя хелаты и являются комплексами, не все комплексы являются хелатами. Несмотря на простоту теории, объясняющей образование хелатов, необходимо строгое соблюдение множества условий для получения стабильного хелата минерала.
Лиганд должен содержать два атома, способных образовывать связи с ионом металла.
Лиганд должен образовывать гетероциклическое кольцо, причём металл должен располагаться «в конце» этого кольца.
Образование хелата металла должно быть пространственно (стерически) возможно. Для достижения стабильности необходимо соблюдать соотношение количества лиганда к минералу.
Истинные хелаты имеют «кольцевую структуру», образованную ковалентно-координационной связью между аминной и карбоксильной группами аминокислоты и ионом металла.
Как правило, хелаты образуются в результате реакции между неорганическими солями минералов, с приготовленной при помощи ферментов смесью аминокислот и небольших пептидов в контролируемых условиях. Такие аминокислотные и пептидные лиганды связываются с ионом металла не в одной точке, а в нескольких, в результате чего атом металла становится частью биологически стабильной кольцевой структуры. Аминокислоты и продукты ферментативного разрушения белков, например, небольшие пептиды, являются идеальными лигандами, поскольку они обладают как минимум двумя функциональными группами (аминной и гидроксильной), необходимыми для образования кольцевой структуры с минералом. Только «переходные элементы», например, медь, железо, марганец и цинк обладают необходимыми физико-химическими характеристиками, позволяющими им образовывать ковалентно-координационные связи с аминокислотами и пептидами с образованием биологически стабильных комплексов.
Аминокислоты и пептиды в качестве лигандов
Существуют различные мнения относительно преимуществ использования аминокислот в сравнении с пептидами при образовании хелатов минералов, ещё больше споров имеется по вопросу биологической доступности таких продуктов. Мы уже рассмотрели общие условия, необходимые для образования биологически стабильных хелатов минералов, однако следует также учитывать и другие факторы, оказывающие влияние на образование хелатов, основными из этих факторов являются:
Очевидно, что такой сложный химический феномен не следует чрезмерно упрощать. Однако чтобы прояснить ситуацию касательно преимуществ аминокислот либо пептидов в процессе образования хелатов минералов, мы рассмотрим факторы, влияющие на состояние равновесия и стабильность таких комплексов.
При растворении в воде соли металла, например, сульфата меди (II), с добавлением аминокислоты в качестве бидентатного лиганда, образуется ряд комплексов, каждый из которых обладает собственной константой стабильности, которая зависит от рН раствора. Это показано на Рисунке 1 (реакция сульфата меди (II) с глицином). Из данных, показанных на этом рисунке можно сделать некоторые важные выводы:
Рисунок 1. График изменения содержания меди, включённой в состав различных соединений, при изменении рН в растворе, содержащем медь (II) (0,001М) и глицин (0,002М). Горизонтальная ось: рН. Вертикальная ось: % Cu++
У различных ионов металлов различные константы стабильности. Поэтому, количество металла, входящего в состав конкретного соединения, зависит не только от величины рН раствора, но и от константы стабильности комплекса.
Стабильность содержащего металл комплекса зависит как от свойств металла, так и от свойств лиганда. Увеличение заряда иона, уменьшение размера и увеличение аффинности электронов способствует большей стабильности. На стабильность комплексов влияют также некоторые характеристики лигандов: (1) щёлочность лиганда, (2) количество металло-хелатных колец на единицу лиганда, (3) размер хелатного кольца, (4) пространственные эффекты, (5) резонансные эффекты и (6) атом лиганда. Поскольку комплексные соединения образуются в результате кислотно-основных реакций, как правило, более щелочные лиганды образуют более стабильные комплексы. Также большое значение имеет размер хелатного кольца.
Ещё глубже проанализировав Рисунок 1, можно заметить наличие существенных отличий между относительной стабильностью хелатов металлов, образованных аминокислотами и стабильностью протеинатов металлов. Поскольку протеинат металла является продуктом реакции хелатообразования между растворимой солью и аминокислотами и/или частично гидролизованным белком, можно предположить, что для конкретного иона металла количество графиков, характеризующих образование различных соединений, в состав которых входит металл, при образовании протеината, будет намного больше, чем при образовании хелата этого же металла с аминокислотой. Если считать график, отражающий распределение количества меди между различными соединениями, индикатором относительной стабильности при данной величине рН, и учитывать бесконечное количество комбинаций, возможных в результате взаимодействия как отдельных аминокислот, так и ди-, три- и даже тетрапептидов, то, теоретически, общая стабильность протеината в широком диапазоне рН должна быть намного больше, чем стабильность хелата данного металла с аминокислотой.
Очевидно, что в реальных условиях рассмотренные дополнительные факторы будут оказывать влияние на стабильность хелата. Однако можно ожидать, что протеинаты металлов будут обладать физико-химическими свойствами, необходимыми для сохранения постоянства характеристик при изменении рН.
Несмотря на наличие некоторой противоречивой информации, образование хелатов металлов – это не такой уж сложный процесс, в основе которого лежат фундаментальные законы химии. Мы можем выделить две формы истинных хелатов минералов, каждая из которых обладает определёнными химическими и биофизическими свойствами. Внимательно изучив факторы, влияющие на образование хелатов минералов, можно выявить различия между продуктами по показателю биологической стабильности и, следовательно, биологической доступности.