Химических элементов меньше чем простых веществ
Химических элементов меньше чем простых веществ
Какие два утверждения верны для характеристики как натрия, так и алюминия?
1) Наличие 12 протонов в ядрах их атомов
2) Нахождение валентных электронов в третьем электронном слое
3) Образование простых веществ-металлов
4) Существование в природе в виде двухатомных молекул
5) Образование ими высших оксидов с общей формулой
Запишите в поле ответа номера выбранных утверждений.
Это элементы одного периода (третьего), поэтому общим для натрия и алюминия является нахождение валентных электронов в третьем электронном слое; также оба образуют простые вещества-металлы.
Какие два утверждения верны для характеристики как магния, так и кремния?
1) Наличие трёх электронных слоёв в их атомах
2) Существование соответствующих им простых веществ в виде двухатомных молекул
3) То, что они относятся к металлам
4) То, что значение их электроотрицательности меньше, чем у фосфора
5) Образование ими высших оксидов с общей формулой
Запишите в поле ответа номера выбранных утверждений.
1. Наличие трёх электронных слоёв в их атомах — да, это элементы 3 периода;
2. Существование соответствующих им простых веществ в виде двухатомных молекул — нет;
4. То, что значение их электроотрицательности меньше, чем у фосфора — да, фосфор находится правее по периоду, значит, его электроотрицательность выше;
5. Образование ими высших оксидов с общей формулой — магний не образует такой оксид, т. к. это элемент IIА группы.
Виды простых и сложных веществ
Простые и сложные вещества в химии
В неорганической химии вещества по составу делятся на простые и сложные.
Сложные вещества — соединения:
Классификация простых веществ
1. Простые вещества условно делят на две группы: металлы и неметаллы.
Неметаллы в Периодической системе — это все элементы VIII А-группы (благородные газы) и VII А-группы (галогены), элементы VI А-группы (кроме полония), элементы V А-группы: азот, фосфор, мышьяк; углерод, кремний (IV А-группа); бор (III А-группа), а также водород. Остальные элементы относят к металлам.
Отличия свойств металлов и неметаллов приведены в таблице 1:
Амфотерные элементы находятся в А-группах Периодической системы: бериллий Be, алюминий Al, галлий Ga, германий Ge, олово Sn, свинец Pb, сурьма Sb, висмут Bi, полоний Po и др., а также большинство элементов Б-групп: хром Cr, марганец Mn, железо Fe, цинк Zn, кадмий Cd, золото Au и др., проявляют и металлические (оснóвные для соединений), и неметаллические (кислотные для соединений) свойства.
Благородные (инертные) газы (VIII А-группа Периодической системы): гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радиоактивный радон Rn:
2. Сложные соединения и их отличия от простых веществ.
Сложные вещества бывают органические, в основе которых лежит углерод, и неорганические (безуглеродные и некоторые углеродсодержащие соединения: карбиды, карбонаты, оксиды углерода и другие). Неорганические чаще всего подразделяют на оксиды, основания, кислоты и соли.
Главные отличия сложных неорганических веществ:
Классификация неорганических соединений и их основные свойства приведены в таблице 2.
Классы и номенклатура неорганических веществ
Номенклатура — способ называния веществ.
Химическая формула — представление состава вещества с использованием символов химических элементов, числовых индексов и других знаков. Химическое название определяется составом вещества и изображается с помощью слова или группы слов. Названия строятся по номенклатурным правилам, с использованием русских названий элементов, кроме случаев, когда традиционно употребляются латинские корни (таблица 3):
Li+1 и O-2→ Li2O; Al+3 и O-2→ Al2O3; N+5 и O-2→ N2O5.
Название оксида: слово «оксид» в именительном падеже + название элемента Э в родительном падеже: оксид лития Li2O, оксид алюминия Al2O3.
Если элемент образует несколько оксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
Оксиды, которым соответствуют кислоты, также называют ангидридами: серный ангидрид SO3, азотный ангидрид N2O5 и др.
K+1 и OH- → KOH, Mg+2 и OH- → Mg(OH)2.
Название: слово «гидроксид» в именительном падеже + название элемента в родительном падеже: гидроксид калия, гидроксид магния.
Если элемент образует несколько гидроксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
Fe(OH)2 — гидроксид железа (II), Cr(OH)3 — гидроксид хрома (III).
Названия бескислородных кислот: корень русского названия элемента, образующего кислоту + суффикс «о» + «-водородная кислота», например: HBr — бромоводородная кислота, HCl — хлороводородная кислота, H2S — сероводородная кислота.
Названия кислородсодержащих кислот: русское название образующего элемента + «кислота», с учетом правил:
Названия наиболее распространенных кислот и их остатков приведены в таблице 4:
| Формула и название кислоты | Название кислотного остатка, образующего соль |
| HAlO2 метаалюминиевая | метаалюминат |
| H3AlO3 ортоалюминиевая | ортоалюминат |
| HAsO3 метамышьяковая | метаарсенат |
| H3AsO4 ортомышьяковая | ортоарсенат |
| H3BO3 ортоборная | ортоборат |
| HBr бромоводородная | бромид |
| HBrO бромноватистая | гипобромит |
| HBrO3 бромноватая | бромат |
| HCN циановодородная | цианид |
| H2CO3 угольная | карбонат |
| HCl хлороводородная | хлорид |
| HClO хлорноватистая | гипохлорит |
| HClO2 хлористая | хлорит |
| HClO3 хлорноватая | хлорат |
| HClO4 хлорная | перхлорат |
| HF фтороводородная | фторид |
| HJ йодоводородная | йодид |
| HMnO4 марганцовая | перманганат |
| HNO2 азотистая | нитрит |
| HNO3 азотная | нитрат |
| HPO3 метафосфорная | метафосфат |
| H3PO4 ортофосфорная | ортофосфат |
| H2S сероводородная | сульфид |
| H2SO3 сернистая | сульфит |
| H2SO4 серная | сульфат |
| H2SiO3 метакремниевая | метасиликат |
| H3SiO4 ортокремниевая | ортосиликат |
Название образуется в зависимости от типа соли.
Бинарные соединения — сложные вещества, состоящие из двух элементов. В таких соединениях встречается два типа химической связи: ковалентная полярная (для неметаллов и некоторых амфотерных элементов) или ионная (для солей бескислородных кислот).
Для некоторых есть тривиальные названия: NH3 — аммиак, SiН4 — силан, PH3 — фосфин и др.
Строение и химические свойства
Простые вещества состоят из атомов одного химического элемента:
Порядок соединения атомов при образовании из них веществ обусловливает особенности строения веществ. Различают вещества молекулярного и немолекулярного строения. Немолекулярное строение имеют все металлы и большинство их соединений, графит, красный фосфор, алмаз, кремний Si и др. Большинство неметаллов и их соединений состоят из молекул, т. е. имеют молекулярное строение.
Химические свойства металлов и неметаллов
1. Химические свойства металлов определяются способностью отдавать свободные электроны с внешнего уровня. Они являются восстановителями. Взаимодействие идет с:
2. Химические свойства неметаллов обусловлены свободными электронами (от 3 до 7) на внешнем электронном уровне.
Химические свойства благородных газов
Строение и основные химические свойства сложных веществ
Сложные соединения имеют ионную или ковалентную связь между атомами.
ZnO + H2SO4 → ZnSO4 + H2О,
ZnO+ 2NaOH + H2O → Na2[Zn(OH)4].
Все основания реагируют с кислотами (реакция нейтрализации):
1. Щелочи взаимодействуют с:
2. Нерастворимые основания разлагаются при нагревании: Cu(OH)2 → CuO + H2O.
Также о химических свойствах неорганических соединений можно почитать в статье «Классы неорганических соединений».
Простые и сложные вещества
Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента).
Пример: H2, O2,Cl2, P4, Na, Cu, Au.
Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов).
Пример: H2O, NH3, OF2, H2SO4, MgCl2, K2SO4.
Аллотропия — способность одного химического элемента образовывать несколько простых веществ, различающихся по строению и свойствам.
Явление аллотропии вызывается двумя причинами:
Основные классы неорганических веществ
Бинарные соединения
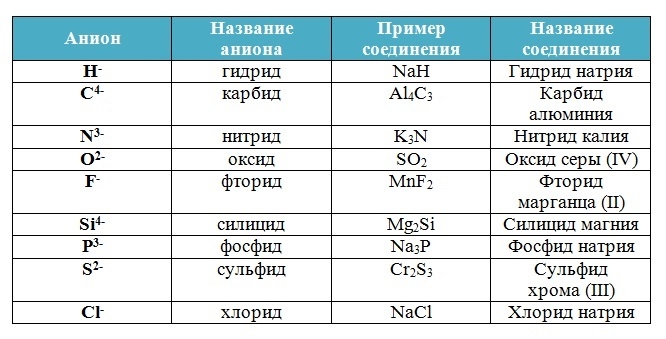
Вещества, состоящие из двух химических элементов называются бинарными (от лат. би – два) или двухэлементными.
Названия бинарных соединений образуют из двух слов – названий входящих в их состав химических элементов.
Первое слово обозначает электроотрицательную часть соединения – неметалл, его латинское название с суффиксом –ид стоит всегда в именительном падеже.
Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название стоит в родительном падеже, затем указывается степень окисления (только в том случае, если она переменная):
Запомни!
Оксиды
Общая формула оксидов: ЭхОу
Основные оксиды
Основные оксиды — оксиды, которым соответствуют основания.
Основные оксиды образованы металлом со степенью окисления +1, +2.
Пример
Соответствие основных оксидов и оснований
Амфотерные оксиды
Амфотерные оксиды — оксиды, которые в зависимости от условий проявляют либо основные, либо кислотные свойства.
Амфотерные оксиды образованы металлом со степенью окисления +3, +4, а также некоторыми металлами (Zn, Be) со степенью окисления +2.
Пример
Кислотные оксиды
Кислотные оксиды — оксиды, которым соответствуют кислоты.
Кислотные оксиды образованы неметаллом, а также металлом со степенью окисления +5, +6, +7.
Пример
Соответствие кислотных оксидов и кислот
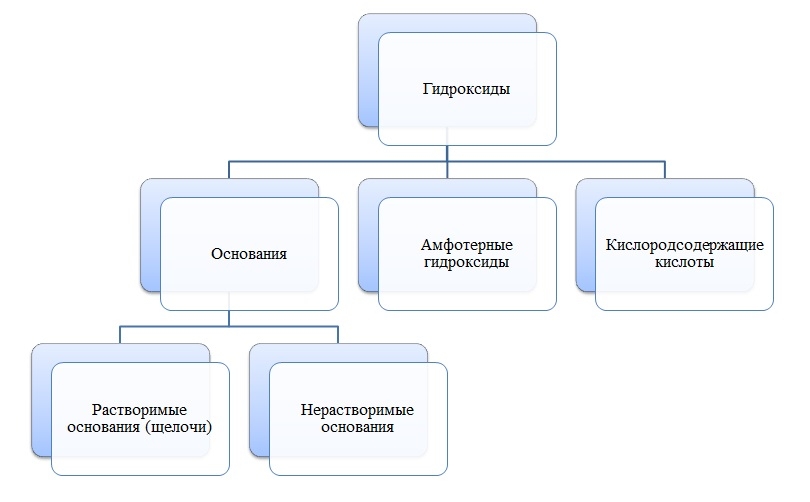
Гидроксиды
Общая формула гидроксидов: ЭхОуНz
Основания
Основания — сложные вещества, состоящие из ионов металла и одной или нескольких гидроксо-групп (ОН-).
В основаниях металл имеет степень окисления +1, +2 или вместо металла стоит ион аммония NH4+
Пример
Амфотерные гидроксиды
Амфотерные гидроксиды — сложные вещества, которые в зависимости от условий проявляют свойства оснований или кислот.
Амфотерные гидроксиды имеют металл со степенью окисления +3, +4, а также некоторые металлы (Zn, Be) со степенью окисления +2.
Пример
Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3
Кислоты
Кислоты — сложные вещества, состоящие из атомов водорода и кислотных остатков.
В состав кислот входит неметалл или металл со степенью окисления +5, +6, +7.
Пример
H2SO4, HNO3, H2Cr2O7, HMnO4
Соли- соединения, состоящие из катионов металлов (или NH4+) и кислотных остатков.
Общая формула солей: MexAcy
Пример
KNO3 — нитрат калия
(NH4)2SO4 — сульфат аммония
Mg(NO3)2 — нитрат магния
Названия кислот и кислотных остатков
| Кислота | Кислотный остаток | ||
| Название | Формула | Название | Формула |
| Соляная (хлороводородная) | HCl | Хлорид | Cl(-) |
| Плавиковая (фтороводородная) | HF | Фторид | F(-) |
| Бромоводородная | HBr | Бромид | Br(-) |
| Иодоводородная | HI | Иодид | I(-) |
| Азотистая | HNO2 | Нитрит | NO2(-) |
| Азотная | HNO3 | Нитрат | NO3(-) |
| Сероводородная | H2S | Сульфид Гидросульфид | S(2-) HS(-) |
| Сернистая | H2SO3 | Сульфит Гидросульфит | SO3(2-) HSO3(-) |
| Серная | H2SO4 | Сульфат Гидросульфат | SO4(2-) HSO4(-) |
| Угольная | H2CO3 | Карбонат Гидрокарбонат | СО3(2-) НСО3(-) |
| Кремниевая | H2SiO3 | Силикат | SiO3(2-) |
| Ортофосфорная | H3PO4 | Ортофосфат Гидроортофосфат Дигидроортофосфат | РО4(3-) НРО4(2-) Н2РО4(-) |
| Муравьиная | НСООН | Формиат | НСОО(-) |
| Уксусная | СН3СООН | Ацетат | СН3СОО(-) |
Полезные ссылки
Дополнительные материалы
Станьте первым, кто оставит
комментарий к данному материалу.
Урок№9. Простые и сложные вещества.
ОТЛИЧИТЕЛЬНЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА СООТВЕТСТВУЮЩИХ ПРОСТЫХ ВЕЩЕСТВ
1. Твёрдое агрегатное состояние (исключение – ртуть)
2. Металлический блеск
3. Хорошие проводники тепла и электричества.
4. Пластичные и ковкие.
2. Металлическим блеском не обладают (исключение йод)
3. Не проводят тепло и электрический ток – ИЗОЛЯТОРЫ.
Об атомах и химических элементах
Другого ничего в природе нет
ни здесь, ни там, в космических глубинах:
все — от песчинок малых до планет —
из элементов состоит единых.
С. П. Щипачев, «Читая Менделеева».
В настоящее время известно более 107 видов атомов, то есть более 107 химических элементов. Нужно различать понятия “химический элемент”, “атом” и “простое вещество”
Простые и сложные вещества
К 70-м гг. XIX в. было уже известно более 60 химических элементов. Их условно классифицировали на металлы и неметаллы
На 2019 год в периодической таблице – 118 химических элементов, которые образуют около 500 простых веществ.
Итак, подытожим вышесказанное. Молекулы вещества бывают двух видов:
1. Простые – молекулы таких веществ состоят из атомов одного вида. В химических реакциях не могут разлагаться с образованием нескольких более простых веществ.
2. Сложные – молекулы таких веществ состоят из атомов разного вида. В химических реакциях могут разлагаться с образованием более простых веществ.
Различие понятий “химический элемент” и “простое вещество”
Отличить понятия “химический элемент” и “простое вещество” можно при сравнении свойств простых и сложных веществ. Например, простое вещество – кислород – бесцветный газ, необходимый для дыхания, поддерживающий горение. Мельчайшая частица простого вещества кислорода – молекула, которая состоит из двух атомов. Кислород входит также в состав оксида углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит химически связанный кислород, который не обладает свойствами простого вещества, в частности он не может быть использован для дыхания. Рыбы, например, дышат не химически связанным кислородом, входящим в состав молекулы воды, а свободным, растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических соединений, следует понимать, что в эти соединения входят не простые вещества, а атомы определенного вида, то есть соответствующие элементы.
При разложении сложных веществ, атомы могут выделяться в свободном состоянии и соединяясь, образовывать простые вещества. Простые вещества состоят из атомов одного элемента. Различие понятий «химический элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент может образовывать несколько простых веществ. Например, атомы элемента кислорода могут образовать двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно различные простые вещества. Этим объясняется тот факт, что простых веществ известно гораздо больше, чем химических элементов.
Пользуясь понятием «химический элемент», можно дать такое определение простым и сложным веществам:
Простыми называют такие вещества, которые состоят из атомов одного химического элемента.
Сложными называют такие вещества, которые состоят из атомов разных химических элементов.
Отличие понятий «смесь» и «химическое соединение»
Сложные вещества часто называют химическими соединениями.
Попробуйте ответить на вопросы:
1.Чем отличаются по составу смеси от химических соединений?
2. Сопоставьте свойства смесей и химических соединений?
3. Какими способами можно разделить на составляющие компоненты смеси и химического соединения?
4. Можно ли судить по внешним признакам об образовании смеси и химического соединения?
Сравнительная характеристика смесей и химических
Чем химический элемент отличается от вещества?
Кратко:
– химический элемент это вид атомов с одинаковым зарядом ядра;
– простое вещество образовано атомами одного химического элемента.
Химический элемент – это условная запись в периодической таблице. Простое вещество – то, с чем мы имеем дело на практике.
Химический элемент – это атомы с одинаковым зарядом ядра.
Можно сказать, что химический элемент это условная выборка атомов по заряду ядра. Химические элементы представлены в периодической таблице Менделеева, но на практике мы всегда имеем дело с простыми веществами.
Обратите внимание: в определении химического элемента указан заряд ядра, но не масса ядра или атома. Почему?
Всё дело в том, что у многих (большинства) химических элементов в природе встречаются изотопы.
Изотопы (греч. isos – одинаковый + topos – место) – это разновидности одного и того же химического элемента, имеющих одинаковый заряд ядра (число протонов), но разное число нейтронов.
А масса атома, прежде всего складывается из числа протонов и нейтронов. Именно поэтому в определении химического элемента используют понятие заряда ядра. Этим, кстати, объясняются дробные значения у большинства химических элементов в периодической таблице (но не у всех).
Примеры изотопов есть на сайте – изотопы водорода.
Известно, что примерно 75% содержащегося в природе хлора представлено изотопами хлора с атомной массой 35. Тогда как примерно 25 % хлора в природе имеет атомную массу равную 37.
Рассчитаем примерное среднее значение относительной атомной массы хлора:
Ar (Cl) = (35/100% * 75%) + (37/100 % * 25%) = 35,5
Относительная атомная масса — значение массы атома, выраженное как отношение массы атома данного элемента к 1⁄12 массе атома изотопа углерода 12 C.
Можно спросить, а как быть с элементами, у которых нет изотопов? Почему у них дробная масса?
Всё дело в так называемом дефекте массы. Опытным путём было доказано, что масса ядра оказывается меньше, чем масса протонов и нейтронов, из которых состоит ядро. Но почему?
Ответ даёт уравнение Эйнштейна: E = mc 2
Нуклоны (протоны и нейтроны) в ядре атома удерживаются силами ядерного взаимодействия, которое выражается формулой выше. Эта величина называется энергией связи ядра. Именно энергия связи порождает дефект массы и создает дробные значения относительной атомной массы у химических элементов без изотопов.
Простое вещество – это вещество, образованное атомами одного химического элемента.
На сегодняшний день известно более 400 простых веществ, но химических элементов в таблице Менделеева около 120. Откуда же еще 300 веществ? Один и тот же химический элемент может образовывать сразу несколько простых веществ.
Аллотро́пия — существование двух и более простых веществ одного и того же химического элемента. Явление аллотропии обусловлено либо различным состоянием молекул простого вещества (аллотропия состава), либо способом размещения атомов или молекул в кристаллической решётке (аллотропия формы).
Безусловным рекордсменом по числу аллотропных модификаций является углерод. Наиболее известные: алмаз, графит, графены, фуллерены, нанотрубки, нановолокна, карбин и графин.
Известные примеры других веществ: кислород и озон, красный и белый фосфор.
Итак, если химический элемент это совокупность атомов с одинаковым зарядом ядра, то простое вещество образовано из этих атомов.
В этом и заключается разница. Химический элемент – это условный вид атомов, вещество – это то, с чем мы имеем дело в жизни.
Путаница может возникнуть ввиду того, что зачастую названия простого вещества и элемента совпадают (кислород, азот, водород, углерод и т.д.).
Как понять когда речь идёт о химическом элементе, а когда – о простом веществе?
Химический элемент не обладает химическими свойствами и физическими характеристиками (температуры плавления и кипения, электрическая проводимость, растворимость, запах, цвет и т.п. – см. подробнее).
Вот пример из учебника 7-го класса.
В каком случае речь идёт о водороде как о простом веществе:
а) водород присутствует в организме человека;
б) водород малорастворим в воде;
в) массовая доля водорода в воде равна 11%;
г) при обычных условиях водород находится в газообразном агрегатном состоянии;
д) в атмосфере водорода живые организмы погибают;
е) в состав оксидов водород не входит?
а) Водород входит в состав большинства органических молекул поэтому речь идёт о химическом элементе.
б) У химического элемента нет такой характеристики как растворимость.
в) В состав воды входят атомы водорода, а не водород как простое вещество.
г) Агрегатное состояние – характеристика простого вещества.
д) Речь идет об атмосфере, т.е. газе. Агрегатное состояние характеристика простого вещества.
е) Простое вещество не может входит в состав вещества сложного (см. определения), а вот атомы – могут.
А что такое сложное вещество?
Сложное вещество – это вещество, образованное атомами разных химических элементов.
Во Вселенной преобладают простые вещества: водород и гелий. Но в окружающем нас мире (на Земле) преобладают сложные вещества. Какое из них самое распространенное? Наверное вода? А вот и нет!
Основная масса Земли сосредоточена в мантии (
30%). Ядро Земли состоит преимущественно из железа и никеля; а мантия – из оксидов кремния, магния и железа в виде различных минералов.
Как видите, масса поверхности Земли ничтожно мала. Да, в мантии тоже присутствует вода и, по оценкам учёных, по объему её содержание сопоставимо со всем мировым океаном. Но даже этого количества ничтожно мало.
Таким образом, самым распространенным (по массе) сложным веществом на Земле является оксид кремния, на втором месте – оксид магния, и на третьем месте – оксиды железа.
А вот если говорить о поверхности Земли, то первое место займет… самый обычный песок! Вода – на втором месте.