Химиотерапия семиномы яичка тест чем
Химиотерапия семиномы яичка тест чем
Герминогенные опухоли яичка относятся к числу крайне агрессивных заболеваний с возможностью отдаленного метастазирования на ранних этапах своего развития. Особой склонностью к метастазированию обладают несеминомы, к которым относятся эмбриональный рак, незрелая тератома, опухоли желточного мешка и хорионкарцинома. Данные морфологические варианты могут встречаться в чистом виде, но чаще в комбинации друг с другом или в сочетании с семиномой. Несеминомные опухоли яичка (НСОЯ) характеризуются продукцией опухолевых маркеров – альфа-фетопротеина (АФН) и хорионического гонадоторопина (ХГ), которые используются для диагностики заболевания и за мониторингом его состояния. В России отсутствуют данные о количестве больных, у которых герминогенные опухоли диагностируются на этапе I стадии (опухоль локализована только в яичке, отсутствуют отдаленные метастазы по данным обследования грудной и брюшной полости с помощью компьютерной томографии, произошла нормализация опухолевых маркеров АФП и ХГ после выполнения орхфуникулэктомии). У больных чистой семиномой I стадии после выполнения орхфуникулэктомии рекомендуется только наблюдение, так как риск прогрессирования составляет менее 20%.У больных НСОЯ риск прогрессирования после орхфуникулэктомии составляет 30%. Основным фактором, предсказывающим вероятность развития отдаленного прогрессирования, является факт наличия лимфоваскулярной инвазии в удаленной опухоли, которая встречается у 40-50% больных. Поэтому важно требовать от морфолога не только определение морфологии ГОЯ, но и описание наличия или отсутствия опухолевых эмболов в просветах лимфатических или кровеносных сосудов. При отсутствии лимфоваскулярной инвазии частота рецидивов заболевания у больных НСОЯ I стадии не превышает 20%. Таким больным рекомендуется наблюдение после выполнения орхфуникулэктомии. В случае наличия лимфоваскулярной инвазии риск прогрессирования составляет уже 50%, и в этом случае целесообразно проведение адъювантной химиотерапии.
Для больных I стадией показано следующий график и процедуры наблюдения [1]:
В нашей стране наблюдение за больными НСОЯ при низком риске прогрессирования не всегда возможно в связи с отсутствием возможности выполнения необходимых диагностических процедур в лечебном учреждении или отказом больного в связи с отдаленным проживанием или рабочим графиком. В этом случае им также возможно проведение адъювантной химиотерапии как альтернативы наблюдению.
В качестве адъювантной химиотерапии еще недавно было рекомендовано проведение 2 курсов химиотерапии комбинацией BEP (цисплатин 20 мг/м 2 1-5 дни, этопозид 100 мг/м 2 1-5 дни и блеомицин 30 мг в/в 1, 3, 5 дни, последующий курс на 22 день от начала предыдущего курса). У больных после адъювантной терапии частота прогрессирования составляет менее 5%. Однако проведение 2 курсов химиотерапии сочетается с серьезной токсичностью, как непосредственной (нейтропения, тромбоцитопения, тошнота и рвота), так и отдаленной (снижение слуха, периферическая нейропатия, нефротоксичность, снижение фертильности). Поэтому актуальной задачей представляется оценка эффективности одного курса BEP для профилактики рецидивирования.
В отделении клинической фармакологии было проведено исследование по оценке наблюдения и адъювантной химиотерапии у 134 больных I стадией НСОЯ. Был сделан вывод о возможности применения как динамического наблюдения, так и 2 курсов адъювантной ХТ по программе ВЕР. Первый подход в группе низкого риска (отсутствие лимфоваскулярной инвазии) ассоциирован с большей частотой рецидивов (27%), однако последующее лечение позволяет достичь 5-летней опухоль-специфичной выживаемости 96%, что сравнимо с группой адъювантной ХТ (98,7%). Всем больным с наличием лимфоваскулярной инвазии проводили адъювантную химиотерапию, и ни у кого из них не отмечено развитие рецидива при последующем наблюдении в течение 2 лет.
Наш опыт, полученный в ходе этой работы, а также исследования, проведенные другими группами, свидетельствуют о том, что проведение 2 курсов ХТ по программе ВЕР позволяет снизить риск рецидива до 0-2%, а ограниченный опыт использования одного курса ВЕР – до 0-4%. Прямое сравнение 1 и 2 курсов ВЕР никогда не проводилось и вряд ли когда либо будет проведено в связи с необходимостью включения большого числа больных, чтобы доказать отсутствие разницы между двумя подходами. Учитывая, что около 99% больных при обоих подходах будут излечены, 1 курс ВЕР представляется наиболее предпочтительным с точки зрения снижения риска поздней токсичности.
Поэтому столь ожидаемыми были исследования, проведенные в Великобритании, по оценке токсичности и эффективности одного курса BEP в качестве адъювантной терапии у больных I стадией НСОЯ с высоким риском (наличие лимфоваскулярной инвазии в опухоли) развития рецидива. Все больные после исключения диссеминации процесса получали один курс стандартной комбинации BEP с профилактическим назначением антибиотиков и Г-КСФ. Статистическая гипотеза предполагала, что исследование будет признано позитивным, если частота прогрессирования заболевания за 2 года наблюдения за каждым больным не превысит 5%.
В исследование было включено 246 больных, получивших лечение в различных онкологических клиниках Великобритании. При медиане наблюдения 39 мес. рецидив заболевания развился у 3 (1,3%) больных. Еще у 3 (1,3%) обнаружена растущая зрелая тератома, которая возникает вследствие успешно проведенного химиотерапевтического лечения субклинических метастазов. Большое внимание в данном исследовании было уделено оценке токсичности. Несмотря на введение Г-КСФ, частота нейтропении 3-4 степени составила 32%. Однако благодаря профилактике с включением Г-КСФ и антибиотиков частота фебрильной нейтропении была только 6,4%. У 20% больных отмечено снижение слуха в верхних частотных диапазонах, оцененное как 2 степень, и у 1 больного – как 3 степень. Другие проявления токсичности были минимальны. Таким образом, 2-летняя безрецидивная выживаемость составила 97%, а 2-летняя общая выживаемость – 99%. На основании этого авторы исследования делают вывод, что один курс BEP эффективен в качестве адъювантной терапии у больных НСОЯ опухолями яичка I стадии с высоким риском прогрессирования в связи с наличием лимфоваскулярной инвазии в опухоли. Результаты данного исследования подтверждают, что один курс химиотерапии BEP показан для проведения адъювантной химиотерапии у больных НСОЯ I стадии.
Ключевые слова: герминогенные опухоли яичка, адъювантная химиотерапия, I стадия.
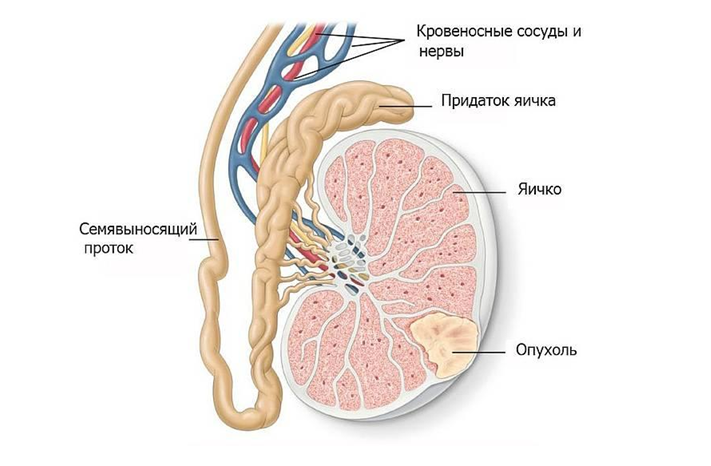
Опухоли яичка
Опухоли яичка – группа образований, развивающаяся из тканей яичек (мужских половых желез, расположенных в мошонке). Опухоли яичка могут быть злокачественными и доброкачественными. Данный вид опухолей относится к визуализируемым и часто обнаруживается пациентами самостоятельно.
Частота злокачественных опухолей составляет до 90 % от всех случаев опухолей яичка. Доброкачественные опухоли яичка встречаются очень редко. Особенность доброкачественных опухолей – отсутствие быстрого роста, они длительно не метастазируют. Лечение доброкачественных опухолей заключается в хирургическом удалении образования.
Рак яичка чаще встречается в молодом возрасте (25-35 лет), являясь самой часто встречающейся опухолью у мужчин до 50 лет.
Виды опухолей яичка
Яички состоят из различных клеток, каждая из которых может стать основной для развития нескольких видов злокачественной опухоли. Знание о том, из каких клеток образовалась опухоль, достаточно важно, поскольку это влияет на выбор тактики лечения и прогноз заболевания.
Определение типа опухоли возможно посредством микроскопического изучения.
Классификация
Наиболее часто из всех опухолей яичка встречаются герминогенные опухоли, они развиваются из зародышевых клеток. Данные опухоли при правильной тактики возможно полностью излечить, однако важным условием является своевременное их обнаружение и лечение в профильном центре.
Герминогенные опухоли (составляют 95 % опухолей яичка)
Опухоли полового канатика и стромы ( Факторы риска развития опухолей яичка
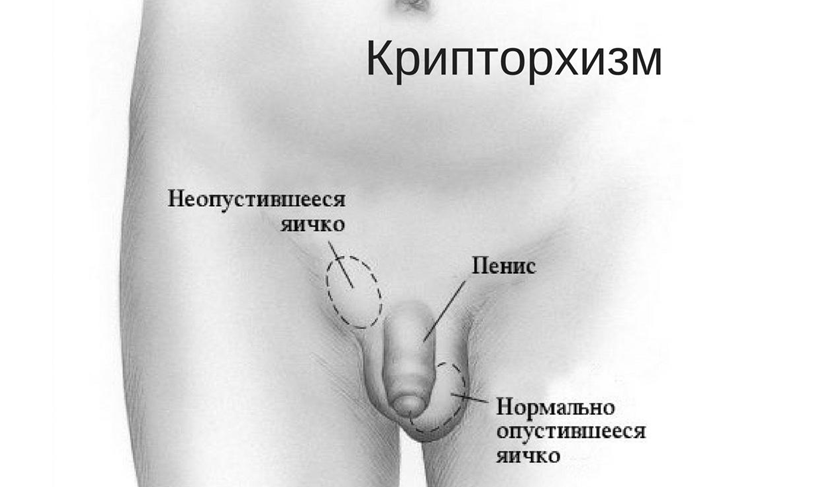
Однозначных факторов риска развития опухолей яичек не существует. К одной из наиболее вероятных причин относят крипторхизм – неопущение яичка. При нормальном развитии яички до рождения находятся в брюшной полости и к моменту рождения ребенка самостоятельно опускаются в мошонку. Примерно у 3 % детей одно или оба яичка могут не опуститься в мошонку. В таких случаях проводится оперативное вмешательство. Хирургическое лечение крипторхизма до пубертатного периода снижает риск развития опухолей яичка.
На увеличение вероятности развития опухоли яичка может повлиять профессиональная деятельность, считается, что у работников газовой, нефтяной промышленности, шахтеров и пожарных риск развития опухоли яичка повышен. Вероятность возникновения опухоли яичка среди белых мужчин в 5-10 раз превышает таковую у афроамериканских мужчин. У мужчин Азии и Африки риск возникновения опухоли яичка очень низкий. Травма и оперативное вмешательство на мочеполовых органах достоверно не увеличивают риск развития опухоли яичек.
Диагностика
Опухоль яичка может проявляться в виде безболезненного образования мошонки или яичка. Ниже в таблице указаны возможные симптомы.
При распространенном процессе больного могут беспокоить различные симптомы: кашель, одышка, боли в спине, головные боли, тошнота, рвота. Если у вас появились эти симптомы, то необходимо срочно обратиться к врачу-онкологу или урологу.
Симптомы опухоли яичка
Опухоль яичка может быть обнаружена пациентом или его половым партнером. При обнаружении любого образования в яичке необходимо срочно обратиться к врачу.
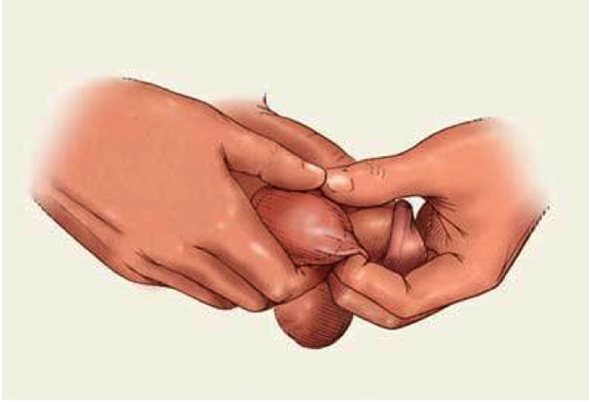
Для своевременного обнаружения опухоли яичка мы рекомендуем выполнять самообследование.
Чаще всего опухоли яичка путают с воспалительными заболеваниями. Эпидидимит – это воспаление придатка яичка, в большинстве случаев инфекционного характера, требующее проведения противовоспалительной терапии. Если болезненность, отек сохраняются после курса лечения, включающего антибиотики, необходима дальнейшая диагностика.
Обследование пациента на приеме у врача начинается с осмотра. Врач проведет процедуру осмотра, пальпацию грудной клетки на предмет гинекомастии (увеличение молочных желез), брюшной полости, яичек, оценит состояние паховых и периферических лимфатических узлов.
Инструментальные методы
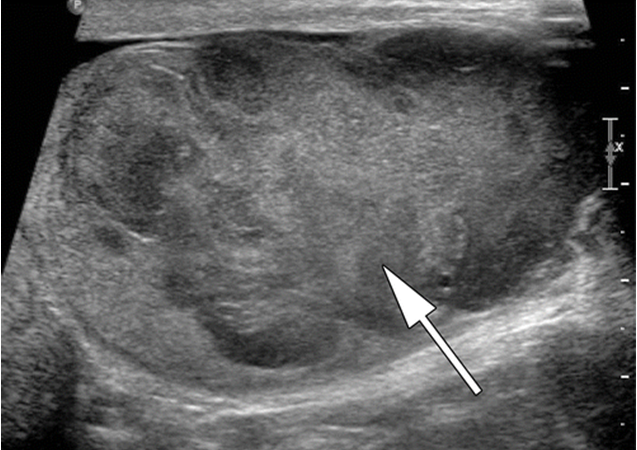
Ультразвуковое исследование (УЗИ) мошонки является предпочтительным начальным визуализирующим исследованием для оценки образования яичка. УЗИ может подтвердить наличие новообразования, определить его расположение и оценить состояние противоположного яичка (рис. 4). Чувствительность метода достаточно высокая – от 92 % до 98 %.
Компьютерная томография органов грудной клетки, брюшной полости, малого таза используются для оценки распространения опухолевого процесса (рис.5).
Как дополнительная диагностическая процедура, может быть использована магнитно-резонансная томография головного мозга.
Наличие опухолевого образования в яичке, выявленное при УЗИ, повышенный уровень опухолевых маркеров (всех или одного из них) требуют немедленного направления пациента на оперативное лечение в специализированный онкологический центр.
При обнаружении первичной опухоли в забрюшинном пространстве необходимо пройти полное обследование, предусмотренное для опухоли яичка.
Стадии
При обнаружении злокачественной опухоли необходимо выяснить, насколько распространился опухолевый процесс, то есть определить стадию заболевания. От этого зависит дальнейшее лечение.
Доброкачественные опухоли яичка не стадируются.
Стадии злокачественного заболевания варьируются от I до III. Самая ранняя стадия рака яичка — это стадия 0 (или неоплазия зародышевых клеток in situ). Выделяют III стадии злокачественной опухоли яичка. В зависимости от стадии заболевания, прогностических признаков (уровень опухолевых маркеров, наличие вторичных опухолевых изменений в органах), согласно разработанным стандартам, принимается решение о лечебной тактике.
Лечение
Лечение пациентов с диагностированными злокачественными опухолями яичка должно проводиться в специализированном центре у онкологов, имеющих большой опыт ведения больных с данным заболеванием.
Если у вас или у вашего близкого появились симптомы, подозрительные на опухоль яичка, необходимо незамедлительно обратиться к врачу.
Хирургическое лечение
Хирургический метод является первичным этапом в лечении всех видов опухолей яичка. На первом этапе при обнаружении опухоли проводят операцию по удалению яичка (орхфуникулэктомию). Как правило, проводится радикальная паховая орхфуникулэктомия (хирургическое удаление яичка). Операция носит лечебно-диагностический характер, поскольку помимо удаления опухоли, позволяет установить морфологический диагноз (определить разновидность опухоли), что необходимо для определения дальнейшей тактики.
Радикальная паховая орхфуникулэктомия
Операция по удалению яичка при раке называется радикальной паховой орхфуникулэктомией. Опухоль удаляется вместе с яичком и семенным канатиком.
Орхфуникулэктомия может быть отложена, если пациент находится в крайне тяжелом состоянии (в этом случае лечение начинают с химиотерапии по жизненным показаниям).
После получения гистологического заключения о характере опухоли, данных обследования: КТ грудной клетки, брюшной полости, КТ/МРТ малого таза, уровень опухолевых маркеров, проводится стадирование, определение прогноза, и командой специалистов принимается решение о лечебной тактике.
При планировании химиотерапии необходимо обсудить с врачом риск нарушения фертильности и необходимость криоконсервации спермы. Процедура должна быть выполнена до начала химиотерапии.
Химиотерапия
Химиотерапия является одним из основных методов лечения при злокачественных опухолях яичка. Данные опухоли обладают высокой чувствительностью к химиотерапии, и полное излечение возможно даже при большом распространении опухолевого процесса. Химиотерапия не используется для лечения доброкачественных опухолей яичка.
Химиотерапия обычно проводится циклами длительностью 3 недели. При злокачественных опухолях яичка очень важно строго соблюдать интервалы между циклами химиотерапии.
Схема и длительность лечения зависят от стадии заболевания, группы прогноза, лечения, полученного ранее, и индивидуальных особенностей пациента.
Возможные побочные эффекты химиотерапии
Химиопрепараты действуют на быстро растущие клетки, делящиеся опухолевые клетки. Но при этом химиотерапия повреждает нормальные ткани организма, такие как клетки костного мозга (где образуются новые клетки крови), слизистой оболочки полости рта, кишечника и волосяных фолликулов. Побочные эффекты химиотерапии зависят от типа и дозы используемых лекарств и продолжительности лечения. Чаще всего из осложнений встречаются: снижение показателей крови (снижение уровня лейкоцитов, нейтрофилов, гемоглобина, тромбоцитов), выпадение волос, стоматит (воспаление слизистой полости рта: отечность, покраснение, появление налетов, язв), тошнота и рвота, слабость, диарея, снижение аппетита.
Большинство побочных эффектов кратковременны и проходят через некоторое время после окончания лечения, но некоторые из них могут длиться долгое время, такие как потеря слуха, повреждение почек или легких. Поэтому химиотерапия должна проводиться по абсолютным показаниям в соответствии с разработанными рекомендациями, и больной в течение длительного времени должен быть под наблюдением онколога.
После проведения химиотерапии и обследования обсуждается вопрос об удалении оставшихся опухолевых очагов. Одним из видов оперативного лечения является удаление забрюшинных лимфатических узлов (забрюшинная лимфодиссекция).
В зависимости от типа опухоли и стадии заболевания лимфатические узлы вокруг крупных кровеносных сосудов (аорта и нижняя полая вена) могут быть удалены после проведения химиотерапии. Не всем пациентам с опухолью яичка необходимо удалять лимфатические узлы, поэтому важно обсудить это (и возможные варианты) со своим врачом. Это сложная и долгая операция. В большинстве случаев делается большой разрез посередине живота для возможности удаления лимфатических узлов. Удаление забрюшинных лимфатических узлов должно выполняться хирургом, который делает это часто. Опыт имеет большое значение.
Последствия лимфодиссекции
Удаление забрюшинных лимфатических узлов – серьезная операция. Она не вызывает импотенции, у мужчин сохраняется эректильная функция. Но во время данной операции могут повреждаться некоторые нервы, контролирующие эякуляцию. Если эти нервы повреждаются, то когда мужчина эякулирует, сперма не выходит через уретру, а уходит обратно в мочевой пузырь. Это называется ретроградной эякуляцией, данное осложнение может затруднить отцовство.
При распространенном процессе (когда есть метастазы в других органах) для получения наилучшего результата и снижения риска возврата заболевания могут проводиться различные виды операций с целью удаления всех опухолевых очагов. Если оставшиеся опухолевые очаги не удаляются или удаляются не полностью, риск возврата заболевания увеличивается в несколько раз.
Чаще операция успешна, когда ее проводят опытные врачи.
Лучевая терапия
Лучевая терапия при опухолях яичка в настоящий момент практически не используется, так как имеет низкую эффективность. Применение лучевой терапии может использоваться в качестве локального (местного) контроля при метастазах в головном мозге.
Фертильность
Злокачественные опухоли яичка наиболее часто возникают у мужчин репродуктивного, молодого возраста, когда они заводят семью и детей. При проведении химиотерапии возникает высокий риск нарушения фертильности, поэтому необходимо до начала лечения обсудить с лечащим врачом необходимость криоконсервации спермы. Криоконсервация спермы – метод хранения эякулята, который подразумевает его замораживание (чаще всего в жидком азоте), с последующим восстановлением функций сперматозоидов после размораживания. Криоконсервация должна быть выполнена до начала химиотерапии.
Обследование перед проведением криоконсервации:
Наблюдение
Все пациенты со злокачественной опухолью яичек должны тщательно длительно наблюдаться – до 10-15 лет после первичного лечения, так как, несмотря на проведенное лечение, остается риск развития рецидива заболевания. Риск рецидива опухоли наиболее высок в течение двух лет после первичного лечения.
Последующее наблюдение включает сбор анамнеза, осмотр, опухолевые маркеры, УЗИ мошонки с эластографией, пахово-подвздошных областей, брюшной полости и забрюшинного пространства, рентгенографию органов грудной клетки. График наблюдения зависит от стадии заболевания. При обнаружении рецидива варианты лечения включают химиотерапию, хирургическое лечение.
Прогноз
Достижения в лечении рака яичек являются одними из величайших достижений современной медицины. Сегодня излечение достижимо у 95 % всех пациентов с опухолями яичек, у 80 % пациентов с распространенной формой заболевания. Несмотря на это, метастатическая форма опухоли остается неизлечимой примерно у 10 % пациентов. Прогноз зависит от гистологического типа рака яичка, распространенности опухолевого процесса, проводимого лечения. В некоторых регионах Российской Федерации выживаемость пациентов с опухолью яичек достигает всего 60 %. Это связано с различными причинами (редкость опухоли, поздняя обращаемость пациентов, низкая осведомленность врачей).
НМИЦ онкологии им. Н. Н. Петрова является специализированным центром по лечению опухолей яичка с многолетним опытом терапии данной группы онкологических заболеваний. В нашем Центре работает команда высококвалифицированных профессионалов – врачей-онкологов, включая хирургов (урологов, торакальных и абдоминальных хирургов), специалистов по лекарственной терапии взрослых и детей (химиотерапевтов, онкопедиатров), лучевой диагностике, морфологов, анестезиологов, реаниматологов, радиологов. Тактика ведения каждого пациента с опухолью яичка неоднократно обсуждается мультидисциплинарной командой.
Если у вас или у вашего близкого появились симптомы, подозрительные на опухоль яичка, необходимо незамедлительно обратиться к врачу. Учитывая высокий процент полного излечения данной группы заболеваний, высокую эффективность лекарственной терапии, в нашем Центре вы сможете оперативно получить всю необходимую помощь у специалистов, имеющих большой опыт в лечении этой патологии.
Список использованной литературы:
Химиотерапия семиномы яичка тест чем
В результате широкого применения лекарственных препаратов для лечения тератомы яичка, в течение последних 25 лет в онкологии был совершен настоящий прорыв. В начале 1960-х годов были известны лишь один или два препарата, обладающие ограниченной эффективностью. На следующем этапе среди различных классов соединений были найдены высокоэффективные препараты. Была обнаружена высокая эффективность винбластина, блеомицина, цисплатина и их производных.
Курсы химиотерапии, разработанные на основе этих соединений, обладали высокой токсичностью, и позже в их состав был добавлен цисплатин как наиболее эффективный из цитостатиков. Цисплатин не обладал токсическим действием на костный мозг и поэтому особенно подходил для лечения. Более 20 лет назад Эйнхорн с сотрудниками из Индианы предложили комбинацию цисплатина, винбластина и блеомицина (PVB) для лечения больных с достаточно распространенным опухолевым процессом.
Иногда эту рецептуру назначают и сегодня, хотя в основном уже используется новая и менее токсичная комбинация блеомицина, этопозида и цисплатина (ВЕР). В большинстве центров США и Европы, где широко применяются химиотерапевтические методы лечения рака яичка, ВЕР считается «золотым стандартом».
Несмотря на успехи, достигнутые в области химиотерапии, серьезной проблемой остается высокая токсичность применяемых схем лечения. Особенно опасны такие проявления токсичности, как расстройства желудочно-кишечного тракта, гранулоцитопения и инфекции, действие на почки и легочный фиброз. По ранним наблюдениям Эйнхорна, при применении PVB в периоде ремиссии умерло четверо больных; причиной смерти двоих было применение лекарственных препаратов.
В этой схеме лечения использовался блеомицин в относительно высоких дозах, и по мере снижения его гематотоксического действия увеличивалась легочная токсичность препарата. Однако в исследованиях Eastern Cooperative Oncology Group в США было показано, что блеомицин остается важнейшим компонентом рецептуры.
В группе больных, получавших ВЕР, безрецидивная и общая выживаемость оказались выше (86% и 95%), чем в группе, леченной комбинацией этопозида и цисплатина (69% и 86%). Однако недавно было продемонстрировано, что 4 цикла лечения ЕР оказываются столь же эффективными, как 3 цикла лечения ВЕР. Поскольку комбинация ЕР менее токсична, удается избежать проблем с легкими, которые возникают при применении блеомицина.
Карбоплатин менее токсичен для желудочно-кишечного тракта, чем цисплатин. Однако он влияет на миелопоэз и поэтому плохо сочетается с винбластином и блеомицином. Ниже обсуждаются последние достижения в области химиотерапии.
Существует определенная категория больных с крайне неблагоприятным прогнозом. Для этих больных характерно присутствие метастазов в печени, костях и в головном мозге; уровень АФП составляет более 1000 нг/мл, ХГЧ более 10000 нг/мл, активность ЛДГ в 10 раз превышает норму; у них диагносцировано поражение средостения, размеры грудных лимфатических узлов составляют более 5 см, или обнаружено более 20 легочных метастазов. Таких больных лучше лечить с применением более интенсивной рецептуры, причем две трети из них удается вылечить.
Вряд ли целесообразно назначать более четырех курсов химиотерапии с применением близких по составу препаратов. Хотя большинство больных удается вылечить, не следует отчаиваться, если в дальнейшем при рентгенографии у них будут обнаружены признаки остаточного заболевания, например метастазы в легких. Иногда через несколько месяцев на рентгенограммах они исчезают. Для лечения поздних рецидивов или устойчивых форм опухолей используются интенсивные курсы химиотерапии, в частности на основе ифосфамида.
При первом назначении проявляется продолжительный эффект, и небольшое число больных вылечивается. Примером схемы терапии, удовлетворяющей логически-обоснованному выбору, является VIP (винкристин, ифосфамид и цисплатин или карбоплатин); примером рецептуры начального уровня — ВЕР. Больные, которым назначается VIP, ранее не должны получать винбластин. Все больше используются высокие дозы препаратов совместно с поддержкой стволовых клеток.
Еще предстоит выяснить целесообразность применения химиотерапии при лечении больных с ранними стадиями развития опухоли. Особенно это относится к случаям умеренного поражения парааортальных лимфатических узлов (стадии IIа и IIb).
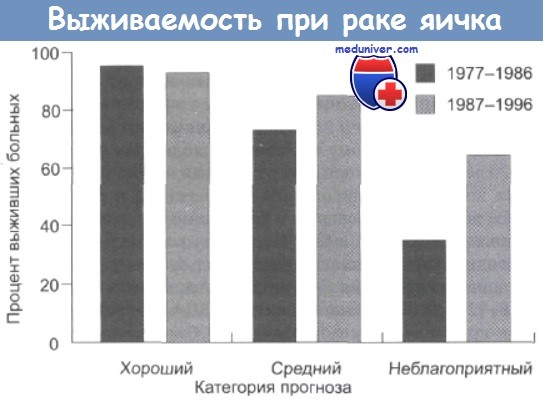
По данным статистического управления страховых обществ.
(IGCCCG — International Germ Cell Consensus Classification Group — classification).
Факт высокой чувствительности семиномы к химиопрепаратам очевиден. В большинстве случаев опухоль удается диагносцировать на ранней стадии, и можно использовать лучевую терапию. Однако на более поздних стадиях или при поздних рецидивах химиотерапия оказывалась малоэффективной до тех пор, пока не появились схемы на основе цисплатина. Сейчас используются комбинации препаратов, аналогичные тем, которые применяются при лечении тератомы, иногда совместно с облучением основных очагов опухоли.
Впрочем, при лечении больных с метастазирующей семиномой изолированное применение цисплатина может давать такой же эффект, как и более сложные схемы, и сейчас это проверяется.
Довольно подробно изучены отдаленные последствия применения химиотерапии. В одной публикации из Германии изложены результаты наблюдений, проведенных в группе из 90 больных (срок наблюдения, в среднем, составлял 58 месяцев). Лишь у 19% больных не проявлялось никаких признаков наличия опухоли. У 33% отмечались симптомы болезни Рейно, у 21% шум в ушах или потеря слуха, и у двух третей был зарегистрирован повышенный уровень фолликулостимулирующего гормона.
Среди других осложнений отмечена устойчивая гипомагнезиемия, нарушение функций клеток Лейдига, артериальная гипертония и развитие периферических нейропатий. К счастью, развитие повторного рака наблюдалось крайне редко.
Использование хирургических методов лечения рака яичка после химио- и лучевой терапии
Хирургия играет важную роль в тех случаях, когда после орхфуникулэктомии снова проявляются признаки онкозаболевания. В таких случаях часто удаляются очаги опухоли в брюшной полости и даже проводится резекция легочных метастазов при повторной торактомии. Если операция откладывается до окончания курса химиотерапии, то последующий гистологический анализ дает картину, отражающую эффективность проведенного лечения, также как и удаление опухоли у больных с признаками остаточного заболевания.
В идеальном случае операцию следует проводить только после того, как уровень онкомаркеров снизился до минимального уровня, и после этого был проведен хотя бы один курс химиотерапии. Во многих случаях имеются четкие доказательства дифференцировки опухолевых клеток в зрелую тератому, которая происходит в результате лечения. Хотя такие наблюдения внушают оптимизм, значение этого феномена и его влияние на выживаемость больных остаются не вполне ясными.
По данным за несколько лет наблюдения большинство больных вылечивается, и рецидивов у них не отмечается.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021