Химия что такое степень окисления
Степень окисления
Темы кодификатора ЕГЭ: Электроотрицательность. Степень окисления и валентность химических элементов.
Степень окисления – это вспомогательный условный заряд атома элемента в соединении, вычисленный из предположения, что все соединения состоят из ионов (все полярные связи – ионные).
Что значит «условный заряд»? Мы просто-напросто договариваемся, что немного упростим ситуацию: будем считать любые полярные связи полностью ионными, и будем считать, что электрон полностью уходит или приходит от одного атома к другому, даже если на самом деле это не так. А уходит условно электрон от менее электроотрицательного атома к более электроотрицательному.
Наверняка, у вас возник вопрос — зачем же придумывать то, чего нет? Это не коварный замысел химиков, все просто: такая модель очень удобна. Представления о степени окисления элементов полезны при составлении классификации химических веществ, описании их свойств, составлении формул соединений и номенклатуры. Особенно часто степени окисления используются при работе с окислительно-восстановительными реакциями.
Степени окисления бывают высшие, низшие и промежуточные.
Высшая степень окисления равна номеру группы со знаком «плюс».
Низшая определяется, как номер группы минус 8.
И промежуточная степень окисления — это почти любое целое число в интервале от низшей степени окисления до высшей.
Для нахождения степеней окисления используют следующие правила :
Примеры :
Задание: определите степени окисления элементов в молекуле дихромата калия: K2Cr2O7.
В бинарных соединениях более электроотрицательный элемент характеризуется отрицательной степенью окисления, менее электроотрицательный – положительной.
Обратите внимание, что понятие степени окисления – очень условно! Степень окисления не показывает реальный заряд атома и не имеет реального физического смысла. Это упрощенная модель, которая эффективно работает, когда нам необходимо, например, уравнять коэффициенты в уравнении химической реакции, или для алгоритмизации классификации веществ.
Степень окисления – это не валентность! Степень окисления и валентность во многих случаях не совпадают. Например, валентность водорода в простом веществе Н2 равна I, а степень окисления, согласно правилу 1, равна 0.
Это базовые правила, которые помогут Вам определить степень окисления атомов в соединениях в большинстве случаев.
В некоторых ситуациях вы можете столкнуться с трудностями при определении степени окисления атома. Рассмотрим некоторые из этих ситуаций, и разберем способы их разрешения:
Потренируемся определять степень окисления атомов в органических соединениях. Для этого необходимо нарисовать полную структурную формулу атома, и выделить атом углерода с его ближайшим окружением — атомами, с которыми он непосредственно соединен.
Валентность и степень окисления
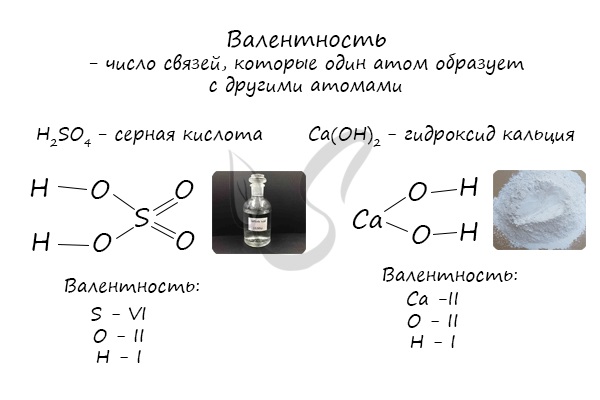
Валентность
Определяют валентность по числу связей, которые один атом образует с другими. Для примера рассмотрим две молекулы
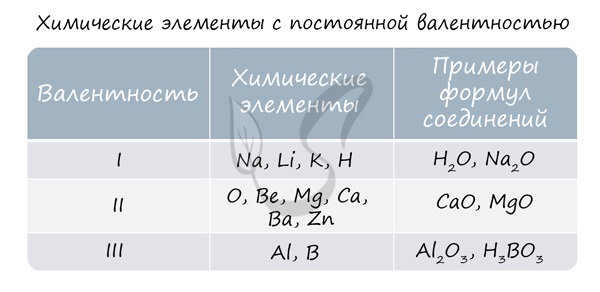
Для определения валентности нужно хорошо представлять графические формулы веществ. В этой статье вы увидите множество формул. Сообщаю вам также о химических элементах с постоянной валентностью, знать которые весьма полезно.
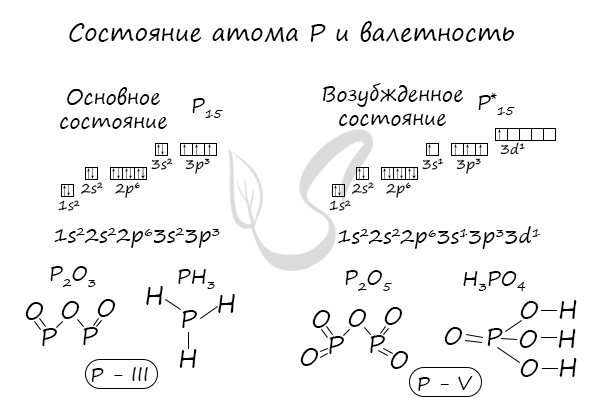
В электронной теории считается, что валентность связи определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии. Мы касались с вами темы валентных электронов и возбужденного состояния атома. На примере фосфора объединим эти две темы для полного понимания.
Подавляющее большинство химических элементов обладает непостоянным значением валентности. Переменная валентность характерна для меди, железа, фосфора, хрома, серы.
Степень окисления
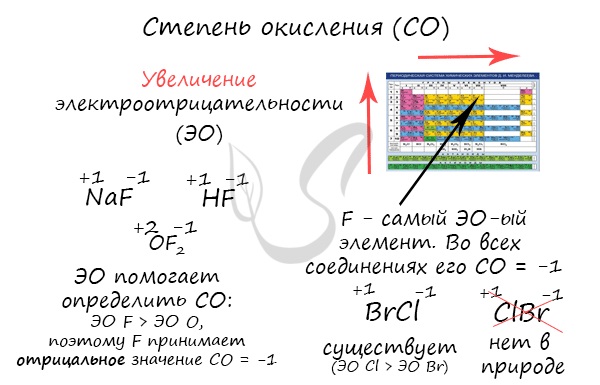
Численно степень окисления равна условному заряду, который можно приписать атому, руководствуясь предположением, что все электроны, образующие связи, перешли к более электроотрицательному элементу.
Зная изменения электроотрицательности в периодах и группах периодической таблицы Д.И. Менделеева, можно сделать вывод о том какой элемент принимает «+», а какой минус. Помогают в этом вопросе и элементы с постоянной степенью окисления.
Самостоятельно определите степени окисления атомов в следующих веществах: RbOH, NaCl, BaO, NaClO3, SO2Cl2, KMnO4, Li2SO3, O2, NaH2PO4. Ниже вы найдете решение этой задачи.
Сравнивайте значение электроотрицательности по таблице Менделеева, и, конечно, пользуйтесь интуицией 🙂 Однако по мере изучения химии, точное знание степеней окисления должно заменить даже самую развитую интуицию 😉
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Валентность и степень окисления
Степень окисления
Сте́пень окисле́ния (окислительное число, формальный заряд) — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций, численная величина электрического заряда, приписываемого атому в молекуле в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов.
Представления о степени окисления положены в основу классификации и номенклатуры неорганических соединений.
Содержание
Описание
Степень окисления соответствует заряду иона или формальному заряду атома в молекуле или в химической формальной единице, например:
Степень окисления указывается сверху над символом элемента. В отличие от указания заряда иона, при указании степени окисления первым ставится знак, а потом численное значение, а не наоборот:


Степень окисления атома в простом веществе равна нулю, например:
Алгебраическая сумма степеней окисления атомов в молекуле всегда равна нулю:
Понятие степени окисления вполне применимо и для нестехиометрических соединений (КС8, Mo5Si3, Nb3B4 и др.). Например в известной реакции обжига пирита:
4FeS2 +11O2 = 2Fe2O3 + 8SO2
удобнее всего принять в исходном соединение степень окисления у железа +3 (хотя реально атом железа смещает от себя 2 электрона, то есть степень окисления железа +2), а у серы −3/2 (!), что совсем не противоречит определению степени окисления, как условной единицы и позволяет так же просто, как и в случае других окислительно-восстановительных процессов, уравнять реакцию.
Суммарная степень окисления атомов в молекуле всегда равна нулю.
Условность
Следует помнить, что степень окисления является сугубо условной величиной, не имеющей физического смысла, но характеризующей образование химической связи межатомарного взаимодействия в молекуле.
Степень окисления в ряде случаев не совпадает с валентностью. Например, в органических соединениях углерод всегда четырёхвалентен, а степень окисления атома углерода в соединениях метана CH4, метилового спирта CH3OH, формальдегида HCOH, муравьиной кислоты HCOOH и диоксида углерода CO2, соответственно, равна −4, −2, 0, +2 и +4.
Истинные заряды атомов в соединениях, определённые экспериментальным путём, также не совпадают со степенями окисления этих элементов. Например, заряды атомов водорода и хлора в молекуле хлороводорода HCl, в действительности, равны соответственно +0,17 и −0,17, хотя их степени окисления в этом соединении равны +1 и −1, а в кристаллах сульфида цинка ZnS заряды атомов цинка и серы равны соответственно +0,86 и −0,86, вместо степеней окисления +2 и −2. [1]
См. также
Примечания
Полезное
Смотреть что такое «Степень окисления» в других словарях:
СТЕПЕНЬ ОКИСЛЕНИЯ — (окислительное число) условный показатель, характеризующий заряд атома в соединениях. В молекулах с ионной связью совпадает с зарядом иона, напр. в NaCl степень окисления натрия +1, хлора 1. В ковалентных соединениях за степень окисления… … Большой Энциклопедический словарь
степень окисления — – целочисленный условный заряд, приписываемый атому в молекуле или ионе на основе совокупности формальных правил, условно допускающих, что все химические связи относятся к ионному типу. Общая химия : учебник / А. В. Жолнин [1] Степень окисления – … Химические термины
степень окисления — (окислительное число), условный показатель, характеризующий заряд атома в соединениях. В молекулах с ионной связью совпадает с зарядом иона, например в NaCl Степень окисления натрия +1, хлора 1. В ковалентных соединениях за степень окисления… … Энциклопедический словарь
степень окисления — oksidacijos laipsnis statusas T sritis Standartizacija ir metrologija apibrėžtis Sąlyginis atomo krūvis junginyje, kurį atomas įgytų netekdamas arba prisijungdamas valentinių elektronų. atitikmenys: angl. degree of oxidation; oxidation degree;… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
степень окисления — oksidacijos laipsnis statusas T sritis chemija apibrėžtis Sąlyginis atomo krūvis junginyje, kurį atomas įgytų netekdamas (prisijungdamas) valentinių elektronų. atitikmenys: angl. oxidation degree; oxidation number; valence number rus. степень… … Chemijos terminų aiškinamasis žodynas
степень окисления — oksidacijos laipsnis statusas T sritis fizika atitikmenys: angl. degree of oxidation; oxidation degree; oxidation ratio vok. Oxydationsstufe, f rus. степень окисления, f pranc. degré d’oxydation, m … Fizikos terminų žodynas
степень окисления — 3.5 степень окисления: Условно оцениваемые коррозионные поражения поверхности основного обрабатываемого металла, имеющие различную химическую и физическую природу. Источник … Словарь-справочник терминов нормативно-технической документации
степень окисления — [oxidation level] характеристика состояния элемента в химическом соединении и его поведения в окислительно восстановительных реакциях; численно определяется зарядом иона атома в соединении; Смотри также: Степень степень черноты степень сокращения … Энциклопедический словарь по металлургии
Степень окисления — то же, что Окислительное число … Большая советская энциклопедия
СТЕПЕНЬ ОКИСЛЕНИЯ — (устар. окислит. число), условный электростатич. заряд атома в хим. соединении, к рый находят, считая хим. связи в соед. чисто ионными и принимая заряды атомов О, М (M Li. Cs) и Н, равными соотв. Ч 2 (в пероксидных соед. 1), Ч1 и +1 (если Н… … Химическая энциклопедия
Степень окисления для «чайников»
Степень окисления или окислительное число дает количественную характеристику состояния атома в соединении.
| Степень окисления — условный заряд атома в соединении, если предположить, что соединение состоит только из ионов |
Исходя из вышесказанного, в окислительно-восстановительных реакциях вычисляют неизвестную степень окисления элементов, исходя из двух моментов:
Составляем и решаем уравнение:
| Высшая степень окисления — наибольшее положительное ее значение |
Высшая степень окисления является очень важной количественной характеристикой элемента, чаще всего, она равна номеру группы элемента в Периодической таблице:
| Низшая степень окисления — наименьшее возможное ее значение для данного элемента |
Если элемент имеет три и более возможных степеней окисления, то все остальные степени окисления, лежащие между высшей и низшей, называются промежуточными или средними.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Химия что такое степень окисления
Ключевые слова конспекта: степень окисления химических элементов.
Атом в целом электронейтрален. Однако при образовании химических связей с атомами других элементов атом, как правило, приобретает частичный заряд. Например, при образовании ковалентной полярной связи между атомами водорода и хлора одноэлектронное s-облако атома водорода перекрывается одноэлектронным р-облаком атома хлора:
При этом общая электронная пара смещается в сторону более электроотрицательного атома хлора, но электрон атома водорода перейдет к атому хлора лишь частично, формируя тем самым частичные заряды атомов δ:
Если общую электронную пару в молекуле хлороводорода полностью «передать» атому хлора, то атом хлора «получит» назад собственный электрон и электрон от атома водорода, принимающий участие в ковалентной связи. Электрон атома водорода сформирует на атоме хлора отрицательный заряд, равный —1. А атом водорода, «потерявший» свой электрон, в этом случает приобретает заряд, равный +1. Эти заряды условны, их называют степенью окисления (СО).
Принято условно считать, что в соединениях с ковалентными полярными связями общие электронные пары полностью переходят к более электроотрицательному атому, а потому такие соединения состоят только из положительно и отрицательно заряженных ионов.
СО может иметь отрицательное, положительное или нулевое значения. Значения СО принято записывать сверху над символами элемента, при этом вначале указывается знак условного заряда, а затем его величина:
При определении СО элемента в химическом соединении необходимо учитывать, что:
При рассмотрении неорганических соединений, большинство из которых имеет ионное строение, обычно используют понятие степень окисления, а в органической химии, где большинство соединений имеют молекулярное строение, как правило, используют понятие валентность.
Пример Пример. Определить СО марганца в соединении K2MnO4.
Пользуясь правилом электронейтральности вещества, составляем уравнение:
(+1) • 2 + х + (–2) • 4 = 0;
х = 8 – 2 = 6.
Таким образом, СО марганца +6:
Конспект урока «Степень окисления химических элементов».
Темы, связанные с настоящим конспектом: