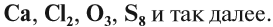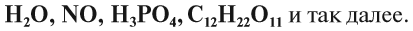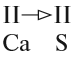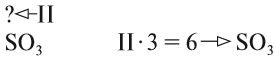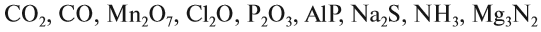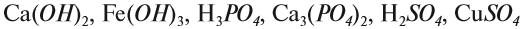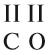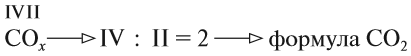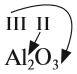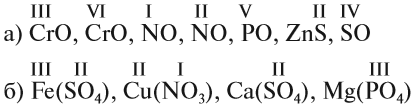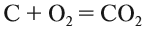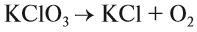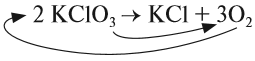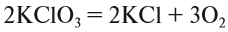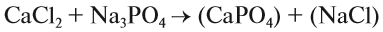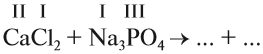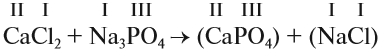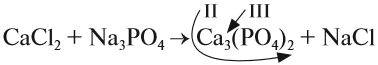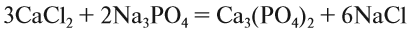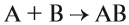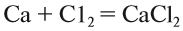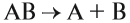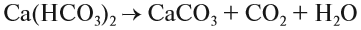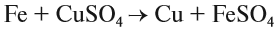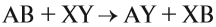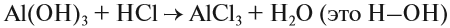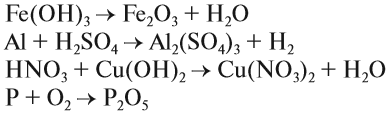Химия с чего начать обучение самостоятельно
Урок 1. Основные понятия и законы предмета «Химия»
Простейшие понятия: вещество, молекула, атом, химический элемент
Что такое химия? Где мы встречаемся с химическими явлениями? Везде. Сама жизнь — это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов…
Что изучает химия? Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество — понятно: это то, из чего состоит окружающий нас мир и мы сами. Но что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество. Изменились молекулы — изменилось вещество (оно стало другим!), — изменились его свойства:
Все эти изменения — следствие сложных и многообразных химических процессов. Итак,
химия — это наука о веществах и их превращениях.
При этом исследуются не всякие превращения, а только такие, при которых
В этом определении встречаются такие понятия, как «вещество», «молекула», «атом». Разберём их подробнее.
Вещество — это то, из чего состоят окружающие нас предметы. Каждому абсолютно чистому веществу (таких в природе, кстати, не существует) приписывают определённую химическую формулу, которая отражает его состав, например:
Выше приведены молекулярные формулы двух веществ. Следует отметить, что далеко не все вещества состоят из молекул, так как существуют вещества, которые состоят из атомов или ионов. Например, алмаз состоит из атомов углерода, а обычная поваренная соль — из ионов Na + и ионов Cl – (условная «молекула» — NaСl).
Наименьшая частица вещества, которая отражает его качественный и количественный состав, называется молекулой.
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака):
Число атомов в молекуле обозначают при помощи индекса:
Но! Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента:
Аналогично изображают число молекул:
Почему атомы водорода и кислорода имеют разное название, разный символ? Потому что это атомы разных химических элементов.
Химический элемент — это частицы с одинаковым зарядом ядер их атомов.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях? Из чего состоит атом*?
* Подробнее о строении атома будет рассказано в уроке 3.
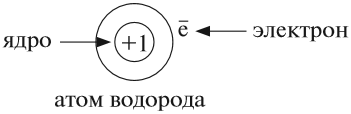
Атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
В ходе химических реакций число электронов любого атома может изменяться, но заряд ядра атома в химических реакциях НЕ МЕНЯЕТСЯ!
Поэтому заряд ядра атома — своеобразный «паспорт» химического элемента. Все атомы с зарядом ядра +1 принадлежат химическому элементу под названием «водород». Атомы с зарядом ядра +8 составляют химический элемент «кислород».
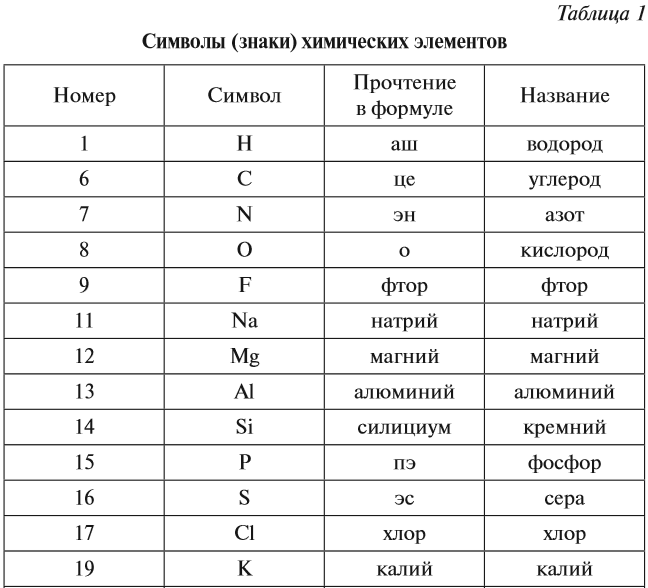
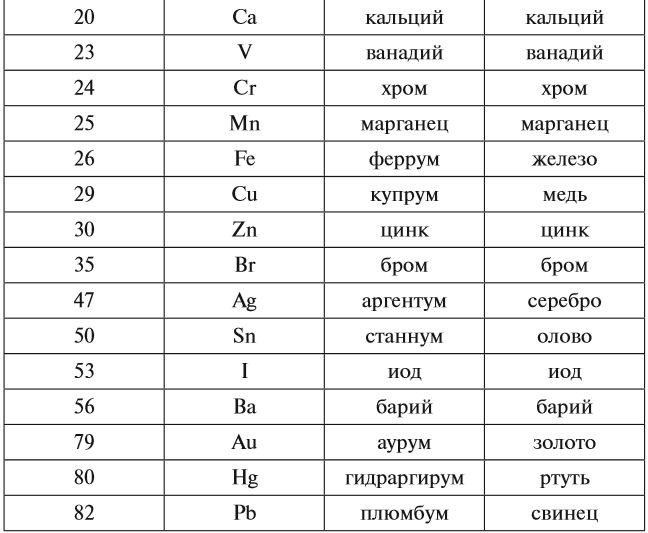
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Менделеева (порядковый номер равен заряду ядра атома); определённое название и, для некоторых химических элементов, особое прочтение символа в химической формуле (табл. 1).
Подведём итог. Вещества состоят из молекул, молекулы состоят из атомов, атомы с одинаковым зарядом ядра относятся к одному и тому же химическому элементу.
Но, если вещество состоит из молекул, то любое изменение состава или строения молекулы приводит к изменению самого вещества, его свойств.
Вопрос. Чем отличаются химические формулы веществ: Н2О и Н2О2?
Хотя по составу молекулы этих веществ отличаются на один атом кислорода, сами вещества по свойствам сильно отличаются друг от друга. Воду Н2О мы пьём и жить без неё не можем, а Н2О2 — перекись водорода, пить нельзя, а в быту её используют для обесцвечивания волос.
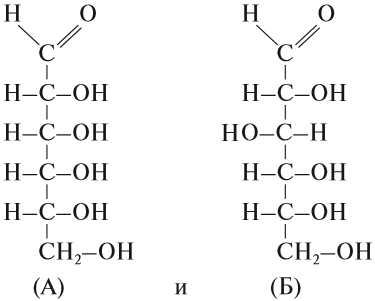
Вопрос. А чем отличаются химические формулы веществ:
Состав этих веществ — аллозы (А) и глюкозы (Б) — одинаков — С6Н12О6. Отличаются они строением молекул, в данном случае — расположением групп ОН в пространстве. Глюкоза — универсальный источник энергии для большинства живых организмов, а аллоза практически не встречается в природе и не может быть источником энергии.
Простые и сложные вещества. Валентность
Вещества бывают простые и сложные. Если молекула состоит из атомов одного химического элемента, — это простое вещество:
Если в состав вещества входят атомы только одного химического элемента — это простое вещество. Причём некоторые химические элементы образуют несколько простых веществ. Так, химический элемент кислород образует простое вещество «кислород» О2 и простое вещество «озон» О3*.
* В 2002 г. появилось сообщение о существовании ещё одного простого вещества кислорода — O4.
А химический элемент углерод образует четыре простых вещества, причём ни одно из них не называется «углерод». Эти вещества отличаются пространственным расположением атомов:
В четвертой модификации «углерода» — фуллерене — атомы углерода образуют сферу, т. е. молекулы фуллерена напоминают мячик.
Существование элемента в виде нескольких простых веществ называется аллотропией. Алмаз, графит, карбин, фуллерен — аллотропные модификации элемента «углерод», а кислород и озон — аллотропные модификации элемента «кислород».
Таким образом, не следует путать эти понятия: «химический элемент» и «простое вещество», а также «молекула» и «атом».
Очень часто в письменных записях слова «молекула» или «атом» заменяют соответствующими символами, но не всегда правильно. Так, нельзя писать: «В состав воды входит Н2», так как речь здесь идёт о химическом элементе водороде — Н. Нужно писать: «В состав воды входит (Н)». Аналогично, правильной будет запись: «При действии металла на раствор кислоты выделится Н2», т. е. вещество водород, молекула которого двухатомна.
Молекулы сложных веществ состоят из атомов разных химических элементов:
Как известно, в состав сложных веществ входят атомы разных химических элементов. Эти атомы соединяются между собой химическими связями: ковалентными, ионными, металлическими.
Способность атома образовывать определённое число ковалентных химических связей называется валентностью. (Подробнее см. урок 4 «Химическая связь».) Правильнее всего определять валентность по графическим или структурным формулам:
В таких формулах одна чёрточка обозначает одну ковалентную связь, т. е. «одну валентность». На практике чаще всего валентность определяют по молекулярной формуле, хотя здесь правильнее говорить о степени окисления элемента (см. урок 7). Иногда результат определения степени окисления соответствует реальному значению валентности, но бывают и неодинаковые результаты.
Задание 1.1. Определите «валентность» (степени окисления) атомов кальция и углерода по формуле СаС2. Совпадает ли полученный результат с реальным значением валентности?
В устойчивой молекуле не может быть «свободных», «лишних» валентностей! Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Для других атомов валентность можно определить (вычислить) из химической формулы вещества.
Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. урок 7). Но поскольку в некоторых соединениях числовые значения этих понятий совпадают, то иногда по формуле можно определять и валентность.
При этом следует учитывать изложенное выше правило о химической связи.
Сделаем практические выводы.
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
4. В остальных случаях ставьте валентности «крест-накрест», т. е. валентность первого атома равна числу атомов второго элемента и наоборот:
Задание 1.2. Определите валентности элементов в соединениях:
Вначале укажите валентности атомов, у которых она постоянна! Аналогично определяется валентность атомных групп (ОН), (РО4), (SО4) и так далее.
Задание 1.3. Определите валентности атомных групп (в формулах выделены курсивом):
Обратите внимание! Одинаковые группы атомов (OH), (РО4), (SO4) имеют одинаковые валентности во всех соединениях.
Зная валентности атома или группы атомов можно составить формулу соединения. Для этого пользуются правилами:
Задание 1.4. Составьте химические формулы соединений:
Уравнения химических реакций
Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением химической реакции. Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O2, образует одну молекулу углекислого газа СО2. Число атомов каждого химического элемента до и после реакции должно быть одинаково! Это правило — следствие Закона сохранения массы вещества: масса исходных веществ равна массе продуктов реакции. Закон был открыт в 18-м веке М. В. Ломоносовым и, независимо от него, А. Л. Лавуазье.
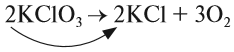
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли КClO3, получается соль КСl и кислород О2:
Число атомов калия и хлора одинаково, а кислорода — разное. Уравняем их:
Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
Теперь между правой и левой частями уравнения можно поставить знак равенства:
Полученная запись показывает, что при разложении двух молекул КClO3 получается две молекулы КСl и три молекулы кислорода O2. Число молекул показывают при помощи коэффициентов.
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым:
Последовательность действий такова:
1. Определим валентность исходных атомов и группы PO4:
2. Перенесём эти числа в правую часть уравнения:
3. Составим химические формулы полученных веществ по валентностям составных частей:
4. Обратим внимание на состав «самого сложного» соединения: Ca3(PO4)2 и уравняем число атомов кальция (их три) и число групп РО4 (их две):
5. Число атомов натрия и хлора до реакции теперь стало равным шести; доставим соответствующий коэффициент:
Эти правила образуют Алгоритм составления уравнений химических реакций обмена, так как, пользуясь этой последовательностью, можно уравнять схемы многих химических реакций, за исключением более сложных окислительно-восстановительных реакций (см. урок 7).
Химические реакции бывают разных типов. Основными являются:
1. Реакции соединения:
Здесь из двух и более веществ образуется одно вещество:
2. Реакции разложения:
Здесь из одного вещества получаются два вещества и более веществ:
3. Реакции замещения:
Здесь реагируют простое и сложное вещества, образуются также простое и сложное вещества, причём простое вещество замещает часть атомов сложного вещества:
4. Реакции обмена:
Здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Существуют и другие типы химических реакций.
Задание 1.5. Расставьте коэффициенты в предложенных выше примерах.
Задание 1.6. Расставьте коэффициенты и определите тип химической реакции:
Выводы
Вещества бывают простые и сложные. Состав веществ показывают при помощи химических формул. Формулы веществ составляют, учитывая валентности составных частей этих веществ. Запись химического процесса при помощи формул называется уравнением химической реакции. Химические реакции бывают разных типов: обмена, замещения, разложения, соединения и другие.
Как быстро выучить химию с нуля, подтянуть знания и оценки
В статье мы подготовили советы, которые помогут быстро выучить химию на «отлично». Разберемся, сколько времени нужно, чтобы освоить предмет с нуля, хватит ли для этого нескольких дней и как легко выучить все формулы.
С чего начать учить химию
Химия – одна из наиболее сложных школьных дисциплин. Физические и химические свойства элементов, особенности протекания реакций между различными веществами, валентность, электролитическая диссоциация и многое другое – все это школьники должны знать и понимать.
3 рекомендации, с чего лучше начать учить химию:
Получится ли освоить предмет самостоятельно
Химию можно выучить и самому, но следует иметь в виду, что процесс не будет быстрым или легким. С какими трудностями сталкиваются школьники, которые занимаются самостоятельно:
Как учиться в домашних условиях
Если хотите подтянуть химию в домашних условиях, то проще и правильнее будет заниматься вместе с преподавателем онлайн.
Уроки с репетитором.
Он оценивает уровень знаний ребенка и составляет индивидуальный план. Занятия проводятся через Скайп: школьник и учитель общаются в режиме реального времени, работают на интерактивной доске. Педагог сразу же отвечает на все вопросы, при необходимости еще раз объясняет сложную тему, указывает на ошибки.
Стоимость онлайн-уроков ниже, чем встречи с преподавателем офлайн, но не уступают им по качеству.
На нашем сайте есть разные сервисы для обучения с репетиторами. В детском разделе можно выбрать программу по цене, срокам подготовки и другим параметрам.
Онлайн-курсы.
Самый эффективный способ выучить химию, подойдет для тех, кто хочет заниматься по индивидуальному графику. Уроки проводят в режиме реального времени и записывают. Если вы не сможете подключиться к онлайн-занятию, то посмотрите видеоурок в личном кабинете в любое время.
Все видеозаписи, конспекты лекций, презентации и другие учебные материалы будут доступны ученику и после курса. Вопросы можно задавать на онлайн-уроке или писать в чат куратору.
Подобрать курс по химии также можно на нашем сайте в детском разделе.
Для вашего удобства, приведем ссылки для разных классов:
Преимущества учебы в онлайн-школах:
Хватит ли года, чтобы понять все темы с 7 по 11 класс
Год – это достаточный срок, чтобы разобраться по всех разделах химии. 5 рекомендаций школьникам, как изучать химию:
Выучить школьный предмет за год легче всего на онлайн-курсах – многие из них длятся с сентября до мая-июня. На занятиях помогут понять химию, подготовят к ОГЭ 9 класса или к ЕГЭ. Например, в онлайн-школе «Фоксфорд» есть углубленные программы, подготовительные и просто развивающие кругозор, например, «Эксперименты и химия вокруг нас».
Как быстро и легко выучить химию с нуля
Как можно ускорить и облегчить процесс, если вы изучаете химию с нуля:
Далее расскажем подробнее, как выучить или повторить химию за месяц, неделю или день.
На нашем сервисе собран список школ с курсами подготовки к ОГЭ и ЕГЭ по химии.
За 1-2 месяца
Если вам нужно вспомнить пройденный материал, чтобы написать годовую контрольную на отлично, то подготовку можно начать за месяц. Но если предстоит сдавать ОГЭ или ЕГЭ, то 2-3 месяцев не хватит, чтобы полноценно выучить всю программу по химии с нуля.
Что делать, если до сдачи экзамена остается не больше 8-10 недель:
Еще один эффективный способ, как можно выучить химию за короткий срок, – это экспресс-курсы. В онлайн-школах есть специальные программы, состоящие из видеоуроков в записи, вы сможете смотреть их 2 и даже 3 раза в неделю. Доступ к новому занятию открывается после сдачи домашней работы по предыдущей теме. Например, видеокурс «Неорганическая химия: практикум для 8-11 классов» от школы «Фоксфорд» включает 8 занятий – его можно пройти за пару недель.
За неделю
Что можно сделать за неделю:
Реально ли подтянуть знания в более короткие сроки
За 1, 2 или 3 дня можно подтянуть знания по химии, если сдаете итоговую работу в четверти. Но если вам предстоит написать годовую контрольную, ОГЭ или ЕГЭ, то подготовку надо начинать заранее – хотя бы за несколько недель/месяцев.
Накануне экзамена можно позаниматься 2-3 часа, почитать лекции, посмотреть решение задач. Но не стоит сидеть над учебниками весь день и тем более ночь – вы только сильнее запутаетесь.
А также не нужно открывать конспекты или зубрить формулы за 5-15 минут до экзамена. Лучше подготовьтесь морально. Чем больше волнения – тем выше риск ошибок из-за невнимательности.
Самоучитель по химии
Пособие для тех, кто не знает, но хочет узнать и понять химию
Часть I. Элементы общей химии
(первый уровень сложности)
Я, Френкель Евгения Николаевна, заслуженный работник высшей школы РФ, выпускница химического факультета МГУ 1972 г., педагогический стаж 34 года. Кроме того, я мать троих детей и бабушка четырех внуков, старший из которых школьник.
Меня волнует проблема школьных учебников. Главная беда многих из них – тяжелый язык, который требует дополнительного «перевода» на понятный школьнику язык изложения учебного материала. Ко мне часто обращаются ученики средней школы с такой просьбой: «Переведите текст учебника, чтобы понятно было». Поэтому я написала «Самоучитель по химии», в котором многие сложные вопросы изложены вполне доступно и в то же время научно. На основе этого «Самоучителя», который был написан в 1991 г., я разработала программу и содержание подготовительных курсов. На них обучались сотни школьников. Многие из них начинали с нуля и за 40 занятий понимали предмет настолько, что сдавали экзамены на «4» и «5». Поэтому в нашем городе мои пособия-самоучители расходятся как горячие пирожки.
Может, и другим пригодятся мои наработки?
Предисловие
Уважаемые читатели! Предлагаемый вашему вниманию «Самоучитель по химии» – не обычный учебник. В нем не просто излагаются какие-то факты или описываются свойства веществ. «Самоучитель» объясняет и учит даже в том случае, если вы, к сожалению, не знаете и не понимаете химии, а к учителю обратиться за разъяснениями не можете или стесняетесь. В виде рукописи эта книга используется школьниками с 1991 г., и не было ни одного ученика, который бы провалился на экзамене по химии и в школе, и в вузах. Причем многие из них совсем не знали химии.
«Самоучитель» рассчитан на самостоятельную работу ученика. Главное – отвечать по ходу чтения на те вопросы, которые встречаются в тексте. Если вы не смогли ответить на вопрос, то читайте внимательнее текст еще раз – все ответы имеются рядом. Желательно также выполнять все упражнения, которые встречаются по ходу объяснения нового материала. В этом помогут многочисленные обучающие алгоритмы, которые практически не встречаются в других учебниках. С их помощью вы научитесь:




В пособии два уровня сложности. Самоучитель первого уровня сложности состоит из трех частей.
I часть. Элементы общей химии (публикуемая).
II часть. Элементы неорганической химии.
III часть. Элементы органической химии.
Книг второго уровня сложности тоже три.
Теоретические основы общей химии.
Теоретические основы неорганической химии.
Теоретические основы органической химии.
Глава 1. Основные понятия химии.
Глава 2. Важнейшие классы неорганических соединений.
Упражнения к главе 2.
Глава 3. Элементарные сведения о строении атома. Периодический закон Д.И.Менделеева.
Глава 4. Понятие о химической связи.
Глава 6. Электролитическая диссоциация.
6.1. Понятие о рН (водородном показателе).
Упражнения к главе 6.
Глава 7. Понятие об окислительно-восстановительных реакциях.
Глава 8. Расчеты по химическим формулам и уравнениям.
8.2. Задачи, решаемые по стандартным формулам.
8.2.1. Задачи по теме «Газы».
8.2.2. Задачи по теме «Способы выражения концентрации растворов».
8.2.3. Задачи по теме «Количественный состав вещества».
8.3. Задачи, решаемые по уравнениям реакций.
8.3.1. Оформление расчетов по уравнениям реакций.
8.3.2. Задачи по теме «Количественный состав растворов и смесей».
8.3.3. Задачи на установление формулы вещества.
8.4. Задачи для самостоятельного решения.
Глава 1. Основные понятия химии
Что такое химия? Где мы встречаемся с химическими явлениями?
Химия – везде. Сама жизнь – это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов.
Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество?
Вещество – это то, из чего состоит окружающий нас мир и мы сами.
Что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество*. Изменились молекулы – изменилось вещество (оно стало другим), изменились его свойства. Например, свежее молоко стало кислым, зеленые листья стали желтыми, сырое мясо при обжаривании изменило запах.
Все эти изменения – следствие сложных и многообразных химических процессов. Однако признаки простых химических реакций, в результате которых изменяется состав и строение молекул, такие же: изменение цвета, вкуса или запаха, выделение газа, света или тепла, появление осадка.
Что же такое молекулы, изменение которых влечет за собой столь разнообразные проявления?
Молекулы – это мельчайшие частицы вещества, отражающие его качественный и количественный состав и его химические свойства.
Изучая состав и строение одной молекулы, можно предсказать многие свойства данного вещества в целом. Такие исследования – одна из главных задач химии.
Как устроены молекулы? Из чего они состоят?
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака). Например, Н – атом водорода, О – атом кислорода.
Число атомов в молекуле обозначают при помощи индекса – цифры внизу справа после символа.
О2 – это молекула вещества кислорода, состоящая из двух атомов кислорода;
Н2О – это молекула вещества воды, состоящая из двух атомов водорода и одного атома кислорода.
Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента – цифры перед символом:
Аналогично изображают число молекул:
2Н2 – две молекулы водорода;
3Н2О – три молекулы воды.
Почему атомы водорода и кислорода имеют разные названия и разные символы? Потому что это атомы разных химических элементов.
Химический элемент – это вид атомов с одинаковым зарядом ядер.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях, из чего состоит атом?
Нейтральный атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
В ходе химических реакций число электронов любого атома может изменяться, а вот заряд ядра атома не меняется. Поэтому заряд ядра атома – своеобразный «паспорт» химического элемента. Все атомы с зарядом ядра +1 принадлежат химическому элементу под названием водород. Атомы с зарядом ядра +8 относятся к химическому элементу кислороду.
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Д.И.Менделеева (порядковый номер равен заряду ядра атома), определенное название, а для некоторых химических элементов – особое прочтение символа в химической формуле (табл. 1).
| № п/п | № в таблице Д.И.Менделеева | Символ | Прочтение в формуле | Название |
| 1 | 1 | H | аш | Водород |
| 2 | 6 | C | це | Углерод |
| 3 | 7 | N | эн | Азот |
| 4 | 8 | O | о | Кислород |
| 5 | 9 | F | фтор | Фтор |
| 6 | 11 | Na | натрий | Натрий |
| 7 | 12 | Mg | магний | Магний |
| 8 | 13 | Al | алюминий | Алюминий |
| 9 | 14 | Si | силициум | Кремний |
| 10 | 15 | P | пэ | Фосфор |
| 11 | 16 | S | эс | Сера |
| 12 | 17 | Cl | хлор | Хлор |
| 13 | 19 | K | калий | Калий |
| 14 | 20 | Ca | кальций | Кальций |
| 15 | 23 | V | ванадий | Ванадий |
| 16 | 24 | Cr | хром | Хром |
| 17 | 25 | Mn | марганец | Марганец |
| 18 | 26 | Fe | феррум | Железо |
| 19 | 29 | Cu | купрум | Медь |
| 20 | 30 | Zn | цинк | Цинк |
| 21 | 35 | Br | бром | Бром |
| 22 | 47 | Ag | аргентум | Серебро |
| 23 | 50 | Sn | станнум | Олово |
| 24 | 53 | I | йод | Йод |
| 25 | 56 | Ba | барий | Барий |
| 26 | 79 | Au | аурум | Золото |
| 27 | 80 | Hg | гидраргирум | Ртуть |
| 28 | 82 | Pb | плюмбум | Cвинец |
Вещества бывают простые и сложные. Если молекула состоит из атомов одного химического элемента, это простое вещество. Простые вещества – Са, Сl2, О3, S8 и т. д.
Молекулы сложных веществ состоят из атомов разных химических элементов. Сложные вещества – H2O, NO, H3PO4, C12H22O11 и т. д.
Задание 1.1. Укажите число атомов в молекулах сложных веществ H2O, NO, H3PO4, C12H22O11, назовите эти атомы.
Возникает вопрос: почему для воды всегда записывается формула Н2О, а не НО или НО2? Опыт доказывает, что состав воды, полученной любым способом или взятой из любого источника, всегда соответствует формуле Н2О (речь идет о чистой воде).
Дело в том, что атомы в молекуле воды и в молекуле любого другого вещества соединены при помощи химических связей. Химическая связь соединяет как минимум два атома. Поэтому, если молекула состоит из двух атомов и один из них образует три химические связи, то другой также образует три химические связи.
Число химических связей, образуемых атомом, называют его валентностью.
Если обозначить каждую химическую связь черточкой, то для молекулы из двух атомов АБ получим А
В данной молекуле атомы А и Б трехвалентны.
Известно, что атом кислорода двухвалентен, атом водорода одновалентен.
В о п р о с. Сколько атомов водорода может присоединиться к одному атому кислорода?
О т в е т. Два атома. Состав воды описывают формулой Н–О–Н, или Н2О.
П о м н и т е! В устойчивой молекуле не может быть «свободных», «лишних» валентностей. Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Символы элементов
Для других атомов валентность** можно определить (вычислить) из химической формулы вещества. При этом нужно учитывать изложенное выше правило о химической связи. Например, определим валентность x марганца Mn по формуле вещества MnO2:
Общее число химических связей, образуемых одним и другим элементом (Mn и О), одинаково:
x · 1 = 4; II · 2 = 4. Отсюда х = 4, т.е. в этой химической формуле марганец четырехвалентен.
П р а к т и ч е с к и е в ы в о д ы
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
4. В остальных случаях ставьте валентности «крест-накрест», т.е. валентность одного элемента равна индексу другого элемента:
Задание 1.2. Определите валентности элементов в соединениях:
П о д с к а з к а. Сначала укажите валентность атомов, у которых она постоянная. Аналогично определяется валентность атомных групп ОН, РО4, SО4 и др.
Задание 1.3. Определите валентности атомных групп (в формулах подчеркнуты):
(Обратите внимание! Одинаковые группы атомов имеют одинаковые валентности во всех соединениях.)
Зная валентности атома или группы атомов, можно составить формулу соединения. Для этого пользуются следующими правилами.
• Если валентности атомов одинаковы, то и число атомов одинаково, т.е. индексы не ставим:
• Если валентности кратны (обе делятся на одно и то же число), то число атомов элемента с меньшей валентностью определяем делением:
• В остальных случаях индексы определяют «крест-накрест»:
Задание 1.4. Составьте химические формулы соединений:
Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением реакции. Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O2, образует одну молекулу углекислого газа СО2. Число атомов каждого химического элемента до и после реакции должно быть одинаково. Это правило – следствие закона сохранения массы вещества. Закон сохранения массы: масса исходных веществ равна массе продуктов реакции.
Закон был открыт в XVIII в. М.В.Ломоносовым и, независимо от него, А.Л.Лавуазье.
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли KClO3 получается соль KСl и кислород О2:
KClO3 
Число атомов калия и хлора одинаково, а кислорода – разное. Уравняем их:
Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
Наконец, между правой и левой частями уравнения можно поставить знак равенства:
Полученная запись показывает, что при разложении сложного вещества KClO3 получаются два новых вещества – сложное KСl и простое – кислород O2. Числа перед формулами веществ в уравнениях химических реакций называют коэффициентами.
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым. Составим уравнение реакции веществ CaCl2 и Na3PO4:
П о с л е д о в а т е л ь н о с т ь д е й с т в и й
1) Определим валентность исходных атомов и группы PO4:
2) Напишем правую часть уравнения (пока без индексов, формулы веществ в скобках надо уточнить):
3) Составим химические формулы полученных веществ по валентностям составных частей:
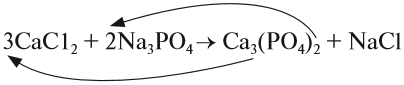
4) Обратим внимание на состав самого сложного соединения Ca3(PO4)2 и уравняем число атомов кальция (их три) и число групп РО4 (их две):
5) Число атомов натрия и хлора до реакции теперь стало равным шести. Поставим соответствующий коэффициент в правую часть схемы перед формулой NaCl:
Пользуясь такой последовательностью, можно уравнять схемы многих химических реакций (за исключением более сложных окислительно-восстановительных реакций, см. главу 7).
Типы химических реакций. Химические реакции бывают разных типов. Основными являются четыре типа – соединение, разложение, замещение и обмен.
1. Реакции соединения – из двух и более веществ образуется одно вещество:
А + В 
2. Реакции разложения – из одного вещества получаются два вещества или более:
АВ 
Ca(HCO3)2 
3. Реакции замещения – реагируют простое и сложное вещества, образуются также простое и сложное вещества, причем простое вещество замещает часть атомов сложного вещества:
А + ВХ 
4. Реакции обмена – здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
АВ + XY 
Существуют и другие типы химических реакций.
Задание 1.5. Расставьте коэффициенты в схемах реакций:
Na + Cl2 
NaHCO3 
Fe + AgNO3 
Fe(OH)3 + HCl 
Задание 1.6. Расставьте коэффициенты и определите типы химических реакций:
Fe(OH)3 
Al + H2SO4 
HNO3 + Cu(OH)2 
P + O2 
Выводы по главе 1. Вещества состоят из молекул, молекулы состоят из атомов, атомы с одинаковым зарядом ядра относятся к одному и тому же химическому элементу.
Вещества бывают простые и сложные. Состав веществ показывают при помощи химических формул. Формулы веществ составляют, учитывая валентности составных частей. Запись химического процесса при помощи формул называется уравнением химической реакции. Химические реакции бывают разных типов: обмена, замещения, разложения, соединения и др.
Упражнения к главе 1
1. Выучите табл. 1. Проверьте себя, напишите химические символы: серы, цинка, олова, магния, марганца, калия, кальция, свинца, железа и фтора.
2. Напишите символы химических элементов, которые в формулах произносятся как: «аш», «о», «купрум», «эс», «пэ», «гидраргирум», «станнум», «плюмбум», «эн», «феррум», «це», «аргентум». Назовите эти элементы.
3. Укажите число атомов каждого химического элемента в формулах соединений:
4. Определите, какие из веществ – простые, а какие – сложные:
Прочитайте формулы этих веществ.
5. Выучите табл. 2. Составьте химические формулы веществ по известной валентности элементов и атомных групп:
6. Определите валентность химических элементов в соединениях:
7. Расставьте коэффициенты и укажите типы химических реакций:
а) Mg + O2 
б) Al + CuCl2 
в) NaNO3 
г) AgNO3 + BaCl2 
д) Al + HCl 
е) KOH + H3PO4 
ж) CH4 
* Существуют вещества, построенные не из молекул. Но об этих веществах речь пойдет позже (см. главу 4).
** Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. главу 7). Однако во многих соединениях числовые значения этих понятий совпадают, поэтому по формуле вещества можно определять и валентность.