Хламидийный простатит что это
Острый и хронический хламидийный простатит
Острый хламидийный простатит возникает как следствие хламидиоза органов мочеполовой системы.
Хронический хламидийный простатит является следствием неправильного лечения острой формы этого заболевания.
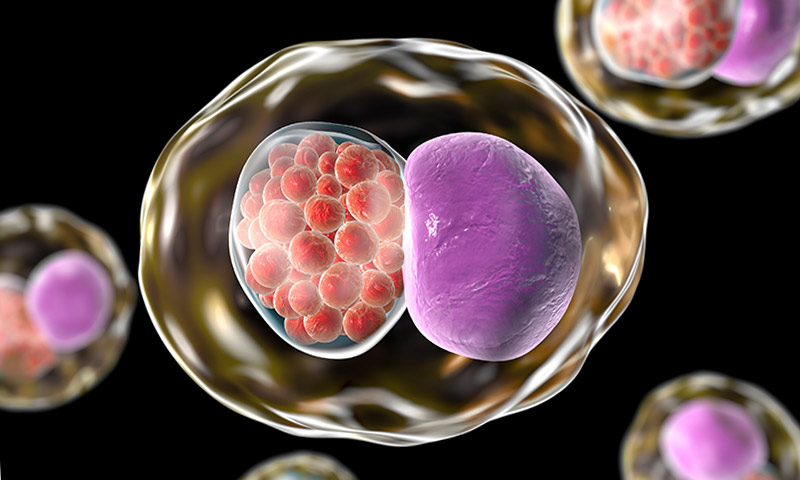
Инфекционным агентом заболевания является хламидия – внутриклеточный паразит.
Заражение преимущественно происходит при незащищенном сексе.
При недостаточном иммунитете или неверно подобранной терапии возбудители болезни поражают предстательную железу.
Важно! Хронический хламидийный простатит и его острая форма составляют 30% от общего числа простатитов.
Лечение хламидийного простатита необходимо для сохранения здоровья мужчины.
Хламидийный простатит: симптомы
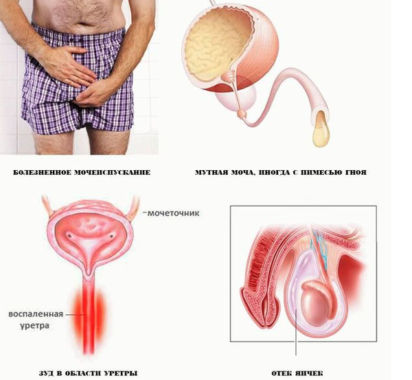
Выделяют следующие признаки хламидийного простатита.
Симптомы могут сопровождаться чувством общей усталости и другими признаками интоксикации организма.
При пальпации или визуальном исследовании простаты отмечается ее увеличение или деформация.
Хронический хламидийный простатит характеризуется чередованием обострений и скрытых периодов болезни.
Возобновление симптомов при хронической форме заболевания происходит на фоне ослабления организма.
Обострение может быть вызвано болезнями, нервной перегрузкой, переохлаждением и другими стрессовыми факторами.
Хламидия трахоматис
Как лечить хламидии у мужчин: все о причинах, симптомах и диагностике
Хламидии трахоматис (Chlamydia trachomatis) – микроорганизмы, которые не относятся ни к бактериям, ни к вирусам. Они заняли промежуточное положение и скорее относятся к паразитам, которые в качестве среды обитания выбирают мочеполовую систему человека.
Хламидии вызывают серьезное заболевание – хламидиоз. Оно встречается даже чаще, чем гонорея, и относится к довольно распространенным. Поэтому лечение хламидий трахоматис у мужчин имеет несколько общеизвестных схем, но в каждом случае терапию подбирают индивидуально.
Причины хламидии трахоматис у мужчин
Хламидии трахоматис у мужчин находятся на первом месте среди заболеваний, передающихся половым путем. Причем в 50% случаев хламидиоз протекает бессимптомно и чаще всего в сочетании с другими инфекциями: трихомонадной, микоплазменной, гонококковой. Повышенный риск заражения хламидиями наблюдается:
Откуда берутся хламидии у мужчин: основной способ – незащищенные половые контакты. Он наиболее распространенный. Контактно-бытовой путь инфицирования встречается реже, поскольку хламидии не способны долгое время существовать вне организма. Поэтому на вопрос, как передаются хламидии мужчинам, можно точно ответить, что половым путем. У мужчин вероятность заражения при однократном половом акте составляет 32%.
По каким симптомам можно заподозрить хламидиоз
У большинства мужчин болезнь не вызывает каких-либо симптомов. Они начинают ощущаться только при ярко выраженном течении болезни. Иногда симптомы появляются и исчезают спустя пару недели. Мужчина думает, что выздоровел, но на самом деле становится носителем инфекции. В таком случае есть риск передачи заболевания при половых контактах.
Характерные симптомы хламидий у мужчин:
Если говорить о том, чем опасны хламидии для мужчин, то стоит в первую очередь отметить заболевания мочевыделительной системы. Чаще всего возникает уретрит, а за ним могут развиваться и другие патологии:
Виды и стадии хламидиоза
То, как проявляются хламидии у мужчин, зависит от формы развития заболевания. При остром течении признаки впервые симптомы возникают в течение двух месяцев после заражения. Хроническая форма заболевания длится долгое время, и ее признаки появляются периодически в форме обострений.
Как диагностируют хламидиоз
Хламидии в крови у мужчин можно выявить только по специальному анализу, который проводят методом ПЦР (полимеразной цепной реакции). На сегодня он наиболее точный, позволяет выявить во взятом материале ДНК возбудителя и точно его определить. Выбор в пользу ПЦР делают по причине того, что такой возбудитель размножается внутри клеток и по-другому его нельзя обнаружить.
В клинике Dr. AkNer предлагают доступные цены для анализа на хламидии у мужчин. Результаты исследования можно получить через 1,5-2 суток после проведения, а в ряде случаев даже на следующий день. Для достоверности анализа соскоб из уретры берут не ранее чем через 3 часа после мочеиспускания и 2 недели после отмены антибиотиков, если мужчина их принимал.
Правильное лечение хламидиоза
Наиболее эффективное лечение хламидий трахоматис у мужчин предполагает прием антибиотиков. Важно отметить, что препараты пенициллинового ряда неэффективны, поскольку паразит не проявляет к ним чувствительность. При хламидиозе назначают тетрациклиновые антибиотики, фторхинолоны и макролиды.
Как правильно лечить хламидии у мужчин:
Лечение хламидий трахоматис у мужчин антибиотиками должно проводиться под контролем врача. Самолечение полностью исключено, поскольку может только ухудшить ситуацию и вызвать устойчивость паразита к антибактериальным препаратам, что только усложнит терапию. Местные антисептические средства при хламидиозе не используют, поскольку они неэффективны.
Клиника Dr. AkNer предлагает комплексное лечение хламидиоза с индивидуальным подбором антибиотика, который принесет результат для конкретного пациента. К терапии этого заболевания нужно подходить очень серьезно, поскольку мужчина может заразить женщину, а еще столкнуться с таким осложнением, как бесплодие.
Чтобы не допустить этого, запишитесь на прием к урологу, позвонив по любому номеру: 8 (495) 098-03-03 или 8 (926) 497-44-44. Мы поможем справиться с заболеванием вне зависимости от стадии и при наличии или отсутствии осложнений.
Урогенитальный хламидиоз как фактор инфертильности у мужчин. Лечение хронического бактериального и хронического простатита, ассоциированного с хламиди
Urogenital chlomidiosis is one of the factors causing disorders in fertilizing ability of spermatozoa. The studies confirm a high therapeutic efficiency of levofloxacin in treatment of nearly all forms of urogenital infection.
Для России, как и для большинства европейских стран, серьезной проблемой является депопуляция населения. После драматической демографической ситуации в постсоветском периоде уровень рождаемости в Российской Федерации в настоящее время все еще носит нестабильный характер.
Следует отметить, что во всем мире низкие показатели естественного прироста населения наблюдаются даже в наиболее благоприятных по качеству жизни странах.
Кроме того, не внушают оптимизма изменения, касающиеся возрастной пирамиды: население планеты неуклонно стареет, причем не только в Европе, но и в Африке. В этой связи стратегическая задача, стоящая перед Российской Федерацией, — стабилизация численности населения страны.
Помимо сугубо социально-экономических причин, ведущее место в демографическом кризисе, безусловно, занимает проблема мужского и женского репродуктивного здоровья.
Известно, что около 40% причин бесплодия в паре связано с мужским фактором, при этом у 70% мужчин выявляется олигоастенотератозооспермия, а у 13% — азооспермия.
Согласно существующим в настоящее время представлениям, в основе нарушения механизма мужской фертильности лежат гормональный дисбаланс, патология тестикул, генетические нарушения, наследственный фактор, аутоиммунная агрессия.
В последнее время повышенный интерес вызывает изучение избыточной продукции активных форм радикалов кислорода (АФК) полиморфноядерными лейкоцитами спермы, которые являются причиной оксидативного стресса, приводящего к повреждению мембраны сперматозоидов, снижению подвижности сперматозоидов и нарушению их оплодотворяющей способности.
Установлено, что повреждение ядерной ДНК, вызывающее нарушение функции сперматозоидов, является основной причиной неразвивающейся беременности, влияет на развитие эмбриона и имплантацию, в несколько раз увеличивает риск спонтанных абортов [1, 2].
Значительное место в развитии патологии репродуктивных органов занимает широкий спектр уропатогенных и условно-патогенных микроорганизмов, в том числе колонизация мочеполовой системы инфекциями, передаваемыми половым путем (ИППП), влекущими за собой патологические изменения в эякуляте.
Нарушение мужской фертильности как следствие инфекционно-воспалительного процесса урогенитального тракта напрямую связано с гиперпродукцией АФК, нарушением функции или проходимости придатка яичка, патологической стимуляцией продукции антиспермальных антител.
Еще одним значимым фактором, приводящим к снижению мужской фертильности, является простатит.
Известно, что изменение секреторной функции железы приводит к нарушению количественного и качественного состава семенной жидкости, а токсическое влияние микроорганизмов и продуктов их жизнедеятельности губительно воздействует на сперматогенез в целом. Имеются данные, что хронический простатит приводит к увеличению продукции АФК в сперме в среднем в 8 раз [3].
Урогенитальный хламидиоз
Во всех странах мира не теряет своей актуальности проблема заболеваемости хламидийной инфекцией, доминирующей по частоте выявления среди всех ИППП.
Урогенитальный хламидиоз, вызываемый C. trachomatis (серовары от D до K), по повреждающему воздействию на репродуктивную систему человека занимает одно из лидирующих мест среди ИППП.
По частоте встречаемости наиболее распространенных возбудителей негонококковых уретритов C. trachomatis занимает от 11% до 43%, тогда как M. genitalium — от 9% до 25%, Tr. vaginalis — от 1% до 20%. При этом на долю мужчин приходится 65% всех наблюдений [4].
Наряду с T. pallidum, N. gonorrhoeae, Tr. vaginalis и M. genitalium, C. trachomatis является абсолютным патогеном и подлежит обязательной санации вследствие высокого риска развития тяжелых осложнений [5, 6].
Несмотря на принятые во многих странах мира программы по борьбе с ИППП, снижения заболеваемости урогенитальной хламидийной инфекцией не наблюдается. Например, в странах Европы ежегодно регистрируется 600 тыс. новых случаев хламидиоза.
Между тем уровень заболеваемости не отражает реальных статистических показателей, поскольку считается, что у 40–50% мужчин хламидиоз протекает бессимптомно, что в свою очередь повышает риск развития серьезных осложнений и дальнейшего распространения инфекции.
В нашей стране проблема хламидиоза, как и проблема ИППП в целом, представляется еще более значимой в связи с изменившейся в последние годы моделью сексуального поведения населения, снизившимся возрастом сексуального дебюта, повышением уровня общего промискуитета и притоком трудовых мигрантов из сопредельных стран.
Важно отметить, что хламидиоз часто протекает в бессимптомной и субклинической формах, что чрезвычайно важно с эпидемиологической точки зрения, может диагностироваться не только как моноинфекция, но и выявляется вместе с другими бактериями и вирусами и их сочетаниями, усугубляя течение патологического процесса.
Кроме того, C. trachomatis также является фактором гиперпродукции АФК, приводящим к окислительному стрессу с последующим нарушением адекватной упаковки хроматина, вызывает фрагментацию ДНК и инициирует опосредованный апоптоз сперматозоидов.
Клинические проявления хламидийной инфекции
У мужчин основным проявлением хламидиоза является уретрит, проявляющийся в виде скудных слизистых или необильных слизисто-гнойных выделений, которым часто сопутствуют жжение, зуд, иногда дизурия, возникающая через несколько дней или недель после незащищенного сексуального контакта. Помимо торпидно протекающих уретритов, колонизация мочеполовой системы хламидийной инфекцией может привести к развитию таких осложнений, как эпидидимит, фуникулит и сопутствующий уретриту простатит, что неизбежно увеличивает вероятность последующей патоспермии.
Кроме того, при различных вариантах сексуальной активности может возникать хламидийный фарингит, хламидиоз аноректальной области, хламидийный конъюнктивит. В ряде случаев диагностируется уретроокулосиновиальный синдром (уретрит, конъюнктивит, реактивный артрит).
Хронический простатит, ассоциированный с хламидийной инфекцией
В последние годы вновь возник интерес к хламидийной инфекции как фактору в инициации хронического простатита. Формально C. trachomatis является недоказанной, но вполне вероятной причиной в развитии простатита [7, 8]. Практические наблюдения свидетельствуют о том, что именно хламидиоз нередко оказывается ведущим инфекционным агентом в этиологии хронического простатита [9].
Основанием для такого утверждения служит выявление C. trachomatis в секрете простаты при отсутствии других инфекций мочевого тракта на фоне характерной симптоматики хронического простатита и лейкоцитоза в секрете предстательной железы.
Диагностика хламидиоза
Верификация диагностики хламидийной инфекции основывается на результатах лабораторных методов исследований с помощью высокочувствительных и специфических методов амплификации нуклеиновых кислот (МАНК) или выделения С. trachomatis в культуре клеток McCoy («золотой стандарт»).
Следует подчеркнуть, что такие скрининговые методы, как прямая иммунофлюоресценция (ПИФ) и серологические исследования (ИФА), в настоящее время не используются в связи с их недостаточной чувствительностью и низкой информативностью.
Лечение
Основная задача лечения хламидийной инфекции — эрадикация С. trachomatis и разрешение клинических проявлений инфекции.
Важно отметить, что выявление у пациента хламидиоза обязывает к проведению профилактического лечения полового партнера.
В рекомендациях Европейской ассоциации урологов (European Association of Urology, EAU) по лечению ИППП [10, 11] и рекомендациях Международного центра по борьбе с половыми инфекциями (International Union against Sexually Transmitted Infections, IUSTI) (2011), также как в Российских национальных рекомендациях по антимикробной терапии и профилактике инфекций почек, мочевыводящих путей и мужских половых органов, из альтернативных препаратов в схемах лечения хламидиоза указаны фторхинолоны (левофлоксацин) [12].
Кроме того, известно, что в США левофлоксацин является единственным фторхинолоном, разрешенным Управлением по надзору за качеством пищевых продуктов и лекарственных средств (Food and Drugs Administration of the United States, FDA) в качестве средства выбора при лечении инфекций мочевыводящих путей (негонококкового уретрита, урогенитального хламидиоза, гонококковой инфекции и хронического бактериального простатита).
Общие принципы терапии неосложненных и осложненных форм хламидийной инфекции представлены в табл. 1 и 2.
Особо следует подчеркнуть, что осложненные формы хламидиоза (эпидидимит, орхит, простатит) требуют увеличения продолжительности антибактериального лечения на срок от 14 до 28 дней.
Кроме того, известно, что при лечении больных с хроническим простатитом требованиям доказательной медицины отвечают только альфа-1-адреноблокаторы, нестероидные противовоспалительные препараты и фторхинолоны (левофлоксацин) [13, 14].
На фармакологическом рынке России левофлоксацин представлен несколькими препаратами, один из которых Ремедиа (активное вещество левофлоксацин гемигидрат 256 мг/512 мг/768 мг, эквивалентный левофлоксацину 250 мг/500 мг/750 мг).
Ремедиа — противомикробное бактерицидное средство широкого спектра действия из группы фторхинолонов. В качестве активного вещества содержит левофлоксацин — левовращающий изомер офлоксацина.
Целью настоящего исследования явилось изучение эффективности и безопасности фторхинолона 3-го поколения левофлоксацина, коммерческое название Ремедиа, в лечении хронического бактериального простатита (ХБП) и хронического простатита (ХП), ассоциированного с урогенитальным хламидиозом.
Материалы и методы исследования
Под наблюдением находились 48 мужчин в возрасте от 32 до 52 лет. Пациенты были разделены на 2 группы: 1-я группа (14 человек) — больные с обострением ХП, обратившиеся с характерными клиническими проявлениями простатита; 2-я группа (34 человека) — мужчины, обратившиеся на обследование перед планированием беременности в семье. После стандартного андрологического клинико-лабораторного обследования и на основании микроскопического и бактериоскопического исследования отделяемого из уретры и секрета простаты (ПЖ)/спермы диагноз ХБП был установлен у 14 пациентов 1-й группы. У 28 мужчин 2-й группы диагностирован ХП (категория IV) и еще у 6 пациентов ХП был ассоциирован с хламидийной инфекцией (C. trachomatis выявлены на культуре клеток МсСоу). При этом у больных 2-й группы на фоне ХП и бактериоспермии были отмечены нарушения нормальных параметров спермы (астенозооспермия, астенотератозооспермия, спермагглютинация, лейкоспермия).
У всех больных возбудители, выявленные при бактериоскопическом обследовании, были чувствительны к Ремедиа. Препарат представлен в трех дозировках 250, 500 и 750 мг. Пациентам с ХБП проведен курс лечения Ремедиа в однократной суточной дозе 500 мг, ежедневно в течение 20 дней; у мужчин, в семьях которых которых планировалась беременность, имевших нарушение фертильности и ХП (категория IV) и ХП, ассоциированный с хламидиозом, длительность лечения составляла 10 дней, препарат назначался в дозе 500 мг 1 раз в сутки.
Помимо базовой терапии Ремедиа все мужчины параллельно получили курс физиотерапии бегущим магнитным полем (аппарат «Интрамаг»), а для достижения лучшей элиминации возбудителя из организма использовали иммуномодулирующие ректальные суппозитории Полиоксидоний или Лонгидаза.
Оценку эффективности Ремедиа проводили через 10–14 дней у больных с ХБП и через 21–30 дней у пациентов с ХП и хламидиозом. Оценка основывалась на данных микроскопического и бактериоскопического исследования ПЖ/сперма, у мужчин 2-й группы исследовали также спермограмму и контроль C. trachomatis.
Микробиологическая излеченность отмечена во всех случаях, количество лейкоцитов в секрете ПЖ/эякулят достигли нормальных значений. При этом у 14 больных ХБП полностью разрешилась симптоматика простатита, а у мужчин с бессимптомной формой ХП и сопутствующей патоспермией параметры эякулята приблизились к нормальным показателям» в контроле — C. trachomatis не выявлены.
Выводы
Наши исследования подтверждают результаты ранее проведенных клинических исследований левофлоксацина, свидетельствующих о его высокой терапевтической эффективности при лечении практически всех форм урогенитальной инфекции.
Профиль фармакокинетики, отличная способность проникновения активного вещества в ткань ПЖ, удобство применения препарата Ремедиа (1 раз в сутки) позволяют рекомендовать его в качестве одного из высокоэффективных антибактериальных средств в лечении больных ХБП и ХП, ассоциированного с хламидийной инфекцией. Нежелательных побочных явлений ни в одном случае отмечено не было.
Урогенитальный хламидиоз — один из факторов, вызывающих нарушения оплодотворяющей способности сперматозоидов.
Литература
ООО «Герпетический центр», Москва
Публикации » Хламидиоз протекает бессимптомно и бьет по мочеполовой системе…
Ахмед Азизов, доктор медицинских наук, профессор.
Когда тебя любят, не нужно требовать от человека доказательств любви, они и так видны…
Лучше поинтересоваться анализами на инфекции…
Современные методы диагностики выявляют наличие хламидий у 43% мужчин с простатитами, у каждой второй женщины с хроническими воспалительными заболеваниями мочеполовой сферы; у 57 процентов женщин, страдающих бесплодием; у 87 процентов женщин с невынашиванием беременности…. У мужчин при негонококковых уретритах, хламидии выявляются в 40% случаев, у женщин при цервицитах — в 36% случаев, а при эрозии шейки матки — в 47% и т. д.
Это говорит о распространенности стертых, бессимптомных форм хламидийной инфекции. Часто бывает, что мужчина оправдывается за свою партнершу, говорит она «порядочная женщина», «у нее муж и я, и больше никого». Я, ему отвечаю, «порядочная женщина», если пошла с вами, имея мужа, и вы ей гарантируете верность вам, а как же ее муж, и его сексуальное поведение, вы что, тоже гарантируете….
Хламидии вызывают различную патологию. У мужчин первично поражается мочеиспускательный канал, а затем и другие органы: предстательная железа, семенные пузырьки, придатки. Хламидийный уретрит у мужчин протекает чаще всего хронически, иногда остро и подостро. В большинстве случаев заболевание сопровождается неприятными ощущениями, зудом в мочеиспускательном канале, учащенными позывами и резью при мочеиспускании, не всегда выделениями из уретры. При одновременном поражении других органов, больные жалуются на боли в мошонке, промежности, в области заднего прохода, крестцовой и поясничной областях, а также по ходу седалищного нерва и в нижних конечностях.
Большинство больных предъявляют незначительные субъективные жалобы. Наиболее типичные признаки уретрита, выделения из мочеиспускательного канала (слизистого, слизисто-гнойного или гнойного характера), очень часто отсутствуют, редко могут быть скудные выделения, чаще в виде капельки по утрам («утренняя капелька»). Они появляются после длительной задержки мочи, иногда при дефекации или в конце мочеиспускания.
Инфекция дает осложнения на предстательную железу. Возникающий хламидийный простатит протекает хронически, периодически обостряясь. У мужчин с хламидийным простатитом могут быть выделения из мочеиспускательного канала, иногда во время акта дефекации (дефекационная простаторея) или во время, а точнее, в конце мочеиспускания (микционная простаторея), зуд, неопределенные неприятные ощущения в мочеиспускательном канале, прямой кишке, непостоянную боль в промежности, в области мошонки, в паховой и крестцовой областях, над лоном, по ходу седалищного нерва.
Некоторые пациенты обращают внимание на слипание губок наружного отверстия мочеиспускательного канала после длительной задержки мочи. У отдельных больных учащается мочеиспускание, иногда по ночам. У мужчин также может наблюдаться хламидийный эпидидимит(воспаление придатка яичка) и орхоэпидидимит (воспаление всего яичка). У больных нередко отмечаются нарушения потенции, а также патология сперматозоидов и другие изменения в спермограмме.
При хламидиозе у женщин чаще поражается канал шейки матки, после чего может возникнуть и восходящая инфекция, захватывающая матку, маточные трубы, яичники, а также брюшину.
Хламидий из мочеиспускательного канала способны проникать в мочевой пузырь, вызывая цистит(воспаление мочевого пузыря) и цистоуретрит (воспаление мочевого пузыря и мочеиспускательного канала). Возможен занос хламидий с отделяемым из шейки матки в прямую кишку.
Хламидийные проктиты остаются часто бессимптомными. Наиболее характерным признаком заболевания является усиление выделений из влагалища. К сожалению, часто этот симптом считается женщиной нормой, и она не обращает на него никакого внимания.
Очень часто хламидиоз выявляется у женщин, страдающих от бесплодия.Хламидийная инфекция может приводит кнепроходимости маточных труб, воспалению придатков. При хламидиозе в момент родов может произойти инфицирование ребенка. Если плацента надежно защищала плод от внутриутробного заражения во время всего срока беременности,то во время прохождения новорожденного по родовым путям, возможно заражение.
Лечение хламидиоза длительное и комплексное: антибиотики широкого спектра действия, иммуностимулирующая, противовирусная терапия, а также, по необходимости, местная терапия (инстиляции, физиопроцедуры). Очень важно своевременно выявить хламидиоз еще и потому, что хроническую форму хламидиоза лечить тяжелее и дольше.
Хламидийный простатит что это
Челябинский областной кожно-венерологический диспансер
Челябинская государственная медицинская академия
Челябинская государственная медицинская академия
Современные методы лечения больных хроническим хламидийным простатитом
Журнал: Клиническая дерматология и венерология. 2010;8(5): 32-37
Зиганшин О. Р., Безпалько Ю. В., Ковалев Ю. Н. Современные методы лечения больных хроническим хламидийным простатитом. Клиническая дерматология и венерология. 2010;8(5):32-37.
Ziganshin O R, Bezpal’ko Iu V, Kovalev Iu N. Modern methods for the treatment of patients with chronic chlamydial prostatitis. Klinicheskaya Dermatologiya i Venerologiya. 2010;8(5):32-37.
Челябинский областной кожно-венерологический диспансер
Челябинский областной кожно-венерологический диспансер
Челябинская государственная медицинская академия
Челябинская государственная медицинская академия
Хронический простатит — самое распространенное урологическое заболевание у мужчин моложе 50 лет и третье по частоте среди урологических диагнозов у мужчин старше 50 лет; составляет 8% амбулаторных визитов к урологу [1]. С увеличением возраста частота заболевания увеличивается и достигает 30—73% [2—4]. По влиянию на качество жизни это заболевание сопоставимо с инфарктом миокарда, стенокардией, болезнью Крона, что обусловливает также значительные психологические и социальные проблемы у больных простатитом мужчин трудоспособного возраста [5]. На долю хронического бактериального простатита приходится 5—15% случаев заболевания [6]. Одной из причин, способствующих увеличению частоты развития воспалительных процессов в органах малого таза и простате, являются урогенитальные передающиеся половым путем инфекции, вызываемые хламидиями, трихомонадами, микоплазмой и др. Это связано как с изменением полового поведения в обществе, так и с появляющейся резистентностью возбудителя к лекарственным препаратам [7, 8]. Кроме того, противомикробные препараты плохо проникают в простату и концентрация их в железе значительно ниже, чем в сыворотке крови [1, 9].
Урогенитальный хламидиоз относится к наиболее распространенным болезням мочеполовой системы мужчин [2]. Течение хронического хламидийного простатита (ХХП), как и простатитов, вызванных другими инфекционными агентами, не бывает монотонным с одинаковой интенсивностью клинических проявлений. Как правило, этому заболеванию свойственны периодические обострения с заметным усилением субъективных и объективных расстройств, сменяющихся периодом затишья. При ХХП развиваются значительные изменения иммунологических показателей, формируется вторичный иммунодефицит, который проявляется дисфункцией системного и местного иммунитета. Рациональное применение иммуностимулирующей терапии в комплексе с антибиотиками и местным медикаментозным лечением по сравнению с моноантибиотикотерапией способствует не только этиотропному излечению ХХП, но и более полной реабилитации больных [3, 7, 10].
Метод иммунокоррекции с использованием иммуномодулятора циклоферона был использован нами как дополнение к комплексной терапии хронического урогенитального хламидиоза. Нами исследована клиническая и иммунологическая эффективность циклоферона при ХХП.
Материал и методы
Исследование проведено у 50 пациентов с хроническим простатитом, у которых методами полимеразной цепной реакции (ПИФ) и прямой иммунофлюоресценции (ПЦР) с праймерами на основе плазмиды C. trachomatis был обнаружен хламидиоз. Материалом для диагностики служили осадок первой порции мочи, секрет простаты, эякулят. Основным критерием инфекционного процесса было выявление в 3-й порции мочи посkt массажf, секрете простаты патогенной микрофлоры (хламидий, трихомонад и др.) или условно-патогенной в концентрации 1·10 4 микробных тел/мл и выше. Средний возраст больных мужчин составил 36,05±0,8 года, средний возраст здоровых — 29,8±0,8 года. Больные ХХП получали комплексную терапию: антибактериальный препарат офлоксин в дозе 400 мг 2 раза в сутки в течение 15 дней, индуктор интерферонов циклоферон, который вводили в виде раствора (125 мг/мл) для внутримышечных инъекций в дозе 2 мл по традиционной схеме, на курс 10 инъекций, кроме того осуществляли коррекцию микроциркуляции и воспаления посредством противовоспалительных препаратов (свечи дикловит, найз), ферментативных препаратов (лонгидаза), α-адреноблокаторов (зоксон по 2 мг ежедневно); одновременно назначали физиотерапию в виде низкоинтенсивного инфракрасного лазерного излучения и магнитотерапию на область промежности (аппарат Интрамаг, Мустанг), массажи простаты, инстилляции в уретру проторгола.
У всех пациентов исследовали состояния местного и системного иммунитета до лечения и через 1 мес после окончания терапии. В периферической крови определяли уровень различных субпопуляций лимфоцитов, активность, интенсивность фагоцитоза, НСТ-тест, иммуноглобулины (Ig) классов А, М, G. В эякуляте больных ХХП определяли общее число лейкоцитов, процент жизнеспособных клеток, лизосомальную активность нейтрофилов, активность фагоцитоза, НСТ-тест.
Контрольную группу составили 50 здоровых мужчин без урогенитальной патологии и урогенитальных инфекций.
Всем пациентам проводили трансабдоминальное ультразвуковое исследование (УЗИ) для определения количество остаточной мочи. Всех пациентов подвергали трансректальному УЗИ простаты.
Эффективность метода лечения подтверждали результатами ПИФ и ПЦР, свидетельствующих об эрадикации хламидий из организма человека. Контроль излеченности проводили через 2 мес после окончания лечения.
Результаты и обсуждение
Эффективность терапии оценивали по этиологическому и клиническому выздоровлению больных (купирование болевого синдрома, дизурии, восстановление половой функции, исчезновению психосоматических расстройств), нормализации клинико-лабораторных показателей. Жалобы сопоставляли до лечения и через 2 мес после окончания терапии.
На основании жалоб, данных анамнеза и результатов лабораторных исследований, хронический катаральный (поверхностный) простатит был диагностирован у 12 (24%) больных, фолликулярная форма — у 28 (56%), паренхиматозный простатит — у 10 (20%).
При исследовании секрета простаты у всех пациентов был выявлен лейкоцитоз, умеренное количество липоидных зерен — у 23 (46%) и небольшое количество — у 27 (54%); кроме того, было характерно наличие слизи, слущенного эпителия, флоры.
Наиболее частыми симптомами у наблюдаемых больных хроническим простатитом были боль (в промежности, над лобком, в паховой области, в области заднего прохода, в пояснице, по внутренней поверхности бедер, в половом члене, в яичках) у 90% больных, дизурические явления — у 31 (62%).
Остаточная моча после акта мочеиспускания отсутствовала или определялась в минимальном количестве (до 10 мл) у 24 (48%), 11—50 мл — у 21 (42%), 51—100 мл у 5 (10%) больных хроническим простатитом. У больных, отмечавших чувство неполного опорожнения мочевого пузыря после акта мочеиспускания, среднее количество остаточной мочи составило 40,1±4,84 мл, а у больных без этого ощущения —11,03±1,41 мл.
Трансректальное УЗИ позволило выявить гиперэхогенные изменения в структуре железы у 88% больных, микрокальцинаты — у 14%. Наиболее характерными находками на эхограммах больных хроническим простатитом были участки чередования мелких зон повышенной эхогенности (участки фиброза, клеточной инфильтрации) и пониженной плотности (зоны воспалительного отека, инфильтрации и ретенционных кист).
У больных, получавших комплексную терапию с использованием циклоферона, через 2 мес после лечения наблюдалось значительное улучшение состояния: исчезали болевые ощущения, императивные позывы на мочеиспускание и позывы на мочеиспускание в предутренние часы, остальные симптомы дизурии значительно ослабели (табл. 1, 2). 
После лечения циклофероном только у 2 (4%) пациентов сохранялись боли при эрекции, боль во время эякуляции перестала беспокоить после лечения всех пациентов с данными жалобами. Ослабление эрекции в группе больных, получавших циклоферон, сохранялось у 6 (12%) мужчин.
Через 1 мес после комплексного лечения ХХП с применением циклоферона гипоэхогенные образования в простате сохранялись лишь у 4 (8%) больных. Расширение перипростатических вен наблюдалось у 3 (6%) мужчин, получавших циклоферон.
После лечения у пациентов жалобы на неполное опорожнение мочевого пузыря отсутствовали. При УЗИ остаточная моча не определялась у всех пациентов.
Результаты анализа проведенных исследований указывают на высокую эффективность комплексной терапии ХХП с применением циклоферона.
Анализ результатов ПЦР и ПИФ, выполненный через 2 мес, позволил выявить, что при применении комплексной терапии с циклофероном элиминация возбудителя в группе больных ХХП наблюдалась в 49 (98%) случаях, в то время как эффективность традиционных схем лечения ХХП колеблется от 85 до 90%.
Важно отметить, что состояние больного, получавшего циклоферон, в терапии которого не удалось добиться полной элиминации возбудителя, оценивалось как стабильное, связанное с персистенцией хламидий. Жалобы и клинические проявления у данного больного отсутствовали.
Нами была произведена оценка показателей системного и местного иммунитета у мужчин с ХХП и иммунологической эффективности терапии циклофероном.
У больных с ХХП по сравнению с группой здоровых мужчин в эякуляте отмечалось повышенное содержание лейкоцитов, увеличение процента жизнеспособных лейкоцитов и активности лизосом, а также повышение НСТ-спонтанной и НСТ-индуцированной активности нейтрофилов. Необходимо отметить, что при этом снижались функциональный резерв нейтрофилов, активность и интенсивность фагоцитоза, процентное содержание нейтрофилов в эякуляте больных ХХП.
После лечения у пациентов, получавших терапию циклофероном, наблюдалось уменьшение количества лейкоцитов, нейтрофилов, снижалась активность лизосом нейтрофилов, НСТ-спонтанная и НСТ-индуцированная активность нейтрофилов, а также процент жизнеспособных лейкоцитов. После лечения пациентов, получавших терапию циклофероном, наблюдалось также увеличение процента содержания нейтрофилов, активности и интенсивности фагоцитоза нейтрофилов и функционального резерва нейтрофилов (табл. 3).
В периферической крови у пациентов с ХХП по сравнению с группой здоровых доноров снижалось содержание лейкоцитов, лимфоцитов, увеличивалось содержание моноцитов при неизменном уровне эозинофилов в периферической крови. Отмечались также изменения в показателях субпопуляций лимфоцитов: понижалось содержание лимфоцитов CD3+, CD4+, регистрировалось уменьшение соотношения CD4+/CD8+. Увеличивалось содержание Ig классов А, М, G, а также циркулирующие иммунные комплексы (ЦИК) у больных ХХП. По сравнению с группой здоровых доноров у больных этой группы увеличивалась НСТ-спонтанная и НСТ-индуцированная активность нейтрофилов при снижении их функционального резерва, а также отмечалось снижение активности и интенсивности фагоцитоза в периферической крови.
Оценка системного иммунитета пациентов, получавших циклоферон, показала, что препарат способствовал увеличению количества лейкоцитов в периферической крови, повышению содержания лимфоцитов, увеличению функционального резерва нейтрофилов за счет снижения спонтанной активности нейтрофилов в НСТ-тесте, повышению активности фагоцитоза (табл. 4).
После лечения с использованием циклоферона в периферической крови пациентов отмечалось, по сравнению с группой больных возрастание лимфоцитов CD3+, СD4+, а также существенное возрастание соотношения CD4+/CD8+ (табл. 5).
Колебания уровней иммуноглобулинов и ЦИК после лечения циклофероном отражены в табл. 6. 
Выводы
Эффективность комплексного лечения больных ХХП с использованием циклоферона доказана не только клиническим выздоровлением, но и высоким процентом элиминации возбудителя из мочеполового тракта, а также улучшением показателей местного и системного иммунитета. Результаты анализа данных показывают, что циклоферон воздействует на большинство звеньев иммунитета. Представленные материалы подтверждают высокую эффективность циклоферона и необходимость применения этого иммунотропного препарата при лечении больных ХХП.

.gif)





