Холестаз печени что это и как лечить
Холестатические заболевания печени
Термином «холестаз» обозначают патологии, сопровождающиеся нарушением образования или выведения желчи. Проблема может возникнуть в любой части печени и протекать с разной степенью тяжести.
Холестатические заболевания делятся на два типа:
В результате возникает застой желчи либо полностью прекращается ее отток. Это агрессивная жидкость, предназначенная для пищеварения. Основные факторы, приводящие к холестазу:
Проявления холестатических заболеваний схожи, поскольку в их основе лежит один и тот же патологический механизм. Элементы желчи, находясь внутри печени, создают давление на стенки сосудов, распирая орган. Из-за сильного воздействия они начинают впитываться в кровь. В связи с этим наблюдаются следующие клинические симптомы: кожный зуд, желтуха, потемнение мочи, осветление кала.
При длительном течении заболевания из-за нехватки желчи в процессе пищеварения нарушаются расщепление и всасывание жирорастворимых веществ, в первую очередь витаминов. Это приводит к нарушению сумеречного зрения, размягчению костей, слабости мышц, появлению кровоподтеков на коже и слизистых. Образуются ксантомы — плоские и мягкие желтоватые образования на лице, руках, груди, спине. Они являются показателем нарушения обмена жиров.
Диагностика холестатических заболеваний печени складывается из опроса и осмотра пациента, лабораторных и инструментальных обследований. К основным методам диагностики относятся:
В отдельных случаях показана биопсия.
Лечение холестаза направлено на устранение причины, снятие симптомов заболевания, облегчение жизни больного.
К сожалению, не всегда удается воздействовать на факторы, вызвавшие проблему. Если при закупорке желчных протоков проводят оперативное вмешательство, в случае вирусного гепатита назначаются противовирусные препараты, то цирроз печени не имеет обратного развития.
С целью снижения уровня желчных кислот в крови прописываются препараты урсодезоксихолевой кислоты, сорбенты.
Важную роль играет питание. Рекомендации по диете при холестазе:
Получить помощь в диагностике, лечении и подборе диеты можно у специалистов нашей клиники.
Холестатические заболевания печени: алгоритмы диагностики и лечения
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
За последнее десятилетие достигнут существенный прогресс в понимании молекулярных основ образования желчи и патофизиологии холестаза. В этом обзоре кратко обобщены современные концепции образования желчи и возникновения холестаза. Определены цели медикаментозной терапии холестаза, которые помогают понять существующие методы лечения и способствуют разработке новых лекарственных препаратов от холестатических заболеваний печени (ХЗП). Лечение ХЗП проиллюстрировано на примере наиболее часто встречающегося хронического ХЗП — первичного билиарного холангита.
Ключевые слова: желчь, холестаз, холестатические заболевания печени, первичный билиарный холангит, урсодезоксихолевая кислота.
Для цитирования: Полунина Т.Е. Холестатические заболевания печени: алгоритмы диагностики и лечения. РМЖ. 2021;6:81-87.
Cholestatic liver diseases: diagnostic and treatment algorithms
A.I. Yevdokimov Moscow State University of Medicine and Dentistry, Moscow
Over the past decade, significant progress has been made in understanding the molecular basis of bilification and the cholestasis pathophysiology. The article presents the goals of cholestasis therapy, which help to understand existing treatment methods and contribute to the development of new drugs for cholestatic liver diseases (CLD). This article also briefly summarizes the current concepts of bilification and cholestasis occurrence. Treatment of CLD is illustrated by the example of the most common chronic cholestatic liver disease — primary biliary cholangitis.
Keywords: bile, cholestasis, cholestatic liver diseases, primary biliary cholangitis, ursodeoxycholic acid.
For citation: Polunina T.E. Cholestatic liver diseases: diagnostic and treatment algorithms. RMJ. 2021;6:81–87 (in Russ.).
Введение
Холестатические заболевания печени (ХЗП) начинают развиваться на фоне поражения билиарных протоков, вызванного нарушением оттока желчи [1–3]. Повреждение клеток желчных протоков (холангиоцитов) приводит к задержке желчных кислот (ЖК), билирубина и других холефилов в печени и крови и дефициту ЖК в кишечнике. Клинические признаки ХЗП проявляются в широком диапазоне: от отдельных нарушений биохимических показателей функции печени до острой печеночной недостаточности или злокачественных образований в гепатобилиарной системе (например, холангиокарциномы). Длительно сохраняющийся холестаз (в течение нескольких месяцев или лет) может привести к развитию цирроза печени [4]. К наиболее распространенным и изученным ХЗП относят первичный билиарный холангит и первичный склерозирующий холангит [2].
Холестатические заболевания печени включают прогрессирующие холангиопатии, которые могут переходить в терминальную стадию заболевания печени. В США с 1988 по 2018 г. на ХЗП приходилось 14,2% всех трансплантаций печени [2]. Высокая заболеваемость и смертность превратились в большую проблему из-за отсутствия эффективных методов лечения. Более того, от 10% до 40% пациентов после трансплантации печени переживают рецидив основного заболевания [5].
Общие патогенные механизмы ХЗП
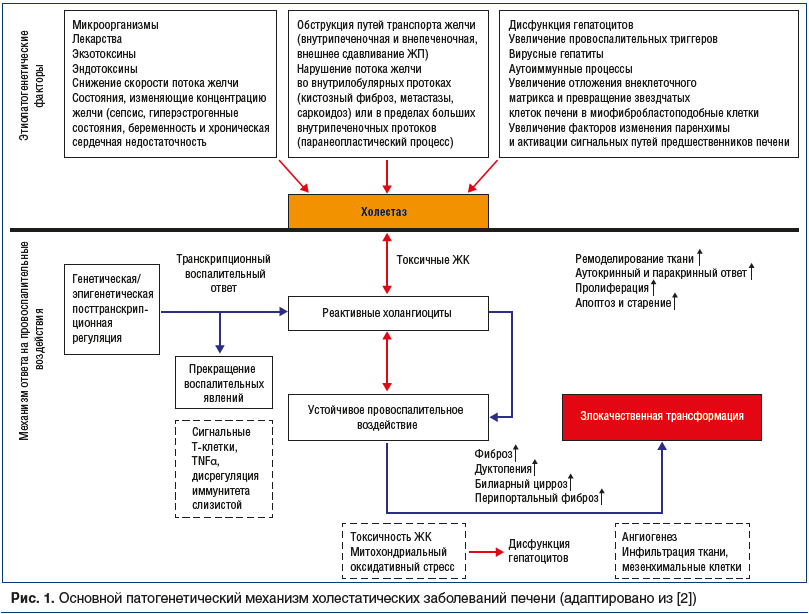
Нарушение оттока желчи может быть обусловлено несколькими факторами (рис. 1), основные из них — антигенные стимулы, экзотоксины, эндотоксины, ксенобиотики и микроорганизмы. Эти внешние факторы вызывают воспалительную реакцию холангиоцитов, которая перерастает в холестатическое состояние [6]. Обструкция транспорта желчи — еще один предрасполагающий фактор. Внутрипеченочная и внепеченочная обструкция может иметь место из-за внешнего доброкачественного сдавления (кистозные заболевания), эффекта злокачественной опухоли (холангиокарциномы), а также вследствие образования или миграции желчных конкрементов по билиарному тракту. Условия, которые замедляют отток желчи, способствуют холестатическому состоянию с повышенной концентрацией ЖК. Сепсис, гиперэстрогенные состояния (беременность), хроническая сердечная недостаточность и дисфункция генов — транспортеров ЖК могут изменять основные характеристики желчи, активируя более цитотоксический компонент ЖК.
Первичная защитная реакция холангиоцитов позволяет купировать повреждение. Однако устойчивое нарушение провоспалительных генетических и/или эпигенетических регуляторных механизмов может вызвать постоянное дисфункциональное расстройство, что в конечном итоге приведет к фиброгенному состоянию с билиарным и перипортальным фиброзом, потерей гомеостаза тканей и аутокринным и паракринным ремоделированием. Пролиферация может вызвать изменение клеточного цикла, старение, апоптоз, дуктопению, мезенхимальную инфильтрацию, а иногда и злокачественную трансформацию.
В настоящее время выделяют несколько концепций возникновения холестаза.
Дуктулярная (канальцевая) реакция — первая основная концепция холестаза. Внутрипеченочные и внепеченочные желчные протоки разного размера выстланы холангиоцитами, которые регулируют и изменяют объем и состав желчи. Они различаются по размеру, скорости метаболизма, а также способности к пролиферации и пластичности. Дуктулярная реакция является частью реакции клеток печени на повреждения при ХЗП [7]. Ответная реакция холангиоцитов на воспаление может привести к уменьшению повреждения, а в случае устойчивого воспалительного воздействия приводит к фиброзу желчных протоков [8].
Цитотоксичность ЖК и митохондриальная дисфункция — вторая фундаментальная основа патогенеза ХЗП, описанная в нескольких исследованиях при внепеченочном холестазе [9].
Влияние иммуногенетических и эпигенетических факторов на иммуновоспалительный ответ — это третий фундаментальный аспект патогенеза ХЗП. У пациентов с ХЗП имеется множество генетических изменений, которые объясняют различные элементы каждого ХЗП. Однако некоторые из этих генов могут быть непосредственно вовлечены в прогрессирование холестатического фенотипа. Следовательно, они могут стать потенциальной мишенью для новых терапевтических средств либо их активаторы транскрипции косвенно могут служить модулирующими мишенями. Эта модуляция представляет собой тип эпигенетического контроля экспрессии генов как патогенного механизма холестаза [2].
Клинический спектр ХЗП [2]:
Идиопатические: первичный билиарный холангит, первичный склерозирующий холангит, аутоиммунный холангит, IgG4-ассоциированный холангит, идиопатическая дуктопения, билиарная атрезия.
Вторичный склерозирующий холангит: холедохолитиаз, лекарственный (токсический) холангит, портально-гипертензивная билиопатия, ВИЧ-ассоциированный холангит, абдоминальная травма, дефицит АВСВ4, ятрогенные билиарные стриктуры, васкулярный/ишемический холангит, серповидно-клеточная болезнь, рецидивирующий пиогенный холангит.
Генетические: муковисцидоз, синдром Кароли, синдром Алажилля, аутосомно-доминантная поликистозная болезнь почек, аутосомно-рецессивная поликистозная болезнь почек, аутосомно-доминантный поликистоз печени, холестаз при беременности.
Дисфункциональные перестройки матрикса и фиброгенез — четвертая концепция патогенеза ХЗП. Фиброгенез — это сложный динамический процесс, связанный с взаимодействием иммуновоспалительных механизмов, изменением секреции тканевых металлопротеиназ, цитокиновых сетей и нарушением инфильтрации мезенхимальных клеток с окончательной потерей поддерживающего гомеостаза тканей. Фиброгенные процессы затрагивают поврежденные и неповрежденные желчные протоки, а также перипортальную синусоидальную систему, что приводит к прогрессирующему холестазу [10].
Диагностика
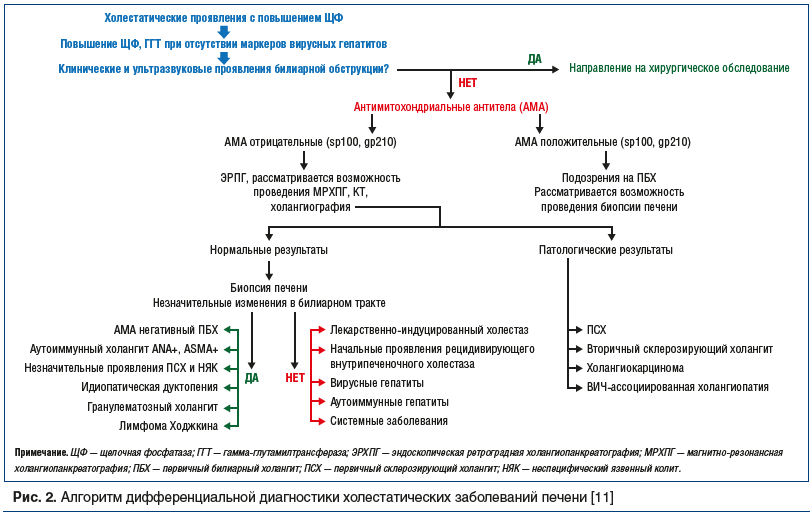
Различить виды холестаза по клиническим симптомам и биохимическим показателям не всегда удается. Чрезвычайно важным является разграничение вне- и внутрипеченочного холестаза с использованием диагностического алгоритма (рис. 2) [11].
Клиническая картина ХЗП различна. У многих пациентов холестаз протекает бессимптомно и диагностируется при оценке стойких холестатических лабораторных аномалий. У пациентов с симптомами могут наблюдаться дискомфорт в правом верхнем квадранте, зуд, усталость и потеря веса.
Первичный билиарный холангит (ПБХ) является аутоиммунным заболеванием и представляет собой наиболее распространенное хроническое ХЗП. Его прежнее название — «первичный билиарный цирроз». Однако от этого термина отказались в пользу «первичного билиарного холангита», поскольку у большинства пациентов нет цирроза. ПБХ возникает под воздействием сочетания генетических факторов и факторов окружающей среды, которые запускают опосредованное Т-лимфоцитами разрушение внутрипеченочных желчных протоков. Большинство (90%) заболевших — женщины, и обычно это заболевание диагностируется в возрасте от 40 до 60 лет. Сопутствующие аутоиммунные заболевания часто встречаются у пациентов с ПБХ, включая синдром Шегрена, заболевания щитовидной железы, ограниченную кожную склеродермию и ревматоидный артрит [12].
Приблизительно 60% пациентов с ПБХ не имеют симптомов на момент постановки диагноза. Обычно диагноз ставится на основании отклонений от нормы биохимических тестов печени. Утомляемость и зуд являются наиболее частыми симптомами у пациентов с ПБХ. Физикальное обследование может выявить гепатомегалию, гиперпигментацию кожи, желтуху, ксантомы или стигматы цирроза и портальной гипертензии на более поздних стадиях. Характерные лабораторные отклонения включают повышение щелочной фосфатазы (ЩФ) с нормальным или умеренным повышением аминотрансфераз в сыворотке крови. Повышение уровня билирубина в сыворотке обычно происходит при прогрессировании заболевания и является плохим прогностическим признаком.
При ПБХ часто встречаются нарушения липидов. Небольшое повышение липопротеинов низкой плотности (ЛПНП) с более выраженным повышением липопротеинов высокой плотности (ЛПВП) часто встречается на ранних стадиях ПБХ, тогда как более заметное повышение ЛПНП и более низкие уровни ЛПВП отмечаются на более поздних стадиях заболевания. ПБХ также может быть связан с метаболическим заболеванием костей, стеатореей и дефицитом жирорастворимых витаминов.
Антимитохондриальные антитела (АМА) — это специфические антитела, которые считаются серологическим признаком ПБХ и присутствуют у 95% пациентов с этим заболеванием. Следовательно, положительный результат теста на АМА в контексте повышения холестатической пробы печени достаточен для установления диагноза ПБХ.
Первичный склерозирующий холангит (ПСХ) — это хроническое ХЗП, характеризующееся воспалением и фиброзом внутри- и внепеченочных желчных протоков. Холангит может быть диагностирован на более поздней стадии болезни, вторичной по отношению к обструкции из-за стриктур. Повышение уровня ЩФ в сыворотке крови является наиболее частым лабораторным отклонением у пациентов с ПСХ. Примерно 50% пациентов с ПСХ могут иметь нормальные показатели ЩФ. Следовательно, нормальные значения ЩФ не исключают диагноз ПСХ. Уровень аминотрансфераз в сыворотке может быть в 2–3 раза выше верхней границы нормы. В отличие от ПБХ, аутоантитела в сыворотке неспецифичны и обычно не используются для постановки диагноза ПСХ. Диагноз ПСХ, связанного с патологией большого протока, устанавливается на основании холангиограммы, и отсутствие патологии при УЗИ брюшной полости не исключает ПСХ. Следовательно, при подозрении на ПСХ предпочтительным диагностическим тестом является магнитно-резонансная холангиопанкреатография. По сравнению с эндоскопической ретроградной холангиопанкреатографией это неинвазивный и точный метод обнаружения ПСХ. Пациенты с ПСХ в малом протоке имеют нормальные холангиограммы и требуют биопсии печени для установления диагноза ПСХ.
Вторичный склерозирующий холангит (ВСХ) — это хроническое ХЗП, которое приводит к прогрессирующему фиброзу печени, нерегулярному уплотнению и расширению желчных протоков. Холангиографическая картина ВСХ аналогична таковой при ПСХ. К наиболее частым обструктивным причинам ВСХ относятся: хирургические травмы, вызванные холецистэктомией, внутрипротоковые камни, рецидивирующий панкреатит и стриктуры желчных путей. Застой в желчевыводящих путях, вызванный обструкцией, предрасполагает к рецидиву холангита и образованию пигментных камней и воспалительных стриктур, которые затем усугубляют холестаз. Ранние изменения, наступившие после обструкции желчных путей, могут регрессировать при ее лечении. Однако со временем такие изменения могут развиться в необратимый обширный перипортальный и перидуктулярный фиброз и вторичный билиарный цирроз.
По клинической картине и лабораторному профилю ВСХ и ПСХ очень похожи. Рецидивирующий бактериальный холангит очень часто встречается на поздних стадиях ВСХ.
В редких случаях биопсия печени требуется для установления диагноза ПБХ, когда проба на АМА отрицательна или когда требуется более точная дифференциальная диагностика с аутоиммунным гепатитом, лекарственным холестазом, рецидивирующим внутрипеченочным холестазом, вирусными гепатитами, системными заболеваниями.
Перспективы проведения биопсии печени зависят от поражений мелких желчных протоков при: ПСХ, идиопатической дуктопении, гранулематозном холангите, лимфоме Ходжкина.
Лечение ХЗП
Распространенным следствием всех форм холестаза является задержка ЖК в гепатоцитах. Повышенный уровень ЖК приводит к апоптозу или некрозу гепатоцитов и в конечном итоге к хроническому ХЗП [13]. При некоторых холестатических расстройствах также происходит проникновение ЖК в перибилиарное пространство, что вызывает воспаление воротной вены и фиброз за счет индукции хемокинов и цитокинов.
В связи с этим выделяют следующие фармакологические мишени для лечения внутрипеченочного холестаза (рис. 3) [13]:
стимуляция ортоградной секреции желчных путей и ретроградной секреции ЖК и других токсичных холефилов в системный кровоток для выведения почками;
стимуляция метаболизма гидрофобных ЖК и других токсичных соединений до более гидрофильных, но менее токсичных метаболитов;
защита пораженных холангиоцитов от токсического действия желчи; ингибирование апоптоза, вызванного повышенным уровнем цитотоксических ЖК;
ингибиция фиброза, вызванного утечкой ЖК в перибилиарное пространство.
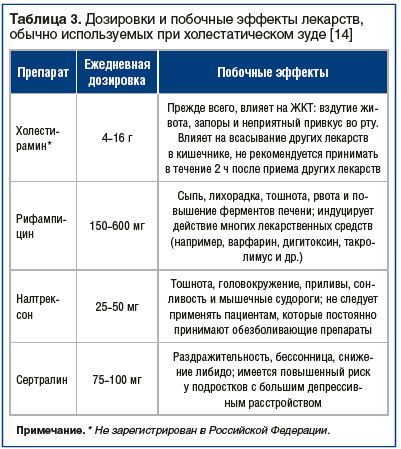
Медикаментозная терапия ХЗП представлена в табл. 1. В табл. 2 и 3 представлены основные симптомы, возникающие при ХЗП, и лекарственные препараты для их купирования.
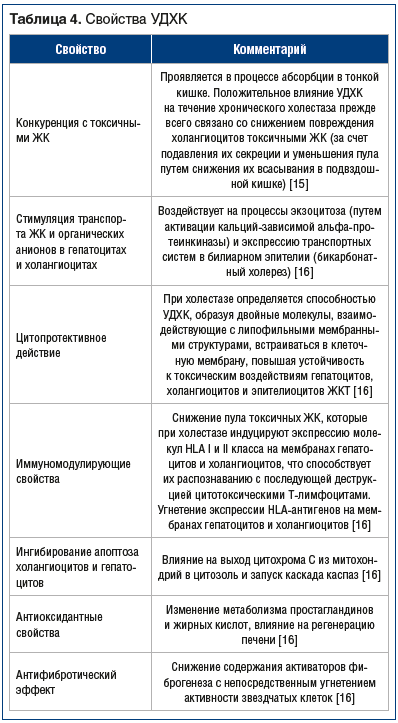
Единственным общепринятым препаратом для медикаментозного лечения большинства хронических ХЗП является урсодезоксихолевая кислота (УДХК) [12, 15–19]. Способность лечить холестаз считается одним из важнейших и наиболее ценным свойством этого лекарственного средства. В табл. 4 представлены основные свойства УДХК, которые, по мнению автора, наиболее полно раскрыты в статьях [15, 16].
Наиболее убедительно доказано положительное действие УДХК при таком холестатическом заболевании, как ПБХ. В комбинированном анализе французских, канадских и североамериканских когорт больных при 2–4-летнем наблюдении отмечено снижение смертности и необходимости трансплантации печени в группах с умеренным и тяжелым течением заболевания. «Барселонское» исследование 192 пациентов, получавших УДХК сроком от 1,5 года до 14 лет, показало, что выживаемость у пациентов, ответивших на терапию УДХК (ответ оценивался по уровню снижения ЩФ), была выше предсказанной по прогностической модели Мейо и соответствовала популяционной [16].
Доза УДХК 13–15 мг/кг/сут при большинстве холестатических заболеваний имеет преимущество по биохимическому ответу и стоимости в сравнении с низкими и высокими дозами. Исключением является муковисцидоз, где рекомендуются дозы 20–30 мг/кг/сут [16]. При ПСХ рекомендуемые дозы не определены.
Имеются данные о положительном влиянии УДХК на лекарственный холестаз, в том числе обусловленный одним из наиболее часто вызывающих гепатотоксичность препаратов — амоксициллином/клавуланатом [16].
Европейская ассоциация по изучению болезней печени (European Association for the Study of the Liver, 2009) [20] и Российская гастроэнтерологическая ассоциация [1] рекомендуют обязательное назначение УДХК в качестве базисной терапии при ряде ХЗП: первичном билиарном циррозе, ПСХ, муковисцидозе, прогрессирующем семейном холестазе 3 типа (Progressive Familial Intrahepatic Cholestasis 3), внутрипеченочном холестазе беременных, а также обсуждают ее назначение при лекарственном холестазе и доброкачественном семейном холестазе.
Концепция структурированной пожизненной терапии ПБХ опирается на 3 основных элемента: 1) стратификацию риска и соответствие ему терапии; 2) определение стадии и наблюдение в соответствии с ней; 3) активное ведение. Помощь всегда строится с учетом индивидуальных особенностей больного и возможностей здравоохранения данной страны, но ее эффективность обеспечивают эти 3 опорных элемента [21].
На сегодня оригинальный препарат УДХК — Урсо (Япония) в России не зарегистрирован. В этой ситуации при выборе дженерических препаратов, широко представленных на отечественном фармацевтическом рынке, следует руководствоваться, прежде всего, соотношением цены и качества. Появившийся в последние годы отечественный препарат УДХК Урдокса ® производства АО «ФП «Оболенское» не уступает ранее зарегистрированным в нашей стране дженерическим формам [16]. Этот отечественный лекарственный препарат обладает характеристиками, позволяющими считать его препаратом выбора на любом этапе медицинской помощи больным с широким спектром нозологий, в том числе при хронических ХЗП. Урдокса ® производится из европейской субстанции (Италия, Industria Chimica Emiliana) на российском предприятии по международному стандарту GMP (Good Manufacturing Practice — Надлежащая производственная практика). Высокий профиль безопасности позволяет применять препарат у детей старше 3 лет [22].
Препарат успешно прошел все предусмотренные законодательством регистрационные процедуры, что позволяет говорить о его биоэквивалентности референтным препаратам, содержащим УДХК [23, 24].
Подтверждением фармацевтической эквивалентности препаратов УДХК является не только одинаковое количество активного вещества и вспомогательных веществ в 1 капсуле препарата, но и наличие идентичных инфракрасных спектров, полученных при инфракрасной спектроскопии готовых лекарственных форм сравниваемых препаратов УДХК [25–27].
Надежность динамики стандартных биохимических показателей функции печени на фоне терапии — простого и информативного диагностического инструмента подтверждена последними 10 годами его широкого использования. Ответ на УДХК-терапию поддается оценке по модели дискретных бинарных переменных или балльных оценочных систем на основе расчета непрерывных переменных [21]. Так, согласно Парижским критериям хорошим биохимическим ответом через 12 мес. терапии УДХК считается уровень сывороточного билирубина ≤17 мкмоль/л (1 мг/дл), уровень ЩФ ≤3 верхней границы нормы и уровень аспартат-аминотрансферазы ≤2 верхней границы нормы.
Заключение
Таким образом, холестаз является очень частым явлением и может встречаться в различных клинических условиях. Понимание особенностей этиопатогенеза холестаза и правильное применение этих особенностей в дифференциальной диагностике и лечении ХЗП способствуют формированию эффективного практического подхода в терапии холестаза общей этиологии. В настоящее время УДХК является препаратом выбора для лечения ХЗП, поскольку она обеспечивает облегчение симптомов, улучшает биохимические и гистологические показатели функции печени, а также, что наиболее важно, увеличивает выживаемость пациентов с ХЗП [16]. Положительные эффекты УДХК были документально подтверждены рандомизированными контролируемыми исследованиями. Терапия с применением препаратов УДХК является определяющей при ряде холестатических расстройств, таких как ПБХ, ПСХ, внутрипеченочный холестаз беременных, заболевания печени при муковисцидозе, прогрессирующий семейный внутрипеченочный холестаз и некоторые формы лекарственного холестаза.
Редакция благодарит АО «Алиум» за оказанную помощь в технической редактуре настоящей публикации.
Только для зарегистрированных пользователей
Синдром холестаза
Застой компонентов желчи в ткани печени принято называть холестазом.
Различают внутри и внепеченочный холестаз. При внутрипеченочном холестазе выделяют внутриклеточную, внутриканальцевую и смешанную формы:
Внепеченочный холестаз развивается при внепеченочной обструкции желчных протоков.
Внутрипеченочный холестаз возникает при отсутствии обструкции магистральных желчных протоков. Он может развиваться на уровне гепатоцитов или внутрипеченочных желчных протоков. Соответственно выделяют холестаз, обусловленный поражением гепатоцитов, каналикул, дуктул или смешанный. Кроме того, различают острый и хронический холестаз, а также желтушную и безжелтушную его формы.
Существует несколько форм холестаза: парциальный харастеризуется уменьшением объема секретируемой желчи; диссоцианный связан с задержкой только отдельных компонентов желчи (на ранних стадиях первичного недеструктивного холангита в сыворотке крови повышается содержание только желчных кислот и активности щелочной фосфатазы, в то время как уровень билирубина, холестерина, фосфолипидов остается в норме); тотальный связан с нарушением поступления желчи в двенадцатиперстную кишку.
Желчь представляет собой жидкость, изоосимчную плазме, состоящую из воды, электролитов, органических веществ (желчных кислот и солей, холестерина, конъюгированного билирубина, цитокинов, эикозаноидов и других веществ) и тяжелых металлов.
За сутки осуществляется синтез и отток от печени около 600 мл желчи Гепатоциты ответственны за секрецию двух фракций желчи зависящей от желчных кислот (около 225 мл/сут) и не зависящей от желчных кислот (около 225 мл/сут) Клетками желчных протоков секретируется 150 мл/сут желчи.
Желчь вырабатывается гепатоцитами и дренируется через сложную систему желчных ходов, расположенных внутри печени. Эта система включает желчные канальцы, желчные протоки и междольковые протоки. Желчные канальцы расположены между гепатоцитами, которые образуют их стенки. Диаметр канальцев 12 мкм (он меньше в третьей и постепенно увеличивается по направлению к первой зоне ацинуса) прилежащих межклеточных пространств канальцы отделены соединительными комплексами соседних гепатоцитов. Из желчных канальцев желчь поступает в желчные протоки (холангиолы или промежуточные канальцы Геринга), имеющие базальную мембрану. Канальцы Геринга устелены эпителием и гепатоцитами. Холангиолы образуют начало желчных ходов. Через пограничную пластинку холангиолы входят в портальные тракты, где приобретают строение междольковых протоков, наиболее мелкие ветви которых имеют диаметр 15-20 мкм. Междольковые протоки выстланы кубическим эпителием, лежащим на базальной мембране. Протоки анастомозируют между собой, увеличиваются в размерах и становятся крупными (септальными или трабекулярными) диаметром до 100 мкм, выстланными высокими призматическими эпителиоцитами с базально расположенными ядрами.
Два главных печеночных протока выходят из правой и левой долей в области ворот печени.
Гепатоцит представляет собой полярную секреторную эпителиальную клетку, имеющую базолатеральную (синусоидальную и латеральную) и апикальную (канальцевую) мембраны. Канальцевая мембрана содержит транспортные белки для желчных кислот, билирубина, катионов и анионов, микроворсинки. Органеллы представлены аппаратом Гольджи и лизосомами. С помощью везикул осуществляется транспорт белков (IgA) от синусоидальной к канальцевой мембране, доставка синтезирующихся в клетке транспортных белков для холестерина, фосфолипидов, желчных кислот. Цитоплазма гепатоцита вокруг канальцев содержит структуры цитоскелета: микротрубочки, микрофиламенты, промежуточные филаменты.
Образование желчи включает захват желчных кислот, других органических и неорганических ионов и их транспорт через синусоидальную мембрану. Этот процесс сопровождается осмотической фильтрацией воды, содержащейся в гепатоците и парацеллюлярном пространстве. Роль движущей силы секреции выполняет Na+,K+ATOa3a синусоидальной мембраны, обеспечивая химический градиент и разность потенциалов между гепатоцитами и окружающим пространством. В результате градиента концентрации натрия (высокая снаружи, низкая внутри) и калия (низкая снаружи, высокая внутри) содержимое клетки имеет отрицательный заряд по сравнению с внеклеточным пространством, что облегчает захват положительно заряженных и экскрецию отрицательно заряженных ионов. Транспортный белок для органических анионов является натрийнезависимым, переносит молекулы ряда соединений, включая желчные кислоты, бромсульфалеин и, вероятно, билирубин. На поверхности синусоидальной мембраны происходит также захват сульфатов, неэтерифицированных жирных кислот, органических катионов. Транспорт желчных кислот в гепатоците осуществляется с помощью цитозольных белков, среди которых основная роль принадлежит Загидроксистероиддегидрогеназе. Меньшее значение имеют белки, связывающие жирные кислоты, глутатион8трансфераза. В переносе желчных кислот участвуют эндоплазматический ретикулум и аппарат Гольджи. Транспорт белков жидкой фазы и лигандов (IgA, липопротеины низкой плотности) осуществляется посредством везикулярного транспорта. Время переноса от базолатеральной до канальцевой мембраны составляет около 10 мин.
Канальцевая мембрана представляет собой специализированный участок плазматической мембраны гепатоцита, содержащий транспортные белки, ответственные за перенос молекул в желчь против градиента концентрации. В канальцевой мембране локализуются ферменты: щелочная фосфатаза, углутамилтранспентидаза. Перенос желчных кислот осуществляется с помощью канальцевого транспорта белка для желчных кислот. Ток желчи, не зависящий от желчных кислот, определяется, повидимому, транспортом глугатиона, а также канальцевой секрецией бикарбоната, возможно, при участии белка. Вода и неорганические ионы (в особенности Na4) экскретируются в желчные капилляры по осмотическому градиенту путем диффузии через отрицательно заряженные полупроницаемые плотные контакты. Секреция желчи регулируется многими гормонами и вторичными мессенджерами, включая цАМФ и протеинкиназу. Эпителильные клетки дистальных протоков вырабатывают обогащенный секрет, модифицирующий состав канальцевой желчи,- к называемый дуктулярный ток желчи. Давление в желчных протоках, при котором происходит секреция желчи составляет 15-25 см вод. ст. Повышение давления до 35 см вод. ст. ведет к подавлению секреции желчи, развитию желтухи.
Что провоцирует / Причины Синдрома холестаза:
Этиология внутрипеченочного холестаза довольно многообразна.
В развитии холестаза важная роль отводится желчным кислотам, обладающим выраженными поверхностноактивными свойствами Желчные кислоты вызывают повреждение клеток печени и усиливают холестаз. Их токсичность зависит от степени липофильности (и, соответственно, гидрофобности). К гепатотоксичным желчным кислотам относят хенодезоксихолевую (первичную желчную кислоту), а также литохолевую и дезоксихолевую кислоты (вторичные кислоты, образующиеся в кишечнике из первичных под действием бактерий). Под влиянием желчных кислот наблюдается повреждение мембран митохондрий, что приводит к уменьшению синтеза АТФ, повышению внутриклеточной концентрации Са2+, стимуляции кальциизависимых гидролаз, повреждающих цитоскелет гепатоцита Желчные кислоты вызывают апоптоз гепатоцитов, аберрантную экспрессию антигенов HLA I класса на гепатоцитах и HLA II класса на эпителиальных клетках желчных протоков, которая может быть фактором развития аутоиммунных реакций против гепатоцитов и желчных протоков.
Синдром холестаза встречается при различных состояниях, которые могут быть объединены в 2 большие группы:
Нарушение образования желчи:
Нарушение тока желчи:
Гепатоцеллюлярный и каналикулярный холестаз могут быть обусловлены вирусным, алкогольным, лекарственным, токсическим поражением печени, застойной сердечной недостаточностью, эндогенными нарушениями (холестаз беременных). Экстралобулярный (дуктулярный) холестаз характерен для таких заболеваний, как цироз.
Симптомы Синдрома холестаза:
Клинические проявления. При холестазе избыточная концентрация компонентов желчи в печени и тканях организма вызывает печеночные и системные патологические процессы, обусловливающие соответствующие клинические и лабораторные проявления болезни.
В основе формирования клинических симптомов лежат 3 фактора:
Выраженность клинических симптомов внутрипеченочного холестаза зависит от основного заболевания, нарушения экскреторной функции гепатоцитов, печеночноклеточной недостаточности. Ведущими клиническими проявлениями холестаза (острого и хронического) являются кожный зуд, нарушение переваривания и всасывания. При хроническом холестазе наблюдаются поражение костей (печеночная остеодистрофия), отложения холестерина (ксантомы и ксантелазмы), пигментация кожи вследствие накопления меланина.
В отличие от гепатоцеллюлярного повреждения такие симптомы как слабость и утомляемость, для холестаза нехарактерны. Печень увеличена с гладким краем, уплотнена, безболезненна. Спленомегалия при отсутствии билиарного цирроза, портальной гипертензии встречается нечасто. Кал обесцвечен Предполагают, что кожный зуд при холестазе вызывают соединения, синтезирующиеся в печени и в норме экскретирующиеся в желчь. Имеется мнение о важной роли опиоидных пептидов в развитии зуда.
Маркерами хронического холестаза являются ксантомы, отражающие задержку липидов в организме (чаще располагаются вокруг глаз, на ладонных складках, под молочными железами, на шее, груди или спине). Образованию ксантом предшествует гиперхолестеринемия на протяжении 3 мес и более Ксантомы могут подвергаться обратному развитию при снижении уровня холестерина. Разновидностью ксантом являются ксантелазмы.
При холестазе наблюдается нарушение обмена меди, способствующее процессам коллагеногенеза. У здорового человека около 80 % всасываемой меди в кишечнике экскретируется с желчью и удаляется с калом
При холестазе медь накапливается в желчи в концентрациях, близких наблюдаемым при болезни ВильсонаКоновалова. В ряде случаев может обнаруживаться пигментное роговичное кольцо Кайзера-Флейа. Медь в ткани печени накапливается в гепатоцитах, холангиоцитах, клетках системы мононуклеарных фагоцитов. Локализация отложения избыточного содержания меди в клетках III или I зоны обусловлена этиологическими факторами. Кроме того, нами установлено, что избыточное отложение меди в клетках Купфера, в отличие от его накопления в паренхиматозных клетках, является прогностически неблагоприятным фактором в развитии избыточного фиброзирования в ткани печени, других органах и тканях.
У больных хроническим холестазом имеют место дегидратация, изменение деятельности сердечно-сосудистой системы. Нарушаются сосудистые реакции в ответ на артериальную гипотензию (вазоконстрикцию), наблюдаются повышенная кровоточивость, нарушение регенерации тканей, высокий риск развития сепсиса. Печеночная недостаточность присоединяется при длительности холестаза более 35 лет. В терминальной стадии развивается печеночная энцефалопатия. Длительный холестаз может осложняться образованием пигментных конкрементов в желчевыводящей системе, осложняющихся бактериальным холангитом. При формировании билиарного цирроза обнаруживаются признаки портальной гипертензии и печеночноклеточной недостаточности.
Диагностика Синдрома холестаза:
В периферической крови выявляются мишеневидные эритроциты, анемия, нейтрофильный лейкоцитоз. В течение 3 нед в сыворотке крови повышается содержание связанного билирубина. Биохимическими маркерами холестаза являются щелочная фосфатаза и углутамилтранспептидаза, лейцинаминопептидаза и 5нуклеотидаза. При хроническом холестазе повышается уровень липидов холестерина, фосфолипидов, триглицеридов, липопротеинов, в основном за счет фракции липопротеинов низкой плотности. В то же время концентрация липопротеинов высокой плотности снижена. В сыворотке повышено содержание хенодезоксихолевой, литохолевой и дезоксихолевой желчных кислот. Уровень альбуминов и глобулинов при остром холестазе не меняется. Активность АсАТ, АлАТ повышается незначительно. В моче обнаруживаются желчные пигменты, уробилин.
Морфологически печень при холестазе увеличена в размерах, зеленоватого цвета, с закругленным краем. На поздних стадиях на ее поверхности видны узлы. При световой микроскопии наблюдается 6илирубиностаз в гепатоцитах, клетках синусоидов, канальцах третьей зоны дольки. Выявляются «перистая» дистрофия гепатоцита, пенистые клетки, окруженные мононуклеарными клетками. Некроз гепатоцитов, регенерация и узловая гиперплазия на начальных этапах холестаза выражены минимально. В портальных трактах (первая зона) наблюдаются пролиферация дуктул, наличие желчных тромбов, гепатоциты превращаются в клетки желчных протоков и формируют 6азальную мембрану. Обструкции желчных протоков способствует развитие фиброза. При холестазе могут образовываться тельца Мэллори. Микроциркуляторное русло печени и ее клеточные элементы подвергаются реактивным изменениям. Наблюдается набухание клеток выстилки синусоидов, их дистрофические изменения, наличие вакуолей, содержащих компоненты желчи или их метаболиты. При электронной микроскопии изменения желчных канальцев неспецифичны и включают дилатацию, отек, утолщение и извитость, потерю микроворсинок, вакуолизацию аппарата Гольджи, гипертрофию эндоплазматического ретикулума. В печени (гепатоциты, клетки Купфера, эпителий желчных протоков) наблюдается избыточное отложение меди и металлопротеинов, липофусцина, холестерина, других липидов. Изменения в биоптате печени на ранних стадиях холестаза могут отсутствовать.
Выделяют следующие виды некроза при холестазе:
Желчные тромбы состоят из зернистых компонентов (собственно желчь) и кольцевиднопластинчатых образований свободного билирубина и имеют грубозернистую структуру, локализованную в мезосомах Связанный билирубин, имея форму мелких зерен, находится в пузырьках ЭПС, а иногда свободно лежит в цитоплазме.
Застой желчи в печени закономерно сопровождается пролиферацией холангиол (дуктулярная пролиферация). Пролиферирующие желчные ходы могут ничем не отличаться от обычных желчных протоков. Иногда пролиферирующие желчные протоки не имеют четкого просвета, образованы двумя рядами овальных клеток с вытянутым ядром и базофильной цитоплазмой. Значительное число протоков в портальном поле говорит об их пролиферации.
Пролиферация желчных ходов имеет приспособительнокомпенсаторное значение и направлена на коррекцию желчевыделения. При устранении причины застоя желчи дуктулярная реакция редуцируется, происходит полное восстановление портальной триады.
Лечение Синдрома холестаза:
Особенностью диеты при холестазе является ограничение количества нейтральных жиров до 40 г/сут, включение в питательный рацион растительных жиров, маргаринов, содержащих триглицериды со средней длиной цепи (их всасывание происходит без участия желчных кислот).
Разрушение цитоскелета гепатоцитов, нарушение везикулярного транспорта требует применения гептрала, антиоксидантов, рифампициа (300-400 мг/сут 12 нед), в основе действия которого лежит индукция микросомальных ферментов печени или ингибирование захвата лчных кислот. Рифампицин оказывает также влияние на состав кислотной микрофлоры, участвующей в метаболизме желчных кислот, являющийся также индуктором микросомальных фертов печени, применяют в дозе 50-150 мг/сут 12 нед.
В лечении кожного зуда доказана эффективность блокаторо-опиатных рецепторов ЦНС: налмефен по 580 мг/сут, налоксоц по 20 мг/сут в/в; блокаторов серотониновых рецепторов (ондансетрон 8 мг в/в). С целью связывания пруритогена в кишечнике используется холестирамин по 4 г до и после завтрака, 4 г после обеда и после ужина (12-16 г) от 1 мес до нескольких лет.
При симптомах остеопороза целесообразен прием витамина D3 по 50 000 ME 3 раза в неделюили 100 000 ME в/м 1 раз в месяц в сочетании с препаратами кальция до 1,5 г/сут (глюконат кальция, кальцевидный D3 никомед). При выраженных болях в костях назначают кальция глюконат в/в капельно 15 мг/кг в 500 мл 5 % раствор глюкозы или декстрозы ежедневно в течение недели. Больным показаны витамин А в дозе 100 000 ME 1 раз в месяц, витамин Е (токоферол) по 30 мг/сут в течение 10-20 дней. При геморрагических проявлениях назначается витамин К (викасол) по 10 мг 1 раз в сутки, курс лечения 5-10 дней, до ликвидации геморрагии, с последующим переходом на одну инъекцию. В ряде случаев больным показаны методы экстракорпоральной гемокоррекции: плазмаферез, лейкоцитаферез, криоплазмосорбция, ультрафиолетовое облучение крови.
Прогноз.Функция печени при синдроме холестаза долгое время остается сохранной. Печеночноклеточная недостаточностьразвивается довольно медленно (как правило, при длительности желтухи более 3 лет). В терминальной стадии развивается печеночная энцефалопатия.