Хондрогард с чем колоть в комплексе
Хондропротекторы в комплексной терапии болей в спине
Опубликовано в журнале:
«Русский медицинский журнал», 2013, №5, с. 1-4 Д.м.н. А.Е. Барулин, д.м.н. О.В. Курушина
Волгоградский государственный медицинский университет
Справедливости ради надо заметить, что вертебро-неврологические заболевания – это мультидисциплинарная проблема, решение которой требует участия многих специалистов, таких как нейрофизиологи, неврологи, альгологи, кинезиологи, мануальные терапевты, травматологи-ортопеды. Связано это, в основном, с тем, что дорсопатии являются многофакторными и полиэтиологическими заболеваниями.
В клинической практике врачей-неврологов в настоящее время формируется парадоксальная тенденция: количество методов и способов диагностики болевых расстройств увеличивается ежегодно, но при этом также возрастает терапевтическая резистентность данных расстройств и их распространенность в популяции.
При этом парадоксальной становится ситуация: расходы на лекарственную терапию боли в спине растут быстрее, чем расходы на обращения в отделения экстренной медицинской помощи, ведение стационарных и амбулаторных больных [Altman R., 2009].
Считается, что дорсопатия по характеру вовлечения структур имеет практически всегда следующие компоненты: мышечный – 100%, фасциально-связочный – 75%, суставной – 50% и лишь дискогенный компонент – 2,5% [Иваничев Г.А., 2010].
Большой интерес в понимании причин развития дорсопатий вызывает теория многофакторности развития, согласно которой для данного заболевания необходима генетическая предрасположенность, а для его проявлений – воздействие различных средовых факторов. В настоящее время к наиболее изученным факторам риска возникновения дорсопатий и их неврологических проявлений относят: женский пол, средний возраст, травму позвоночника в анамнезе, наследственность, тяжелые и несбалансированные физические нагрузки, длительное нахождение в вынужденной и нефизиологической позе, монотонную работу, курение, ожирение, неудовлетворенность профессиональной деятельностью и т.д.
Несмотря на все разнообразие факторов, практически во всех теориях развития дорсопатий фигурируют два основных аспекта: декомпенсация в трофических системах и перегрузки позвоночно-двигательных сегментов (ПДС). Локальные перегрузки ПДС возникают под воздействием как экзогенных (перегрузки в быту, на производстве), так и эндогенных (врожденные особенности функционирования мышечно-связочного аппарата) факторов. Все это является еще и предопределяющим условием для разрушающего воздействия на хрящевую ткань, с вовлечением как межпозвонковых дисков, так и межпозвонковых суставов.
Хрящевая ткань представляет собой разновидность соединительной ткани и внешне напоминает гель. Толщина хряща составляет 1–7 мм и зависит от типа сустава и его функциональной нагрузки. Суставной хрящ представляет собой высокоспециализированную хрящевую ткань, покрытую надхрящницей, которая выполняет в организме две важнейшие функции – обеспечивает скольжение суставных поверхностей, а также равномерно распределяет нагрузку при воздействии механических факторов, снижая тем самым травмирующий эффект при движении.
В межпозвоночных дисках, подвижных сочленениях находится волокнистая, или фиброзная, хрящевая ткань. Ее межклеточное вещество содержит параллельно направленные коллагеновые пучки, которые составляют до 97%, постепенно разрыхляющиеся и переходящие в гиалиновый хрящ. Кроме коллагеновых волокон ее межклеточное вещество, или внеклеточный матрикс, состоит из основного вещества, включающего до 70% воды, гиалуроновой кислоты и протеогликанов – около 10–20%. Целостность этой матрицы, соответственно, определяет биомеханические свойства суставного хряща. Структура протеогликана обеспечивает очень высокую гидрофобность, что в сочетании с низкой вязкостью делает его идеальной молекулой для противодействия нагрузке на сустав.
Хрящ не имеет нервных окончаний и сосудов. Его питание осуществляется пассивно из синовиальной жидкости и сосудов подлежащей кости, которая носит название субхондральная кость. Поэтому, по мере старения организма, в хрящевой ткани уменьшаются концентрация протеогликанов и связанная с ними гидрофильность ткани. Ослабляются процессы размножения хондробластов и молодых хондроцитов.
Ряд авторов считают, что дегенеративная болезнь диска и артроз фасеточных суставов являются главными компонентами формирования остеоартроза позвоночника.
Тем не менее, по данным Kendall N., Linton S., Main C., 1997; Оssrau G., 2008; Zaproudina N., 2009, суть диагностики вертеброневрологической патологии в западноевропейской практике сводится в основном к «сортировке» пациентов со специфическими и неспецифическими болями путем выявления так называемых «красных флажков», при необходимости проводятся дополнительные методы исследования (рентгенологическое исследование позвоночника, рентгеновская компьютерная (КТ) или магнитно-резонансная (МРТ) томография позвоночника, общий и биохимический анализ крови и др.).
У пожилых пациентов (чаще, чем в популяции) боль в спине может быть обусловлена невертеброгенными причинами. Заболевания внутренних органов сопровождаются в ряде случаев отраженной болью в спине. Необходимо дифференцировать с заболеваниями почек и мочевыводящих путей, поджелудочной железы, ретроверсией и опущением матки, объемными и воспалительными процессами в малом тазу и т.д. И в случае возможных данных заболеваний требуется принципиально иное лечение.
Лечение неспецифических болей в спине
Учитывая, что врач часто сталкивается с затруднениями в оценке эффективности и объективизации результатов лечения, начнем с клинических критериев эффективности лечения:
Использование данных рекомендаций позволяет наглядно демонстрировать динамику состояния пациента в процессе лечения, что дает возможность и врачу, и, что немаловажно, пациенту (учитывая психологические аспекты) видеть результаты проведенного лечения. Прежде чем приступать к лечению, необходимо вспомнить нецелесообразные методы:
Пациенту необходимо дать адекватную информацию о заболевании и убедить его в доброкачественности состояния.
В рекомендациях Европейского симпозиума, посвященного проблеме боли в спине, важное место выделено советам по активизации больных в период острой боли (это положение имеет доказательную базу А). В случаях без компрессии корешка постельный режим не должен превышать 48 ч. С точки зрения доказательной медицины ранняя активизация больных в момент периода острой боли дает:
Постельный режим отрицательно сказывается на результатах терапии.
Двигательный рацион должен расширяться постепенно, в начальный период с ограничением физической активности (поднятие тяжестей, наклоны, длительное сидение и т.д.). Необходимо научить пациента правильно совершать движения. Раннее возвращение к привычному для больного уровню двигательной активности способствует более быстрому купированию боли и предупреждает ее хронизацию. Предикторами хронизации болевого синдрома являются [Valat J. et al., 2000]:
Учитывая мировой опыт, комбинированную анальгетическую терапию боли рекомендуют применять многие официальные медицинские организации, в частности ВОЗ, Американская ассоциация боли, дополняя при этом ее введением хондропротективных препаратов.
Хондропротекторы
Это препараты, обладающие симптом-модифицирующим действием (уменьшают боль и способствуют улучшению функции суставов и позвоночника) и структурно-модифицирующим эффектом (задерживают или приостанавливают прогрессирование дегенеративно-дистрофического процесса). Данная группа препаратов включена в рекомендации российских и зарубежных руководств по лечению остеоартроза и иных дегенеративно-дистрофических заболеваний.
Принимая во внимание родство патогенетических механизмов дегенеративных процессов позвоночника и крупных суставов, в настоящее время в базисную терапию стали все чаще включать препараты, обладающие хондропротективной активностью.
В комплексном лечении хронических неспецифических болей в области спины у пациентов с клиническими признаками спондилоартроза («фасеточный синдром») целесообразным является включение препаратов группы хондропротекторов, замедляющих процессы дегенерации хрящевой ткани.
На основании международных критериев выделено несколько химических соединений, используемых для лечения остеоартроза крупных и мелких суставов, в т.ч. позвоночника.
Препараты со структурно-модифицирующими свойствами:
Наиболее изученными на сегодняшней день являются хондроитина сульфат и глюкозамин.
Хондроитина сульфат – гетерогенная группа соединений, имеющих различную молекулярную массу и удельный вес. Особенностью хондроитина является его способность сохранять воду в толще хряща в виде водных полостей, создающих хорошую амортизацию и поглощающих удары, что в итоге повышает прочность соединительной ткани.
Впервые применение хондропротекторов (хондроитина сульфата) при хронической болях в спине было предпринято в исследовании Christensen K.D., Bucci L.R. в 1989 г., в котором была продемонстрирована их эффективность. Эффективность применения хондроитина сульфата подтверждена в таких исследованиях, как STOPP, GUIDE. Данные, приведенные в рекомендациях Международного научно-исследовательского общества по проблемам остеоартрита (OARSI), показывают, что уровень доказательности данного препарата повышается. Однако практически не существует работ, направленных на изучение локального введения препаратов с включением в региональный кровоток. Ввиду вышеизложенного на базе кафедры неврологии, нейрохирургии с курсом медицинской генетики Волгоградского государственного медицинского университета было проведено исследование «Хондроитина сульфат (Хондрогард) в комплексном лечении болевых синдромов в области спины».
Все группы были стратифицированы по возрастному, гендерному признакам и соматотипам. При формировании групп был применен способ случайного распределения пациентов (рандомизация). Общими критериями включения для всех групп являлись: наличие мышечно-рефлекторных проявлений дорсопатий различных отделов позвоночника, подострый период заболевания.
Общие критерии исключения: наличие органических заболеваний нервной системы, психических заболеваний, травм головного мозга и позвоночника в анамнезе, соматические заболевания в стадии декомпенсации. Дополнительные критерия исключения для группы пациентов: секвестрированные грыжи и грыжи дисков более 8 мм; выраженная гипермобильность, спондилолистезы более 5 мм; наличие деструктивных изменений в телах позвонков.
В исследовании для группы пациентов были использованы диагностические критерии Международной классификации болезней 10-го пересмотра (МКБ-10) (ВОЗ, 1984).
Возрастной диапазон обследуемых варьировал от 35 до 55 лет включительно, что соответствовало второй группе зрелого возраста. По характеру трудовой деятельности больные распределились следующим образом: лица, занимающиеся физическим трудом, – 23,1%, служащие – 76,9%. Анализ занятости больных показал, что гиподинамия, статические нагрузки, позозависимые положения, работа за компьютером, профессиональные и психоэмоциональные перегрузки в последние годы выходят на ведущее место среди причин развития заболеваний позвоночника и мягких тканей.
Разделение пациентов на группы по способу введения хондроитина сульфата (Хондрогард):
Все пациенты неоднократно в течение предыдущих лет принимали лечение: амбулаторно, стационарно, а также проходили санаторно-курортное лечение.
Интенсивность болевого синдрома оценивалась по визуальной аналоговой шкале – ВАШ (Association for the Study of Pain, 1986). Количественная оценка миогенного болевого синдрома осуществлялась с помощью балльной оценки по Хабирову.
Оценивались обзорные рентгенограммы отделов позвоночника. Для уточнения патологических изменений костных структур позвоночника и изучения структурных изменений в межпозвонковых дисках, спинном мозге проводилась МРТ.
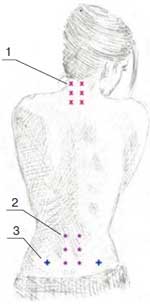
Методика введения препарата. В первый день для определения чувствительности и переносимости вводилось 100 мг (1 мл) Хондрогарда. Доза распределялась на 2 точки инъекций, расположенные в паравертебральных зонах. В последующие дни препарат вводился в дозе 200 мг (2,0 мл) в 4 точки. Выбор точек введения зависел от локализации болевого синдрома и определялся с помощью исследования вертеброневрологического статуса и пальпации триггерных точек. Пример введения в триггерные точки представлен на рисунке 1.
Рис. 1. Точки введения препарата:1 – шейный отдел; 2 – поясничный отдел; 3 – точки введения КПС
Необходимо отметить, что препарат вводился внутримышечно, что обеспечивало его быстрое распределение в регионарном кровотоке. Как известно, при внутримышечном введении он обнаруживается в крови в значительных концентрациях уже через 30 мин. после инъекции. Максимальная концентрация (Сmах) Хондрогарда в плазме достигается через 1 ч, затем постепенно снижается в течение 2 сут. Однако выбор точек, наиболее приближенных к патогенной зоне, обеспечивает максимальную концентрацию именно в синовиальной жидкости пораженных суставов.
Хондрогард накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава.
В экспериментах показано, что через 15 мин. после внутримышечной инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Сmах достигается через 48 ч.
При введении Хондрогард можно сочетать с анестетиками, например с раствором новокаина 0,25% – 10 мл, что обеспечивает дополнительный обезболивающий эффект. В таком случае дополнительно комплекс препаратов можно вводить в точки максимальной болезненности, которые выявляются у каждого пациента.
Курс терапии Хондрогардом зависит от степени выраженности изменений и может составлять от 10 до 20 паравертебральных внутримышечных инъекций, которые проводятся через день.
Следует отметить, что введение препарата Хондрогард не сопровождалось серьезными нежелательными явлениями. Препарат обладает высоким профилем безопасности, что подчеркивается рекомендациями EULAR, которая рассматривает хондроитина сульфат в качестве одного из самых безопасных лекарственных препаратов терапии остеоартроза. Местные побочные явления (небольшие гематомы в месте введения препарата, болезненные уплотнения в месте инъекции, чувство жара после инъекции) возникали редко и никогда не приводили к отказу пациента от продолжения лечения.
Результаты
Все пациенты хорошо переносили терапию. Из побочных явлений были выявлены только геморрагии в месте инъекций у 3 пациентов.
Выводы
Хондроитина сульфат (Хондрогард) целесообразно вводить паравертебрально и (или) локально возле крупного сустава (внутримышечно), что позволяет быстрее и эффективнее достигать его максимальных концентраций в региональном кровотоке пораженных участков опорно-двигательного аппарата, а это приводит к укорочению сроков нетрудоспособности и повышению эффективности лечения.
Хондрогард®
Инструкция
Торговое название
Хондрогард®
Международное непатентованное название
Лекарственная форма
Раствор для внутримышечного введения 100 мг/мл
Состав
вспомогательные вещества: бензиловый спирт, натрия метабисульфит,
натрия гидроксид, вода для инъекций.
Описание
Прозрачный бесцветный или со слегка желтоватым оттенком раствор с запахом бензилового спирта
Фармакотерапевтическая группа
Нестероидные противовоспалительные препараты другие.
Фармакологическое действие
Фармакокинетика
После внутримышечного введения хондроитина сульфат быстро распределяется. Уже через 30 мин после инъекции он обнаруживается в крови в значительных концентрациях. Максимальная концентрация (Cmax) хондроитина сульфата в плазме достигается через 1 ч, затем постепенно снижается в течение 2 суток.
Хондроитина сульфат накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава. В экспериментах показано, что через 15 мин после внутримышечной инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч. Выводится из организма в течение 24 часов. Элиминируется преимущественно почками.
Фармакодинамика
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. При лечении дегенеративных изменений
суставов с развитием вторичного синовита, положительный эффект может
наблюдаться уже через 2-3 недели после начала введения препарата уменьшается боль в суставах, исчезают клинические проявления реактивного
синовита, увеличивается объем движений в пораженных суставах.
Терапевтический эффект сохраняется длительное время после окончания
Показания к применению
Дегенеративно-дистрофические заболевания суставов и позвоночника:
— остеоартроз с преимущественным поражением крупных суставов
Способ применения и дозы
Препарат назначают внутримышечно по 100 мг через день. При хорошей переносимости дозу увеличивают до 200 мг, начиная с четвертой инъекции.
Побочное действие
Аллергические реакции (кожный зуд, эритема, крапивница, дерматит),
геморрагии в месте инъекции
Противопоказания
— повышенная чувствительность к препарату или к его компонентам
— кровотечения и склонность к кровоточивости
— беременность и период лактации
— детский возраст до 18 лет
Лекарственные взаимодействия
При сочетанном применении с нестероидными противовоспалительными средствами Хондрогард позволяет снизить дозу нестероидных противовоспалительных средств. Препарат усиливает действие непрямых антикоагулянтов, антиагрегантов, фибринолитиков, что требует более частого контроля показателей свертывания крови при совместном применении.
Особые указания
Для достижения стабильного клинического эффекта необходимо не менее 25 инъекций Хондрогарда. Для предупреждения обострений показаны повторные курсы лечения.
Использование в педиатрии
Данные об эффективности и безопасности применения хондроитина сульфата у детей в настоящее время отсутствуют.
Особенности влияния лекарственного средства на способность управлять
транспортным средством или потенциально опасными механизмами
Передозировка
В настоящее время о случаях передозировки хондроитина сульфата не
Форма выпуска и упаковка
Раствор для внутримышечного введения 100 мг/мл.
По 1 мл в ампулы бесцветного нейтрального стекла с цветным кольцом
разлома или с цветной точкой и насечкой и/или с дополнительными
цветными идентификационными кольцами или иной кодировкой.
По 5 ампул в контурной ячейковой упаковке из пленки поливинилхлоридной
и фольги алюминиевой, или пленки полимерной, или без фольги и пленки.
По 2 контурные ячейковые упаковки вместе с инструкцией по медицинскому
применению на государственном и русском языках в пачке из картона.
Условия хранения
Хранить в защищённом от света месте при температуре не выше 25°С.
Хранить в недоступном для детей месте!
Срок хранения
Не использовать по истечении срока годности.
Условия отпуска из аптек
Производитель
Закрытое акционерное общество «ФармФирма «Сотекс», Россия
141345, Московская обл., Сергиево-Посадский муниципальный район,
сельское поселение Березняковское, пос. Беликово, д. 11
Тел./факс: (495) 956-29-30.
Наименование и страна владельца регистрационного удостоверения
Закрытое акционерное общество «ФармФирма «Сотекс», Россия
Адрес организации, принимающей на территории Республики Казахстан
претензии от потребителей по качеству продукции (товара)
ТОО «EL Company (ЕЛ компани)», Республика Казахстан,
Хондрогард ® (Chondroguard) инструкция по применению
Владелец регистрационного удостоверения:
Контакты для обращений:
Лекарственные формы
Форма выпуска, упаковка и состав препарата Хондрогард ®
Раствор для в/м и внутрисуставного введения прозрачный, бесцветный или со слегка желтоватым оттенком, с запахом бензилового спирта.
| 1 мл | |
| хондроитина сульфат натрия | 100 мг |
Раствор для в/м и внутрисуставного введения прозрачный, бесцветный или со слегка желтоватым оттенком, с запахом бензилового спирта.
| 1 мл | 1 амп. | |
| хондроитина сульфат натрия | 100 мг | 200 мг |
× пачка с двух сторон с наклейками из самоклеящегося материала для контроля вскрытия или без наклеек.
* шприцы с иглой, с защитным колпачком или без иглы, с защитной пробкой и дополнительным колпачком или без дополнительного колпачка, или с дополнительным колпачком с контролем первого вскрытия.
Шприцы с иглой могут комплектоваться дополнительным автоматическим или неавтоматическим устройством для защиты иглы после использования шприца.
В пачку со шприцами без игл может дополнительно вкладываться комплект из 5 или 10 игл.
Фармакологическое действие
Высокомолекулярный мукополисахарид, влияющий на обменные процессы в гиалиновом хряще. Уменьшает дегенеративные изменения в хрящевой ткани суставов, ускоряет процессы ее восстановления, стимулирует синтез протеогликанов.
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. При лечении дегенеративных изменений суставов с развитием вторичного синовита, положительный эффект может наблюдаться уже через 2-3 недели после начала введения препарата: уменьшается боль в суставах, исчезают клинические проявления реактивного синовита, увеличивается объем движений в пораженных суставах. Терапевтический эффект сохраняется длительное время после окончания курса лечения.
Фармакокинетика
После в/м введения Cmax хондроитина сульфата в плазме достигается через 1 ч, затем постепенно снижается в течение 2 сут. При однократном внутрисуставном введении препарата в дозе 200 мг Cmax хондроитина сульфата в плазме наблюдается через 1-2 ч и составляет 52.5-86.9 нг/мл.
После в/м введения хондроитина сульфат быстро распределяется. Уже через 30 мин после инъекции он обнаруживается в крови в значительных концентрациях.
Хондроитина сульфат накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава. В экспериментах показано, что через 15 мин после в/м инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч.
При внутрисуставном введении наблюдается удерживание хондроитина сульфата в тканях сустава и его постепенный выход в кровоток.
Т1/2 при внутрисуставном введении составляет 2.5 ч.
Показания препарата Хондрогард ®
Дегенеративно-дистрофические заболевания суставов и позвоночника:
Для ускорения формирования костной мозоли при переломах.
Исследование эффективности, переносимости и безопасности препарата Хондрогард у пациентов с остеоартрозом
Л.И. Алексеева, С.Г. Аникин, Е.М. Зайцева, Н.Г. Кашеварова, Т.А. Короткова, Е.П. Шарапова, Н.В. Чичасова, Г.Р. Имаметдинова, Н.В. Бадокин, С.А. Колова
ФГБУ НИИР РАМН, Москва
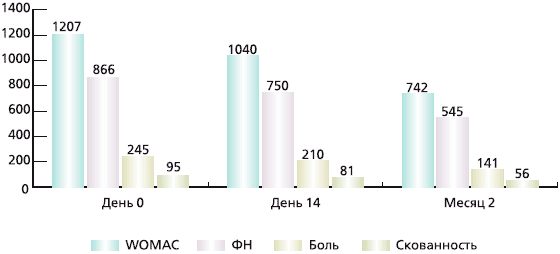
Представлены результаты исследования по оценке эффективности, переносимости и безопасности внутримышечного введения хондроитина сульфата (ХС) больным остеоартрозом (ОА) коленных суставов. В 2-месячном проспективном исследовании приняли участие 70 человек, 67 (96 %) женщин и 3 (4 %) мужчины в возрасте 45-70 лет с первичным ОА коленных суставов II (79 %) и III (21 %) рентгенологических стадий по Kellgren-Lawrence, нуждавшихся в приеме нестероидных противовоспалительных средств (НПВС). Препарат ХС Хондрогарт вводили внутримышечно через день (всего 30 инъекций), исследование завершили 66 (94 %) человек. Результаты исследования показали, что терапевтический эффект наступал в среднем на 23-й день от начала лечения. Таким образом, Хондрогард обладает достоверным симптоматическим эффектом, уменьшая боль, скованность и улучшая функциональные показатели. Преимуществом препарата являются быстрое наступление эффекта, возможность отмены или снижения дозы НПВС на фоне лечения и хорошая переносимость. Препарат Хондрогард может быть рекомендован лицам, страдающим ОА, в качестве первого средства, дающего более быстрый эффект с последующей заменой его на пероральные формы.
Ключевые слова: остеоартроз, нестероидные противовоспалительные средства, хондроитина сульфат
The results of the study aimed to evaluation the efficacy, tolerability and safety of intramuscular administration of chondroitin sulfate (CS) in patients with osteoarthrosis (OA) of the knee are presented. The 2-month prospective study involved 70 patients, 67 (96 %) women and 3 (4 %) men aged 45-70 years with primary OA of knee joints II (79 % ) and III (21 %) radiographic stages by Kellgren-Lawrence, who were in need of administration of nonsteroidal anti-inflammatory drugs (NSAIDs). The drug Chondrogard was administered intramuscularly each alternate day (a total of 30 injections); 66 (94 %) patients have completed the study. The results showed that the therapeutic effect occurred at the 23th day of treatment on average. Thus, Chondrogard has significant symptomatic effect, reducing pain, stiffness, and improving functional performance. The advantages include the rapid onset of drug effect, potential for the withdrawal or reducing the NSAID dose during treatment, and good tolerability. The drug Chondrogard can be recommended to the OA patients as a first-line drug with a more immediate effect, with subsequent replacement by oral forms of drug.
Key words: osteoarthrosis, nonsteroidal anti-inflammatory drugs, chondroitin sulfate
Фармакокинетика и биологическая активность ХС в значительной степени определяются массой молекулы и степенью сульфатирования [10]. В качестве исходного сырья для получения ХС используется хрящевая ткань крупного рогатого скота, свиней, цыплят или рыб 12. Разные источники получения ХС определяют особенности молекулярной структуры ХС, что в свою очередь помимо степени очистки оказывает влияние на эффективность применения того или иного препарата.
Большая часть ХС выпускается в виде форм для перорального применения. При попадании в ЖКТ происходит разрушение большинства молекул ХС, и в системный кровоток, как правило, попадают низкомолекулярные дериваты, обладающие небольшой терапевтической активностью. По некоторым данным, доля нативных молекул в системном кровотоке при пероральном приеме составляет всего 10 %. Максимальная концентрация препарата в крови достигается через 3-4 часа после приема, а в синовиальной жидкости — через 4-5 часов. В целом же биодоступность ХС при пероральном приеме составляет в среднем от 10 до 20 % 17.
При внутримышечном введении ХС выявляется в значительных концентрациях в системном кровотоке уже через 30 минут, а максимальная концентрация достигается через час. В синовиальной жидкости препарат выявляется через 15 минут после внутримышечной инъекции, а максимальная концентрация в хрящевой ткани достигается через 48 часов [18]. Внутримышечный способ введения ХС увеличивает биодоступность и долю нативных молекул в системном кровотоке, благодаря чему может повышаться как эффективность проводимой терапии, так и более быстрое развитие симптоматического эффекта.
Целью исследования явилась оценка эффективности, переносимости и безопасности ХС (Хондрогарда) для пациентов с ОА коленных суставов при внутримышечном применении.
Материал и методы
В 2-месячное проспективное когортное исследование были включены 70 человек с диагнозом ОА коленных суставов, среди них были 67 (96 %) женщин и 3 (4 %) мужчины. Диагноз остеоартроза устанавливался на основе классификационных критериев Американской коллегии ревматологов (АКР) 1986 г. [5].
В исследование не включали лиц с вторичным гонартрозом, внутрисуставным введением любых препаратов за последние 6 недель до начала исследования, наличием хондрокальциноза, асептического некроза мыщелков бедренных и большеберцовых костей, оперативных вмешательств на коленном суставе, а также с известной повышенной чувствительностью к ХС, тяжелыми сопутствующими заболеваниями, язвой желудка или двенадцатиперстной кишки в течение последнего месяца, кровотечениями в анамнезе, тромбофлебитами, беременностью и периодом лактации, принимавшими препараты с симптоматическими и структурно-модифицирующими свойствами. Разрешалось использование НПВС, которые пациенты принимали на момент включения в исследование. Не допускались внутрисуставные инъекции, в т. ч. глюкокортикоидов и препаратов гиалуроновой кислоты, прием антикоагулянтов, антиагрегантов, фибринолитиков, проведение физиотерапевтических процедур.
Характеристика участников исследования представлена в табл. 1.
Таблица 1
Характеристика участников исследования