Как сделать диперекись ацетона
Диперекись ацетона в домашних условиях
Перекись ацетона, как и все пероксиды, обладает высокими отбеливающими и окислительными свойствами.
Вещество зарегистрировано в качестве пищевой добавки для улучшения муки и хлеба.
Опасность при работе с взрывоопасным продуктом заставило исключить его из разрешающих документов.
Уже много лет я изучаю проблему ДИАБЕТА. Страшно, когда столько людей умирают, а еще больше становятся инвалидами из-за сахарного диабета.
Название продукта
Перекись ацетона — официальное наименование добавки. В европейской кодификации продукт зарегистрирован под номером Е 929 (Е–929).
Международное название — Acetone Peroxide.
Тип вещества

Вещество представляет собой органический пероксид.
Получают продукт в процессе взаимодействия ацетона с концентрированным пероксидом водорода. Реакция протекает в присутствии минеральной одноосновной кислоты: серной (чаще всего), азотной, соляной. Молекула содержит обычно 2 или 3 пероксидные группы. Легче получить триперекись ацетона, но и она будет содержать димер в качестве примеси.
Свойства
| Показатель | Стандартные значения |
| Цвет | белый |
| Состав | перекись ацетона, эмпирическая формула C6H12O4 |
| Внешний вид | мелкодисперсный порошок, после длительного хранения — кристаллы правильной формы |
| Запах | резкий характерный |
| Вкус | без вкуса |
| Содержание основного вещества | 96% |
| Растворимость | хорошо в эфире, бензоле, ацетоне, уксусной кислоте. Нерастворим в воде |
| Плотность вещества | 1,3 г/см³ |
| Другие | не гигроскопична; при обычных условиях хранения не разлагается; обладает повышенной летучестью, при комнатной температуре испаряется в течение 2 часов; при нагревании с раствором серной кислоты распадается до ацетона и перекиси водорода; устойчива в кислотных и щелочных растворах; не корродирует металлы (исключение — свинец); проявляет окислительные свойства; плавится при температуре 97ºC. Взрывоопасна! |
Упаковка
Добавка Е 929 — взрывчатое вещество, относится к категории опасных грузов. Расфасовка продукта должна осуществляться в тару, устойчивую к вибрации, изменению температуры, давления и влажности. Обычно с этой целью используют металлические барабаны или бочки.
Будьте осторожны
По данным ВОЗ каждый год в мире от сахарного диабета и вызванных им осложнений умирает 2 миллиона человек. При отсутствии квалифицированной поддержки организма диабет приводит к различного рода осложнениям, постепенно разрушая организм человека.
Из осложнений чаще всего встречаются: диабетическая гангрена, нефропатия, ретинопатия, трофические язвы, гипогликемия, кетоацидоз. Диабет может приводить и к развитию раковых опухолей. Практически во всех случаях диабетик или умирает, борясь с мучительной болезнью, или превращается в настоящего инвалида.
Что же делать людям с сахарным диабетом? Эндокринологическому научному центру РАМН удалось сделать средство полностью вылечивающее сахарный диабет.
Применение
Добавка E 929 запрещена в производстве пищевых продуктов. Несколько лет назад перекись ацетона применялась некоторыми странами (например, Канадой) для отбеливания и улучшения качества хлебопекарной муки.

В настоящее время перекись ацетона не имеет промышленного применения ни в одной стране мира.
Ограниченно продукт разрешено использовать в химической отрасли при синтезе полимеров. Добавка Е 929 выступает катализатором свободнорадикальной полимеризации.
Наши читатели пишут
Болезнь продолжала развиваться, начались периодические приступы, скорая буквально возвращала меня с того света. Все время думала, что этот раз окажется последним.
Все изменилось, когда дочка дала прочитать мне одну статью в интернете. Не представляете на сколько я ей за это благодарна. Эта статья помогла мне полностью избавиться от сахарного диабета, якобы неизлечимой болезни. Последние 2 года начала больше двигаться, весной и летом каждый день езжу на дачу, с мужем ведём активный образ жизни, много путешествуем. Все удивляются, как я все успеваю, откуда столько сил и энергии, все никак не поверят, что мне 66 лет.
Благодаря простоте получения и доступности компонентов перекись ацетона нередко используют химики-любители для изготовления петард в домашних условиях.
Следует знать! В России производство, хранение, распространение перекиси ацетона, как и других взрывчатых веществ, запрещено и карается ст. 222, 223.1 УК.
Польза и вред
Исследования влияния добавки E 929 на здоровье человека при попадании вещества внутрь не проводили.

Работа с веществом без специальных навыков может иметь трагические последствия. Перекись ацетона отличается высокой взрывчатой силой: 5500 кДж/кг (это почти на 20% выше того же показателя для тринитротолуола, входящего в состав динамита).
Истории наших читателей
Читать статью полностью >>>
Сухой порошок может сдетонировать при легком нагреве (например, при сушке на батарее отопления) или от искры статического электричества, образующего на одежде.
В расплавленном виде перекись ацетона чувствительная к трению: для сильного взрыва достаточно поскрести вещество ногтем.
На данный момент силикат цинка запрещено использовать в производстве пищевых продуктов. С чем это связано, читайте в нашей статье.
В каких сферах применяется карбамид? Об этом мы рассказали здесь.
Основные производители

В России небольшие объемы продукта китайского производства строго для химической промышленности предлагает компания «ЮгТехКом» (город Краснодар).
Многие из нас в детстве увлекались взрывчатыми веществами. Но самодельная «взрывчатка» не всегда срабатывала, или вещество получалось недостаточно мощное. Всегда ждёшь от взрыва нечто большее, чем просто оглушающий звук. Так вот, сегодня мы разберём свойства, получение и применение такого взрывоопасного соединения, как перекись ацетона.
Сразу стоит предупредить, что получение этого вещества в домашних условиях не только очень опасно, но и карается Уголовным кодексом Российской Федерации.
Начнём мы с истории открытия этого замечательного вещества.
История
Однако всё было не так просто в этом веществе. Дело в том, что Рихард Вольфенштейн обнаружил триперекись ацетона. А в 1899 году ещё один немецкий химик Адольф Байер вместе с Виктором Виллигером синтезировал димерную модификацию пероксида ацетона. В 1947 году было изучено влияние различных кислот на скорость образования этого соединения. Как оказалось, соляная, серная, фосфорная и азотная кислоты значительно ускоряют окисление ацетона в присутствии перекиси водорода. Органические кислоты, такие как уксусная и бензойная, напротив, препятствуют образованию продукта.
Продолжим описание такого важного соединения, как перекись ацетона. Получение мы обсудим позже. А пока — немного теории.
Что такое перекись ацетона
Сейчас поговорим немного о видах перекиси ацетона (точнее, её модификациях), их свойствах и способах синтеза. Это достаточно интересная тема, учитывая, что все виды отличаются друг от друга физическими и химическими характеристиками.
Модификации перекиси ацетона
Не все вещества, состоящие из молекул, устойчивы в обычном состоянии. Многие образуют полимерные формы. Одним из них и является обсуждаемое сегодня нами вещество. Поэтому однозначно нельзя сказать, какая формула перекиси ацетона. Она имеет несколько модификаций: три димера (полимер, состоящий из двух молекул) и один тример (состоит из трёх молекул). Но, перед тем как разобрать строение конкретно таких структур, мы обсудим формулу мономера, то есть одной отдельно взятой молекулы перекиси ацетона. В общем виде её можно представить так:
Но если попытаться нарисовать структурную формулу такого вещества, мы столкнёмся с некоторыми трудностями.
Перекись чего-либо — это вещество с дополнительным атомом кислорода, который соединяется с другим таким же атомом в этом соединении и образует так называемую «очковую» связь (так как в структурном виде она выглядит как очки: О-О). В ацетоне атом кислорода связан двойной связью с углеродом. Во-первых, эта связь достаточно прочная, и чтобы присоединить к атому углерода второй кислород, нужно приложить большую энергию. Во-вторых, если это всё же удалось (благодаря сильным окислителям, к которым также относится перекись водорода), устойчивость получившегося соединения крайне низкая из-за наличия двух атомов кислорода у одного атома углерода и недостатка электронов в системе. Для того чтобы создать устойчивую форму, молекулы группируются по две или по три и образуют полимеры.
Диперекись ацетона
Самый частый вариант группировки, которую принимает перекись ацетона, — это димер. Он состоит из двух молекул, связанных между собой через атомы кислорода. Такой продукт наиболее устойчив, но всё же разлагается за 15 минут сильными кислотами. Получить его сложнее, чем следующую модификацию, но об этом чуть позже.
Триперекись ацетона
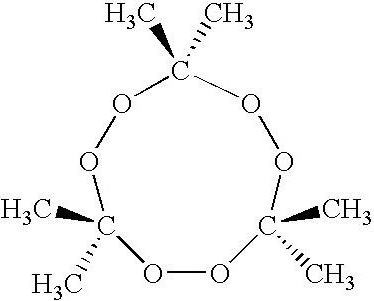
Вообще, большей частью перекись ацетона (взрывчатое вещество) состоит из тримера (триперекиси) и получается достаточно легко в домашних условиях. По физическим свойствам немного отличается от других модификаций: легко возгоняется, особенно при повышении температуры, хорошо растворяется во многих органических растворителях, но выпадает в осадок в воде. Очень интересно то, что тример взрывается, даже если четверть его массы составляет вода. Ниже вы можете увидеть, как графически выглядит перекись ацетона, формула которой соответствует тримеру.
Синтез
Перекись ацетона, получение которой происходит только для технологических нужд, используется в пищевой промышленности. Удивительно, что такое взрывоопасное вещество используется как пищевая добавка под номером Е-929. Однако переживать не стоит: кроме детонирующих свойств это соединение обладает консервирующим действием. О его применении мы поговорим позже. А сейчас немного о способах получения.
Многие интересуются: как получить перекись ацетона без кислоты? Это самый простой способ её синтеза. Вообще, в лаборатории первый раз это соединение получили, смешав равные объёмы концентрированной (10-процентной) перекиси водорода и ацетона. Для ускорения реакции добавляют какую-либо минеральную кислоту, в роли которой может выступать как серная или соляная, так и фосфорная. Таким способом получают почти чистую триперекись. Для синтеза димера используют более сложный способ. Для этого в раствор ацетона добавляют 86-процентный пероксид водорода, ацетонитрил и серную кислоту. Всю систему охлаждают и в конце выделяют продукт с выходом 94 процента. Как стало понятно, чтобы получить димерную перекись ацетона в домашних условиях, надо очень хорошо постараться. Но есть ещё один способ. Подойдёт он для тех, у кого под рукой есть персульфат калия и разбавленная серная кислота. Смешение этих реагентов с ацетоном также даёт обсуждаемое нами соединение.
Можно использовать при получении разные кислоты, но они будут давать разные результаты. Например, при синтезе с использованием метансульфокислоты, серной или хлорной кислот, тример пероксида ацетона самопроизвольно превращается в димерную форму. Но такого не происходит, если использовать хлорид олова, соляную или азотную кислоту. Однако в самом простом случае не требуется ни кислот, ни каких-либо манипуляций с системой: только смешение равных объёмов исходных веществ.
Мы разобрали лабораторные методы, с помощью которых можно получить перекись ацетона. Как сделать это соединение в домашних условиях, мы не будем говорить, так как получение и хранение взрывоопасных веществ запрещено и уголовно наказуемо. Стоит рассказать ещё о нескольких интересных вещах. Перейдём к реакциям, в которых участвует перекись ацетона.
Свойства и химические реакции
Начнём с химических свойств. Их достаточно мало, потому что исследований на эту тему проводилось не много. Большинство реакций описывают разложение перекиси ацетона на различные продукты в определённых условиях. Например, при добавлении разбавленной серной кислоты и нагревании на водяной бане наше соединение разлагается с образованием исходных продуктов: ацетона и перекиси водорода. Реакцию, которая описывает это взаимодействие, можно записать так:
Ещё одно хорошо изученное свойство этого соединения — детонация. Пожалуй, оно является основополагающим для перекиси ацетона, ведь основное применение этого вещества — пиротехника.
Но, перед тем как подробно разобрать сам процесс воспламенения, изложим некоторые теоретические основы. Для начала следует понять, что представляет собой химическая реакция взрыва. Детонация — это процесс выделения газов, который происходит с очень большой скоростью. При этом выделяется огромное количество теплоты. За счёт всего этого и создаётся взрывная волна: горячие газы с большой скоростью распространяются вокруг очага детонации и наносят большой ущерб всему, что находится рядом. Как правило, ударная волна распространяется со скоростью больше скорости звука.
Перейдём непосредственно к нашей реакции, которая приводит к детонации. В результате удара или какого-либо другого воздействия на перекись ацетона, она может сдетонировать. При этом происходит следующая реакция:
Есть также данные ещё об одном свойстве — коррозионной активности. Конечно, так как триперекись ацетона обладает окислительными свойствами, она может коррозировать (вызывать коррозию) некоторые металлы, например свинец. Однако большинство металлов она не в силах окислить.
А теперь ещё один интересный раздел, касающийся физических свойств данного соединения. Для любителей пиротехники будет полезно это прочитать, так как присутствует очень много практических сведений.
Физические свойства
Перекись ацетона обладает очень сильной взрывчатой силой. Всё это благодаря количеству выделяемых газов и теплоте, образуемой в результате реакции разложения. Эта величина достигает 5500 кДж/кг, что примерно на 20 процентов больше аналогичного показателя для тринитротолуола (сокращённо «тнт» — вещество, входящее в состав динамита).
Возможно приготовление таблеток из сухого вещества разной плотности. При этом меняются некоторые физические характеристики. Например, очень сильно плотность влияет на скорость детонации. При 0,92 г/см 3 величина скорости детонации равна примерно 3750 м/с, а при 1,18 г/см 3 этот показатель будет равен 5300 м/с. Конечно, это всё закономерно: при увеличении плотности увеличивается количество вещества в единице объёма, а значит, и при взрыве скорость распространения волны в пространстве будет расти за счёт увеличения количества тепла и газов, выделяемых в ходе реакции.
Есть также такой показатель, как скорость горения. Он отличается от скорости детонации тем, что показывает, как быстро может сгореть образец в присутствии кислорода. На самом деле, детонируя, перекись ацетона не использует кислород, то есть она не горит. А при взаимодействии с кислородом происходит следующая реакция: С3Н6О2 + 3,5О2 = 3СО2 + 3Н2О. Так вот, скорость горения, как правило, значительно ниже скорости детонации, и для перекиси ацетона она составляет 0,95 см/с. Очень скромный показатель в сравнении с 5300 м/с.
Применение перекиси ацетона
Основное применение — это, конечно, все области, так или иначе связанные с использованием взрывчатых веществ. Например, очень активно это соединение используется в горном деле для разработки новых месторождений. Там оно применяется либо в смеси с другими веществами как инициатор реакции детонации, либо очень редко как отдельный основной элемент взрывчатого заряда.
Мы уже говорили о применении пероксида ацетона в качестве пищевой добавки в пищевой промышленности. Тут стоит отметить, что для организма она безвредна и содержит в себе, как правило, такой процент влаги, что просто не способна сдетонировать. Поэтому не стоит опасаться продуктов, если увидите в их составе добавку Е-929. Это всего лишь консервант, не дающий продуктам испортиться.
Заключение
В этой статье мы попытались осветить обширную и интересную тему о получении и применении одного из самых популярных у террористов и молодых пиротехников взрывчатых веществ — перекиси ацетона. Мы разобрали свойства, лабораторные методы получения и применение этого вещества.
Эта статья ни в коем случае не призывает вас самостоятельно делать перекись ацетона в домашних условиях! Помните, что, помимо того что есть опасность получить серьёзные травмы, за хранение и использование этого вещества вы можете понести уголовную ответственность.
| Рецепт диперекиси ацетона |
|---|
| Уровень: 1 |
| Будет получен предмет: |
Медицина Навык в ветке «Поддержка» : 40;
Модификация Навык в ветке «Поддержка» : 40;
Удача Навык в ветке «Поддержка» : 20;
Ацетон, перекись водорода и серная кислота из автомобильного аккумулятора.
Делаем выводы
Если вы читаете эти строки, можно сделать вывод, что Вы или Ваши близкие больны сахарным диабетом.
Мы провели расследование, изучили кучу материалов и самое главное проверили большинство методик и препаратов от сахарного диабета. Вердикт таков:
На данный момент это единственный препарат, который способен полностью излечить сахарный диабет. Особенно сильное действие Дифорт показал на ранних стадиях развития сахарного диабета.
Мы обратились с просьбой в Министерство Здравоохранения:
И для читателей нашего сайта теперь есть возможность
получить Дифорт БЕСПЛАТНО!