Ципрофлоксацин таваник в чем разница
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
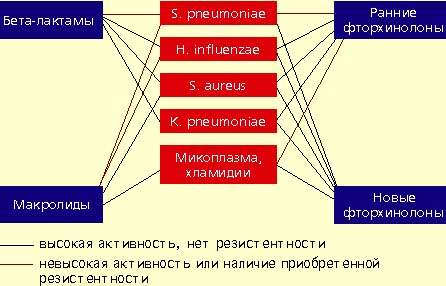 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Применение Таваника в урологии
Аляев Ю.Г., Султанова Е.А., Шпоть Е.В.
Таваник (левофлоксацин) обладает широким спектром антимикробного действия. Он входит в новую группу фторхинолонов, отличительной особенностью которых наряду с высокой активностью в отношении многих грамотрицательных бактерий является повышенная активность в отношении грамположительных микробов, атипичных микроорганизмов и анаэробов. Важным свойством препарата является его высокая активность в отношении внутриклеточных патогенов [5].
Таваник блокирует ДНК–гиразу (топоизомеразу II) и топоизомеразу IV, нарушает суперспирализацию и сшивку разрывов ДНК, ингибирует синтез ДНК, вызывает глубокие морфологические изменения в цитоплазме, клеточной стенке и мембранах.
Таваник, как и другие фторхинолоны, имеет выраженный постантибиотический эффект – продолжение антимикробного действия после удаления препарата из среды, длительность которого зависит от вида микроорганизма и величины ранее действовавшей концентрации [5].
Таваник характеризуется высокой степенью биодоступности и устойчивостью к трансформации в организме. Он хорошо проникает в разные органы и ткани; в тканях мочеполовой системы концентрация Таваника при использовании в терапевтических дозах соответствует или превышает концентрацию в сыворотке крови [3,4].
Выводится препарат преимущественно с мочой (70%), в которой создаются высокие концентрации, достаточные для подавления чувствительной к нему микрофлоры в течение долгого времени [5].
Длительная циркуляция препарата в организме в терапевтических концентрациях позволяет применять его 1 раз в сутки [5].
Как правило, Таваник хорошо переносится пациентами. Из побочных эффектов (3–10% случаев) следует отметить тошноту, рвоту, диарею, запор, головную боль, фототоксичность, реакции гиперчувствительности, удлинение интервала QT на ЭКГ, тендинит. Противопоказаниями к приему препарата служат гиперчувствительность, возраст до 18 лет, беременность, кормление грудью, эпилепсия, дефицит глюкозо–6–фосфатдегидрогеназы [5].
Таваник применяется в урологической практике для лечения таких заболеваний, как неосложненные и осложненные инфекции мочевых путей (ИМП), бактериальный простатит, неспецифический уретрит и некоторые виды специфических уретритов (вызванных инфекциями, передаваемыми половым путем), а также орхит и эпидидимит.
Неосложненные инфекции мочевых путей
Острая неосложненная ИМП – эпизод острой инфекции нижних (уретрит, цистит) или верхних (пиелонефрит) мочевых путей у пациентов при отсутствии у них каких–либо нарушений оттока мочи из почек и мочевого пузыря, структурных изменений в органах мочевой системы и серьезных фоновых заболеваний, которые могут утяжелить ее течение или привести к неэффективности проводимой терапии.
Рецидивирующая неосложненная ИМП – возникновение более двух эпизодов ИМП в течение 6 месяцев или трех эпизодов в течение 1 года.
Бессимптомная бактериурия – наличие двух последовательных (с промежутком в 1 неделю) положительных результатов бактериологического исследования мочи, при которых был выявлен один и тот же штамм возбудителя ИМП; клинические проявления заболевания при этом отсутствуют [2].
Неосложненные ИМП чаще встречаются у женщин. Каждая вторая женщина в мире, по меньшей мере, 1 раз в жизни переносит эпизод ИМП, из них у 25–40% женщин в течение ближайших 6–12 месяцев отмечается рецидив заболевания.
Лечение острых неосложненных ИМП можно проводить амбулаторно; госпитализация необходима лишь в серьезных случаях.
Richard G.A. et. al. изучили эффективность и безопасность применения Таваника в дозировке 250 мг один раз в сутки в сравнении с ципрофлоксацином в дозировке 500 мг дважды в сутки в течение 10 дней в лечении 385 пациентов, страдающих инфекцией мочевыводящих путей в рамках рандомизированного двойного слепого мультицентрового исследования. Всем больным перед началом лечения выполнен посев мочи, по данным которого у всех пациентов выявлен рост патогенной микрофлоры и микробное число составило 105 микробных тел в 1 мл мочи. Клиническое выздоровление отмечено у 92% пациентов, получавших Таваник, и у 88% пациентов, получавших ципрофлоксацин. Побочные эффекты отмечены у 4 и 3% пациентов соответственно. Авторы делают вывод, что эффективность и безопасность терапии Таваником сравнима с таковыми при использовании ципрофлоксацина, а в некоторых случаях даже превосходит их [7,8].
Схемы лечения больных острыми неосложненными инфекциями мочевых путей представлены ниже.
Острый неосложненный цистит: Таваник внутрь 250–500 мг 1 раз в сутки в течение 3–5 сут.
Острый неосложненный пиелонефрит легкого течения: Таваник внутрь 250–500 мг 1 раз в сутки в течение 7–14 суток.
При отсутствии улучшения или ухудшении состояния пациента показана госпитализация для дополнительного обследования, выявления осложняющих факторов, дренирования мочевых путей и возможного оперативного лечения. Госпитализация показана также при исходном среднетяжелом и тяжелом течении острого неосложненного пиелонефрита, наличии симптомов интоксикации, уросепсиса [2].
Острый неосложненный пиелонефрит среднетяжелого и тяжелого течения: Таваник внутривенно 500 мг 1 раз в сутки в течение 3–5 суток, затем внутрь 500 мг 1 раз в сутки (суммарный курс лечения – 2–3 недели).
Неосложненные ИМП (за исключением заболеваний, передаваемых половым путем) у молодых здоровых мужчин в возрасте от 15 до 50 лет встречаются очень редко. Как правило, ИМП у мужчин являются осложненными и обусловлены урологическими аномалиями, инфравезикальной обструкцией, инструментальными вмешательствами и дренированием мочевых путей [2].
Неспецифический уретрит у молодых мужчин: Таваник внутрь 250–500 мг 1 раз в сутки в течение 7 суток.
При обострении рецидивирующей неосложненной ИМП возможно применение Таваника по схемам, приведенным выше. Однако длительный прием препарата в качестве поддерживающей терапии часто является необоснованным из–за высокого риска развития дисбактериоза.
Осложненные инфекции мочевых путей
Осложненная ИМП – ИМП, которая развивается на фоне структурных или анатомических аномалий мочеполовых органов, а также сопутствующих заболеваний, снижающих защитные силы организма и увеличивающих риск восходящей инфекции или неэффективности лечения.
Для осложненной ИМП характерно наличие одного или более из следующих факторов:
• наличие постоянного мочепузырного катетера, катетера–стента, дренажей, интермиттирующая катетеризация мочевого пузыря;
• наличие остаточной мочи;
• обструктивная уропатия (инфравезикальная обструкция, нейрогенный мочевой пузырь, камни, опухоли мочевых путей и т.д.);
• пузырно–мочеточниковый рефлюкс и другие функциональные аномалии;
• реконструктивные операции на мочевых путях;
• химическое или радиационное поражение уротелия;
• пери– и послеоперационная ИМП;
• почечная недостаточность, сахарный диабет, трансплантация почки, иммунодефицитные состояния [2].
Тактика лечения зависит от тяжести заболевания и возможности устранения осложняющих факторов. В противном случае полное излечение ИМП невозможно. Лечение осложненной ИМП часто требует госпитализации больного. При этом антибактериальную терапию желательно проводить под контролем бактериологического исследования мочи.
Из антибактериальных средств наиболее эффективны фторхинолоны, которые экскретируются преимущественно почками, имеют широкий спектр антимикробного действия и достигают высокой концентрации как в моче, так и в тканях органов мочеполовой системы.
Y. Kawada, Y. Aso et. al. сравнили эффективность терапии Таваником в дозировке 250 мг дважды в сутки (135 пациентов) и офлоксацина в дозировке 200 мг дважды в сутки (126 пациентов) в терапии пациентов с осложненной мочевой инфекцией. Положительный клинический эффект получен у 83,7% пациентов в группе терапии Таваником и у 79,4% пациентов в группе терапии офлоксацином. С точки зрения статистики различий в эффективности лечения двух вышеописанных групп не было. Побочные эффекты отмечены у 4,9% пациентов в группе офлоксацина. В группе Таваника подобных эффектов отмечено не было, что, по мнению авторов, говорит о лучшей переносимости препарата [6].
Несмотря на то, что согласно различным исследованиям эффективность препарата близка к эффективности других хинолонов, очевидными преимуществами Таваника являются низкий уровень побочных эффектов, хорошая переносимость и возможность однократного суточного приема. При наличии камней почек или мочевого пузыря эрадикация возбудителя может способствовать торможению их роста. Если полное удаление камней невозможно, больному требуется длительная антимикробная терапия.
Присоединение инфекции на фоне обструкции верхних мочевых путей является крайне опасным и требует их экстренного дренирования. Проведение активной антимикробной терапии можно начинать только после устранения обструкции из–за высокого риска развития бактериотоксического шока.
Лечение бессимптомной бактериурии при наличии у больных постоянных катетеров или дренажей в мочевых путях, а также при интермиттирующей катетеризации мочевого пузыря не рекомендуется, т.к. приводит к селекции резистентных штаммов микроорганизмов и неэффективно для лечения микроорганизмов, входящих в состав пленки–biofilm. При наличии клинических проявлений таким больным показаны 7–10–дневные курсы антибиотиками широкого спектра действия.
Наличие сахарного диабета или иммунодефицита является показанием к лечению даже бессимптомной бактериурии.
В клиники урологии ММА имени И.М. Сеченова Таваник был назначен 114 пациентам с неосложненными инфекциями и 86 пациентам с осложненными инфекциями мочевых путей (острый обструктивный пиелонефрит) в возрасте от 19 до 63 лет (средний возраст 41 год). Среди пациентов с неосложненными инфекциями у 76 пациенток имел место острый цистит, у 38 – острый необструктивный пиелонефрит. Препарат назначался больным в дозировке 500 мг в сутки в течение 10 дней при неосложненных инфекциях и 14 дней – при осложненных. Результаты лечения оценивались на основании субъективной оценки эффективности и безопасности лечения пациентами и врачом, а также анализа объективных показателей: мониторинга анализов крови и мочи, ультразвукового мониторинга. Отсутствие клинического эффекта лечения определялось как сохранение или усиление клинических проявлений после 2 дней лечения.
В результате анализа данных, полученных в процессе исследования, положительный клинический и лабораторный эффект от лечения достигнут у 91% пациентов с неосложненными и у 82% – с осложненными инфекциями. При контрольном бактериологическом исследовании, выполненном через 2 недели после лечения, у пациентов с хорошим клиническим эффектом антибиотикотерапии, роста возбудителя не выявлено. Побочные эффекты применения Таваника отмечены у 3% пациентов. Наиболее часто встречались побочные реакции в виде тошноты и диареи. Следует отметить, что вышеописанное явления имели крайне низкую степень выраженности. Ни одному из пациентов не потребовалось проведение специального лечения в связи с вышеуказанными побочными реакциями, и ни один из них не покинул исследование.
Таким образом, фторхинолоны в настоящее время сохранили лидирующее место в лечении инфекций мочевых путей. По клинической эффективности эти препараты сравнимы с аминогликозидами и цефалоспоринами нового поколения, а в некоторых случаях (при смешанных инфекциях) превосходят их. Действие препаратов носит преимущественно патогенетический характер, и направлено на элиминацию из организма возбудителей воспаления.
При осложненных ИМП (за исключением случаев резистентности) Таваник применяют по следующей схеме: Таваник внутривенно 500 мг 1 раз в сутки в течение 7–14 суток.
При наличии показаний длительность лечения может быть увеличена до 3 недель.
ИМП при почечной недостаточности или трансплантации почки: Таваник внутрь 250–500 мг 1 раз в сутки в течение 10–14 суток.
В случае применения Таваника у больных с почечной недостаточностью следует учитывать, что при снижении клубочковой фильтрации Бактериальный простатит
Простатит – воспаление предстательной железы, которое может быть острым или хроническим (симптомы сохраняются >3 месяцев) [2].
Сегодня лечение хронического простатита не представляется без антибиотиков и противомикробных препаратов, среди которых наиболее предпочтительными являются фторхинолоны, отличающиеся широким спектром антимикробного действия, высокой бактерицидной активностью и хорошей фармакокинетикой. Фторхинолоны в отличие от нефторированных хинолонов имеют большой объем распределения, создают высокие концентрации в органах и тканях, проникают внутрь клеток.
Лечение простатита должно быть комплексным: помимо антимикробной терапии, необходимо адекватное дренирование выводных протоков ацинусов предстательной железы (при хроническом простатите проводится массаж простаты), а также применение различных физических методов (физиотерапии) с целью улучшения кровотока и обеспечения более активного противовоспалительного эффекта.
При выборе антибактериального средства следует учитывать спектр его антимикробной активности, а также способность проникать в ткань предстательной железы.
Фторхинолоны обладают хорошим внутритканевым проникновением, широким спектром антимикробной активности и являются препаратами выбора при лечении простатита. Возможность однократного применения делает предпочтительным назначение Таваника.
В клиники урологии ММА имени И.М.Сеченова эффективность Таваника оценена у 96 пациентов с хроническим бактериальным простатитом. Всем больным для подтверждения диагноза «хронический простатит» проводилась микроскопия секрета простаты. В редких случаях (около 10%), когда не удавалось получить сок предстательной железы, выполнялась спермограмма.
Большинству пациентов выполнялось исследование соскоба из уретры методом ПЦР. Отказ от выполнения соскоба уретры у ряда пациентов был связан с отрицательным результатом данного анализа до обращения в нашу клинику.
Материалом для бактериологического посева являлась сперма, собранная утром в день исследования в стерильную банку. Данный анализ проводился не всем пациентам. Критерием отбора для выполнения данного исследования являлся длительный анамнез лечения хронического простатита, что могло быть причиной множественной антибиотикорезистентности возбудителя.
Критерием исключения из исследования являлась полирезистентная флора, выявленная при бактериологическом исследовании.
Возбудители, выявленные при бактериологическом исследовании у пациентов основной и контрольной группы, обладали чувствительностью к большинству препаратов, в том числе фторхинолонам.
Оценка эффективности препарата проводилась через 1 месяц после начала лечения. Контрольное обследование включало микроскопическое исследование секрета простаты, бактериологическое исследование спермы и исследование соскоба из уретры методом ПЦР.
После лечения больных хроническим бактериальным простатитом жалобы полностью отсутствовали у 79 (82,3%) больных. У 3 пациентов отмечалось уменьшение клинической симптоматики. У 14 пациентов жалобы сохранялись, однако только у 5 среди 14 при контрольном микроскопическом исследовании секрета простаты сохранялись признаки воспаления.
Процент больных, у которых возбудители при контрольном обследовании не были выявлены, составил 89,6.
Клиническая эффективность применение Таваника у больных хроническим бактериальным простатитом составила 85,4%, эффективность микробиологическая – 89,6%.