Цистинурия это что за болезнь
Цистинурия это что за болезнь
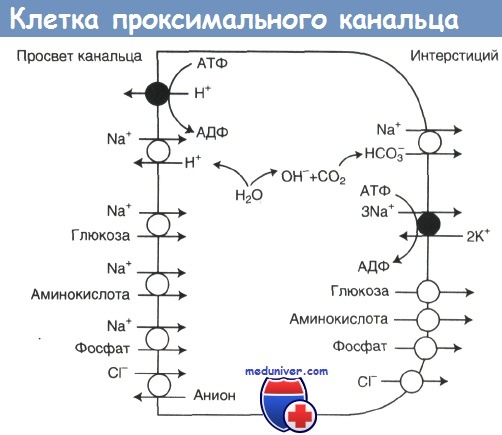
Отфильтровавшиеся в клубочках аминокислоты реабсорбируются в проксимальных канальцах. Как и в случае глюкозы, перенос аминокислот через апикальную мембрану осуществляется путем котранспорта с натрием, а перенос через базолатеральную мембрану — путем облегченной диффузии.
Аминоацидурия может возникать:
1) при повышении СКФ и избыточном поступлении аминокислот в проксимальные канальцы;
2) при врожденных нарушениях метаболизма, приводящих к повышению концентрации определенных аминокислот в крови;
3) при нарушении реабсорбции аминокислот вследствие дефекта белков-переносчиков.
Цистинурия — самое частое нарушение канальцевого транспорта аминокислот. Она наследуется аутосомно-рецессивно и вызвана мутацией гена SLC3A1, кодирующего белок — переносчик диаминомонокарбоновых аминокислот (лизина, аргинина, орнитина и цистина). Экскреция всех этих аминокислот увеличена. Из-за плохой растворимости цистина в моче он образует мочевые камни.
Камни возникают в любом возрасте, но чаще между 10 и 30 годами. Рецидивы мочекаменной болезни вызывают нарастающее повреждение почек.
Цистинурию следует заподозрить у любого больного с рецидивами мочекаменной болезни. Экскреция цистина с мочой более 250 мг на 1 г креатинина подтверждает диагноз цистинурии. В моче видны характерные шестиугольные кристаллы цистина. Лечение направлено на предупреждение образования мочевых камней.
Важно, чтобы больной пил много жидкости, не допуская повышения концентрации цистина в моче. Ощелачивание мочи (рН выше 6,5—7) повышает растворимость цистина, но избыточное ощелачивание повышает риск образования фосфатных камней. Некоторым больным показаны комплексобразующие средства: тиопронин или пеницилламин.
Иминоглицинурия — аутосомно-рецессивное заболевание, при котором нарушен канальцевый транспорт глицина, пролина и гидроксипролина. У некоторых больных нарушено также всасывание этих аминокислот в кишечнике. В отличие от гиперпролинемии, гидроксипролинемии, а также от глицинемии без кетоза при иминоглицинурии уровень этих аминокислот в плазме остается в норме. Заболевание доброкачественное, лечение не требуется.
Хартнуповская болезнь — нарушение транспорта моноаминомонокарбоновых аминокислот в почках и тонкой кишке. Уровень этих аминокислот в плазме в норме или понижен. Заболевание наследуется аутосомно-рецессивно, у большинства больных оно протекает бессимптомно, но у некоторых возникают симптомы пеллагры: дерматит по типу солнечного ожога на открытых участках кожи, атаксия и поведенческие расстройства.
К этому приводит дефицит никотиновой кислоты из-за нарушения ее всасывания в кишечнике и повышенного выведения триптофана с мочой. Больным назначают никотинамид.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гомоцистинурия
Гомоцистинурия – наследственный дефект метаболизма, первичным звеном которого выступает нарушение обмена серосодержащих аминокислот, приводящее к поражению нервной, костно-мышечной и сердечно-сосудистой систем. Гомоцистинурия сопровождается умственной отсталостью, судорожным синдромом, подвывихом хрусталиков, катарактой, глаукомой, атрофией зрительных нервов, деформацией грудной клетки, сколиозом, арахнодактилией, артериальными и венозными тромбозами. Диагностика гомоцистинурии включает медико-генетическое консультирование, биохимическое исследование крови и мочи, офтальмологическое обследование, рентген-диагностику костной системы. Терапия гомоцистинурии проводится с учетом формы заболевания и включает диетическое питание, прием витаминов группы В.
Общие сведения
Гомоцистинурия – генетически обусловленная энзимопатия, характеризующаяся нарушением обмена незаменимой аминокислоты метионина, повышением уровня гомоцистина в биологических жидкостях и тканях, приводящим к повреждению органов и систем. Начало изучению заболевания положено в 1962 г. Частота гомоцистинурии в популяции составляет 1 случай на 200 000 новорожденных. Течение гомоцистинурии сопровождается нервно-психическими нарушениями, глазной патологией, изменениями со стороны опорно-двигательного аппарата, склонностью к тромбоэмболиям. В связи с многообразием последствий метаболических расстройств гомоцистинурия рассматривается с позиций различных медицинских дисциплин, главным образом, генетики, педиатрии, неврологии, офтальмологии, ортопедии.
Причины гомоцистинурии
Гомоцистинурия обусловлена аутосомно-рецессивным типом наследования. На сегодняшний день известны 4 типа метаболических нарушений, которые могут лежать в основе патологии, в связи с чем выделяют следующие биохимические варианты заболевания:
Непосредственные патогенетические механизмы патологии связаны с нарушением метаболизма незаменимой аминокислоты метионина. Метаболические процессы контролируются рядом ферментов, при инактивации которых происходит энзиматический блок: в крови и тканях накапливается промежуточный продукт обмена метионина – гомоцистин, который экскретируется с мочой; при этом также уменьшается содержание цистатионина и цистина. Возможной причиной нарушения метаболического пути также может служить гиповитаминоз В6 и В12, а также фолиевой кислоты.
Высокие концентрации метионина и гомоцистина оказывают повреждающее действие на внутреннюю стенку артерий, что сопровождается усилением агрегации тромбоцитов и созданием условий для тромбообразования. Кроме этого, отмечается токсическое действие гомоцистина на нервную, соединительную и другие ткани. В зависимости от особенностей патогенеза различают две формы гомоцистинурии – пиридоксинзависимую (витамин B6-чувствительную) и пиридоксинрезистентную (витамин B6-нечувствительную), что определяет выбор метода лечебного воздействия на организм.
Симптомы гомоцистинурии
Проявления гомоцистинурии нарастают постепенно. Дети рождаются без каких-либо специфических отклонений. В течение первого года жизни развивается умеренно выраженная гипотрофия. Попытки устранить отставание в весе и росте за счет дополнительного введения в рацион белка в виде кефира или творога лишь усугубляют течение заболевания: нарастает дефицит массы тела, нарушается сон, ребенок становится раздражительным и плаксивым, отмечается позднее закрытие родничков, деформации конечностей, задержка психомоторного развития.
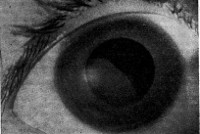
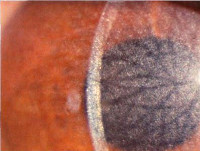
Обычно ярко выраженная клиника гомоцистинурии развивается в течение первых 10 лет жизни, однако часто диагноз становится очевидным уже в раннем детском возрасте. К этому времени у ребенка появляются высокоспецифичные глазные симптомы: подвывих хрусталиков, выраженная близорукость, дрожание радужки (иридодонез). Несколько позднее присоединяются астигматизм, глаукома, катаракта, отслойка сетчатки, атрофия зрительных нервов. Часто гомоцистинурии сопутствуют умственная отсталость, нарушения мышечного тонуса, гиперкинезы, судорожный синдром, поведенческие нарушения. Поражение опорно-двигательного аппарата включает килевидную деформацию грудной клетки, арахнодактилию, кифосколиоз, остеопороз, искривление голеней, полую стопу или плоскостопие, готическое нёбо. Практически половина пациентов с гомоцистинурией сталкивается с артериальными тромбозами (окклюзией церебральных, коронарных, почечных и периферических сосудов), а также венозными тромбозами (ТЭЛА).
Лица, страдающие гомоцистинурией, имеют определенные фенотипические черты: высокий рост, диспропорциональное телосложение (тонкие удлиненные конечности и укороченное туловище), голубые глаза, редкие светлые волосы. У них часто встречаются эритематозные пятна в области скуловых дуг, телеангиэктазии. Внешние проявления гомоцистинурии обладают определенным сходством с синдромом Марфана, однако для последнего не характерно снижение интеллекта и ряд других проявлений.
Диагностика гомоцистинурии
Пациенты с подозрением на гомоцистинурию должны направляться к медицинскому генетику для анализа генеалогических данных и проведения молекулярно-генетической диагностики. Диагноз устанавливается с помощью биохимического исследования крови и мочи: при гомоцистинурии в моче, плазме крови, ликворе обнаруживаются значительные количества гомоцистина, повышение содержания метионина при сниженном уровне цистина. В биоптатах кожи и печени выявляется специфический ферментативный дефект.
Рентгенологическое исследование трубчатых костей и позвоночника обнаруживает системный остеопороз. На ЭЭГ регистрируются нарушения биоэлектрической активности головного мозга, иногда пароксизмального характера. Консультация офтальмолога позволяет подтвердить характерные для гомоцистинурии нарушения со стороны зрительной системы. Также больные дети нуждаются в наблюдении и оценке развития со стороны педиатра, невролога, ортопеда, психиатра. Дифференциальная диагностика гомоцистинурии осуществляется с синдромом Марфана, последствиями родовой травмы и внутриутробных инфекций, другими энзимопатиями.
Лечение гомоцистинурии
Лечебная тактика зависит от формы заболевания (В6-зависимой или В6-резистентной) и во многом схожа с лечением фенилкетонурии. При В6-резистентной форме гомоцистинурии необходимо соблюдение низкобелковой диеты, основанной на ограничении поступления в организм метионина. Рацион пациентов должен состоять, главным образом, из растительной пищи при исключении или значительном снижении употребления продуктов животного происхождения. Для возмещения потребности в незаменимых аминокислотах назначаются специальные аминокислотные смеси, лишенные метионина (XMET Analog, XMET Maxamum, XMET Maxamaid, XMET Homidon). При В6-зависимой гомоцистинурии активность фермента удается активизировать назначением больших доз пиридоксина гидрохлорида.
При любых формах гомоцистинурии снижению уровня гомоцистина в биологических жидкостях способствует назначение фолиевой кислоты, бетаина. Для минимизации риска тромбозов показан постоянный прием ацетилсалициловой кислоты в низкой дозировке. По показаниям больным назначаются гепатопротекторы, ноотропы, препараты кальция, железа; проводятся курсы массажа, лазерной акупунктуры и рефлексотерапии, ЛФК.
Прогноз гомоцистинурии
Выявление заболевания на доклинической стадии, раннее начало лечения и соблюдение лечебной диеты позволяют отсрочить или предотвратить инвалидизирующие осложнения (интеллектуальные нарушения, параличи, атрофию зрительных нервов, легочное сердце, тяжелую артериальную гипертонию, инсульты, инфаркты внутренних органов и др.). В семьях, где есть носители гена гомоцистинурии, необходимо проведение инвазивной пренатальной диагностики с определением активности фермента в культуре клеток ворсин хориона или амниотической жидкости. В отношении детей с гомоцистинурией актуальны вопросы специализированного обучения, профессиональной ориентации, социальной адаптации, диспансерного наблюдения специалистов.
Цистинурия
, MD, Perelman School of Medicine at The University of Pennsylvania
Первоначально цистинурию классифицировали в соответствии с экскрецией цистина с мочой и двухосновных аминокислот в облигатных носителях. В этой классификации родители пострадавших детей были оценены как имеющие либо нормальное (тип I), умеренное (тип III), или значительное (тип II) повышение экскреции цистина.
Более новая классификация основана на генотипе: пациенты типа А имеют гомозиготные мутации гена SLC3A1 и пациенты типа B имеют гомозиготные мутации в SLC7A9. Эти гены кодируют белки, которые в совокупности образуют гетеродимер, ответственный за транспорт цистина и двухосновных аминокислот в проксимальных канальцах. Цистинурию не следует путать с цистинозом ( Наследственный синдром Фанкони Наследственный синдром Фанкони Синдром Фанкони состоит из множественных дефектов реабсорбции в почечных проксимальных канальцах, вызывающих глюкозурию, фосфатурию, генерализованную аминоацидурию и бикарбонатную потерю. Он. Прочитайте дополнительные сведения ).
Патофизиология
При цистинурии реабсорбция других основных аминокислот (лизина, орнитина, аргинина) также нарушена, однако не вызывает никаких расстройств, поскольку для этих аминокислот в отличие от цистина существуют альтернативные системы транспорта. Кроме того, они более растворимы в моче, чем цистин, и их повышенная экскреция не приводит к образованию кристаллов или камней. Их абсорбция (и цистина) также снижена в тонкой кишке.
Клинические проявления
Диагностика
Микроскопическое исследование осадка мочи
Измерение экскреции цистина с мочой
Анализ камней, собранных в почках
Рентгеноконтрастные цистиновые камни образуются в почечных лоханках или мочевом пузыре. Характерно образование коралловидных камней.
Цистин можно обнаружить в моче в виде желто-коричневых гексагональных кристаллов, которые являются диагностическим признаком. Чрезмерное содержание цистина в моче может быть выявлено с использованием теста с нитропруссидом цианида. При цистинурии количественная экскреция цистина, как правило, составляет > 400 мг/день (норма – 30 мг/день).
Лечение
Прием большого количества жидкости
Ограничение потребления натрия
Ограничение потребления белков (при возможности)
Конечная стадия почечной недостаточности Хроническая болезнь почек Хроническая болезнь почек (ХБП) представляет собой длительное прогрессивное снижение почечной функции. Симптомы развиваются медленно и на продвинутых стадиях включают в себя анорексию, тошноту. Прочитайте дополнительные сведения 
Справочные материалы по лечению
1. Claes DJ, Jackson E: Cystinuria: Mechanisms and management. Pediatr Nephrol 27(11):2031–2038, 2012. doi: 10.1007/s00467-011-2092-6
2. Sahota A, Tischfield JA, Goldfarb DS, et al: Cystinuria: Genetic aspects, mouse models, and a new approach to therapy. Urolithiasis 47(1):57–66, 2019. doi: 10.1007/s00240-018-1101-7
Ключевые моменты
Нарушенная мочевая реабсорбция цистина увеличивает уровни цистина в моче, что приводит к образованию цистиновых камней в почках, а иногда и к развитию хронической болезни почек.
Желто-коричневые гексагональные кристаллы в моче являются патогномоничными; количественная экскреция цистина, как правило, составляет > 400 мг/день.
Следует назначить лечение с повышенным потреблением жидкости для обеспечения объема выведения мочи 1,5–2 л/м2/день, и подщелачиванием мочи с помощью калия цитрата или калия бикарбоната.
Необходимо ограничить потребление натрия и белка.
Лекарственные препараты, такие как пеницилламин, тиопронин (в РФ не зарегистрирован) или каптоприл, могут быть необходимыми, но побочные эффекты являются проблемой.
Гомоцистинурия у детей
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Гомоцистинурия у детей
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 3 года)
Гомоцистинурия – наследственное заболевание из группы аминоацидопатий, обусловленное нарушением метаболизма серосодержащих аминокислот, в первую очередь метионина. Относится к классу редких (орфанных) заболеваний.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Две следующие формы гомоцистинурии связаны с генетически детерминированными дефектами реметилирования метионина, возникающими вследствие нарушения активности 5-метилтетрагидрофолат-гомоцистеин-метилтрансферазы (3-я форма, метаболический блок 3 на рисунке 1) и блоком фермента N(5,10)-метилентетрагидрофолатредуктазы(4-я форма, метаболический блок 4 на рис. 1). Указанные две формы сопровождаются не повышением, а снижением концентрации метионина в крови. В педиатрической практике чаще встречаются две первые формы болезни, именуемые классической гомоцистинурией [1,2,11, 14].

Рисунок 1. Схема метаболических процессов, приводящих к развитию гомоцистинурии (по UpTodate.com с изменениями)
Эпидемиология
Средняя частота в общей популяции не определена из-за отсутствия повсеместного неонатального скрининга, есть данные, что она составляет от 1: 58 000 до 1: 335 000, в странах Ближнего Востока (Катар) от 1: 1 800 до 1:8 000. Ген локализован на длинном плече хромосомы 21, в локусе 21q22.1.
Диагностика
В анамнезе возможны указания на родственный брак, наличие сибсов с аналогичными клиническими признаками, наличие у близких родственников ранних инфарктов/инсультов.