Цитограмма ключевые клетки что это значит
Ключевые клетки в мазке на флору: что это значит?

Получить помощь высококвалифицированного гинеколога можно в медицинском центре «МедПросвет». Используя современные методы диагностики, врач быстро определит, почему обнаружены ключевые клетки в мазке у женщины, и подберет оптимальный способ коррекции состояния.
Что значит «ключевые клетки в мазке»?
Ключевыми называют клетки эпителия с нечеткими границами. Они образуются в избыточном количестве с внутреннего слоя стенки влагалища в случае повышения активности микроорганизмов, способных вызывать изменения воспалительного характера. Бесформенность краев обусловлена прикреплением к мембране бактерий, чаще всего гарднерелл.
В норме ключевые клетки в мазке у женщин отсутствуют. Выявление подобных элементов микроскопическим путем указывает на бактериальный вагиноз. Состояние характеризуется нарушением баланса микрофлоры и предрасполагает к развитию воспалительных процессов.
Причины появления ключевых клеток
Микрофлора влагалища в основном представлена палочковыми бактериями (другие названия – молочнокислые бактерии, лактобациллы и палочки Дедерляйна). Продукты их жизнедеятельности обладают следующими свойствами:
Здоровая микрофлора поддерживает стабильность биоценоза влагалища и укрепляет местный иммунитет.
Под действием определенных факторов (прием антибиотиков, применение спермицидов, стрессы, гормональные сбои, погрешности в питании, заражение половыми инфекциями и пр.) количество полезных микроорганизмов может уменьшаться. При этом pH среды половых органов повышается до щелочной реакции, что создает благоприятные условия для размножения условно-патогенных микроорганизмов. В норме они не вызывают заболеваний, но при увеличении численности могут спровоцировать развитие воспалительного процесса.
Чаще всего активизируются микроорганизмы из группы анаэробов, а именно, гарднереллы. Продукты жизнедеятельности этих патогенов повреждают эпителий влагалища. Бактерии прикрепляются к клеткам, чтобы использовать их в качестве питательного субстрата, формируя при этом так называемые ключевые клетки.
Какими симптомами проявляется состояние?
Опасно ли появление ключевых клеток?
Выявление в мазке ключевых клеток указывает на наличие проблем в сфере гинекологии. Опасность представляют не эпителиальные тельца, а микроорганизмы, которые спровоцировали их появление.
Дисбиоз влагалища считается не заболеванием, а синдромом, при котором повышается риск развития инфекционно-воспалительных процессов в органах малого таза. Повышение активности гарднерелл может быть связано с заражением половой инфекцией. Наличие ключевых клеток в мазке на микрофлору служит сигналом о необходимости проведения более детального обследования, поскольку некоторые половые инфекции весьма опасны для репродуктивного и общего здоровья женщины.
Может ли заразиться партнер?
Некоторых женщин волнует, нужно ли ограничивать сексуальные контакты с мужчиной при выявлении ключевых клеток в мазке для профилактики заражения партнера. Дисбиоз влагалища не опасен для здоровых мужчин. При попадании условно-патогенных микроорганизмов в урогенитальный тракт, они быстро нейтрализуются силами местного иммунитета.
Риск возникновения вторичного воспалительного процесса повышается, если женщина игнорирует нарушение микрофлоры и не занимается лечением. В этом случае регулярные незащищенные половые контакты сопровождаются масштабным обсеменением мужских половых органов условно-патогенной флорой и при определенном стечении обстоятельств у партнера может развиться неспецифический уретрит или цистит.
Лечение при ключевых клетках в мазке
При выявлении ключевых клеток в мазке женщине назначают лечение, направленное на устранение патогенных и условно-патогенных микроорганизмов, а также увеличение количества полезных лактобацилл. С этой целью применяют противомикробные средства, а также про- и эубиотики для перорального или интравагинального применения.
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Бактериальный вагиноз
Опубликовано в «РОССИЙСКИЙ ВЕСТНИК АКУШЕРА-ГИНЕКОЛОГА», №6, 2006г. И.С. СИДОРОВА, И.О. МАКАРОВ
Кафедра акушерства и гинекологии факультета последипломного профессионального обучения врачей (зав. — член-корр. РАМН проф. И.С. Сидорова) Московской медицинской академии им. И.М. Сеченова
Bacterial vaginosis
I.S. SIDOROVA, I.O. MAKAROV
Среди женщин репродуктивного возраста бактериальный вагиноз (БВ) встречается у 21—64% [2— 5], среди беременных — у 10—26%. БВ является одним из трех наиболее часто встречающихся инфекционных заболеваний нижнего отдела половой системы, составляя среди них 30—35%, наряду с вагинальным кандидозом (20—25%) и вагинитом, вызванным Trichomonas vaginalis (5—25%).
Термин «бактериальный вагиноз» является адаптированным для того, чтобы подчеркнуть, что бактерии, не являющиеся возбудителями специфических заболеваний, приводят к развитию данной патологии. Бактериальный вагиноз представляет собой клинический синдром, не сопровождающийся явлениями выраженного воспаления и лейкоцитарной реакции, обусловленный патологическим изменением микробиоценоза влагалищной среды, что проявляется чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов (Prevotella/Porphyromonas spp., Bacteroids spp., Peptostreptococcus spp., Eubacterium spp., Fusobacterium spp., Mobiluncus spp., Gardnerella vaginalis— ГВ) и резким снижением числа или отсутствием молочнокислых бактерий [4, 5, 7, 8].
Следует отметить, что широкое распространение ГВ в половых путях здоровых женщин (68% и более) позволяет расценивать эти микроорганизмы как комменсалов, которые только при определенных условиях способны приобретать и проявлять патогенные свойства вместе с другими возбудителями, характерными для БВ. Таким образом, термин «гарднереллез», широко распространенный в отчественной литературе для обозначения «бактериального вагиноза», на самом деле совершенно для этого неприемлем. Под термином «гарднереллез» можно понимать наличие некоего количества гардрелелл во влагалищном содержимом, что не обязательно сопровождается наличием заболевания.
К патологическому изменению микробиоценоза влагалища могут приводить различные патогенные факторы, включая:
Любая инвазия в здоровый эпителий практически всегда сопровождается изменением состава микрофлоры.
Во время беременности причинами нарушения нормального состава микрофлоры влагалища могут являться соответствующие гормональные изменения, использование антибиотиков и т.п. Mobiluncus и некоторые бактероиды в процессе метаболизма вырабатывают янтарную кислоту, оказывающую отрицательное действие на защитную функцию влагалищной среды по отношению к патогенным бактериям. Белковые токсины, вырабатываемые G. vaginalis, оказывают отрицательное воздействие на эритроциты, эндотелиальные клетки и нейтрофилы.
При замещении нормальной лактобациллярной флоры молочнокислыми бактериями, которые не продуцируют перекись водорода, создаются благоприятные условия для развития патогенной микрофлоры. Кроме того, уменьшение количества молочнокислых палочек приводит к снижению содержания молочной кислоты и способствует увеличению рН, что стимулирует рост числа анаэробных микроорганизмов [9, 10].
Клинические проявления и диагностика бактериального вагиноза. Инкубационный период продолжается от 3 до 14 дней. Выделяют 2 варианта течения БВ: бессимптомное (скрытое) и с выраженными симптомами [3—6]. Более чем у половины всех женщин с БВ при наличии положительных лабораторных признаков какие-либо субъективные жалобы и патологические выделения из половых путей (бели) отсутствуют. Воспалительная реакция влагалищного эпителия не является характерным признаком БВ. При БВ с выраженными симптомами отмечаются длительные обильные, жидкие, молочного или серовато-белого цвета гомогенные выделения (бели), преимущественно с неприятным «рыбным» запахом, который может быть постоянным или появляться периодически, во время менструации или полового контакта. Многие пациентки отмечают также начало таких выделений после смены полового партнера. Часто имеет место сочетание БВ с патологическими изменениями шейки матки (явления эктропиона, псевдоэрозии шейки матки и пр.), а само заболевание приобретает рецидивирующее течение. Длительность существования этих симптомов может исчисляться годами [9, 10]. При прогрессирующем процессе выделения приобретают желтовато-зеленоватую окраску, становятся более густыми, тягучими и липкими, обладают свойством пениться, равномерно распределяются по стенкам влагалища. Количество белей варьирует от умеренных до весьма обильных.
Диагностика БВ в настоящее время не представляет трудностей. Необходимо тщательно собрать анамнез с полной характеристикой симптомов, оценкой их продолжительности и выраженности.
Среди перенесенных гинекологических заболеваний у пациенток с БВ наиболее часто встречаются кольпиты. Кроме того, у большинства из них часто выявляются фоновые заболевания шейки матки, такие как эктопия шейки матки, реже — лейкоплакия шейки матки, эндоцервицит и эндометриоз шейки матки с частым рецидивированием патологического процесса после проведенной терапии. Следует отметить, что БВ нередко возникает на фоне нарушений менструального цикла преимущественно по типу олигоменореи или неполноценной лютеиновой фазы.
Во время наружного осмотра пациентки обращают внимание на состояние преддверия и слизистой оболочки влагалища, определяют характер отделяемого, которое оценивают по количеству, цвету, консистенции и запаху. Рекомендуется также провести пальпацию больших желез преддверия влагалища. В области преддверия влагалища отмечаются типичные для БВ бели. Если выделения слишком обильные, то они могут также стекать и на область промежности. При этом обычно наружные половые органы не гиперемированы и не отечны. Однако при наличии сопутствующей инфекции наблюдаются отек и гиперемия слизистой оболочки влагалища.
При исследовании с помощью зеркал также выявляются гомогенные выделения, которые равномерно скапливаются в большей степени по стенкам влагалища, чем в заднем своде, и легко удаляются при помощи тампона. Гиперемия и отечность стенок влагалища также не выявляются.
Материалом для лабораторного исследования является отделяемое сводов и стенок влагалища, цервикального канала и уретры.
Обычно рН влагалищного отделяемого у здоровых женщин репродуктивного возраста менее 4,5. У пациенток с БВ этот показатель значительно выше, составляя обычно 5,0—6,0. рН содержимого влагалища менее 4,5 фактически позволяет исключить диагноз БВ. Следует помнить, что рН содержимого цервикального канала всегда выше, чем содержимого влагалища. Для того чтобы избежать диагностической ошибки, рН исследуют только в содержимом влагалища.
Другим наиболее частым клиническим симптомом БВ является наличие неприятного «рыбного» запаха, который может быть подтвержден с помощью аминового теста с 10% раствором КОН. У здоровых пациенток под действием этого раствора запах не появляется.
Аминовый тест позволяет объективно поставить диагноз у 94% больных БВ. Аналогичным образом объясняется появление «рыбного» запаха во время менструации или полового контакта, когда сперма, имеющая рН около 7, попадает во влагалище и увеличивает рН влагалищного содержимого.
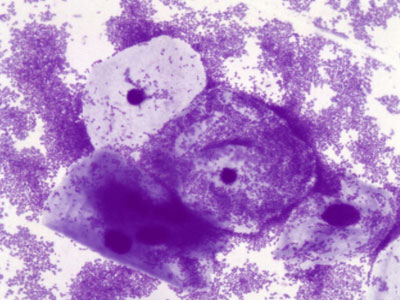
Одним из наиболее специфичных диагностических критериев БВ является обнаружение в отделяемом из влагалища «ключевых» клеток (выявляются при микроскопическом исследовании), которые представляют собой зрелые клетки влагалищного эпителия с адгезированными на них в большом количестве микроорганизмами, расположенными в основном хаотично (как на клеточных элементах, так и вне их). Характерен полиморфизм адгезированных бактерий: кокки, палочки, диплобациллы разной величины с преобладанием мелких форм.
Среди 98,8% женщин, у которых выявляются «ключевые» клетки, имеется БВ.
Однако выявление «ключевых» клеток при микроскопии влажного неокрашенного мазка увеличивает вероятность получения ложноположительного результата, так как часто «ложноключевые» клетки (эпителиальные клетки с адгезированными на них лактобациллами) отождествляют с истинными, что ведет к гипердиагностике БВ.
Более достоверную информацию можно получить при микроскопии вагинальных мазков, окрашенных по Граму, когда «ключевые» клетки легко дифференцировать от «ложноключевых».
Клиническая диагностика БВ основывается на следующих критериях:
Микроскопическая картина влажного препарата мазка отделяемого из влагалища у здоровых женщин представляет собой следующее:
У пациенток с БВ в отсутствие цервицита или вагинита наблюдается следующая микроскопическая картина влагалищного отделяемого:
При БВ во влагалищном отделяемом отмечается резкое снижение количества лейкоцитов, но в цервикальном канале может наблюдаться лейкоцитоз, а в отделяемом уретры содержание лейкоцитов может быть в пределах нормы. Обнаруживаемое увеличение количества базальных и парабазальных клеток может свидетельствовать о воспалительной реакции на стенках влагалища, а также об эстрогенном дефиците. У пациенток с БВ не все эпителиальные клетки могут преобразоваться в «ключевые». Как уже было отмечено, у пациенток с БВ клетки влагалищного эпителия преобладают над лейкоцитами. Если выявлено преобладание лейкоцитов, то, возможно, у этой пациентки имеется другое заболевание, передающееся половым путем. Следует отметить, что, если во влагалищном отделяемом выявляются Т. vaginalis, то весьма вероятно (до 86% наблюдений), что у пациентки имеется и БВ.
При выраженном клиническом течении хламидиоза гарднереллы в мазках встречаются редко и в небольших количествах. По мере редукции хламидий, более чем в 90% случаев отмечается выраженное увеличение количества гарднерелл. В этой связи значительное количество гарднерелл можно расценивать как один из признаков вялотекущего хламидиоза.
Для диагностики БВ возможно также исследование мазков содержимого влагалища, окрашенных по Граму. Чувствительность и специфичность теста в этом случае повышаются до 100%. Однако этот метод не является общепринятым. Подсчет количества микроорганизмов осуществляется при увеличении 1000 и интерпретируется как 1+ ( 30 в поле зрения). В том случае, если в мазке обнаруживаются только молочнокислые палочки или в комбинации с G. vaginalis с преобладанием первых, такая картина характеризуется как нормальная. Для БВ характерны общая массивная микробная обсемененность. Среди микробов преобладают морфотипы облигатных анаэробов и гарднереллы. Лактоморфотипы лактобацилл либо отсутствуют, либо количество их исчисляется единицами (не более 5 в поле зрения). Вагинальный эпителий представлен эпителиальными клетками поверхностных слоев. В 100% случаев обнаруживают «ключевые» клетки. Отмечается отсутствие выраженной лейкоцитарной реакции. Результаты этого исследования имеют прямую взаимосвязь с клинической картиной.
Диагноз БВ может быть также подтвержден при помощи газожидкостной хроматографии. При наличии БВ отмечается увеличение концентрации эфира янтарной кислоты и снижение уровня молочной кислоты, что указывает на вытеснение лактобацилл анаэробными микроорганизмами. Соотношение между этими веществами более 0,4 является патогномоничным признаком БВ. Результаты газожидкостной хроматографии четко коррелируют с клиническими данными и могут служить достоверным средством контроля за эффективностью проводимой терапии. Однако этот метод не является общепринятым для диагностики БВ.
В подавляющем большинстве наблюдений правильно и полно собранный анамнез, внимательное объективное исследование и использование доступных лабораторных тестов позволяет поставить точный диагноз и начать своевременное лечение.
Отмечено, что имеется определенная взаимосвязь БВ с развитием дисплазии шейки матки, воспалительными заболеваниями внутренних половых органов и мочевыводящих путей [1].
БВ и беременность. БВ встречается у 15—20% беременных и является серьезным фактором риска развития инфекционных осложнений. Отмечена выраженная взаимосвязь БВ с преждевременным прерыванием беременности и несвоевременным разрывом околоплодных оболочек. Риск развития этих осложнений по сравнению со здоровыми беременными у пациенток с БВ увеличивается в 2,6 раза. Установлено, что многие бактерии, выявляемые при БВ (Fusobacterium, G. vaginalis, Peptostreptococcus, Micoplasma hominis и др.), обладают способностью вырабатывать в больших количествах α2-фосфолипазу, что вызывает в свою очередь повышенный синтез простагландинов и может привести к развитию преждевременных родов и несвоевременному разрыву околоплодных оболочек. Более того, повышение рН влагалищной среды более 4,5, характерное для БВ, само по себе может привести к преждевременному разрыву околоплодных оболочек. Приблизительно у 10% преждевременно родивших женщин из амниотической жидкости выделяются гарднереллы и другие микроорганизмы, тогда как в норме амниотическая жидкость стерильна. Отмечено, что у женщин, родивших при сроке беременности менее 37 нед имеется высокая вероятность наличия БВ. Хориоамнионит, выявляемый у 1% беременных, является тяжелым осложнением, угрожающим жизни матери и плода. Развитие хориоамнионита, связанное с БВ, у матери впоследствии может привести к возникновению преждевременного прерывания беременности или преждевременному излитию околоплодных вод. Наличие хориоамнионита у пациенток с БВ гистологически подтверждается выявлением соответствующих патогенных микроорганизмов в плацентарной ткани, что также может быть причиной преждевременных родов.
При изучении околоплодных вод у пациенток с БВ также чаще всего выявляется G. vaginalis, Fusobacterium nucleatum, Prevotella melaninogenica, ureaplasma, Candida albicans, E. coli.
Отмечается также связь между наличием БВ и развитием послеродового эндометрита, в том числе после кесарева сечения.
Микробная флора, выявляемая в эндометрии у пациенток с эндометритом, часто бывает аналогична таковой при БВ. Особенно это касается анаэробных микроорганизмов. При нормальном течении послеродового периода на 3-й день количество анаэробов уменьшается в логарифмической прогрессии. Однако у пациенток с БВ этого не происходит, так как обсемененность влагалища анаэробными бактериями у них во много раз превосходит нормальные показатели еще задолго до родов. Установлено, что риск развития послеродового эндометрита у беременных с БВ в 10 раз выше, чем у здоровых женщин.
Смешанная микрофлора при БВ может приводить к развитию и других воспалительных осложнений, таких как абсцесс молочной железы, воспаление пупочной раны и др.
Таким образом, пациентки с БВ входят в группу повышенного риска развития воспалительных заболеваний тазовых органов, преждевременного прерывания беременности, несвоевременного излитая околоплодных вод, возникновения хориоамнионита, послеородового и послеоперационного эндометрита. Высокая концентрация вирулентных микроорганизмов во влагалище пациенток, страдающих БВ, является фактором риска проникновения бактерий в более высокие отделы мочеполовой системы.
Лечение. Целью лечения пациенток с БВ является восстановление у них нормального микробиоценоза влагалища. При этом следует помнить, что у таких больных нередко одновременно могут иметь место и другие заболевания урогенитального тракта (вагинальный кандидоз, трихомонадный вагинит и др.). Поэтому терапия должна носить комплексный этиотропный и патогенетически обоснованный характер, а используемые препараты должны оказывать эффективное разнонаправленное действие.
В процессе лечения необходимо соблюдать правила личной гигиены. До окончания лечения и контрольного наблюдения целесообразно использовать барьерные методы контрацепции.
В настоящее время для этиотропного лечения БВ предлагается целый ряд медикаментозных средств.
Примером комплексного препарата для лечения БВ служит тержинан, который используют местно в виде вагинальных таблеток.
Лечебный эффект препарата и его широконаправленный спектр действия обусловлены его составом.
В препарате содержатся:
Особенностью препарата являются эффективность и быстрота лечебного действия. Тержинан осуществляет качественную санацию влагалища при сопутствующей инфекции, которая с высокой частотой встречается при БВ. Десенсибилизирующее действие в сочетании выраженным противовоспалительным эффектом улучшает кровоснабжение, восстанавливает слизистую оболочку влагалища. Тержинан не подавляет естественную флору влагалища, что упрощает лечение и не требует дополнительного проведения курсов эубиотиков.
Обычно тержинан назначают интравагинально по 1 таблетке в течение 10 дней.
(В целях профилактики достаточно проводить лечение в течение 6 дней).
В качестве иммунокорригирующей терапии в рамках лечения БВ целесообразно использовать кипферон-суппозитории, представляющие собой смесь комплексного иммуноглобулинового препарата (КИП) и интерферона человеческого рекомбинантного альфа-2. Суппозитории вводят ректально 2 раза в день в течение 10 дней.
Обоснованным является и назначение десенсибилизирующих препаратов: кларитин 10 мг 1 раз в день, супрастин по 25 мг 2—3 раза в день и др.
Однако, несмотря на проводимое лечение, отмечаются рецидивы заболевания, возникающие в различные сроки после лечения. В первую очередь это связано с тем, что используемые антибактериальные препараты, уничтожая условно-патогенные микроорганизмы, не способствуют созданию условий для достаточно быстрого восстановления лактобактерий [9, 10].
В этой связи для профилактики возможного рецидива заболевания через 3 нед после окончания основного курса лечения следует исследовать состав микрофлоры влагалища.
В отсутствие кандидоза назначают биопрепараты, действие которых направлено на нормализацию микробиоценоза влагалища.
Лактобактерин, бифидин вводят интравагинально по 2,5—3 дозы 2 раза в день с 10—12-часовыми интервалами, в течение 7—10 дней. Перед употреблением препараты разводят в 5 мл кипяченой воды с добавлением лактозы.
Ацилакт в свечах назначают интравагинально 2 раза в день в течение 7—10 дней.
Если при исследовании мазка будет обнаружен кандидоз, то следует сначала провести его лечение, и только после этого (убедившись что явлений кандидоза нет), назначить перечисленные биопрепараты. При необходимости системной терапии кандидоза рекомендуется использование флюконазола (дифлюкан, флюкостат) однократно внутрь 150 мг. При наличии показаний проводят коррекцию гипофункции яичников общепринятыми средствами. Среди немедикаментозных методов воздействия рекомендуется применение низкочастотного ультразвука.
Критериями эффективности лечения БВ является исчезновение негативных субъективных проявлений заболевания и нормализация лабораторных показателей. Первое контрольное клинико-лабораторное исследование следует проводить через неделю после завершения всей терапии, повторное — через 4—6 нед.
Лечение БВ во время беременности является очень важной задачей, так как изменения флоры влагалищного содержимого могут привести к преждевременному прерыванию беременности, развитию хориоамнионита, послеродового эндометрита и раневой инфекции. При этом нельзя исключать неблагоприятное влияние используемых препаратов. Из-за возможного отрицательного воздействия на плод лечение беременных с БВ назначают обычно после 20 нед гестации.
Одним из наиболее частых сопутствующих осложнений является кандидозный вагинит. Для его профилактики следует назначать нистатин, одновременно с началом лечения. Кроме того, во время беременности для лечения кандидоза широко используют такие препараты, как клотримазол, пимафуцин, и др.
Бактериальный вагиноз и ЗППП. Официально БВ не относят к группе заболеваний, передающихся половым путем. Частое обнаружение ГВ у здоровых женщин позволяет рассматривать данные бактерии как компонент нормальной микрофлоры влагалища. В пользу эндогенного происхождения БВ свидетельствуют патогенетические аспекты развития заболевания вследствие воздействия упоминавшихся ранее факторов, негативно влияющих на состав влагалищной микрофлоры.
Носительство ГВ у здоровых мужчин наблюдается редко. При обнаружении этих микроорганизмов в уретре их не удается выделить из препуциального мешка или аноректальной области. Считается, что простатическая жидкость здоровых мужчин является неблагоприятной средой для ГВ, так как содержит соли цинка, в высоких концентрациях обладающих антибактериальной активностью.
Однако, с одной стороны, отмечена высокая частота реинфекций у излеченных женщин, половые партнеры которых не лечились одновременно. С другой стороны, известно, что БВ преимущественно выявляют у женщин, ведущих активную половую жизнь, часто меняющих половых партнеров. При этом с патогенетической точки зрения, вероятно, частая смена спермы, имеющей свойства подавлять иммунную систему, вызывает местные изменения иммунитета, которые влекут за собой нарушения микробиоценоза влагалища. Кроме того, имеются достоверные данные о том, что попытки лечения половых партнеров не привели к снижению числа рецидивов заболевания у женщин, страдающих БВ.