Цитокинового шторма что это такое при коронавирусе
Неочевидная роль витамина B6 в профилактике цитокинового шторма при Covid-19
Коллектив авторов указывает на растущее количество доказательств того, что витамин B6 обладает защитным эффектом против многих хронических заболеваний
Роль витамина B6 в поддержании иммунного ответа против новой коронавирусной инфекции считается неочевидной для исследователей-нутрициологов.
Фокус исследований в нутрициологии преимущественнно установлен на положительные и широко обсуждаемые свойства витамина D и C, а также таких минералов как цинк и магний, в формировании иммунитета, в том числе на Covid-19. Однако исследования витамина B6 практически не проводятся. Ведущий автор новой статьи из журнала Frontiers in Nutrition надеется, что его работа станет первым важным шагом в раскрытии потенциала витамина B6 в снижении вероятности развития цитокинового шторма.
«В дополнение к базовым гигиеническим мерам, правильное питание также стоит на первой линии профилактики коронавирусной инфекции. Еда – наше первое лекарство, а кухня – первая аптека», – рассказывает доцент Высшей школы интегрированных наук Хиросимского университета Thanutchaporn Kumrungsee.
В своей работе коллектив авторов указывает на растущее количество доказательств того, что витамин B6 обладает защитным эффектом против многих хронических заболеваний, в том числе патологии сердечно-сосудистой системы и сахарного диабета, благодаря подавлению воспалительных процессов, окислительного и карбонильного стресса.
Витамин B6 – собирательное название водорастворимых производных 3-гидрокси-2-метилпиридинов, обладающих биологической активностью пиридоксина. Среди растительных продуктов он содержится в бананах, питайе, батате и фундуке. Пиридоксин синтезируется некоторыми бактериями. Тунец и лосось характеризуются высоким содержанием витамина B6. Также он присутствует в мясных и молочных продуктах, но он менее устойчив к высоким температурам, чем другие формы витамина B, поэтому в варёных и жареных мясных продуктах его мало.
В дальнейшем исследователи из Хиросимского университета планируют проверить гипотезу на клинических испытаниях.
Вторая онлайн-конференция «Covid-19» «Как остановить цитокиновый шторм»
Объявлены 6 победителей Премии Правительства Москвы в области медицины
Церемония вручения Премии Москвы в области медицины состоится 13 ноября в 16:00
Доступ к международным базам данных в области науки и технологий
9 апреля 2020 состоялась вторая онлайн-конференция «Covid-19» «Как остановить цитокиновый шторм».
В конференции принимали участие эксперты из Германии, США, России.
В ходе мероприятия обсуждались проблемы тяжелого течения болезни, цитокинового шторма, ингибирования IL-6, новые алгоритмы ведения больных в стационаре, проблемы выбора оптимального времени для начала патогенетической терапии.
Ниже приведены ответы экспертов на наиболее важные, сложные и актуальные вопросы, поднимаемые на конференции.
Никонов Е.Л.: С момента нашей последней телеконференции произошли достаточно значимые изменения, мы больше не ориентируемся на ПЦР диагностику COVID-19. В настоящее время диагноз коронавирусной инфекции ставится на основании КТ легких, лабораторных анализов и наличия лихорадки.
Мазус А.И: В продолжение разговора в отношении цитокинового шторма. Ведется активная работа с блокаторами IL-6 и есть интересные данные для обсуждения.
Алгоритмы лечения больных COVID-19, выбор оптимального времени для начала патогенетической терапии.
Д. С. Фомина: Презентация.
Я бы хотела обратить внимание на лечение пациентов с COVID-19 Тоцилизумабом.
Данный препарат имеется у нас в клинике (протокол одобрен Департаментом здравоохранения города Москвы)
При обследовании пациентов проводилось стандартное физикальное исследование с оценкой степени тяжести состояния. Для оценки состояния использована новейшая шкала NEWS (National Early Warning Score), рекомендованная к использованию для пациентов с COVID-19.
Выполняется компьютерная томография легких для выявления пневмонии, а также проводятся лабораторные исследования (стандартные и ПЦР) для выявления хронических патологий и оценка ЧДД, ЧСС, АД, SpO2.
Для оценки поражения легких при визуализации на КТ используется 4 значимая шкала (СT-1; CT-2; CT-3; CT-4). ( Усовершенствованная 3 значимая шкала)
Для отобранных больных подбирается тактика лечения.
У пациентов со степенью поражения CT-1 без факторов риска проводится инфузионная и противовоспалительная терапия.
У пациентов с поражением легких 1 степени (CT-1) и 2 и более факторами риска, начинаем лечение с гидроксихлорохина, с возможностью дальнейшей комбинации с азитромицином.
К данной терапии можно добавить препарат Калетра (лопинавир+ритонавир). В данной ситуации мы используем азитромицин с целью иммуномодуляции, а не его бактериальных свойств.
Тактика выбранного лечения зависит от оценки состояния легких на КТ и факторов риска, согласно протоколу. Если терапия не эффективна, то стоит назначить Тоцилизумаб.
Накоплен опыт лечения 77 пациентов при помощи Тоцилизумаба.
Согласно рекомендациям, мы начинали лечение пациентов с COVID-19 Тоцилизумабом, когда они находятся на ИВЛ. Однако мы считаем, что данные сроки лечения не компетентны. Мы считаем, что данный препарат лучше использовать как можно раньше, если стандартный алгоритм лечения не эффективен. Таким образом, появляется шанс, что симптомы быстрее купируются. Преимущества раннего применения Тоцилизумаба – это снижение риска присоединения бактериальной флоры и снижение доли пациентов, которые нуждаются в ИВЛ. Необходимо проанализировать полученные результаты, мы можем набрать контроль-группу с такими же клиническими проявлениями и КТ-рисунком, но не лечившиеся Тоцилизумабом, чтобы сравнить исход.
Юрген Рокштро: у нас у всех достаточно ограниченный опыт в изучении данного вопроса, вследствие, небольшого количества пациентов.
Предвестники цитокинового шторма.
Леонид Марголис: Цитокиновый шторм это очень грозное осложнение, важно выявление его ранних предвестников, чтобы не доводить до стадии, когда необходимо серьезное медикаментозное лечение. В нашей лаборатории на протяжении многих лет изучаются цитокины и цитокиновое высвобождение следствием которого является непосредственно цитокиновый шторм.
Мы не можем не отдать должное цитокиновой сети. Мы знаем о многих цитокинах, об их способностях активировать и дезактивировать целые процессы. Мы изучали цитокиновый шторм в контексте ВИЧ-инфицированных больных и осложненной беременности. Многие цитокины взаимодействуют в первую очередь друг с другом, поэтому когда их изучат по отдельности могут быть отрицательно-положительные или отрицательно-отрицательные результаты.
При изучении преэклампсии и тяжелых родов изучались кривые цитокинового ряда, на которых отчетливо видно их взаимосвязь, а самое главное – все связи пересекались в центре (как круг). Я предлагаю выделить основные цитокины и посмотреть, может быть они и есть предвестники цитокинового шторма, чтобы начать более раннюю и адекватную лекарственную терапию.
Леонид Марголис: У нас есть мультиплекс анализов для измерения 33-36 цитокинов и небольшого количества 25 микролитров. Система действительно очень сложна, и должна быть изучена медицинскими информатиками, она может предоставить дополнительную информацию о ранних предвестниках цитокинового шторма.
Исследование предвестников цитокинового шторма.
Васильева Е.Ю.:
О значении IL-1β
Цыганова Е.В.: Презентация
О значении IL-1β, который может принимать участие в синдроме цитокинового шторма
В патогенезе гриппа IL-1β связан с цитокиновым штормом, приводящим к тяжелым осложнениям и смерти. Также этот цитокин является медиатором воспаления легких и фиброза легких.
Здесь можно увидеть потенциальные показания для блокаторов интерлейкина-1.
Вопрос: «Что вы думаете о таких препаратах, как блокаторы интерлейкина-1; Можно ли использовать их среди пациентов с COVID-19 в тяжелом состоянии?».
Майкл Ледерман: Раз уж мы не знаем, что здесь выступает движущим фактором и регулятором. Здесь перечислены на самом деле очень хорошие схемы. И при таком раскладе каждый получает что-то, и, по крайней мере, вы будете знать, какая из двух стратегий, которые вы сравниваете, более ценна.
Майкл Ледерман: мульти-панельные выделения цитокинов в жидкостях, таких как плазма, а также влияние на иммунные клетки, моноциты, T-клетки, натуральных киллеров, возможно, другие будут очень ценными.
Майкл Ледерман: Мне нравится, предложение взять два разных препарата, сравнивать Тоцилизумаб с одним из них, потому что можно получить гораздо больше от клинического исследования.
Майкл Ледерман: мне нравится подход, когда всё делается сразу, потому что мы находимся в чрезвычайной ситуации.
Предложение взять два разных препарата, сравнивать Тоцилизумаб с одним из них, потому что таким образом вы получите гораздо больше от клинического исследования.
Фомина Д.С.: У меня есть некоторые опасения по поводу пациентов с сопутствующими заболеваниями.
Майкл Ледерман: Вы предлагаете исключить людей с определенными сопутствующими заболеваниями.
Фомина Д.С.: Нет, я думаю, что, если мы включим пациентов с определенными сопутствующими заболеваниями, в которые также вовлечены цитокины, которые мы обсуждаем, мы не раскроем истинную картину, которая имеет место быть при COVID. Это тогда уже будет некая комбинация.
Майкл Ледерман: Я думаю, что это справедливые замечание и опасения. Но я считаю, что величина воздействия, таких как сахарный диабет на цитокины, в которых мы заинтересованы довольно скромные, в сравнение со степенью влияния у больных с COVID.
Юрген Рокштро: Позвольте мне добавить, в настоящее время здесь есть преимущество, что большинство препаратов, которые есть в вашем списке, все лекарства уже лицензированы, и у нас есть огромный опыт применения при других заболеваниях.
К счастью, мы уже имеем огромный опыт назначения (в том числе в сочетании) тех препаратов, которые Вы перечислили. Все это, безусловно, большой плюс для нас.
Материал подготовлен при содействии
Международного учебно-методического центра
Медицинского института Российского университета дружбы народов
Принимайте участие в мероприятиях, событиях и акциях.
Цитокиновый шторм при различных вариантах течения COVID-19
В декабре 2019 года в городе Ухань, Китай, был обнаружен новый штамм коронавируса, вызывающий тяжелый острый респираторный синдром — коронавирус 2 (SARS-CoV-2). Наряду с SARS-CoV и коронавирусом, ассоциированным с ближневосточным респираторным синдромом — (MERS-CoV), SARS-CoV-2 является третьим коронавирусом, вызывающим тяжелые респираторные заболевания у людей, объединенных под названием «коронавирусная болезнь 2019 года» (COVID-19). Эта вспышка была признана Всемирной организацией здравоохранения (ВОЗ) в марте 2020 года пандемией и оказала значительное влияние на экономику и здравоохранение во всем в мире.
Хотя ситуация развивается стремительно, тяжелое течение заболевания, проявляющееся лихорадкой и пневмонией, приводящее к острому респираторному дистресс-синдрому (ОРДС), было описано в 20 % случаев COVID-19. Это напоминает течение ОРДС, вызванного синдромом выброса цитокинов (цитокиновый шторм), и вторичный гемофагоцитарный лимфогистиоцитоз, наблюдаемый у пациентов с SARS-CoV и MERS-CoV, а также у пациентов с лейкемией, получающих Т-клеточную терапию. Учитывая этот опыт, необходимо создание терапевтических средств, основанных на подавлении синдрома выброса цитокинов, таких как тоцилизумаб, которые прошли клинические испытания для лечения COVID-19.
SARS-CoV-2 — это бета-коронавирус, который наиболее тесно связан с SARS-CoV. Оба вируса используют рецептор ангиотензинпревращающего фермента, связанный с карбоксипептидазой (ACE2), чтобы проникнуть в клетки. Этот рецептор повсеместно экспрессируется в сердечной и легочной ткани, а также в некоторых кроветворных клетках, включая моноциты и макрофаги. Ключевой особенностью инфекции COVID-19 является лимфопения (низкий уровень лимфоцитов в крови), которая коррелирует с клинической тяжестью процесса. При SARS-CoV инфицируются моноциты и дендритные клетки, тогда как при MERS-CoV инфицируются моноциты и Т-клетки через дипептидилпептидазу 4 (DPP4). Возможно, что SARS-CoV-2 также поражает дендритные клетки. Апоптоз и истощение пула Т-клеток в результате нарушения процессов активации из-за дисфункции дендритных клеток может способствовать патологии иммунной системы при COVID-19. Однако лимфопения не является специфическим биомаркером неблагоприятного прогноза при COVID-19, поскольку она также является биомаркером, который коррелирует с летальным исходом в пандемии гриппа A (H1N1) 2009 года.
Было установлено, что цитокиновый шторм является основным фактором тяжелого течения SARS-CoV и MERS-CoV у пациентов. Повышенные сывороточные концентрации интерлейкина-6 (IL-6) и других провоспалительных цитокинов являются признаками тяжелого течения инфекции MERS-CoV. Синдром высвобождения цитокинов часто встречается у пациентов с COVID-19, а повышенный уровень IL-6 в сыворотке коррелирует с дыхательной недостаточностью, ОРДС и неблагоприятными клиническими исходами. Повышенный уровень C-реактивного белка (CРБ),экспрессия которого стимулируется IL-6, также является биомаркером тяжелой бета-коронавирусной инфекции.
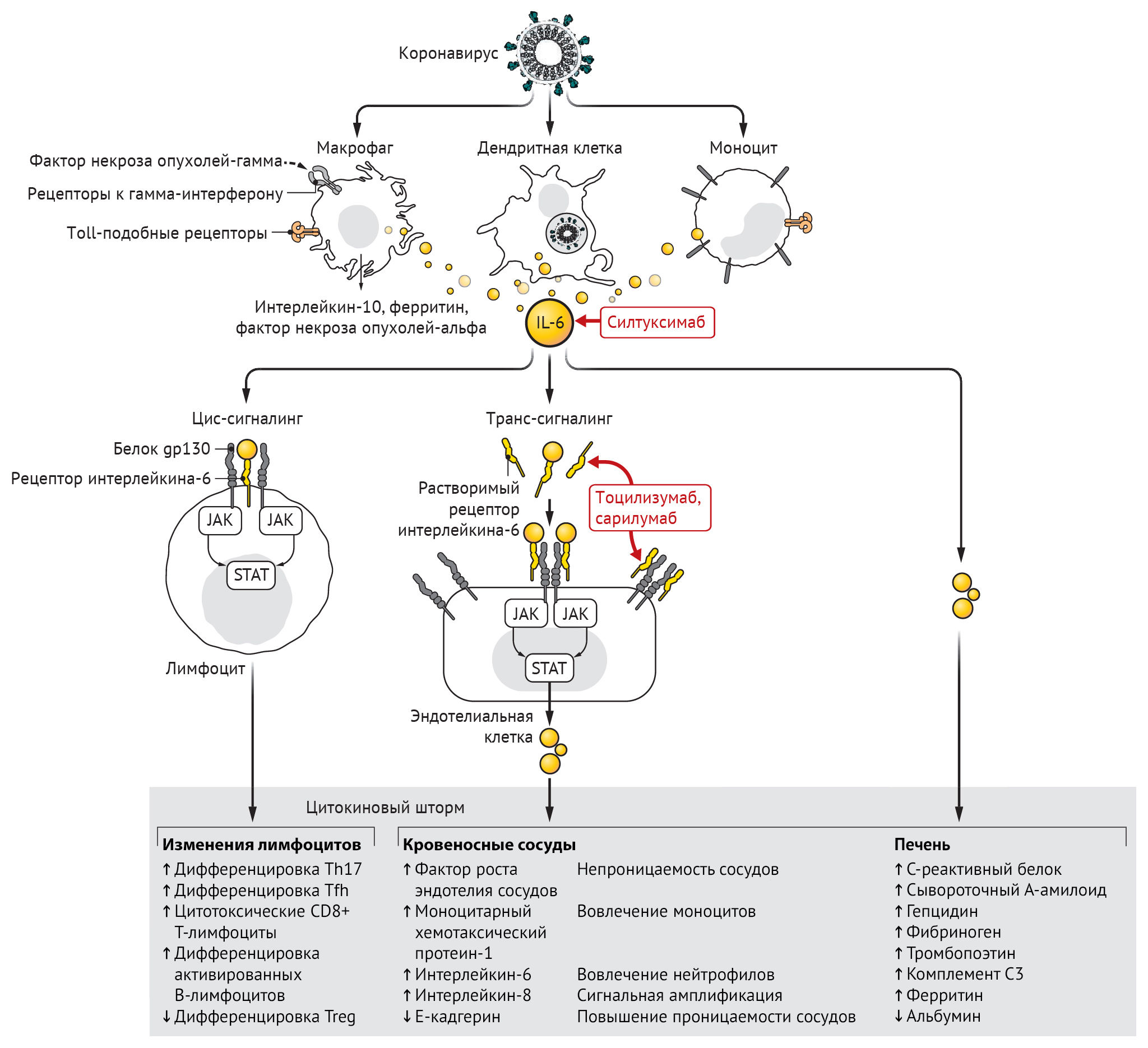
Инфицирование бета-коронавирусом моноцитов, макрофагов и дендритных клеток приводит к их активации и секреции IL-6 и других провоспалительных цитокинов. IL-6 обладает выраженными провоспалительными свойствами (см. рис. 1). IL-6 может передавать сигналы по двум основным путям, которые называются классической цис-передачей или транс-передачей. При передаче цис-сигналов IL-6 связывается с мембраносвязанным рецептором IL-6 (mIL-6R) в комплексе с gp130; нисходящая сигнальная трансдукция опосредуется, в свою очередь, JAKs (Janus kinases) и STAT3 (сигнальный преобразователь и активатор транскрипции-3). Связанный с мембраной комплекс gp130 экспрессируется повсеместно, в отличие от mIL-6R, экспрессия которого ограничена в основном иммунными клетками. Активация передачи сигналов в рамках цис-передачи приводит к плейотропным эффектам на приобретенный иммунитет (В- и Т-клетки), а также врожденную иммунную систему [нейтрофилы, макрофаги и естественные клетки-киллеры (NK)], которые могут вносить вклад в возникновение цитокинового шторма.
При передаче сигналов высокие концентрации циркулирующих IL-6 связываются с растворимой формой IL-6R (sIL-6R), образуя комплекс с димером gp130 на всех клеточных поверхностях. В результате сигнальный каскад IL-6-sIL-6R-JAK-STAT-3 активируется в клетках, которые не экспрессируют mIL-6R, таких как эндотелиальные клетки. Это приводит к системному «цитокиновому шторму», включающему секрецию сосудистого эндотелиального фактора роста (VEGF), хемоаттрактантного белка моноцитов–1 (МСР-1), IL-8 и дополнительного IL-6, а также снижение экспрессии E-кадгерина на эндотелиальные клетки. VEGF и пониженная экспрессия E-кадгерина способствуют проницаемости сосудов, которые участвуют в патофизиологии гипотонии и легочной дисфункции при ОРДС.
Вторичный гемофагоцитарный лимфогистиоцитоз — это гипервоспалительный синдром, характеризующийся высвобождением цитокинов, цитопенией (низкое количество клеток крови) и полиорганной недостаточностью (включая печеночную). У взрослых вторичный гемофагоцитарный лимфогистиоцитоз чаще всего связан с тяжелыми вирусными инфекциями, но также встречается у пациентов с лейкемией, получающих специальную Т-клеточную терапию. В дополнение к повышенным уровням цитокинов для вторичного гемофагоцитарного лимфогистиоцитоза характерны высокие уровни ферритина в сыворотке крови. Экспрессирующие CD163 макрофаги выступают в качестве источника ферритина. Учитывая их роль в передаче сигналов ретикулоэндотелиального железа, вторичный гемофагоцитарный лимфогистиоцитоз известен также как синдром активации макрофагов. Ретроспективное исследование пациентов с COVID-19 показало, что повышение сывороточного ферритина и IL-6 коррелировало с уровнем выживаемости и наблюдалось у погибших.
У пациентов, получающих CART-терапию (лечение Т-клетками химерного рецептора антигена (chimeric antigen receptor — CAR)), также могут развиться как цитокиновый шторм, так и вторичный гемофагоцитарный лимфогистиоцитоз. CART-терапия включает перепрограммирование Т-лимфоцитов пациента с целью повышения экспрессии на них молекул CAR, которые распознают антигены на опухолевых клетках. При переливании этих перепрограммированных клеток обратно пациенту они нацеливаются на опухолевые клетки, тем самым активируя противоопухолевый иммунный ответ. Эмили Уайтхед, первый пациент, получивший CD19-нацеленные Т-клетки CAR-19 с целью лечения острого лимфобластного лейкоза в 2012 году, побочным эффектом получила тяжелую форму цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза, что привело к развитию ОРДС, полиорганной недостаточности и гипотонии, которая была невосприимчива к стандартному лечению стероидами. Из-за значительного повышения сывороточного IL-6 у этой пациентки эмпирически было принято решение о начале терапии тоцилизумабом, антагонистом IL-6R, одобренным в то время для лечения ревматических состояний, таких как ювенильный идиопатический артрит. Она получала однократную дозу тоцилизумаба на 7-й день после введения CARТ-лимфоцитов. Спустя несколько часов у пациентки снизилась температура, после чего было принято решение об отмене лечения гипотонии и отказ от поддержки ИВЛ после разрешения ОРДС. В настоящее время тоцилизумаб с подтвержденной эффективностью и минимальными побочными эффектами у сотен пациентов одобрен Управлением по контролю за продуктами и лекарствами США (FDA) для лечения заболеваний, протекающих с синдромом цитокинового шторма, вызванного CARТ-терапией.
Эффективность антагонистов IL-6-IL-6R для лечения цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза подчеркивает центральную роль передачи сигналов IL-6 в патофизиологии цитокин-управляемых гипервоспалительных синдромов. Тяжелые случаи COVID-19 можно лечить как раз путем ингибирования пути IL-6, учитывая связанные с цитокиновым штормом и подобным вторичному гемофагоцитарному лимфогистиоцитозу повышения цитокинов в сыворотке крови. Действительно, предварительные результаты исследования 21 пациента с COVID-19, получавшего тоцилизумаб в Китае, обнадеживают: лихорадка спадала у всех пациентов в течение первого же дня приема тоцилизумаба. Потребность в кислороде была снижена у 75 % пациентов.
Во всем мире проводятся контролируемые клинические испытания с целью тестирования эффективности антагонистов IL-6 и IL-6R для лечения пациентов с COVID-19 с тяжелыми респираторными осложнениями. Один вопрос, который необходимо решить, заключается в том, будет ли иметь место дифференциальная эффективность между антагонистами IL-6 и антагонистами IL-6R. Относительно этого поднимается вопрос, что ингибиторы IL-6R могут подавлять как цис-, так и транс-передачу сигналов, а также транс-презентацию, недавно описанный третий способ передачи сигналов. Транс-презентация включает связывание IL-6 с mIL-6R, экспрессируемым на иммунной клетке, которая образует комплекс с gp130 на клетках T-хелпера-17 (TH17), что приводит к передаче сигналов Т-клеток вниз по каскаду, который может приводить к ОРДС. Однако ингибиторы IL-6 могут подавлять только цис- и транс-передачу сигналов. Непосредственная цель применения антагонистов IL-6 состоит в том, чтобы облегчить течение тяжелых случаев COVID-19 и свести к минимуму потребности в интенсивной терапии данных пациентов. Долгосрочная цель должна заключаться в разработке противовирусных препаратов и вакцин, которые предотвращают инфекцию или облегчают ее течение.
Есть ряд предостережений, которые необходимо брать во внимание, учитывая глобальную потребность в терапии COVID-19. При сепсис-ассоциированном ОРДС часто назначают кортикостероиды. Однако применение кортикостероидов у пациентов с SARS и MERS не улучшило показатели выживаемости и не привело к каким-либо изменениям вирусного клиренса. В результате консенсус экспертов-инфекционистов из профильных институтов и ВОЗ рекомендует клиницистам избегать системных кортикостероидов у пациентов с COVID-19 в настоящее время. Теоретическая возможность состоит в том, что подавление воспаления антагонистами IL-6 может задержать выведение вируса из организма. Однако блокада IL-6 также приводит к быстрому снижению сывороточного IL-10, иммуносупрессивного цитокина, секретируемого макрофагами, что может смягчить опасения по поводу продления клиренса вируса. Более того, одна или две дозы антагониста IL-6 вряд ли приведут к таким осложнениям, как грибковые инфекции или остеонекроз челюсти, возникающие у пациентов, которым ежемесячно вводят эти препараты для лечения хронических состояний, например, ревматоидного артрита. Примечательно, что тоцилизумаб был впервые одобрен для лечения ревматических заболеваний, а затем — цитокинового шторма у пациентов, получающих CARТ-терапию, и в настоящее время подвергается «перепрофилированию» для борьбы с пандемией COVID-19. Вполне возможно, что направленная на IL-6 терапия будет использоваться в лечении пациентов на случай будущих пандемий, вызванных другими вирусами, таких как грипп и лихорадка Эбола.
Не ПЦРом единым. Как не пропустить опасные осложнения COVID-19
Часто осложнения COVID-19 опаснее самой инфекции, и большинство летальных исходов при коронавирусной инфекции связаны именно с осложнениями. Учитывая стремительное ухудшение эпидемиологической обстановки, постоянные мутации вируса и увеличение случаев тяжелого течения COVID-19 даже среди молодых людей, чтобы спасать жизни, необходимо действовать очень быстро. В большинстве случаев развитие осложнений можно предотвратить, если вовремя на них отреагировать и выработать индивидуальную стратегию медицинского сопровождения. А спрогнозировать тяжелое течение и вовремя принять необходимые лечебные меры поможет лабораторная диагностика.
SARS-CoV 2 затрагивает не только легкие – под ударом весь организм. Осложнения COVID-19 проявляются в виде поражения сердца и сосудов, мозга, печени и почек, системы кроветворения, а новый штамм «Дельта» почти в 15% случаев затрагивает еще и ЖКТ. Особо опасны изменения в системе гемостаза, воспалительные процессы в органах и системах, а также присоединение бактериальной инфекции. Поэтому жизненно важно контролировать состояние не только легких, но оценивать изменения биохимических и гематологических маркеров, параметров гемостаза и лабораторных предикторов острого воспаления.
Для оценки степени поражения самых уязвимых органов и систем в ДІЛА доступны следующие комплексные исследования:
Комплексы помогут обнаружить специфические биологические маркеры развития осложнений и снизить вероятность их появления.
В программу «Оценка состояния организма при COVID-19, минимальный» входит исследования наиболее важных показателей:
Таким образом, лабораторные комплексы от ДІЛА помогут определить общее состояние как системы кроветворения, так и других органов и систем организма, выявить острые воспалительные процессы, контролировать развитие дыхательной недостаточности и септических осложнений у пациентов с диагностированным COVID-19. Маркеры, входящие в состав программ, также позволят диагностировать обменные нарушения, развитие полиорганной недостаточности, наличие процессов тромбообразования.
Самые опасные осложнения
Несмотря на то, что COVID-19 является, прежде всего, инфекцией дыхательных путей, опыт борьбы с SARS-COV-2 во всем мире указывает, что COVID-19 – заболевание системное, затрагивающее не только легкие, но также сердечно-сосудистую, нервную, кроветворную, пищеварительную, иммунную и эндокринную системы.
Большинство этих осложнений проявляются характерными изменениями биохимических маркеров – С-реактивного белка, ферритина и Д-димера, а также изменениями коагулограммы и результатов общего анализа крови. Рассмотрим эти маркеры подробнее.
Лабораторные предикторы осложнений
Воспаления и «цитокиновый шторм». В ответ на инфицирование SARS-CoV-2 запускается реакция макрофагов, которые провоцируют воспалительный процесс. Воспаление проявляется повышением уровня специфических маркеров:
На фоне воспалительных процессов и «цитокинового шторма» развивается прогрессирующая полиорганная недостаточность, поэтому расширенные комплексы дополнительно включают определение уровней креатинина, АСТ, АЛТ, общего билирубина и лактатдегидрогеназы (ЛДГ), а также тропонина I и прокальцитонина:
Также диагностическую ценность имеет определение концентрации интерлейкина IL-6 – противовоспалительного цитокина, являющегося главным участником цитокинового шторма. Интерлейкин-6 – чувствительный маркер острых системных воспалений, который поможет вовремя выявить повышенный нерегулируемый иммунный ответ организма под воздействием коронавируса (синдром высвобождения цитокинов). Он приводит к повреждению тканей (часто легочной) и органов, тяжелому течению инфекции с возможным летальным исходом. Определение уровня IL-6 показано пациентам с тяжелым течением COVID-19.
Нарушения со стороны системы кроветворения. COVID-19-ассоциированная коагулопатия, которая сопровождается нарушением системы свертываемости крови, может стать причиной почечной недостаточности, ухудшения работы печени, сердца, органов ЖКТ. Страдают также эндокринная и нервная системы. Поэтому мониторинг маркеров коагуляции является важным критерием оценки рисков тромбоэмболических осложнений у пациентов с диагностированным COVID-19.
К этим маркерам относятся:
Систематический контроль параметров гемостаза требуется не только при тяжелом течении COVID-19, но даже в случае отсутствия характерных клинических проявлений инфекции. В совокупности все эти гемостатические изменения могут указывать на опасные формы коагулопатии и предрасположенность к тромбоэмболическим проявлениям.
Для оценки общего состояния всей системы кроветворения в состав всех комплексов также включен развернутый анализ крови. Он позволяет своевременно обнаружить и отследить в динамике опасные состояния:
Изменения гематологических параметров также прогностически опасны.
Как видно, программы содержат множество показателей и предназначены для всесторонней оценки состояния разных органов и систем при диагностированном COVID-19. Оценить полученные результаты может только врач. Поэтому с полученными результатами исследования необходимо обратиться к терапевту или семейному врачу, а если есть отклонения от референсных значений – обратиться немедленно, так как состояния вроде цитокинового шторма опасны для жизни и могут развиваться очень быстро.
Когда и кому проходить исследование?
Комплексы позволяют из одной пробы крови получить все необходимые данные для быстрой оценки состояния организма и определить, входите ли вы в группу риска по развитию осложнений COVID-19.
Исследование рекомендуется пройти в обязательном порядке людям следующих категорий:
Даже если вы не относитесь ни к одной из групп риска и у вас легкое либо среднетяжелое течение коронавирусной инфекции, но вы ощущаете ухудшение самочувствия и состояния (обычно наблюдается на 5-10 день болезни), также рекомендуется пройти обследование. Это необходимо для оценки тяжести состояния, обширности поражений и определения потребности в госпитализации, в том числе экстренной.
Заключение
Тяжелое инфекционное заболевание, вызванное коронавирусом SARS-CoV 2, с эпидемической вспышки в Ухане быстро переросло в пандемию с миллионами летальных случаев и сотнями миллионов зараженных. В Украине и в мире количество больных вновь увеличивается. И, если год назад COVID-19 называли, прежде всего, инфекцией дыхательных путей, то сегодня его рассматривают как системное заболевание, поражающее многие органы и системы.
Наряду с такими факторами риска, как возраст и наличие сопутствующих заболеваний, некоторые лабораторные параметры заблаговременно могут указывать на тяжелое течение COVID-19 и повышенный риск смертности:
Комплексы рекомендуется проходить не только людям из группы риска, но и всем, у кого ПЦР-тест подтвердил инфицирование коронавирусом SARS-COV-2. Маркеры, входящие в состав программы, позволят диагностировать опасные для жизни осложнения и своевременно назначить соответствующую терапию.
Не стоит забывать, что осложнения и последствия COVID-19 могут сохраняться в течение нескольких месяцев, и проявляться в виде постковидного синдрома, диагностика и мониторинг которого также проводится с помощью лабораторных маркеров. Поэтому переболевшим обязательно нужно проверять состояние своего здоровье и вовремя принимать соответствующие меры.