Цитомегаловирус что это такое симптомы
Цитомегаловирус. Чем он опасен и как можно заразиться. Симптомы, диагностика и лечение цитомегаловируса.
1. Что такое цитомегаловирус и способы заражения?
Цитомегаловирус – это вирус герпеса. Он встречается очень часто. Цитомагаловирусом к 40 годам заражены примерно 80% людей. Но обычно вирус находится в спящем состоянии и не причиняет никакого беспокойства большинству людей. Здоровая иммунная система легко сдерживает проявление цитомегаловируса. Тем не менее, цитомегаловирус может вызвать тяжелые заболевания у людей с ВИЧ (вирусом иммунодефицита человека). Вирус становится активным, когда иммунная система ослаблена, поэтому его называют оппортунистической инфекцией. Самые распространенные заболевания, которые может вызвать цитомегаловирус – это ретинит, глазная инфекция, способная привести к слепоте.
Как можно заразиться цитомегаловирусом?
Заражение цитомегаловирусом от случайного прикосновения носителя вируса маловероятно. Но заразиться можно, прикоснувшись к глазам, носу или рту после контакта со слюной, спермой, вагинальными выделениями, кровью, мочой, грудным молоком зараженного человека. Кроме того, заразиться цитомегаловирусом можно при сексуальном контакте, переливании крови и пересадке органов.
Младенец может заразиться цитомегаловирусом еще до рождения. Дети получают вирус и вместе с грудным молоком. Это обычно происходит, если женщина впервые заражается цитомегаловирусом во время беременности.
2. Симптомы заболевания
Большинство людей, которые инфицированы цитомегаловирусом, не знают об этом. Вирус обычно не вызывает никаких симптомов. Тем не менее, из-за цитомегаловируса могут появиться слабые симптомы – усталость, опухание желез, лихорадка. Эти симптомы цитомегаловируса легко спутать с признаками других заболеваний. Если цитомегаловирус не лечить, он может распространиться по организму и вызвать целый ряд разных симптомов:
3. Диагностика цитомегаловируса
Врач может диагностировать цитомегаловирус следующими способами:
4. Лечение болезни
Для лечения цитомегаловируса используются специальные препараты. Часто их нужно вводить внутривенно, к примеру, курсом в течение двух недель. После того, как инфекцию удается взять под контроль, может назначаться поддерживающая терапия – ежедневный прием таблеток. Есть препараты, которые целенаправленно используются для лечения поражений глаз от цитомегаловируса.
Есть ряд препаратов, которые напрямую не лечат цитомегаловирус, но сдерживают его рост и замедляют развитие болезни.
Лекарства для лечения цитомегаловируса достаточно сильные и могут вызвать серьезные побочные эффекты – нейтропению (снижение количества белых клеток крови), усталость (анемию), тошноту или рвоту, сыпь, снижение уровня гормона тестостерона. Ряд препаратов дает побочный эффект в виде проблем с почками. Впрочем, ряд препаратов поможет справиться с этими неприятными проблемами во время лечения цитомегаловируса.
Заболевания 
Жалобы и симптомы 
Диагностика 
Наши цены 
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения
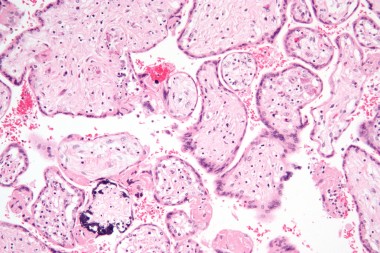
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
История
Исходя из теории ко-эволюции вирусов с их хозяевами, считается, что герпетические вирусы появились в кембрийский период. В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
Характеристика возбудителя
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Патогенез
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Клиника ЦМВИ
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
У новорожденного антенатальная ЦМВИ проявляется симптомами «тяжелой инфекции» с полисистемным поражением: задержкой внутриутробного развития, часто — недоношенностью, гепатоспленомегалией, затяжной неконъюгационной и конъюгационной желтухой, тромбоцитопенической пурпурой, анемией, ДВС-синдромом с кровоизлиянием во внутренние органы, прежде всего в мозг, пневмонией, микроцефалией, хориоретинитом, увеитом, кардитом, различными вариантами поражения центральной нервной системы, в том числе продуктивным вентрикулоэнцефалитом с прогрессирующей гидроцефалией, а также — кортикальными или мозжечковыми пороками развития [13]. В дальнейшем этим детям присущи недостаточная прибавка веса, задержки психического и моторного развития, мышечная слабость, часто — длительная субфебрильная температура, стойкая анемия и тромбоцитопения, длительный гепатит с холестатическим синдромом и высоким риском фиброза и цирроза печени, мальабсорбция.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Цитомегаловирус

Наиболее распространенным методом обнаружения ЦМВИ (цитомегаловирусной инфекции) является анализ крови на цитомегаловирус. Существуют различные методики обнаружения возбудителя, которые позволяют надежно определить наличие возбудителя. Большинство тестов основано на обнаружении специфических антител, вырабатываемых организмом в ответ на возбудитель. Возможна и ПЦР диагностика, которая дает информацию о наличии ДНК возбудителя в крови, позволяет оценить активность протекания инфекционного процесса и степень распространения возбудителя в организме.
Наиболее распространенным методом обнаружения ЦМВИ (цитомегаловирусной инфекции) является анализ крови на цитомегаловирус. Существуют различные методики обнаружения возбудителя, которые позволяют надежно определить наличие возбудителя. Большинство тестов основано на обнаружении специфических антител, вырабатываемых организмом в ответ на возбудитель. Возможна и ПЦР диагностика, которая дает информацию о наличии ДНК возбудителя в крови, позволяет оценить активность протекания инфекционного процесса и степень распространения возбудителя в организме.
Цитомегаловирусная инфекция человека это вирусное антропонозное заболевание поражающее практически весь организм. Характеризуется большой вариабельностью форм и симптоматики – от бессимптомного носительства до тяжелейших поражений дыхательной, выделительной и других систем организма.
Возбудители инфекции, ее источники
Цитомегаловирус (Cytomegalovirus hominis) относится к роду ДНК-вирусов, отличается большими размерами вириона (до 300 нм), входит в семейство герпесвирусов. Зарегистрировано несколько штаммов возбудителя:
Источником заражения является больной либо носитель. Возбудитель определяется в биологических жидкостях и выделениях. Пути проникновения вируса:
Большинство штаммов малоизученны, достоверно известно, что все они могут репродуцироваться, не уничтожая клетку-носитель. Вирус способен длительно сохранятся при комнатной температуре, но чувствителен к нагреву и действию дезинфицирующих средств.
По статистическим данным показатель инфицированности составляет до 95%, в зависимости от региона и страны.
Классификация
Общепринятой на мировом уровне системы классификации цитомегаловирусной инфекции (ЦМВИ) нет. На практике применяется классификация, разработанная в 1980 году. Согласно этой системе ЦМВИ делится на:
По длительности течения выделяют ЦМВИ:
В зависимости от тяжести течения бывает легкая, среднетяжелая, тяжелая формы протекания.
Механизм зарождения и развития болезни
Вирус попадает в организм через слизистый эпителий различных органов. Свободное нахождение вирусных частиц в кровеносном русле быстро заканчивается внедрением возбудителя в фагоциты мононуклеарного типа. В них происходит начальная репликация цитомегаловируса.
Зараженные клетки увеличиваются, в них можно обнаружить крупные внутриядерные включения, которые являются скоплениями вирусных тел. Увеличение количества пораженных клеток проявляется развитием множественных узелковых инфильтратов либо кальцификатов в тканях. Особенно активно размножение возбудителя в слюнных железах, в которых его проще всего обнаружить.
Возбудитель способен длительно сохранятся в клетках, единственным проявлением инфекции будет подавление клеточного иммунитета. У большинства болезнь протекает скрыто и переходит в бессимптомное носительство.
Обострение ЦМВИ возникает у больных с подавленным иммунитетом. Наиболее частые причины ослабления защитных сил организма:
В результате вирус активируется, начинается активное размножение возбудителя во всех органах и тканях, развивается клиника одной из форм заболевания. Тяжелые поражения ЦМВИ в большинстве случаев ассоциированы с ВИЧ-инфекцией.
Клиническая картина
Продолжительность инкубационного периода остается невыясненной так как начальные формы ЦМВИ протекают латентно. Характерные клинические симптомы развиваются в результате воздействия факторов, ослабляющих иммунитет.
Врожденная ЦМВИ-инфекция у детей в ранних периодах жизни также протекает как бессимптомное носительство. Затем проявляется в виде различных тяжелых осложнений, наиболее частые:
В особо тяжелых случаях врожденная ЦМВ-инфекция приводит к возникновению вторичных патологий и летальному исходу в первые недели жизни. Избежать этих последствий можно сделав анализ крови на цитомегаловирус перед зачатием ребенка.
Острая врождённая ЦМВИ
Является следствием первичного заражения матери в процессе беременности. Развивается примерно у 5% детей заразившихся ЦМВ-инфекцией внутриутробно. В остальных случаях протекает скрыто, не приводит к серьезным последствиям. Летальность острой врожденной ЦМВ-инфекции высока, составляет до 30% от заболевших. Выжившие дети зачастую страдают от тяжелых последствий, в их перечень входят:
Если заражение ребенка произошло на ранних сроках эмбриогенеза, плод с высокой вероятностью погибнет. У выживших наблюдаются серьезные дефекты и аномалии развития:
Летальность при развитии этой формы инфекции невысока, она характеризуется развитием тяжелых патологий органов и систем ребенка. В их число входят: гидро- и микроцефалия, помутнение хрусталика, глухота, микрогирия (недоразвитость извилин головного мозга).
Приобретённая ЦМВ-инфекция
У большинства зараженных протекает без выраженной клиники, в виде субклинической формы либо латентного вирусоносительства. Переход в клинически выраженное заболевание наблюдается при различных нарушениях в работе иммунитета возникающих под воздействием разнообразных факторов риска.
При этом развивается острая приобретенная ЦМВИ, симптомы которой схожи с вирусным гепатитом либо инфекционным мононуклеозом. Может протекать скрытно, выявляется случайно при скрининговом анализе крови на цитомегаловирус.
Еще одна часто встречающаяся форма приобретенной ЦМВ-инфекции – мононуклеозоподобный синдром. Клинические проявления этой формы практически идентичны другому заболеванию, вызванному герпесвирусом Эпштейна-Барра – инфекционному мононуклеозу.
Период инкубации может длиться до 60 дней. Активная фаза заболевания начинается с гриппоподобных симптомов: длительной лихорадки, озноба, выраженных болей в мышцах, суставах, сильной утомляемости. Больные часто жалуются на першение в горле, наблюдается увеличение региональных лимфоузлов, кожные высыпания.
Изредка возможно проявление симптомов гепатита, таких как желтуха. В анализе крови наблюдается увеличение ферментов печени (АлАТ, АсАТ). Возможно развитие пневмонии, вероятность поражения легких составляет 5-6%.
Длительность заболевания может составлять до 1-2 месяцев, после чего у большинства больных происходит полное выздоровление. Некоторые симптомы сохраняются дольше, например, увеличенные лимфоузлы могут сохраняться на срок до полугода.
Приобретенная Цитомегаловирусная инфекция у новорожденных
Развивается в результате инфицирования новорожденного при прохождении родовых путей либо на начальных этапах жизни – при вскармливании грудью, контактах с носителями вируса. У большинства детей бессимптомно преобразуется в форму носительства.
Клинические симптомы проявляются в случае тяжелой недоношенности либо маловесности ребенка. Инфекция протекает в виде длительной пневмонии, часто присоединяется бактериальное поражение дыхательной системы. Не исключено развитие гепатита, увеличение лимфоузлов, задержки в умственном, физическом развитии. При беременности необходимо сдавать массу анализов, которые помогают выявить наличие не только ЦМВ-инфекции, но и токсоплазмоза.
Генерализованная форма ЦМВ-инфекции
Развивается у зараженных с крайне ослабленным иммунитетом. Отличается серьезным повреждением печени, нервной системы, ЖКТ, легких. Степень тяжести патологии зависит от состояния иммунной системы, особенно тяжелые проявления наблюдаются у принимающих иммуносупрессоры и больных СПИДом.
Основные клинические проявления при генерализованной ЦМВ-инфекции:
Диагностика инфекции
В обычном анализе крови у страдающих ЦМВ-инфекцией наблюдается:
В пробах спинномозговой жидкости у пациентов с поражением ЦНС выявляют увеличение белковых компонентов, нейтрофильный плеоцитоз и значительное снижения уровня глюкозы.
Лечение
Основана на проведении серологических исследований крови на цитомегаловирус – обнаруживаются специфические для этой инфекции антитела. В их число входят:
Профилактика
Субклинические формы ЦМВ-инфекции и латентное носительство крайне распространены, поэтому в большинстве случаев не требуют специфического лечения, даже при выявлении специфических антител. Лечения таких форм цитомегаловируса направлено на усиление защитных сил организма при помощи иммуномодуляторов и профилактику факторов риска, которые приводят к обострению заболевания.
Для лечения клинически активных форм ЦМВ-инфекции применяют 3 препарата, обладающих достаточной эффективностью:
Эти препараты противопоказаны для применения беременным. В этом случае назначается патогенетическая терапия. В нее входят разнообразные препараты интерферона (виферон, роферон) а также индукторы выработки собственных интерферонов – циклоферон, неовир.
Введение интерферонов и других иммуномодулирующих препаратов происходит под контролем иммунологического статуса. При неэффективности иммуномодуляторов возможно назначение курса, человеческого иммуноглобулина который вводится путем внутримышечных инъекций в количестве от 3 до 5 с промежутком в 2-3 дня.
Различные формы ЦМВ-инфекции могут маскировать под схожие по симптомам заболевания. Поэтому требуется дифференциальная диагностика с:
Специфическая диагностика
Основное направление в профилактике ЦМВИ – соблюдение правил личной гигиены, индивидуальная защита при контакте с больными цитомегаловирусом. Особенно важно соблюдать профилактические рекомендации людям, входящим в группу риска:
Средства для специфической профилактики находятся в разработке. Единственный препарат, который позволяет проводить профилактику у пациентов после трансплантации – летермовир. Широкого применения он пока не нашел, рекомендован к использованию только в США.
Обследование на цитомегаловирусную инфекцию в Медарт
Лаборатория клиники Медарт оборудована современным высокоточным оборудованием, которое позволяет выполнить любые виды диагностики цитомегаловирусной инфекции и другие виды серологической диагностики инфекционных заболеваний (диагностика на ВИЧ, сифилис, гепатит, лямблиоз, Helicobacter pylory, токсоплазмоз).
Анализ крови на цитомегаловирус входит в комплекс анализов на ИППП (инфекции, передающиеся половым путем). Также есть возможность провести диагностику ЦМВИ по индивидуальным показателям, например, при планировании беременности.
При необходимости результаты теста можно получить в день сдачи материала. Это особенно важно при тяжелых формах ЦМВ-инфекции, когда решающую роль играет скорость постановки диагноза и назначения эффективного лечения. Преимущества клиники:
Пациенты клиники Медарт получают полный спектр медицинских услуг – от предварительного приема и лабораторной диагностики цитомегаловируса до назначения эффективной терапии и получения рекомендаций по профилактике и реабилитации после перенесенного заболевания.