Фракция внеклеточной фетоплацентарной днк что такое
Низкая фетальная фракция внеклеточной ДНК при проведении неинвазивного пренатального ДНК-скрининга: возможные причины, клиническое значение и тактические решения
Цель исследования: провести сравнение частоты хромосомных аномалий (ХА) у плодов при первичном и повторном неинвазивном пренатальном ДНК-скрининге (НИПС) в связи с низким уровнем фетальной фракции или низким качеством внеклеточной эмбриональной ДНК.
Дизайн: ретроспективное когортное исследование.
Материалы и методы. В исследование включены 21 042 женщины, которым был проведен НИПС в России в 2013–2018 гг. Основную группу составили согласившиеся на повторный НИПС 1025 из 1044 пациенток с неинформативными данными исследования (низкое содержание фетальной фракции, не дающее возможность определить риск ХА). В контрольную группу вошли 19 998 женщин с информативным НИПС при первичном исследовании. Группу исключения составили женщины с низким уровнем фетальной фракции, отказавшиеся от повторного скрининга. Метод исследования — таргетный НИПС. Проводили забор крови из вены и центрифугирование крови для получения плазмы. Внеклеточную фетальную ДНК анализировали с помощью метода NGS (метода секвенирования однонуклеотидных полиморфизмов, запатентованного компанией Natera).
Результаты. НИПС оказался нерезультативным у 1044 (5%) пациенток, у 821 (80,1%) из 1025 со второго раза был получен результат. Среди участниц, получивших результат при первичном исследовании, частота хромосомных анеуплоидий составила 2,4%. Среди тех пациенток, у которых провели повторное результативное исследование НИПС, ХА у плода в итоге были выявлены у 27 (3,3%). В подгруппе женщин, только с третьего раза получивших результат, распространенность ХА — 9,3% (7 случаев из 75). Показано, что в I триместре средний уровень фетальной фракции у беременных с трисомиями 18, 13 или моносомией Х значимо ниже, чем в норме. Во II триместре значимо более низкий уровень фетальной фракции по сравнению с нормой определялся при наличии трисомии 18 или моносомии Х. Получены статистически значимые различия между уровнями фетальной фракции у пациенток с массой тела Заключение. Риск выявить ХА у плода при повторном НИПС значимо выше, чем при первичном исследовании. В случае неинформативного теста пациентке целесообразно повторно выполнить скрининг, если он не даст результатов, необходимо решать вопрос о проведении инвазивной пренатальной диагностики. С повышением массы тела пациентки снижается уровень фетальной фракции, в связи с чем женщинам с избыточной массой тела и ожирением следует рекомендовать другие методы пренатальной диагностики.
Вклад авторов: Кудрявцева Е.В. — сбор клинического материала, обзор публикаций по теме статьи, статистическая обработка данных, написание текста рукописи; Ковалёв В.В. — разработка дизайна исследования; Баранов И.И. — проверка критически важного содержания, утверждение рукописи для публикации; Канивец И.В. — сбор клинического материала; Киевская Ю.К. — сбор клинического материала, обзор публикаций по теме статьи; Коростелёв С.А. — сбор клинического материала, проверка критически важного содержания.
Конфликт интересов: авторы заявляют об отсутствии возможных конфликтов интересов.
Фетоплацентарная ДНК — новый пазл в пренатальной диагностике
При каждой беременности существует риск хромосомных нарушений. Наиболее диагностически значимым является выявление анеуплоидий, то есть наличия аномального числа хромосом в клетке (в отличие от эуплоидной клетки с 46 хромосомами).
Установленные программы скрининга определяют риск возникновения синдрома Дауна (относительно высокая частота — 1/800 живорождений), также рассматривают синдром Эдвардса (трисомия 18), синдром Патау (трисомия 13) и синдром Шерешевского-Тернера (чаще полное отсутствие одной из Х хромосом — моносомия 45, X0, либо аномалии второй Х-хромосомы) [1].
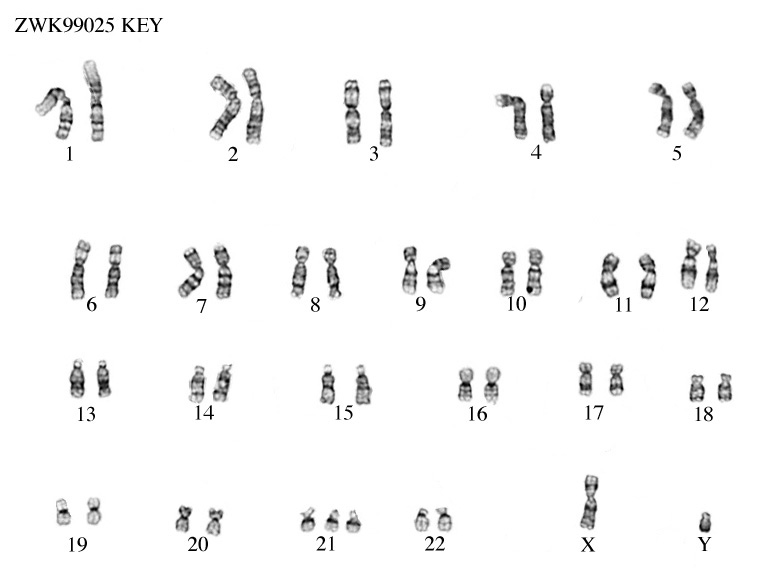
Пренатальная диагностика и скрининг проводятся как инвазивными, так и неинвазивными методами. Инвазивные подходы, такие как взятие проб ворсин хориона (CVS) и амниоцентез, включают хирургическое введение зондов в матку и являются высокоточными. Хромосомный анализ культивируемых ворсин хориона и клеток амниотической жидкости может выявить не только анеуплоидию плода (рис. 1), но и структурные перестройки, такие как транслокации и инверсии, а также относительно большие дупликации и делеции, обычно размером более 5 мБ (мБ — мегабаза, единица длины фрагмента ДНК, равная 1 млн нуклеотидов) [2]. Хромосомный анализ клеток околоплодных вод считается «золотым стандартом» в пренатальном скрининге ввиду крайне низкого процента ошибок (менее 0,01–0,02 %). Кроме методов обычной цитогенетики, используются молекулярно-генетические исследования: флуоресцентная гибридизация in situ (FISH), количественная флуоресцентная полимеразная цепная реакция в реальном времени (QF-ПЦР) и мультиплексная, зависимая от лигирования амплификация зонда (MLPA). Данные методы позволяют получить более быстрый результат, но имеют ограничения по спектру выявляемой патологии, для них рекомендовано дальнейшее подтверждение кариотипированием. Однако все инвазивные методы вызывают физический дискомфорт и потенциально вредны для плода, а также ассоциируются с 1–2 % риском потери беременности [1].
Рисунок 1 | Кариотипирование — синдром Дауна: 47, XY, + 21, трисомия 21 [2].
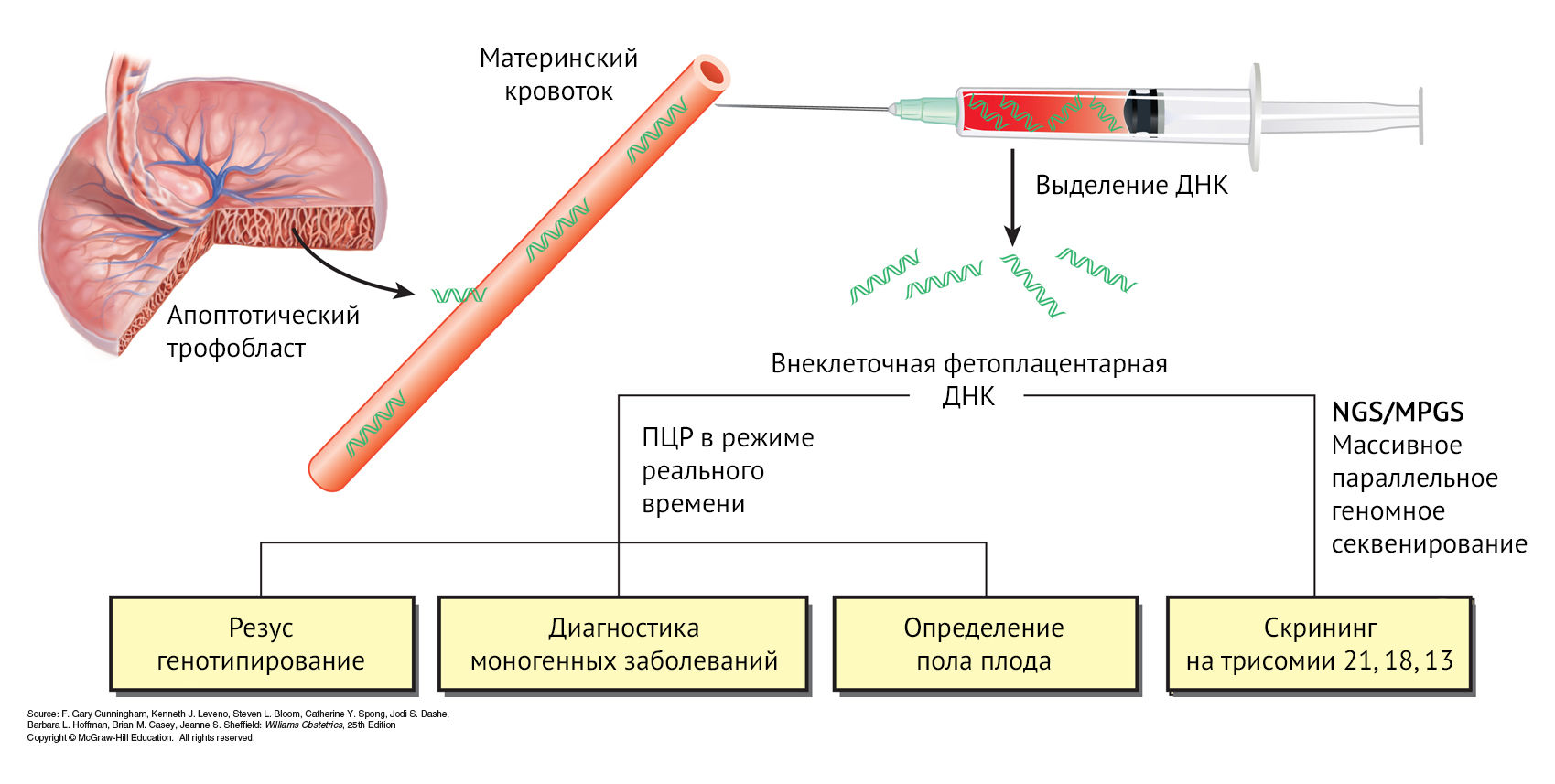
Напротив, неинвазивные тесты на основе изменения уровня внеклеточной эмбриональной ДНК (cell-free DNA, cfDNA) являются безопасными и обеспечивают раннее обнаружение распространенных анеуплоидий со значительно более высокой чувствительностью и специфичностью, по сравнению с ультразвуковым исследованием. В 1997 году Lo с коллегами обнаружили ДНК фетальных трофобластов в крови матери. Часто используется термин «эмбриональная ДНК», хотя происходит она из структур плаценты, поэтому более точным является понятие фетоплацентарной ДНК (рис. 2) [3]. Постоянное обновление ворсинчатого трофобласта приводит к вытеснению апоптотического материала в материнскую циркуляцию. При этом бесклеточная фетоплацентарная ДНК составляет всего 3 % от общей бесклеточной циркулирующей ДНК на ранних сроках беременности, увеличиваясь до 6 % на поздних сроках беременности. Отличить собственно материнскую и фетоплацентарную внеклеточную ДНК позволяет значительно меньшие размеры последней — около 200 пар нуклеотидов [4].
Рисунок 2 | Неинвазивная пренатальная диагностика с использованием анализа внеклеточной фетоплацентарной ДНК.
Real-time ПЦР — количественная полимеразная цепная реакция (ПЦР) в режиме реального времени — используется для одновременной амплификации (увеличения числа копий) и измерения количества данной молекулы ДНК. Измеряется количество амплифицированной ДНК в реальном времени после каждого цикла амплификации. MPS — массивное параллельное секвенирование или секвенирование следующего поколения (next-generation sequencing, NGS). Секвенирование — анализ последовательности нуклеотидов в составе макромолекул, являющихся единицами наследственной информации.
Соответственно, неинвазивный пренатальный скрининг (NIPS) становится все более распространенным в качестве надежной процедуры выявления анеуплоидий. Американский колледж медицинской генетики и геномики (ACMG) предложил NIPS всем беременным женщинам, независимо от их статуса риска для скрининга анеуплоидий с участием хромосом 21, 18 и 13 [5].
На сегодняшний день подавляющее большинство методов NIPS используют массивное параллельное секвенирование (MPS) или секвенирование нового поколения (next-generation sequencing, NGS), позволяющее одновременно определять нуклеотидные последовательности множества различных нитей ДНК, для измерения количества хромосомных копий с использованием cfDNA, полученной из материнской плазмы, в которой ДНК фетоплацентарного происхождения составляет от 2 % до 40 % от общей свободной ДНК. Фактическая фракция ДНК плода зависит от таких факторов, как гестационный возраст (концентрация возрастает с увеличением срока гестации, раннее обнаружение возможно уже с 5 недели и практически всегда — с 7 недели), вес матери (обратная зависимость: чем выше вес, тем меньше концентрация) и метод экстракции. Для анализа секвенирования используется такой показатель как фракция плода (ff). Ff — это количество внеклеточной эмбриональной ДНК в данном образце по отношению к общему количеству внеклеточной ДНК. В любом гестационном возрасте ff имеет нормальное (Гауссово, симметричное, колоколообразное) распределение, которое достигает максимума между 10 и 20 % на 10–21 неделе [6].
Повышение уровня фетальной внеклеточной ДНК в материнской крови отражает активацию апоптотических, некротических и воспалительных процессов в плаценте, что делает этот маркер перспективным для оценки риска развития таких осложнений беременности, как преэклампсия, преждевременные роды, задержка роста плода [7].
Внеклеточная фетоплацентарная ДНК является новым биомаркером, который может стать важным фрагментом в воспроизведении полной картины плоидности эмбриона, состояния плаценты, прогнозирования различных клинических проблем. Трудности в интерпретации все еще сохраняются, требуется более полное изучение факторов, влияющих на выработку, метаболизм и клиренс фетоплацентарной ДНК. Важным ограничением использования cfDNA является то, что пациентки с низкой фракцией плода для своего срока гестации, приводящей к «нерегистрируемому результату», зачастую имеют повышенный риск анеуплоидии плода. В этом случае требуется применение инвазивных методов цитогенетики.
Фракция внеклеточной фетоплацентарной днк что такое
Риск развития хромосомных аномалий у будущего ребенка напрямую зависит от возраста матери. Чем старше женщина, тем такой риск выше. Тем не менее, большинство детей с синдромом Дауна рождается у женщин моложе 35 лет, потому что в данной возрастной категории происходит большее количество родов. По этой причине пренатальный скриниг важно проводить женщинам любого возраста.
Сегодня для пренатального выявления врожденных пороков развития и хромосомных аномалий будущего ребенка во всем мире проводится скрининг 1 триместра беременности, основанный на оценке возраста матери, ультразвуковых и биохимических показателях. Хуан Акуна отметил, что «информативность такого обследования в реальности не превышает 70%». По его результатам 1 из 20 будущих мам ставится высокий риск рождения ребенка с хромосомной аномалией. Чтобы получить точный ответ, женщин с высоким риском направляют на так называемую инвазивную диагностику (прокол плодных оболочек и взятие материала для определения хромосомного набора ребенка). Инвазивная процедура несет риски прерывания беременности и поэтому многие женщины часто от нее отказываются. При этом у 99 из 100 женщин по результатам инвазивной диагностики патологии не выявляется и оказывается, что исследование проводилось зря.
По словам профессора Хуана Акуны в дополнение к традиционному скринингу специалистам необходим метод, который позволит существенно снизить столь высокую частоту проведения инвазивной диагностики. И сегодня таким методом является неинвазивная пренатальная диагностика – исследование ДНК плода по крови беременной женщины. По данным разных исследований, неинвазивная диагностика повышает частоту выявления хромосомных аномалий до 99%, существенно снижает процент ложноположительных результатов до 0,08%, а значит, снижает частоту неоправданных инвазивных вмешательств.
Неинвазивную диагностику можно проводить с 10-й недели беременности. Ее точность зависит от количества ДНК плода ребенка (фетальная фракция) в крови женщины. Чтобы получить достоверный диагностический результат фетальная фракция должна составлять не менее 4%. Исследования показали, что у 2% женщин в крови содержится менее 4% ДНК ребенка. К сожалению не все неинвазивные тесты предусматривают измерение количества фетальной фракции перед проведением диагностики. По данным обширных исследований, проведенных на более чем 22 000 женщин, самой достоверной в настоящее время является методика Harmony. Чувствительность этого теста составляет 100%. В России это исследование известно под названием Prenetix.
Хуан Акуна также отметил, что «неинвазивная пренатальная диагностика является лучшим из всех доступных в клинической практике методов скрининга хромосомных аномалий плода. Исследование существенно превосходит биохимические методы, но не заменяет ультразвуковое исследование».
Узнать пол ребенка до УЗИ по ДНК?
Интернет пестрит различными методами: гадание на кофейной гуще, народные приметы, китайские таблицы, таблицы обновления крови, Однако эффективность этих методов не доказана.
Предугадать пол будущего ребенка невозможно. Шансы 50 на 50.
Внеклеточная ДНК плода
Открытие наличия внеклеточной фетальной фракции ДНК в крови матери стало прорывом в пренатальных исследований. Все отмершие клетки плода попадают в кровоток матери через плаценту. Именно через ее стенки происходит обмен различными питательными веществами, кислородом и продуктами жизнедеятельности плода.
Таким образом фетальная ДНК начинает накапливаться в крови матери уже с первого месяца беременности. Достаточное количество фетальной фракции для проведения неинвазивного исследования достигается не раньше 9 недель беременности. В среднем содержание фетальной фракции у беременных женщин на таком сроке составляет 4-5%.
Принцип анализа определение пола будущего малыша
Свободно-циркулирующая внеклеточная ДНК выделяется из плазмы актикоагулированной цельной крови матери. Выделенная ДНК используется для анализа с целью определения содержания генетического материала мужской Y-хромосомы при помощи количественной полимеразной цепной реакции в реальном времени.
Наличие генетического материала мужской Y-хромосомы свидетельствует о плоде с мужским генетическим полом. Отсутствие такого материала свидетельствует о женском генетическом поле плода.
Раньше чем первое УЗИ.
Определение пола плода возможно с использованием УЗИ-диагностики, однако данный метод применим с 22-й акушерской недели беременности, а достоверность его не превышает 70%.
Первое УЗИ проводят с 11-ти недель беременности, однако вероятность определения пола слишком мала. Неинвазивный тест на определение пола плода можно проводить уже с 9-ти недель беременности.
Точность такого анализа 99%
На точность может повлиять низкое содержание фетальной фракции в крови матери, поэтому не рекомендуется торопиться и проводить анализ раньше 9-ти акушерских или 7-ми эмбриональных недель беременности.
Безопасность 100%
Неинвазивный метод полностью безопасен для мамы и будущего малыша, т.к. подразумевает обычный забор венозной крови.
Результат через 5 дней
Результат неинвазивного теста, как правило, готов в течение 5 рабочих дней или раньше.
ООО «Медикал Геномикс» Лицензия № ЛО-69-01-002086 от 06.10.2017
Юр. адрес: г. Тверь, ул. Желябова, 48
ООО «Лаб-Трейдинг», ИНН: 6950225035, ОГРН: 1186952017053, КПП:695001001
Юр. адрес: г. Тверь, ул. 1-Я За Линией Октябрьской Ж/Д, 2, оф. 22
НИПТ ( неинвазивный пренатальный тест ) – это исследование генетического материала ребёнка, происходящего преимущественно из плаценты, который появляется в крови женщины с 4-5-й недели беременности.
НИПТ абсолютно безопасен для малыша: для этого теста берётся кровь у беременной женщины из вены, выделяется из данного образца ДНК плода и исследуется.
К 9-10-й неделе беременности в крови мамы детской ДНК становится достаточно, чтобы определить, есть ли у будущего ребёнка хромосомные аномалии, возникающие случайно.
Почему же это важное исследование нельзя сделать раньше 9-10 недели? Для того, чтобы корректно провести НИПТ, нам необходимо, чтобы в крови будущей матери присутствовала внеклеточная ДНК более 4% плода. Обычно этот уровень концентрации достигается именно на сроке 9-10 недель и больше, вплоть до родов.
Показания для проведения исследования:
⠀ Существует 2 основных варианта НИПТ:
1.Т аргетный тест на аномалии 5 хромосом: 13, 18, 21, X, Y (стоимость 20 900 в Санкт-Петербурге) и
2. Полногеномный тест на аномалии всех хромосом (стоимость 23 000 в Санкт-Петербурге).
⠀ Срок выполнения исследования: 14 рабочих дней.
⠀ Достоверность результата для определения аномалий хромосом 13,18 и 21 – не менее 99%, а для определения аномалий хромосом X и Y – не менее 95%.
⠀ В чем разница между НИПТ и скринингом 1 триместра?
1. НИПТ — это прямой метод, мы исследуем саму внеклеточную ДНК, её количество, а в комбинированном пренатальном скрининге использованы косвенные методы оценки.
2. Комбинированный скрининг имеет точность около 70-85%, а НИПТ — 99,9%
3. Комбинированный скрининг не предоставляет информацию о наличии/отсутствии риска хромосомной патологии половых хромосом, а НИПТ – предоставляет с достоверностью 95% и более.
4. НИПТ не предоставляет информацию о правильности строения органов малыша, как это делает УЗИ в рамках скрининга.
5. Комбинированный скрининг проводится бесплатно в женской консультации, НИПТ же во всех городах России (за исключением Москвы) возможно пройти только платно.
Важные особенности НИПТ:
1. НИПТ – это скрининг, то есть метод, рассчитывающий риск наличия заболевания, а не абсолютно точная диагностика, поэтому возможно получение ложноположительных и ложноотрицательных результатов (хоть и вероятность этого крайне мала).
2. НИПТ не заменяет комбинированный пренатальный скрининг беременной в 11-13 недель беременности, а может только дополнять его.
3. НИПТ ни в коем случае не заменяет инвазивную пренатальную диагностику, но сможет помочь маме принять решение для отказа или согласия на неё.
4. При выявлении повышенного риска необходимо проконсультироваться с врачом-генетиком о прохождении инвазивной пренатальной диагностики (амнио- или кордоцентез) с целью определения кариотипа плода.
5. Пол будущего ребёнка сообщается после 12-й недели беременности согласно Конвенции о правах человека и биомедицине (Овьедо, 4 апреля 1997 год), за исключением случаев аномалий половых хромосом и сцепленных с полом заболеваний
Противопоказания к НИПТ:
Как понять значение результатов НИПТ?
В документе с результатами НИПТ будет один из трёх вариантов:
1. Низкий риск хромосомной патологии (указано, по какой именно хромосоме). В данном случае рекомендуется обычное наблюдение беременности, скрининговое УЗИ I (11-13 недель 6 дней), II (18-22 недели) и III триместра (30-34 недели).
2. Высокий риск хромосомной патологии (указано, по какой именно хромосоме). В данном случае ОБЯЗАТЕЛЬНО проведение инвазивной диагностики с целью подтверждения/исключения результата.
3. Риск хромосомной патологии не определён (1-6% от всех НИПТ). Причины этого могут быть разные: низкая фракция фетальной ДНК, многочисленные технические нюансы. Рекомендовано медико-генетическое консультирование для определение индивидуальной тактики дообследования плода.
Как подготовиться к исследованию?
Где можно провести НИПТ?
Лаборатория «Сербалаб» сотрудничает с медицинскими центрами по всей стране, в которых можно сдать кровь для анализов. Если же пациент проживает в городе, в котором нет партнеров лаборатории, он может связаться с лабораторией и ему будет выслан курьером специальный набор для взятия материала. В набор входит комплект необходимых документов (информированное согласие, направление на проведение исследования НИПТ, информационное письмо и инструкция по забору материала), а также пробирка со специальной транспортной средой, которая сохранит кровь пациента в свежем состоянии при длительной транспортировке. Человеку только требуется найти мед.кабинет, где ему соберут кровь в предоставленную лабораторией пробирку. После этого человек снова связывается с лабораторией и курьером забирается материал на исследование.
По готовности результатов лаборатория высылает данные либо врачу, направившему на исследование, либо на личную электронную почту пациенту.
© 2021 «vMedCentre.ru»