Хелатный комплекс это что
Какие минералы лучше усваиваются?
Для существования человеческому организму необходимо огромное количество полезных веществ. Цинк, магний, медь, железо, кальций – это не просто элементы периодической таблицы Менделеева из школьной программы по химии. Это важнейшие минералы для существования и правильного функционирования всего человеческого организма.
Чтобы наши иммунные клетки могли защитить нас от вражеского вторжения вирусов необходим цинк. Магний – ключевой элемент нашей нервной системы и мышц. Прочные кости и крепкие зубы – это заслуга кальция. Без железа падает уровень гемоглобина, что может привести к развитию анемии. А медь поддерживает нашу красоту и молодость за счет сохранения цвета волос и участию в выработке коллагена и эластина.
С современным питанием все эти минералы попадают в наш организм в ничтожно малых количествах. Из витаминных комплексов они практически не усваиваются и даже могут вызывать побочные эффекты… Как же быть? Есть ли решение этой проблемы, или человек обречен с возрастом испытывать все больший дефицит этих минералов?

Хелаты – новое слово в науке
Настоящий фурор во всем европейском научном сообществе произвели хелатные формы минералов. Было известно, что в отличие от минералов организм очень легко усваивает аминокислоты. Это подтолкнуло ученых присоединить молекулу минерала к аминокислоте. И это действительно сработало. Такая форма получила название – хелатная.
Степень усвоения хелатов в разы выше, чем у неорганических форм, таких как карбонаты, цитраты и т.д. В такой форме минералы усваиваются максимально.
А самое главное то, что организм очень легко переносит хелатные минералы в больших дозировках. Они не вызывают побочного нарушения пищеварения и вздутия, так как не влияют на уровень кислотности желудка, а также усваиваются без побочных отложений в сосудах, почках, суставах и даже разрешены беременным и кормящим.
Кальций хелат Эвалар – быстро восполняет дефицит кальция в организме, обеспечивая его максимальное усвоение. Кроме того, кальций в хелатной форме не откладывается на стенках сосудов, в почках, а идет напрямую в кости. Кальций хелат Эвалар способствует поддержанию нормального состояния костной ткани, зубов, улучшению состояния сердца и сосудов.
Как принимать минералы?
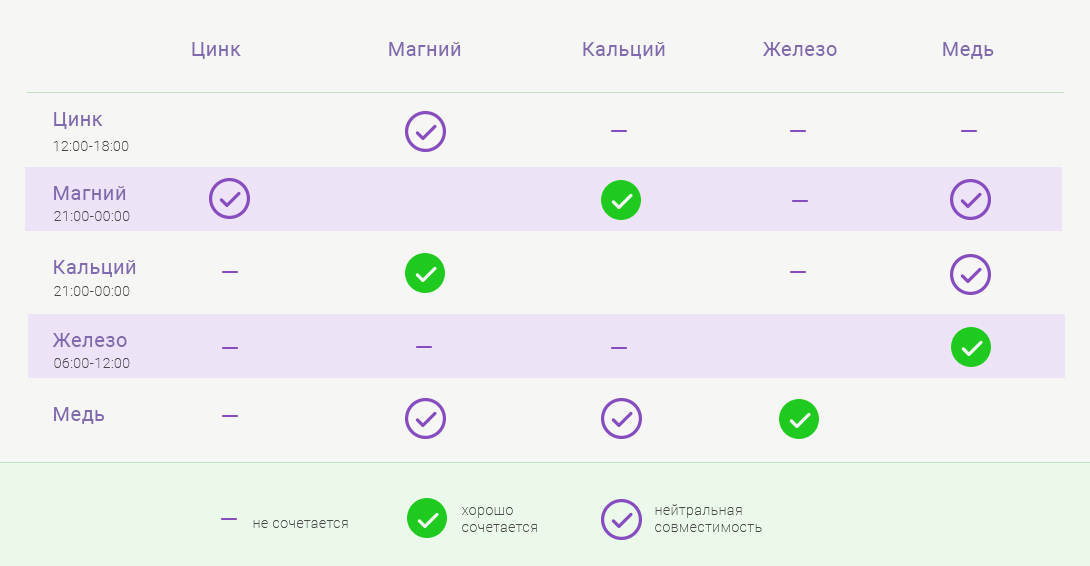
Если вы решили принимать сразу несколько минералов необходимо знать, какие минералы сочетаются между собой, а какие категорически нельзя совмещать во время одного приема. Кальций и магний хорошо сочетаются. Оптимально принимать их вечером, так как кальций лучше усваивается ночью, а магний улучшает сон. Железо и медь следует принимать утром, а цинк отлично усваивается в обеденное время.
Усваивайте минералы по максимуму! Выбирайте хелатные формы от Эвалар, ведь это:
• Максимальная степень усвоения в отличие от других форм
Хелаты: как в них разобраться?
На рынке присутствуют разнообразные формы комплексных соединений металлов, используемых в кормлении животных. Все эти разнообразные формы называют «органическими микроэлементами», поскольку входящие в их состав микроэлементы образуют комплексы, или другие типы химических соединений, с органическими молекулами.
Химические процессы комплексообразования, или образования хелатов, понимаются по-разному различными специалистами отрасли кормопроизводства, что приводит к возникновению путаницы в терминах и интерпретации свойств продуктов. Часто встречаются такие термины, как «комплекс металла и аминокислот», «хелат металла и аминокислот», «комплекс металла с полисахаридом», «протеинат металла», однако официальные определения этих терминов расплывчаты и не проясняют ситуацию. В качестве примера в Таблице 1 приведены различные определения органических микроэлементов, используемых в сельском хозяйстве, в формулировках Ассоциации американских контролёров качества кормов (AAFCO, 1998).
Таблица 1. Органические комплексы минералов – определения терминов в формулировках AAFCO.
Комплекс металла и аминокислоты – продукт, образующийся при формировании комплекса между растворимой солью металла и аминокислотой.
Чтобы разобраться в запутанных определениях, характеризующих химические и физические свойства микроэлементов, прежде всего, необходимо выявить отличия между терминами «комплекс» и «хелат».
Комплексы или хелаты
Термин «комплекс» может использоваться при описании соединений, образующихся при взаимодействии иона металла с молекулой или ионом (лигандом), которые обладают свободной парой электронов. Такие ионы металлов связываются с лигандом посредством атомов-доноров, например, кислорода, азота или серы. Лиганды, обладающие только одним атомом-донором, называются монодентатными, а лиганды, обладающие двумя и более атомами-донорами, называеются би-, три- или тетрадентатными, также их иногда называют полидентатными.
Аминокислоты являются бидентатными лигандами, образующими связи с ионами металла посредством кислорода карбоксильной группы и азота аминогруппы.
Этилендиаминтетрауксусная кислота (ЭДТА) является примером гексадентатного лиганда, который содержит шесть атомов-доноров. ЭДТА образует очень прочные комплексы с большинством ионов металлов, и не очень подходит для образования хелатов минералов, поскольку биологическая доступность таких комплексов невысока.
Хотя могут образовываться хелаты, содержащие четыре, пять, шесть или семь колец, установлено, что наиболее стабильными являются хелаты, содержащие пять колец.
Также необходимо помнить о том, что хотя хелаты и являются комплексами, не все комплексы являются хелатами. Несмотря на простоту теории, объясняющей образование хелатов, необходимо строгое соблюдение множества условий для получения стабильного хелата минерала.
Лиганд должен содержать два атома, способных образовывать связи с ионом металла.
Лиганд должен образовывать гетероциклическое кольцо, причём металл должен располагаться «в конце» этого кольца.
Образование хелата металла должно быть пространственно (стерически) возможно. Для достижения стабильности необходимо соблюдать соотношение количества лиганда к минералу.
Истинные хелаты имеют «кольцевую структуру», образованную ковалентно-координационной связью между аминной и карбоксильной группами аминокислоты и ионом металла.
Как правило, хелаты образуются в результате реакции между неорганическими солями минералов, с приготовленной при помощи ферментов смесью аминокислот и небольших пептидов в контролируемых условиях. Такие аминокислотные и пептидные лиганды связываются с ионом металла не в одной точке, а в нескольких, в результате чего атом металла становится частью биологически стабильной кольцевой структуры. Аминокислоты и продукты ферментативного разрушения белков, например, небольшие пептиды, являются идеальными лигандами, поскольку они обладают как минимум двумя функциональными группами (аминной и гидроксильной), необходимыми для образования кольцевой структуры с минералом. Только «переходные элементы», например, медь, железо, марганец и цинк обладают необходимыми физико-химическими характеристиками, позволяющими им образовывать ковалентно-координационные связи с аминокислотами и пептидами с образованием биологически стабильных комплексов.
Аминокислоты и пептиды в качестве лигандов
Существуют различные мнения относительно преимуществ использования аминокислот в сравнении с пептидами при образовании хелатов минералов, ещё больше споров имеется по вопросу биологической доступности таких продуктов. Мы уже рассмотрели общие условия, необходимые для образования биологически стабильных хелатов минералов, однако следует также учитывать и другие факторы, оказывающие влияние на образование хелатов, основными из этих факторов являются:
Очевидно, что такой сложный химический феномен не следует чрезмерно упрощать. Однако чтобы прояснить ситуацию касательно преимуществ аминокислот либо пептидов в процессе образования хелатов минералов, мы рассмотрим факторы, влияющие на состояние равновесия и стабильность таких комплексов.
При растворении в воде соли металла, например, сульфата меди (II), с добавлением аминокислоты в качестве бидентатного лиганда, образуется ряд комплексов, каждый из которых обладает собственной константой стабильности, которая зависит от рН раствора. Это показано на Рисунке 1 (реакция сульфата меди (II) с глицином). Из данных, показанных на этом рисунке можно сделать некоторые важные выводы:
Рисунок 1. График изменения содержания меди, включённой в состав различных соединений, при изменении рН в растворе, содержащем медь (II) (0,001М) и глицин (0,002М). Горизонтальная ось: рН. Вертикальная ось: % Cu++
У различных ионов металлов различные константы стабильности. Поэтому, количество металла, входящего в состав конкретного соединения, зависит не только от величины рН раствора, но и от константы стабильности комплекса.
Стабильность содержащего металл комплекса зависит как от свойств металла, так и от свойств лиганда. Увеличение заряда иона, уменьшение размера и увеличение аффинности электронов способствует большей стабильности. На стабильность комплексов влияют также некоторые характеристики лигандов: (1) щёлочность лиганда, (2) количество металло-хелатных колец на единицу лиганда, (3) размер хелатного кольца, (4) пространственные эффекты, (5) резонансные эффекты и (6) атом лиганда. Поскольку комплексные соединения образуются в результате кислотно-основных реакций, как правило, более щелочные лиганды образуют более стабильные комплексы. Также большое значение имеет размер хелатного кольца.
Ещё глубже проанализировав Рисунок 1, можно заметить наличие существенных отличий между относительной стабильностью хелатов металлов, образованных аминокислотами и стабильностью протеинатов металлов. Поскольку протеинат металла является продуктом реакции хелатообразования между растворимой солью и аминокислотами и/или частично гидролизованным белком, можно предположить, что для конкретного иона металла количество графиков, характеризующих образование различных соединений, в состав которых входит металл, при образовании протеината, будет намного больше, чем при образовании хелата этого же металла с аминокислотой. Если считать график, отражающий распределение количества меди между различными соединениями, индикатором относительной стабильности при данной величине рН, и учитывать бесконечное количество комбинаций, возможных в результате взаимодействия как отдельных аминокислот, так и ди-, три- и даже тетрапептидов, то, теоретически, общая стабильность протеината в широком диапазоне рН должна быть намного больше, чем стабильность хелата данного металла с аминокислотой.
Очевидно, что в реальных условиях рассмотренные дополнительные факторы будут оказывать влияние на стабильность хелата. Однако можно ожидать, что протеинаты металлов будут обладать физико-химическими свойствами, необходимыми для сохранения постоянства характеристик при изменении рН.
Несмотря на наличие некоторой противоречивой информации, образование хелатов металлов – это не такой уж сложный процесс, в основе которого лежат фундаментальные законы химии. Мы можем выделить две формы истинных хелатов минералов, каждая из которых обладает определёнными химическими и биофизическими свойствами. Внимательно изучив факторы, влияющие на образование хелатов минералов, можно выявить различия между продуктами по показателю биологической стабильности и, следовательно, биологической доступности.
Хелатный комплекс это что
Название происходит от лат. chelate — клешня. Для образования хелата необходим лиганд, в котором число донорных центров, образующих связь с центральным атомом, не меньше двух. Число таких центров называют дентатностью лиганда. Лиганды, образующие хелатные циклы, называются хелатирующими (хелатообразующими) реагентами. Примеры полидентатных лигандов: этилендиамин H 2NCH 2CH 2NH 2, глицерин HOCH 2CH(OH)CH 2OH, этилендиаминотетрауксусная кислота (рис.). Образование химических связей между полидентатным лигандом и центральным атомом называется хелатированием или хелатообразованием. Хелатообразование — один из путей образования супрамолекулярных комплексов «гость–хозяин».
Наиболее обширный и важный класс хелатов — хелатные комплексы металлов (металлохелаты). Способность координировать лиганды присуща металлам всех степеней окисления.
Хелаты значительно устойчивее, чем близкие по природе комплексы, образованные монодентатными лигандами. Это явление называют хелатным эффектом. Во многом благодаря наличию хелатного цикла хелаты обладают уникальными физическими, химическими и биологическими свойствами. Они широко применяются в аналитической химии для определения металлов. Наночастицы, покрытые хелатообразующими соединениями, способны образовывать хелатные комплексы с гадолинием (Gd), что позволяет их использовать в качестве контрастирующего агента в ядерно-магнитной томографии. Большую роль хелаты играют в процессах жизнедеятельности: хелатами являются гемоглобин, хлорофилл, витамин B12.
ХЕЛАТЫ
Хелаты: каталог
О роли витаминов и минералов в жизни человека
Что такое хелаты
Хелаты: свойства
Эти формы соединений минеральных элементов обладают целым рядом ценных свойств:
— они не токсичны;
— растворяются в воде;
— в широком диапазоне кислотности сохраняют свои свойства;
— хелаты адсорбируются в почве и на листьях;
— устойчивы к губительному воздействию различных микроорганизмов;
— не влияют на уровень желудочной кислоты;
— хелатные формы продолжительное время не разрушаются.
К примеру, неорганические соли минералов (не хелатная форма) имеют биодоступный уровень около 10%, т.е. 90% их количества, попавших в организм, не усваиваются им, и даже вредят ему.
Хелаты компании Альтера Холдинг
Пожалуй, наиболее эффективные минеральные препараты, которые выпускаются в хелатной форме, это препараты компании Альтера Холдинг. И среди этих препаратов важнейшие для нашего организма:
— хелат железа
— хелат кальция
— кальций магний хелат
— хром хелат
— цинк хелат
Над разработкой этих препаратов трудились ведущие ученые-нутрициологи нашей страны и на сегодняшний день эти препараты не имеют аналогов.
Хотим еще добавить, что при производстве этих препаратов хелатной формы используется передовая технология микрокапсулирования: каждый микроэлемент «помещается» в микрокапсулу, которая «доставляет» этот хелат в определенный отдел организма где происходит его усвоение (важно чтобы хелат усвоился именно в определенном месте, а не где попало).
Хелаты: купить
Купить хелатные комплексы различных минералов у нас двумя способами:
— позвоните нашему менеджеру и закажите препарат;
— сделайте заказ через специальную форму на нашем сайте.
Наша цена на любой препарат на соответствующей странице рядом с его изображением.
Доставка препарата в кратчайшие сроки и без задержек (как по Москве, так и по регионам России, а так же зарубежью), оплата в любой удобной для вас форме.
Хелаты: отзывы
Наталья Евгеньевна М, 58 лет, г. Нальчик
«. 10 лет страдаю остеопорозом, да и сердце побаливает. Мой врач посоветовал мне кальций/магний хелат компании Альтера Холдинг. Пью препарат шесть месяцев, он мне помогает, забыло обо всех болячках. «
Сергей Петрович, 52 года, г. Орел
«. После того, как стал регулярно употреблять цинк хелат, перестал болеть инфекционными заболеваниями, ушли проблемы с простатой. «
Что такое хелатная форма удобрений
Рассмотрим что такое хелаты и хелатирующие агенты металлов, их структура и особенности применения данного типа эффективного водорастворимого удобрения в качестве дополнительной легкоусвояемой подкормки растительным культурам.
Представлят собой современное высокоэффективное комплексное удобрение в форме хелатов (complex chelate fertilizer), или комплексное микроудобрение в хелатной форме. особенности хелатирующих агентов ЕДТА, ДТРА, ЕДДНА могут отличаться. Modern highly effective complex fertilizer in the form of chelates, or complex micronutrient in chelate form. Features of chelating agents EDTA, DTRA, EDNA.
сложные органические соединения хелаты / chelates complexorganic compounds
В дополнение к их организмам, хелаты Это также экономически важно.
Ион металла и хелатирующий агент / Metal ion and chelating agent
Хелатирующий агент молекулы (Molecule chelating agent) может образовывать несколько связей с одним ионом металла. Другими словами, хелатирующий агент представляет собой полудентатный лиганд (semi-dentate ligand).
Пример простого хелатирующего агента является этилендиамин (Этилендиамин (1,2-диаминоэтан) H2NCH2CH2NH2 — органическое соединение класса аминов): NH2 ; CH2 ; CH2 ; NH2 ;
В виде хелатов используют металлы / Metals are used as chelates
Хелаты в такие реакции не вступают, а также не связываются почвой.
В результате, если обычные микроэлементы усваиваются растениями на 30-40%, то микроэлементы в хелатной форме на 90%. Проще говоря хелатная форма- это такая форма макро и микроэлементов, которые организм легко усваивает. Причем хелаты применяются не только в растительном, но и в животном мире при создании витаминов и лекарственных препаратов.
ЕДТА, ДТРА, ЕДДНА хелатирующие агенты / EDTA, DTRA, EDNA chelating agents
В различных удобрениях используются разные хелатирующие агенты / Different chelating agents are used in various fertilizers:
| — | Хелатирующий агент | Стабильность при диапазоне рН: | — | Stability at pH range: |
| 1) | ЕДТА | Стабилен при рН-от 1,5- 6,0 | — | stable at pH from 1.5-6.0 |
| 2) | ДТРА | Стабилен при рН от 1,5-7,0 | — | stable at pH –1.5–7.0 |
| 3) | ЕДДНА | Стабилен при рН от 3,0-10 | — | stable at pH from 3.0-10 |
Чем лучше хелатирующий агент, тем он стабильнее в водном растворе (Стабильность хелатов, хелатирующего агента в водном растворе ).