Химерный онкоген bcr abl p210 что это
Химерный онкоген bcr abl p210 что это
Этиология и встречаемость хронического миелоидного лейкоза (ХМЛ). Хронический миелоидный лейкоз (ХМЛ) (MIM №608232) — клональная экспансия трансформированных кроветворных клеток-предшественниц, при которой возрастает число циркулирующих миелоидных клеток. Трансформация клеток-предшественниц происходит за счет экспрессии онкогена BCR-ABL.
Хронический миелоидный лейкоз (ХМЛ) составляет до 15% всех случаев лейкоза у взрослых и встречается с частотой 1-2 на 100 000; скорректированная возрастная встречаемость более высокая среди мужчин, чем среди женщин (1,3-1,7 против 1,0).
Патогенез хронического миелоидного лейкоза (ХМЛ)
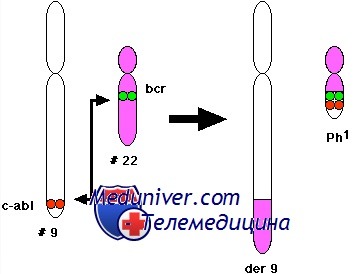
Приблизительно 95% пациентов с хроническим миелоидным лейкозом (ХМЛ) имеют филадельфийскую хромосому; остальные — сложные варианты транслокаций. Протоонкоген Абельсона (ABL), кодирующий нерецепторную тирозинкиназу, находится в сегменте 9q34, а ген точечного разрыва кластерного региона (BCR), кодирующий фосфопротеин, — в 22qll.
При образовании филадельфийской хромосомы ген ABL разрывается в интроне 1, а ген BCR в одном из трех кластерных регионов разрыва; в производной хромосоме 22 фрагменты генов BCR и ABL соединяются «голова в хвост». Объединенный ген BCR-ABL в транслоцированной хромосоме 22 генерирует белок, изменяющийся по величине в зависимости от длины пептида Bcr, присоединяющегося к N-концу.
До настоящего времени функции белков Abl и Bcr в норме окончательно не определены. Белок Abl довольно хорошо сохраняется в ходе эволюции многоклеточных. Он присутствует как в ядре, так и в цитоплазме и связан с внутренней цитоплазматической мембраной. Относительное количество белка Abl в этих частях клетки изменяется в различных типах клеток, а также в ответ на стимулы.
Abl участвует в клеточном цикле, ответе на стресс, передаче сигналов от интегринов и в нервном развитии. Функциональные области Bcr включают двойную спираль для полимеризации с другими белками, область треонин-серин-киназы, область обмена ГДФ-ГТФ, вовлеченную в регуляцию белков семейства Ras, и область активации ГТФ, участвующую в регуляции Rac и Rho ГТФаз.
Экспрессия Abl не приводит к трансформации клеток, вызываемой экспрессией химерного белка Bcr-Abl. У трансгенных мышей, вырабатывающих химерный Bcr-Abl с рождения, развивается острый лейкоз, а инфицирование здоровых мышей ретровирусами, экспрессирующими Bcr-Abl, вызывает ряд острых и хронических лейкозов, в зависимости от генетического фона.
В отличие от белка Abl, химерный белок Bcr-Abl имеет активность конститутивной тирозинкиназы и ограничен цитоплазмой, где энергично связывает микрофибриллы актина. Bcr-Abl фосфорилирует несколько цитоплазматических субстратов и тем самым активизирует сигнальные каскады, управляющие ростом, дифференцировкой и, возможно, адгезией кроветворных клеток.
Неправильная активизация этого сигнального пути приводит к неуправляемому распространению гемопоэтических стволовых клеток, выходу незрелых клеток из костного мозга, и, в конце концов, к хроническому миелоидному лейкозу (ХМЛ).
По мере развития хронического миелоидного лейкоза (ХМЛ) становится все более агрессивным. В ходе этой эволюции клетки опухоли у 50-80% пациентов приобретают дополнительные хромосомные изменения [трисомию 8,i(17q), или трисомию 19], вторую филадельфийскую хромосому. Кроме описанных цитогенетических изменений, при развитии хронического миелоидного лейкоза (ХМЛ) также часто мутируют гены-супрессоры опухолевого роста и протоонкогены.
Фенотип и развитие хронического миелоидного лейкоза (ХМЛ)
Хронический миелоидный лейкоз (ХМЛ) — двух- или трехфазная болезнь. Начальный, или хронический этап характеризуется незаметно подкрадывающимся началом с постепенным развитием усталости, недомогания, потери массы тела и минимальным или умеренным увеличением селезенки. Со временем хронический миелоидный лейкоз (ХМЛ) обычно переходит в фазу акселерации и затем в бластный криз, хотя некоторые пациенты переходят непосредственно от хронической фазы в бластный криз.
Развитие хронического миелоидного лейкоза (ХМЛ) включает появление дополнительных хромосомных аномалий в клетках опухоли, прогрессирующего лейкоцитоза, анемии, тромбоцитоза или тромбоцитопении, всевозрастающую спленомегалию, лихорадку и костные нарушения. Властный криз — состояние острого лейкоза, бласты могут быть миелоидными, лимфоидными, эритроидными или недифференцированными. Фаза акселерации — промежуточная между хронической фазой и бластным кризом.
Приблизительно 85% больных диагностируют в хронической фазе. В зависимости от метода исследования, средний возраст постановки диагноза колеблется от 45 до 65 лет, хотя заболеванию подвержены лица любых возрастов. При отсутствии лечения показатель перехода из хронической фазы в бластный криз составляет приблизительно 5-10% в первые 2 года и затем 20% за год. Поскольку бластный криз быстро приводит к летальному исходу, развитие криза равнозначно смерти.
Особенности фенотипических проявлений хронического миелоидного лейкоза (ХМЛ):
• Возраст начала: от середины до конца зрелости
• Лейкоцитоз
• Спленомегалия
• Усталость и недомогание
Лечение хронического миелоидного лейкоза (ХМЛ)
Выяснение молекулярной основы хронического миелоидного лейкоза (ХМЛ) привело к разработке специфического ингибитора тирозинкиназы Bcr-Abl — иматиниба (гливек). Теперь это лекарство — основной препарат при лечении хронического миелоидного лейкоза (ХМЛ). Более 85% больных дают четкий цитогенетический ответ на терапию иматинибом, с исчезновением t(9;22) в клетках, получаемых при пункции костного мозга.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Химерный онкоген bcr abl p210 что это
Молекулярно-биологическое исследование, позволяющее количественно оценить содержание в клетках белкового продукта мутантного гена BCR-ABL, который играет основную роль в развитии хронического миелолейкоза.
Количественная ПЦР в реальном времени, транскрипт химерного гена BCR-ABL.
BCR/ABL1, mRNA Detection, Reverse Transcription-PCR (RT-PCR), Quantitative, Monitoring Chronic Myeloid Leukemia (CML); Tyrosine kinase inhibitor (TKI) therapy monitoring, PCR.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Исследование проводится методом полимеразной цепной реакции. Принцип метода основан на обнаружении в исследуемом материале фрагментов ДНК химерного гена BCR-ABL, их избирательном синтезе с образованием большого числа копий. Копирование ДНК мутантного гена происходит после добавления в реакцию праймеров – последовательностей ДНК, аналогичных BCR-ABL. При этом праймеры должны быть идентичны той разновидности гена, содержание которой исследуется в образце, – для генов, кодирующих белки с разной молекулярной массой (р190, р210 и р230), нужны разные праймеры, так как их ДНК, хоть и совсем незначительно, но отличаются друг от друга. При проведении исследования в рамках первичной диагностики могут быть сделаны ПЦР на разные транскрипты гена, но в последующих измерениях целесообразно определять транскрипт, выявленный изначально, чтобы оценивать динамику его снижения. Одновременно с копированием мутантного гена производится копирование контрольного гена, исходное количество которого заведомо известно. Уровень мутантного гена рассчитывают относительно контрольного в процентах, в соответствии с международной шкалой экспрессии гена BCR-ABL (IS), или по уровню снижения в логарифмах (в 10 раз – 1 log, в 100 раз – 2 log) по сравнению с выявленным до начала лечения. При этом оценка по IS более предпочтительна.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Результат выражается в процентах – уровень экспрессии мутантного гена BCR-ABL относительно контрольного гена. Уровни достигнутого ответа дифференцируются следующим образом:
0,1% и менее – большой молекулярный ответ – снижение транскрипта в 1000 раз (или на 3 логарифма) от исходного;
0,001% и менее или не определяется – полный молекулярный ответ.
Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с обязательной микроскопией мазка крови)
Стандартное кариотипирование клеток костного мозга
Кто назначает исследование?
Гематолог, онколог, терапевт, врач общей практики.
Wintrobe’s clinical hematology / editors, John P. Greer, Daniel A. Arber, Bertil Glader, Alan F. List, Robert T. Means Jr., Frixos Paraskevas, George M. Rodgers. – 13th edition. Lippincott Williams & Wilkins, 2014. Pages 1711-1712.
NCCN Clinical Practice Guidelines in Oncology: Chronic Myeloid Leukemia. Version 4.2018 – January 24, 2018. Available at www.nccn.org.
BCR-ABL
Что такое BCR-ABL?
BCR-ABL — гибридный белок, продукт гибридного гена BCR-ABL1, формирующегося в результатереципрокной транслокации между хромосомами 9 и 22 (филадельфийская хромосома). BCR-ABL является конститутивно активной тирозинкиназой, ответственной за онкогенную трансформацию клеток (онкобелком). Постоянная активность этой тирозинкиназы делает клетку нечувствительной к воздействию факторов роста и вызывает её избыточную пролиферацию..
Белок BCR-ABL существует в трёх формах: p190, p210 и p230, в зависимости от места прерывания BCR-фрагмента.
Новый ген вызывает синтез нового белка, приводящего к формированию злокачественных клеток крови в костном мозге.
Хронический миелолейкоз (ХМЛ)
Данная форма лейкоза характеризуется ускоренной и нерегулируемой пролиферацией преимущественно миелоидных клеток в костном мозге с их накоплением в крови.
У абсолютного большинства людей с этим диагнозом наблюдается «филадельфийская хромосома» (BCR-ABL). К факторам риска, способствующим появлению болезни, относятся воздействие бензола и высоких доз радиации.
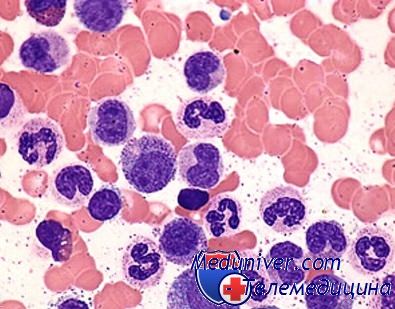
Большинство пациентов узнают о своей болезни случайно, после получения результатов обычного анализа крови. При данном диагнозе отмечается резкое увеличение количества молодых лейкоцитов. В случае, когда результаты анализа крови вызывают подозрение на лейкоз, пациента направляют на биопсию костного мозга.
Продолжительность хронической фазы зависит от того, насколько рано было диагностировано заболевание, а также от успешности проведённого лечения. Несвоевременное выявление болезни ведет к возникновению ускоренной стадии и острой форме лейкоза.
Лечение ХМЛ: таргетная (целевая) терапия ингибиторами тирозинкиназ: иматиниб, нилотиниб, дазатиниб и др. Данная терапия значительно улучшила показатели выживаемости.
Острый B-лимфобластный лейкоз (ОЛЛ)
Считается самым распространенным видом лейкоза у детей, но нередко встречается и у взрослых. В противоположность хроническому лейкозу развивается очень быстро. Термин «лимфобластный» означает, что незрелые клетки, составляющие основу болезни, являются лимфобластами, то есть предшественниками лимфоцитов.
Вероятность возникновения ОЛЛ несколько повышена у людей, проходивших лечение с использованием облучения или определенных видов химиотерапии.
Самые неблагоприятные прогнозы и сложное лечение болезни отмечается именно при наличии у больного мутантной филадельфийской хромосомы (BCR-ABL). Без лечения ОЛЛ приводит к гибели в течение нескольких месяцев или даже недель.
Вероятность достижения ремиссии:
Точечная мутация T315I в BCR-ABL области может вызвать резистентность пациента к назначаемым препаратам.
Следовательно, перед началом лечения следует подтвердить или опровергнуть наличие данной мутации.
Выявление и количественное определение мРНК химерного гена bcr-abl (р210) в Москве
Лабораторный анализ основного маркера хронического миелоидного лейкоза.
Приём и исследование биоматериала
Когда нужно сдавать анализ Выявление и количественное определение мРНК химерного гена bcr-abl (р210)?
Подробное описание исследования
Хронический миелоидный лейкоз (ХМЛ), или миелолейкоз, — клональное онкогенетическое заболевание, которое происходит из мутировавших злокачественных кроветворных — миелоидных — клеток костного мозга. На данный момент причины, по которым развивается миелолейкоз, не установлены. К факторам риска в основном относят инфекционные заболевания и радиационное облучение.
Для хронического миелоидного лейкоза характерны:
Ph, или филадельфийская хромосома, — это аномальная хромосома, которая возникает при обмене участков 9 и 22 хромосом. Данный обмен называют транслокацией, в результате неё возникает химерный онкоген BCR-ABL, который приводит к бесконтрольному росту клеток миелоидной линии (нейтрофилов, эозинофилов, базофилов и моноцитов). В норме избыточное кроветворение блокируется специфическими сигналами, однако аномальный белок BCR-ABL не воспринимает их. Со временем опухолевая масса вытесняет нормальные клетки кровяного ростка костного мозга.
При обмене участков 9 и 22 хромосом в местах обмена образуются разрывы. В зависимости от места разрыва могут быть разные транскрипты — генетические материалы в виде молекулы РНК — BCR-ABL. Основной транскрипт (мРНК) этого гена — p210. Данное исследование направлено на количественное определение именного этого варианта транскрипта BCR-ABL.
Клиническая картина хронического миелоидного лейкоза протекает в три фазы: хроническая, фаза акселерации и бластный криз. Заболевание начинается бессимптомно, затем появляется интоксикация и характерный синдром — гепатоспленомегалия (увеличение размеров печени и селезенки). В этот период в крови можно обнаружить избыточный уровень лейкоцитов. По мере прогрессирования болезни объем селезенки увеличивается в несколько раз, в крови выявляется анемия и низкий показатель тромбоцитов, а также появляются бластные клетки. Клинически у пациентов могут быть следующие симптомы:
Диагноз хронический миелолейкоз устанавливают при помощи полимеразной цепной реакции (ПЦР), который количественно определяет мРНК BCR-ABL p210. Помимо этого, данный метод используют у пациентов с выявленным ХМЛ для оценки эффективности получаемого лечения, проводимого в основном таргетными препаратами — ингибиторами BCR/ABL тирозинкиназы.
Химерный онкоген bcr abl p210 что это
Молекулярно-биологическое исследование, направленное на выявление точечных мутаций в гене BCR-ABL, которые могут обуславливать резистентность хронического миелолейкоза к некоторым ингибиторам тирозинкиназ.
Определение мутаций киназного домена BCR-ABL.
BCR/ABL1, Tyrosine Kinase Inhibitor Resistance, Kinase Domain Mutation Screen; Kinase domain mutation, ABL.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Хронический миелолейкоз является опухолевым заболеванием кроветворной системы, в результате которого в периферической крови наблюдается повышение уровня определенного вида лейкоцитов. Развитие заболевания связано с возникновением в стволовой клетке крови генетической аномалии, которая получила название филадельфийской хромосомы. У человека на девятой хромосоме локализуется ген ABL, который кодирует образование белка, стимулирующего рост и деление клеток. При хроническом миелолейкозе часть гена ABL перемещается на хромосому 22, такая мутация называется транслокацией. Место разрыва 22-й хромосомы, куда чаще всего встраивается перемещенная часть гена ABL, называется M-bcr (от английского major breakpoint claster region). В норме в этом участке хромосомы расположен ген BCR, кодирующий белок, функция которого в настоящее время достоверно не изучена, однако есть сведения, что он участвует в процессах деления и дифференцировки клеток. В результате транслокации на 22-й хромосоме образуется сливной, или химерный, ген BCR-ABL, при считывании информации с которого продуцируется белок р210. От части гена ABL этот белок получает способности тирозинкиназы – внутриклеточного фермента, участвующего в передаче сигналов пролиферации, а часть, кодируемая геном BCR, способствует его активации. Таким образом, в результате описанной мутации на 22-й хромосоме формируется ген, белковый продукт которого – тирозинкиназа с повышенной активностью – стимулирует деление клеток с полной независимостью от внешних регуляторных механизмов. Лейкозные клетки становятся нечувствительными к сигналам самоуничтожения, приобретают способность выходить из костного мозга в периферическую кровь, не дожидаясь созревания.
В первое время лейкозные клетки полностью контролируются геном BCR-ABL, они сохраняют способность к дифференцировке и функционируют практически полноценно. Однако в процессе течения заболевания ген BCR-ABL индуцирует нестабильность генома, вследствие неконтролируемой пролиферации возникают точечные мутации, в том числе в самом гене BCR-ABL. Некоторые мутации могут приводить к перестройке той части молекулы BCR-ABL-тирозинкиназы, к которой присоединяются таргетные лекарственные препараты, подавляющие её активность. В результате этого препарат теряет способность связываться с мутантной тирозинкиназой и ингибировать её. По этой причине, несмотря на продолжающийся постоянный прием лекарства, отмечается прогрессирование заболевания. К настоящему времени обнаружено свыше 50 различных мутаций гена BCR-ABL, которые могут обуславливать резистентность опухолевого клона к одному или нескольким ингибиторам тирозинкиназ.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Результат исследования представляет собой название обнаруженной мутации гена BCR-ABL и сведения о её влиянии на чувствительность к определенным ингибиторам тирозинкиназ.
Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с обязательной микроскопией мазка крови)
Кто назначает исследование?
Гематолог, онколог, терапевт, врач общей практики.
NCCN Clinical Practice Guidelines in Oncology: Chronic Myeloid Leukemia. Version 4.2018 – January 24, 2018. Available at www.nccn.org.