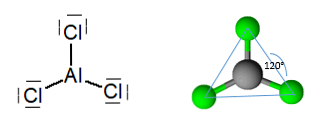Хлорид алюминия с чем взаимодействует
Алюминий. Химия алюминия и его соединений
Бинарные соединения алюминия
Алюминий
Положение в периодической системе химических элементов
Алюминий расположен в главной подгруппе III группы (или в 13 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение алюминия и свойства
Электронная конфигурация алюминия в основном состоянии :
+13Al 1s 2 2s 2 2p 6 3s 2 3p 1 1s 



Электронная конфигурация алюминия в возбужденном состоянии :
+13Al * 1s 2 2s 2 2p 6 3s 1 3p 2 1s 



Алюминий проявляет парамагнитные свойства. Алюминий на воздухе быстро образует прочные оксидные плёнки, защищающие поверхность от дальнейшего взаимодействия, поэтому устойчив к коррозии.
Физические свойства
Алюминий – лёгкий металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Обладает высокой тепло- и электропроводностью.
Алюминий — один из наиболее ценных цветных металлов для вторичной переработки. На протяжении последних лет, цена на лом алюминия в пунктах приема непреклонно растет. По ссылке можно узнать о том, как сдать лом алюминия.
Нахождение в природе
Алюминий — самый распространенный металл в природе, и 3-й по распространенности среди всех элементов (после кислорода и кремния). Содержание в земной коре — около 8%.
В природе алюминий встречается в виде соединений:
Корунд Al2O3. Красный корунд называют рубином, синий корунд называют сапфиром.
Способы получения
Алюминий образует прочную химическую связь с кислородом. Поэтому традиционные способы получения алюминия восстановлением из оксида протекают требуют больших затрат энергии. Для промышленного получения алюминия используют процесс Холла-Эру. Для понижения температуры плавления оксид алюминия растворяют в расплавленном криолите (при температуре 960-970 о С) Na3AlF6, а затем подвергают электролизу с углеродными электродами. При растворении в расплаве криолита оксид алюминия распадается на ионы:
На катоде происходит восстановление ионов алюминия:
Катод: Al 3+ +3e → Al 0
На аноде происходит окисление алюминат-ионов:
Суммарное уравнение электролиза расплава оксида алюминия:
Лабораторный способ получения алюминия заключается в восстановлении алюминия из безводного хлорида алюминия металлическим калием:
AlCl3 + 3K → Al + 3KCl
Качественные реакции
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид алюминия растворяется с образованием тетрагидроксоалюмината:
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Соли алюминия можно обнаружить с помощью водного раствора аммиака. При взаимодействии растворимых солей алюминия с водным раствором аммиака также в ыпадает полупрозрачный студенистый осадок гидроксида алюминия.
AlCl3 + 3NH3·H2O = Al(OH)3 ↓ + 3NH4Cl
Al 3+ + 3NH3·H2O = Al(OH)3 ↓ + 3NH4 +
Видеоопыт взаимодействия раствора хлорида алюминия с раствором аммиака можно посмотреть здесь.
Химические свойства
1.1. Алюминий реагируют с галогенами с образованием галогенидов:
1.2. Алюминий реагирует с серой с образованием сульфидов:
Al + P → AlP
1.4. С азотом алюминий реагирует при нагревании до 1000 о С с образованием нитрида:
2Al + N2 → 2AlN
1.5. Алюминий реагирует с углеродом с образованием карбида алюминия:
1.6. Алюминий взаимодействует с кислородом с образованием оксида:
Видеоопыт взаимодействия алюминия с кислородом воздуха (горение алюминия на воздухе) можно посмотреть здесь.
2. Алюминий взаимодействует со сложными веществами:
2.1. Реагирует ли алюминий с водой? Ответ на этот вопрос вы без труда найдете, если покопаетесь немного в своей памяти. Наверняка хотя бы раз в жизни вы встречались с алюминиевыми кастрюлями или алюминиевыми столовыми приборами. Такой вопрос я любил задавать студентам на экзаменах. Что самое удивительное, ответы я получал разные — у кого-то алюминий таки реагировал с водой. И очень, очень многие сдавались после вопроса: «Может быть, алюминий реагирует с водой при нагревании?» При нагревании алюминий реагировал с водой уже у половины респондентов))
2Al 0 + 6 H2 + O → 2 Al +3 ( OH)3 + 3 H2 0
Амальгаму алюминия можно получить, выдержав кусочки алюминия в растворе хлорида ртути ( II ):
3HgCl2 + 2Al → 2AlCl3 + 3Hg
Видеоопыт взаимодействия амальгамы алюминия с водой можно посмотреть здесь.
2.2. Алюминий взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль и водород.
2Al + 6HCl = 2AlCl3 + 3H2↑
2.3. При обычных условиях алюминий не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат алюминия и вода:
2.4. Алюминий не реагирует с концентрированной азотной кислотой также из-за пассивации.
С разбавленной азотной кислотой алюминий реагирует с образованием молекулярного азота:
При взаимодействии алюминия в виде порошка с очень разбавленной азотной кислотой может образоваться нитрат аммония:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2 ↑
Видеоопыт взаимодействия алюминия со щелочью и водой можно посмотреть здесь.
Алюминий реагирует с расплавом щелочи с образованием алюмината и водорода:
2Al + 6NaOH → 2Na3AlO3 + 3H2 ↑
Эту же реакцию можно записать в другом виде (в ЕГЭ рекомендую записывать реакцию именно в таком виде):
2Al + 6NaOH → 2NaAlO2 + 3H2↑ + 2Na2O
2Al + 3CuO → 3Cu + Al2O3
Еще пример : алюминий восстанавливает железо из железной окалины, оксида железа (II, III):
Восстановительные свойства алюминия также проявляются при взаимодействии его с сильными окислителями: пероксидом натрия, нитратами и нитритами в щелочной среде, перманганатами, соединениями хрома (VI):
Хлорид алюминия (AlCl3) химическая структура, свойства, использование
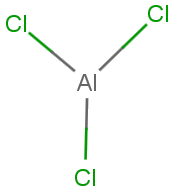
хлорид алюминия или трихлорид алюминия (AlCl3бинарная соль, образованная алюминием и хлором. Иногда это выглядит как желтый порошок, потому что он содержит примеси из-за присутствия хлорида железа (III).
Это получается путем объединения его элементов. Алюминий, который имеет три электрона на своем последнем энергетическом уровне (семейство IIIA), имеет тенденцию давать их из-за своего металлического характера. Хлор с семью электронами на последнем энергетическом уровне (семейство VIIA) стремится получить их для завершения своего октета.
Считается, что связь, образованная между алюминием и хлором в трихлориде алюминия, является ковалентной, хотя это соединение между металлом и неметаллом..
Существует два вида хлорида алюминия:
Химическая структура
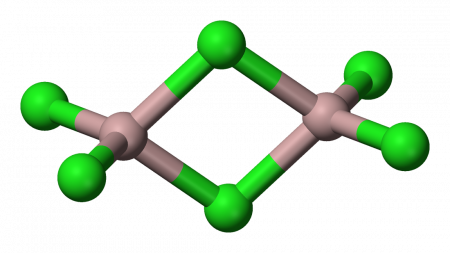
Тем не менее, молекула организована в виде димеры, в котором атом хлора жертвует пару электронов для образования связей. Они известны как скоординированные ковалентные связи.
Так определяется организация димеров трихлорида алюминия..
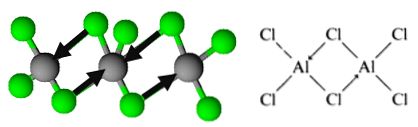
Эта организация позволяет соединению формировать сети димерных слоев. Когда вода наливается на твердый трихлорид алюминия, они не диссоциируют, как ожидается от ионных соединений, но подвергаются интенсивному гидролизу.
Напротив, в разбавленном водном растворе находятся координированные ионы [Al (H).2O)6] +3 и хлорид. Эти структуры очень похожи на диборан.
Таким образом, у вас есть формула Al2Cl6
Если измеряется разница в электроотрицательности атомов, составляющих связи в этом соединении, можно наблюдать следующее:
Согласно правилам теории связи, чтобы соединение было ионным, оно должно иметь разность электроотрицательности атомов, составляющих связь, на величину, большую или равную 1,7 С..
В случае связи Al-Cl разница в электроотрицательности составляет 1,55 ° С, что дает треххлористому алюминию структуру ковалентной связи. Это небольшое значение можно отнести к координированным ковалентным связям, представленным молекулой.
свойства
физическое
внешний вид: белое твердое вещество, иногда желтое из-за примесей, вызванных хлоридом железа
плотность: 2,48 г / мл
Молярная масса: 133,34 г / моль
сублимация: сублимируется при 178 ° C, поэтому температура его плавления и кипения очень низкая.
вождение: плохо проводит электричество.
растворимость: он не растворяется в воде, потому что это кислота Льюиса. Растворим в органических растворителях, таких как бензол, четыреххлористый углерод и хлороформ.
химическая
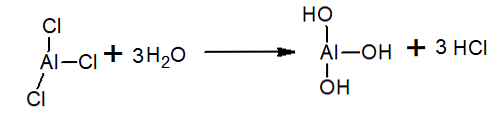
В воде трихлорид алюминия гидролизуется с образованием HCl, иона гидроксония и гидроксида алюминия:
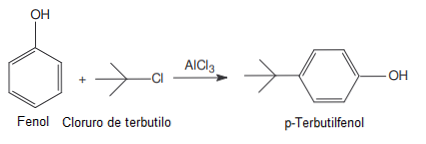
Он используется в реакциях Фриделя-Крафтса в качестве катализатора (вещество, которое может быть извлечено в конце реакции, потому что оно только в нем, чтобы ускорить, замедлить или инициировать реакцию).
Это едкое вещество.
При разложении, когда он бурно реагирует с водой, образуется оксид алюминия и опасные газы, такие как хлористый водород.
приложений
Риски: возможные последствия
рекомендации
Избегайте воздействия продукта без необходимых мер безопасности. Обязательно используйте, защитные очки, перчатки, соответствующую одежду, накрытую обувь.
В случае контакта с кожей. AlCl3 Это вызывает коррозию. Это может вызвать раздражение или ожоги с покраснением и болью. Вымойте сразу после контакта с большим количеством воды в течение не менее 20 минут. Не нейтрализуйте и не добавляйте вещества, кроме воды. Снять загрязненную одежду и выстирать ее перед повторным использованием. немедленно обратиться к врачу в случае травмы.
При попадании в глаза. AlCl3 Это вызывает коррозию. Это вызывает сильную боль, помутнение зрения и повреждение тканей. Немедленно промойте глаза водой в течение не менее 20 минут и держите веки открытыми, чтобы очистить весь глаз и ткани века. Промывание глаз в считанные секунды необходимо для достижения максимальной эффективности. Если у вас есть контактные линзы, снимите их через первые 5 минут, а затем продолжайте промывать глаза. Проконсультируйтесь с врачом. Это может привести к серьезному повреждению роговицы, конъюнктивы или других частей глаза..
В случае проглатывания. AlCl3 Это вызывает коррозию. Жжение может вызвать боль во рту и пищеводе и ожоги слизистых оболочек. Он может вызывать желудочно-кишечный дискомфорт при болях в животе, тошноте, рвоте и диарее. НЕ вызывать рвоту. Прополощите рот и дайте пить воду. Никогда не давайте ничего в устной форме человеку без сознания. Позвони доктору. Если рвота возникает спонтанно, положите пострадавшего на бок, чтобы снизить риск аспирации..
Люди с имеющимися кожными заболеваниями, проблемами со зрением или нарушениями дыхательной функции могут быть более подвержены воздействию вещества
Упаковка и хранение соединения AlCl3 должно быть сделано в проветриваемых, чистых и сухих местах.
Хлорид алюминия
(80 °C) 48,6 г/100 мл (100 °C) 49 г/100 мл
слабо растворим в бензоле
крысы, перорально: 380 мг/кг
гексагидрат
крысы, орально: 3,311 г/кг

Хлорид алюминия (хлористый алюминий) — неорганическое соединение, соль алюминия и соляной кислоты с химической формулой AlCl3.
Содержание
Свойства
В воде хорошо растворим (44,38 г в 100 г H2O при 25 °C). Из водных растворов выпадает в виде кристаллогидрата AlCl3·6H2O — желтовато-белые расплывающиеся на воздухе кристаллы. Хорошо растворим во многих органических соединениях (в этаноле — 100 г в 100 г спирта при 25 °C, в ацетоне, 1,2-дихлорэтане, этиленгликоле, нитробензоле, тетрахлоруглероде и др.); практически не растворяется в бензоле и толуоле.
Получение
Важнейший способ получения хлорида алюминия в промышленности — действие смеси Cl2 и CO на обезвоженный каолин или боксит в шахтных печах:
При температуре в 900 °C трихлорид бора и фосфид алюминия образуют фосфид бора и хлорид алюминия:
BCl3 + AlP → 900oC BP + AlCl3
Также есть и другие способы получения хлорида алюминия:
Al + FeCl3 → AlCl3 + Fe Al(OH)3 + 3 HCl → AlCl3 + 3 H2O 3 CuCl2 + 2 Al → 2 AlCl3 + 3 C u 2 Al + 6 HCl → 2 AlCl3 + 3 H2
Применение
Безводный хлорид алюминия образует аддукты со многими неорганическими (например, NH3, H2S, SO2) и органическими (хлорангидриды кислот, эфиры и др.) веществами, с чем связано важнейшее техническое применение AlCl3 как катализатора при переработке нефти и при органических синтезах (например, реакция Фриделя — Крафтса).
Гексагидрат хлорида алюминия и его растворы используются при очистке сточных вод, обработке древесины, производстве антиперспирантов и пр.
Токсичность и безопасность
Хлорид алюминия токсичен при попадании в организм, а также обладает коррозионной активностью.
2.2.3. Характерные химические свойства алюминия.
Взаимодействие алюминия с простыми веществами
с кислородом
При контакте абсолютно чистого алюминия с воздухом атомы алюминия, находящиеся в поверхностном слое, мгновенно взаимодействуют с кислородом воздуха и образуют тончайшую, толщиной в несколько десятков атомарных слоев, прочную оксидную пленку состава Al2O3, которая защищает алюминий от дальнейшего окисления. Невозможно и окисление крупных образцов алюминия даже при очень высоких температурах. Тем не менее, мелкодисперсный порошок алюминия довольно легко сгорает в пламени горелки:
с галогенами
Алюминий очень энергично реагирует со всеми галогенами. Так, реакция между перемешанными порошками алюминия и йода протекает уже при комнатной температуре после добавления капли воды в качестве катализатора. Уравнение взаимодействия йода с алюминием:
С бромом, представляющим собой тёмно-бурую жидкость, алюминий также реагирует без нагревания. Образец алюминия достаточно просто внести в жидкий бром: тут же начинается бурная реакция с выделением большого количества тепла и света:
Реакция между алюминием и хлором протекает при внесении нагретой алюминиевой фольги или мелкодисперсного порошка алюминия в заполненную хлором колбу. Алюминий эффектно сгорает в хлоре в соответствии с уравнением:
с серой
При нагревании до 150-200 о С или после поджигания смеси порошкообразных алюминия и серы между ними начинается интенсивная экзотермическая реакция с выделением света:
— сульфид алюминия
с азотом
При взаимодействии алюминия с азотом при температуре около 800 o C образуется нитрид алюминия:
с углеродом
Взаимодействие алюминия со сложными веществами
с водой
Как уже было сказано выше, стойкая и прочная оксидная пленка из Al2O3 не дает алюминию окисляться на воздухе. Эта же защитная оксидная пленка делает алюминий инертным и по отношению к воде. При снятии защитной оксидной пленки с поверхности такими методами, как обработка водными растворами щелочи, хлорида аммония или солей ртути (амальгирование), алюминий начинает энергично реагировать с водой с образованием гидроксида алюминия и газообразного водорода:
с оксидами металлов
После поджигания смеси алюминия с оксидами менее активных металлов (правее алюминия в ряду активности) начинается крайне бурная сильно-экзотермическая реакция. Так, в случае взаимодействия алюминия с оксидом железа (III) развивается температура 2500-3000 о С. В результате этой реакции образуется высокочистое расплавленное железо:
Данный метод получения металлов из их оксидов путем восстановления алюминием называется алюмотермией или алюминотермией.
с кислотами-неокислителями
Взаимодействие алюминия с кислотами-неокислителями, т.е. практически всеми кислотами, кроме концентрированной серной и азотной кислот, приводит к образованию соли алюминия соответствующей кислоты и газообразного водорода:
2Аl 0 + 6Н + = 2Аl 3+ + 3H2 0 ;
с кислотами-окислителями
-концентрированной серной кислотой
Взаимодействие алюминия с концентрированной серной кислотой в обычных условиях, а также низких температурах не происходит вследствие эффекта, называемого пассивацией. При нагревании реакция возможна и приводит к образованию сульфата алюминия, воды и сероводорода, который образуется в результате восстановления серы, входящей в состав серной кислоты:
— концентрированной азотной кислотой
Концентрированная азотная кислота в обычных условиях также пассивирует алюминий, что делает возможным ее хранение в алюминиевых емкостях. Так же, как и в случае с концентрированной серной, взаимодействие алюминия с концентрированной азотной кислотой становится возможным при сильном нагревании, при этом преимущественно параллельно протекают реакции:
— разбавленной азотной кислотой
Взаимодействие алюминия с разбавленной по сравнению с концентрированной азотной кислотой приводит к продуктам более глубокого восстановления азота. Вместо NO в зависимости от степени разбавления могут образовываться N2O и NH4NO3:
со щелочами
Алюминий реагирует как с водными растворами щелочей:
так и с чистыми щелочами при сплавлении:
В обоих случаях реакция начинается с растворения защитной пленки оксида алюминия:
В случае водного раствора алюминий, очищенный от защитной оксидной пленки, начинает реагировать с водой по уравнению:
Образующийся гидроксид алюминия, будучи амфотерным, реагирует с водным раствором гидроксида натрия с образованием растворимого тетрагидроксоалюмината натрия: