Хлорметилен что это такое
Метиленхлорид
Метиленхлорид
| Дихлорметан | |
 | |
 | |
| Общие | |
|---|---|
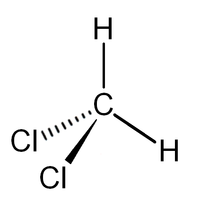
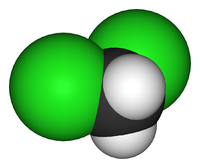
| Систематическое наименование | дихлорметан |
| Сокращения | ДХМ |
| Традиционные названия | дихлорметан, метилен хлористый |
| Химическая формула | CH2Cl2 |
| Эмпирическая формула | CH2Cl2 |
| Молярная масса | 84.9 г/моль |
| Физические свойства | |
| Плотность вещества | 1.3266 г/см³ |
| Примеси | хлорметаны |
| Состояние (ст. усл.) | подвижная прозрачная жидкость |
| Термические свойства | |
| Температура плавления | -96.7 °C |
| Температура кипения | 40 °C |
| Температура вспышки | 14 °C |
| Критическая точка | 245 |
| Энтальпия (ст. усл.) | -87.86 кДж/моль |
| Удельная теплота парообразования | 336,4 Дж/кг |
| Давление пара | 470 |
| Химические свойства | |
| Растворимость в воде | 20 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4242 |
| Классификация | |
| номер CAS | 75-09-2 |
| RTECS | PA8050000 |
Дихлорметан (хлористый метилен, ДХМ, CH2Cl2) — прозрачная лекгоподвижная и легколетучая жидкость с характерным для галогенпроизводных сладковатым запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету. В целом наиболее безопасен среди галогеналканов.
Содержание
Получение
Получают прямым хлорированием метана хлором в условиях радикального механизма при 400—500 °С при соотношении равном 5:1
В результате получается смесь всех возможных хлоридов: хлорметан, дихлорметан, хлороформ и четырёххлористый углерод, которые потом разделяются дистилляцей. После чего он имеет чистоту не менее 99,7% В 1995 году годовое производство оценивалось в 500 миллионов тонн.
Свойства
Применение
Дешевизна, высокая способность растворять многие органические вещества, легкость удаления, относительно малая токсичность привела к широкому применению его как растворитель для проведения реакций, экстракций в том числе и в лабораториях. Используют в смесях для снятия лака, обезжиривания поверхностей. В пищевой промышленности используют для приготовления быстрорастворимого кофе, экстракта хмеля и других пищевых препаратов. Для растворение смол, жиров, битума. Его высокая летучесть используется для вспенивания полиуретанов. Также используется в хроматографии. В промышленности в смеси с полимерами используют для создания формы которая быстро застывает за счёт испарения дихлорметана. Он же используется для склеивания этих пластиков: полистирол, поликарбонат, полиэтилентерефталат, АБС-пластик, но не для полиэтилена и полипропилена.
Очистка в лаборатории
Специализированные применения
Используется в составах для склеивания пластиков. В смеси с метанолом используют как пропеллент, в качестве хладагента.
Безопасность
Хотя он и является наименее ядовитым среди галогеналканов, но нужно быть осторожным при обращении, так как он очень летуч и может вызвать острое отравление. Вытяжная вентиляция необходима. В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлрометаном может вызвать накопление его в жировых тканях и привести к ожогу. Также при длительной работе с ним возможно поражение печени и нейропатия. На крысах показано, что он может вызывать рак лёгких, печени и поджелудочной железы. В тоже время не было отмечено какого либо влияния на развития эмбрионов у женщин имевших контакт с ДХМ.
Общая безопасность и методы устранения аварий [3]
Дихлорметан
| Дихлорметан | |
 | |
 | |
| Общие | |
|---|---|
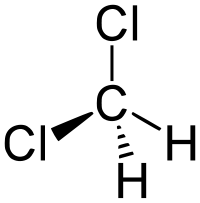
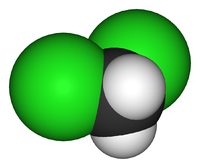
| Систематическое наименование | дихлорметан |
| Сокращения | ДХМ |
| Традиционные названия | дихлорметан, метилен хлористый |
| Химическая формула | CH2Cl2 |
| Эмпирическая формула | CH2Cl2 |
| Физические свойства | |
| Состояние (ст. усл.) | подвижная прозрачная жидкость |
| Примеси | хлорметаны |
| Молярная масса | 84.9 г/моль |
| Плотность | 1.3266 г/см³ |
| Термические свойства | |
| Температура плавления | -96.7 °C |
| Температура кипения | 40 °C |
| Температура вспышки | 14 °C |
| Критическая точка | 245 |
| Энтальпия образования (ст. усл.) | -87.86 кДж/моль |
| Удельная теплота испарения | 336,4 Дж/кг |
| Давление пара | 470 |
| Химические свойства | |
| Растворимость в воде | при 20 °C 1.3 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4242 |
| Классификация | |
| Рег. номер CAS | 75-09-2 |
| SMILES | C(Cl)Cl |
| RTECS | PA8050000 |
Дихлормета́н (хлористый метилен, ДХМ, CH2Cl2) — прозрачная легкоподвижная и легколетучая жидкость с характерным для галогенпроизводных сладковатым запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету. В целом наиболее безопасен среди галогеналканов.
Содержание
Получение
Получают прямым хлорированием метана хлором в условиях радикального механизма при 400—500 °C при соотношении равном 5:1
В результате получается смесь всех возможных хлоридов: хлорметан, дихлорметан, хлороформ и четырёххлористый углерод, которые потом разделяются дистилляцией. После чего он имеет чистоту не менее 99,7 % В 1995 году годовое производство оценивалось в 500 миллионов тонн.
Свойства
Растворимость в воде 2% по массе (13 г/л), смешивается с большинством органических растворителей. Легколетуч (40 °C), образует азеотропную смесь с водой (т.кип. 38,1 °C, 98,5 % дихлорметана). Метиленхлорид (дихлорметан) реагирует с хлором с образованием хлороформа и четырёххлористого углерода. С йодом при 200 °C дает СН2l2, с бромом при 25-30 °C в присутствии алюминия — бромхлорметан. При нагревании с водой гидролизуется до СН2О и НСl. При нагревании со спиртовым раствором NH3 до 100—125 °C образует гексаметилентетрамин. Реакция с водным раствором NH3 при 200 °C приводит к метиламину,муравьиной кислоте и НСl. С ароматическими соединениями в присутствии АlСl3 метиленхлорид вступает в реакцию Фриделя — Крафтса, например с бензолом образует дифенилметан. [1]
Применение
Дешевизна, высокая способность растворять многие органические вещества, легкость удаления, относительно малая токсичность привела к широкому применению его как растворителя для проведения реакций, экстракций в том числе и в лабораториях. Используют в смесях для снятия лака, обезжиривания поверхностей. В пищевой промышленности используют для приготовления быстрорастворимого кофе, экстракта хмеля и других пищевых препаратов. Для растворения смол, жиров, битума. Его высокая летучесть используется для вспенивания полиуретанов.
Также используется в хроматографии.
В промышленности в смеси с полимерами используют для создания формы, которая быстро застывает за счёт испарения дихлорметана. Он также используется для склеивания пластмасс: полистирола, поликарбонатов, полиэтилентерефталата, АБС-пластиков, но не для полиэтилена и полипропилена.
Очистка в лаборатории
Специализированные применения
Дихлорметан используется в составах для склеивания пластиков. В смеси с метанолом используют как пропеллент, в качестве хладагента.
Безопасность
Хотя он и является наименее ядовитым среди галогеналканов, но нужно быть осторожным при обращении, так как он очень летуч и может вызвать острое отравление. Работы следует проводить при работающей вытяжной вентиляции.
В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлорметаном может вызвать его накопление в жировых тканях и привести к ожогу. Также при длительной работе с ним возможно поражение печени и нейропатия.
В Евросоюзе запрещены краски с дихлорметаном как для личного пользования, так и для профессонального применения.
Для регулярной работы с дихлорметаном не подходят перчатки из латекса или нитриловые.
Контакт дихлорметана с щелочными металлами приводит к взрыву.
ПДК в рабочей зоне 50мг/м³, в воде водоёмов не более 7.5 мг/л. КПВ 12-22 %
Метиленхлорид — популярный промышленный растворитель
Метиленхлорид — органическое соединение, 
Впервые был синтезирован в 1840-м году: в лаборатории соединили газообразный хлор с хлористым метилом и выдерживали смесь на свету. Для массового производства дихлорметан получают химическим синтезом из метана, выделенного из коксовых газов, и газообразного хлора. Другой метод: получение хлорметила из метанола и соляной кислоты, с последующим хлорированием.
Свойства
Подвижная прозрачная жидкость без цвета, летучая, с характерным резким, сладковатым запахом эфира. В воде растворяется слабо, хорошо — в орг. растворителях. При растворении в горячей воде разрушается, разлагаясь на соляную кислоту и формальдегид. Малотоксичен по сравнению с другими растворителями.
Вступает в реакцию с хлором, с получением хлороформа. Реагирует и с другими галогенами: йодом, бромом. Взаимодействует со спиртовым и водным растворами аммиака. В результате реакции с водным аммиаком получается муравьиная и соляная кислоты и метиламин. Вступает в реакции с ароматическими углеводородами, например, с бензолом.
Очень бурно реагирует (вплоть до взрыва) со щелочными металлами.
 | 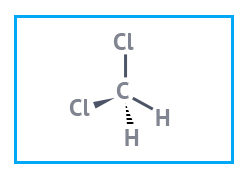 |
| Вытяжной шкаф ВА-102, комплектация «Стандарт» | Метиленхлорид (дихлорметан) «хч» 1000 мл |
Реактив токсичен, плохо горит, но горение поддерживает; смеси с воздухом взрывоопасны. Обладает канцерогенным действием.
Проглатывание реактива и длительное вдыхание паров или аэрозолей приводит к раздражению слизистых глаз и органов дыхания, отравлению, головокружению и головным болям, обморокам, диарее, заболеваниям печени и поджелудочной железы. Тяжелое отравление может привести к остановке дыхания. Длительное воздействие вещества на кожу может вызвать химический ожог.
При работе с метиленхлоридом следует использовать средства защиты: очки, резиновые перчатки (не нитриловые и не латексные), одежду с длинными рукавами, респиратор. В лабораториях все эксперименты проводят в вытяжном шкафу.
Хранят реактив обычно в стальных контейнерах или бочках. Допускается хранение вне помещения, под навесом. Предпочтительнее в прохладных, вентилируемых, сухих складах.
Перевозить ДХМ можно любыми видами транспорта, контейнеры и транспорт маркируются символом опасности Xn (вредное вещество).
Применение
Реагент гораздо менее токсичен, чем другие органические растворители, легко удаляется, отличается невысокой стоимостью, поэтому широко используется во многих сферах промышленности, включая пищепром и фармацевтику.
Хлористый метилен
 | Хлорорганические растворители импортного производства | |
|---|---|---|
| Наименование вещества: | Метилен хлористый | |
| Синонимы: | дихлорметан ДХМ METHYLENE CHLORIDE | |
метилен дихлорид
хладон 30, фреон 30.
Каталожный номер на метилен хлористый: CAS 75-09-2
Фасовка: Бочки 200 литровые
Российский стандарт на метилен хлористый: ГОСТ 9968-86
Описание метилена хлористого
Легкоподвижная прозрачная и легколетучая жидкость с, характерным для хлорпроизводных, едким сладковатым запахом.
Хорошо растворим в органических растворителях, плохо растворяется в воде.
Спецификация на метилен хлористый импортного производства, и сравнительная характеристика с нормами ГОСТ 9968-86 по результатом проведенной экспертизы
| Наименование показателя | единица измерения | Норма по ГОСТ 9968-86 Для высшего сорта | Значение согласно спецификации Производителя |
| Плотность при 20 град.С | г/см(куб) | 1,326-1,328 | 1,326-1,328 |
| Содержание основного вещества метилена хлористого, не менее | мас % | 99,7 | 99,9 |
| Содержание воды в метилене хлористом, не более | мас % | 0,01 | 0,010 |
| Кислотность (в пересчете на HCl) | мас % | 0,0004 | 0,0004 |
| Остаток после прокаливания, не более | мас % | 0,0005 | 0,0005 |
| Массовая доля железа, не более | мас % | 0,0001 | 0,0001 |
| массовая доля хлорорганических примесей, не более | мас % | 0,23 | 0,08 согласно данным гжх анализа |
| в том числе массовая доля хлороформа, не более | мас % | 0,05 согласно данным ГЖХ анализа | — |
| Цветность фосфорной кислоты (единицы Хазена), не более | не нормируется | 10 |
прим. 1. Для первого сорта (продажа которого распространена по России ) содержание основного вещества 98,8%, а хлороформа 0,8%
прим. 2. Может быть стабилизирован, для увеличения срока хранения при этом содержание основного вещества уменьшается смотри ГОСТ 9968-88
Результаты экспертизы. Согласно представленным данным Метилен хлористый поставляемый нашей компанией соответствует. требованиям ГОСТ 9968-88 а по параметрам, таким как, основное вещество, и содержание хлороформа превосходит ГОСТ 9968-88. Параметр содержание хлорорганики и хлороформа особенно важен, поскольку определяет силу запаха и токсичность продукта!!
Основные физ.хим. параметры вещества метилен хлористый
| Физическое состояние: | жидкое вещество |
| Цвет | прозрачный |
| Запах: | характерный запах |
| Порог восприятия запаха: | 250 PPM |
| Температура вспышки в закрытом тигле, ASTM D 56 град.С по ГОСТ | — 14 град |
| Пределы воспламеняемости на воздухе | Низкая: 14 %(об.) по ГОСТ 16,2% Высокая: 22 %(об.) по ГОСТ 19,1% |
| Температура самовоспламенения | 556 C согласно ГОСТ 580 C (разница методик измерения) |
| Давление паров | 47,33 кПа при 20 град.C |
| Температура кипения (760 мм ртутного столба) | 39,8 град.C |
| Плотность паров (плотность воздуха = 1) | 2,93 |
| Относительная плотность (плотность воды = 1) | 1,320 при 25 град.C/град.25 C |
| Температура замерзания | -96,7 град C |
| Температура плавления | -96,7 град.C |
| Растворимость в воде (по весу) | 1,3 % при 25 град. C |
| pH | Не применимо |
| Температура разложения: | Данные испытаний отсутствуют |
| Коэффициент разделения, октанолl/ вода (log Pow) | 1,25 |
| Скорость испарения (бутил ацетат = 1) | Данные испытаний отсутствуют |
| Динамическая вязкость | 0,41 мПа-с |
| Кинематическая вязкость | 0,31 мм2/с при 25 C Рассчитано |
Устойчивость продукта
Трудногорюч, но при определенных условиях, способен образовывать взрывоопасные смеси с воздухом.
При пожаре дым может содержать исходный материал в
добавление к неустановленным токсичным и/или вызывающим раздражение соединениям.
Опасные побочные продукты сгорания могут включать и не ограничиваются: Хлорид водорода и следовые количества хлора и фосгена
Опасность для человека
В Евросоюзе не рекомендован для прямых продаж населению.
В России по ГОСТ 12.1.005-88 отнесен к 4 класс опасности (малоопасные и безопасные вещества).
ПДК в рабочей зоне
50мг/м(куб), в воде водоёмов не более 7.5 мг/л
Хотя он и является наименее ядовитым среди галогеналканов, но он очень летуч и при превышение ПДК может вызвать острое отравление. В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлрометаном может вызвать накопление его в жировых тканях и привести к ожогу.
Также при длительной работе с ним возможно поражение печени и нейропатия. На крысах показано, что он может вызывать рак лёгких, печени и поджелудочной железы. В то же время не было отмечено какого-либо влияния на развития эмбрионов у женщин имевших контакт с ДХМ.
Ограничения в Евросоюзе
В Евросоюзе запрещены краски с дихлорметаном, как для личного пользования, так и для профессионального применения. Для регулярной работы с дихлорметаном не подходят перчатки из латекса или нитриловые.
Хлористый метилен
Хлористый метилен
| Дихлорметан | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | дихлорметан |
| Сокращения | ДХМ |
| Традиционные названия | дихлорметан, метилен хлористый |
| Химическая формула | CH2Cl2 |
| Эмпирическая формула | CH2Cl2 |
| Молярная масса | 84.9 г/моль |
| Физические свойства | |
| Плотность вещества | 1.3266 г/см³ |
| Примеси | хлорметаны |
| Состояние (ст. усл.) | подвижная прозрачная жидкость |
| Термические свойства | |
| Температура плавления | -96.7 °C |
| Температура кипения | 40 °C |
| Температура вспышки | 14 °C |
| Критическая точка | 245 |
| Энтальпия (ст. усл.) | -87.86 кДж/моль |
| Удельная теплота парообразования | 336,4 Дж/кг |
| Давление пара | 470 |
| Химические свойства | |
| Растворимость в воде | 20 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4242 |
| Классификация | |
| номер CAS | 75-09-2 |
| RTECS | PA8050000 |
Дихлорметан (хлористый метилен, ДХМ, CH2Cl2) — прозрачная лекгоподвижная и легколетучая жидкость с характерным для галогенпроизводных сладковатым запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету. В целом наиболее безопасен среди галогеналканов.
Содержание
Получение
Получают прямым хлорированием метана хлором в условиях радикального механизма при 400—500 °С при соотношении равном 5:1
В результате получается смесь всех возможных хлоридов: хлорметан, дихлорметан, хлороформ и четырёххлористый углерод, которые потом разделяются дистилляцей. После чего он имеет чистоту не менее 99,7% В 1995 году годовое производство оценивалось в 500 миллионов тонн.
Свойства
Применение
Дешевизна, высокая способность растворять многие органические вещества, легкость удаления, относительно малая токсичность привела к широкому применению его как растворитель для проведения реакций, экстракций в том числе и в лабораториях. Используют в смесях для снятия лака, обезжиривания поверхностей. В пищевой промышленности используют для приготовления быстрорастворимого кофе, экстракта хмеля и других пищевых препаратов. Для растворение смол, жиров, битума. Его высокая летучесть используется для вспенивания полиуретанов. Также используется в хроматографии. В промышленности в смеси с полимерами используют для создания формы которая быстро застывает за счёт испарения дихлорметана. Он же используется для склеивания этих пластиков: полистирол, поликарбонат, полиэтилентерефталат, АБС-пластик, но не для полиэтилена и полипропилена.
Очистка в лаборатории
Специализированные применения
Используется в составах для склеивания пластиков. В смеси с метанолом используют как пропеллент, в качестве хладагента.
Безопасность
Хотя он и является наименее ядовитым среди галогеналканов, но нужно быть осторожным при обращении, так как он очень летуч и может вызвать острое отравление. Вытяжная вентиляция необходима. В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлрометаном может вызвать накопление его в жировых тканях и привести к ожогу. Также при длительной работе с ним возможно поражение печени и нейропатия. На крысах показано, что он может вызывать рак лёгких, печени и поджелудочной железы. В тоже время не было отмечено какого либо влияния на развития эмбрионов у женщин имевших контакт с ДХМ.
Общая безопасность и методы устранения аварий [3]
Примечания
Полезное
Смотреть что такое «Хлористый метилен» в других словарях:
Хлористый метилен — (хим.), дихлорметан СН2Cl2, получен впервые Реньо при действии хлора на X. метил: СН3Cl + Cl2 = CH2Cl2 + HCl; впоследствии он получен Бутлеровым при пропускании струи хлора в йодистый метилен: СН2J2 + Cl2 = CH2Cl2 + J2 и Перкиным при действии… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
хлористый метилен — дихлорметан … Cловарь химических синонимов I
дихлорметан — хлористый метилен … Cловарь химических синонимов I
Болотный газ или метан — (также водородистый метил, формен) предельный углеводород состава СН4, первый член ряда СnН2n+n, одно из простейших соединений углерода, вокруг которого группируются все остальные и от которого могут быть произведены через замещение атомов… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Химическое строение — Настоящая статья имеет задачей изложение истории возникновения теории X. строения органических соединений и ее связи с предыдущими теориями. В значительной мере это уже выяснено в статьях Замещение, Унитарная система, Химических типов теория и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Галоидопроизводные — Этим именем в органической химии обозначаются вообще продукты, происходящие из различных органических веществ (углеводородов, спиртов, кислот, альдегидов, кетонов, аминов и пр.) через замещение в них атомов водорода углеводородных групп галоидами … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Термохимия — отдел химии, занимающийся превращениями внутренней энергии тел в тепло при химических процессах. Почти каждая химическая реакция связана с тем или иным тепловым эффектом: химическое превращение сопровождается или выделением, или поглощением тепла … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Отравления — I Отравления (острые) Отравления заболевания, развивающиеся вследствие экзогенного воздействия на организм человека или животного химических соединений в количествах, вызывающих нарушения физиологических функций и создающих опасность для жизни. В … Медицинская энциклопедия
Дихлорметан — Дихлорметан … Википедия