Хмпз эссенциальная тромбоцитемия что это
Хмпз эссенциальная тромбоцитемия что это
Целями лечения при эссенциальной тромбоцитемии являются:
1) нормализация числа тромбоцитов;
2) профилактика тромботических и геморрагических осложнений.
Нормализация количества тромбоцитов при эссенциальной тромбоцитемии
Для циторедукции в качестве терапии первой линии используются:
1) гидроксимочевина,
2) анагрелид;
3) а-интерферон.
Циторедуктивная терапия обязательна при количестве тромбоцитов более 1500 • 10 9 /л, при меньшем тромбоцитозе лечение назначают по дифференцированным показаниям. При высоком тромбоцитозе, тромбофилических и геморрагических осложнениях гидроксимочевину назначают по 2-4 г/сут за 2 приема с постепенным уменьшением до 1 г и до 0,5 г при достижении ремиссии.
При умеренном лейкоцитозе доза составляет 15 мг/(кг•сут) с дальнейшим переходом на поддерживающую терапию.
Анагрелид используется при необходимости быстрого снижения количества тромбоцитов, особенно у лиц молодого возраста, при развитии сосудистых осложнений и подготовке к операции. Начальная доза препарата составляет 0,5 мг каждые 12 часов в течение 7 дней, в дальнейшем доза увеличивается на 0,5 мг/сут еженедельно до наступления эффекта.
Максимальная рекомендуемая суточная доза — 3,5-4 мг. Поддерживающая терапия проводится в дозе 2-2,5 мг/сут. При лечении необходим тщательный контроль состояния сердечно-сосудистой системы (ЭКГ, ЭхоКГ).
Интерферон-альфа эффективно подавляет продукцию тромбоцитов и практически не обладает лейкозогенным действием. Схема лечения аналогична другим хроническим миелопролиферативным заболеваниям: 1 млн ME подкожно в первый день, 2 млн ME во второй день и по 3 млн ME ежедневно с третьего дня.
Оценка ответа производится через 6 месяцев. При полной клинико-гематологической ремиссии (достигается у 90% больных) отмечается нормализация размеров селезенки, количество тромбоцитов меньше 400•10 9 /л. При достижении полного ответа лечение в поддерживающей дозе (3 млн ME 3 раза в неделю) проводится в течение двух лет.
При развитии частичной ремиссии размеры селезенки уменьшаются на 50% от исходных, количество тромбоцитов не превышает 600•10 9 /л. В этом случае к лечению добавляют гидроксимочевину в дозе 500-1500 мг/сут и продолжают лечение еще в течение 6 месяцев. В дальнейшем в зависимости от результатов лечения переходят на поддерживающую терапию или используют другие препараты.
Лечение и профилактика сосудистых осложнений при эссенциальной тромбоцитемии
При микрососудистых тромбофилических осложнениях применяется ацетилсалициловая кислота, при отсутствии эффекта дополнительно назначаются низкомолекулярный гепарин и трансфузии свежезамороженной плазмы (400 мл 2 раза в неделю). Для быстрого снижения уровня тромбоцитов используют тромбоцитаферез.
Для лечения геморрагического синдрома в ряде случаев требуются трансфузии концентрата тромбоцитов, поскольку тромбоциты больных эссенциальной тромбоцитемией качественно неполноценны.
Для профилактики микроциркуляторных тромбофилических осложнений до достижения гематологической ремиссии и у больных с ремиссией — по дополнительным показаниям используется ацетилсалициловая кислота в дозе 40-300 мг/сут.
Прогноз эссенциальной тромбоцитемии
Эссенциальная тромбоцитемия — индолентное заболевание, которое характеризуется длительным бессимптомным течением с редкими тромбоэмболическими или геморрагическими осложнениями. Вероятность летального исхода, обусловленного тромбозами, трансформацией в острый миелоидный лейкоз или миелодиспластические синдромы (в связи с предшествующей цитотоксической терапией), менее 5%.
Медиана выживаемости превышает 10-15 лет. В связи с тем что в большинстве случаев заболевание возникает в среднем и пожилом возрасте, продолжительность жизни обычно не отличается от популяционной.
Необходимо помнить, что селезенка является местом секвестрации тромбоцитов, поэтому спленэктомия часто приводит к резкому нарастанию тромбоцитоза и ухудшению прогноза.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Эссенциальный Тромбоцитоз
(эссенциальный тромбоцитоз; первичная тромбоцитемия)
, MD, James P. Wilmot Cancer Institute, University of Rochester Medical Center
Этиология эссенциальной тромбоцитемии
Патофизиология эссенциального тромбоцитоза
Тромбоцитемия может привести к:
Окклюзии мелких сосудов (обычно обратимы)
Тромбозу крупных сосудов
Остается неясным, повышен ли риск тромбоза крупных сосудов, вызывающего тромбоз глубоких вен или легочную эмболию у пациентов с эссенциальной тромбоцитемией, частично из-за того, что тромбоциты в первую очередь участвуют в артериальном тромбозе, и нет корреляции между количеством тромбоцитов и тромбозом крупных сосудов.
Симптомы и признаки эссенциальной тромбоцитемии
К частым симптомам относятся:
Кровоподтеки и кровоизлияния
Парестезии кистей рук и стоп
Тромбоз может вызывать симптомы в пораженном участке (например, неврологический дефицит при инсульте или транзиторных ишемических атаках).
Кровотечения, как правило, небольшие, редко спонтанные и проявляются эпистаксисом, желудочно-кишечными кровотечениями или склонностью к образованию гематом. Однако в небольшом проценте случаев тяжелого тромбоцитоза может возникнуть тяжелое кровотечение.
Может появиться эритромелалгия (жгучие боли в руках и ногах, сопровождающиеся приливом жара, эритемой и, иногда, дигитальной ишемией). Селезенку можно пропальпировать, но значительная спленомегалия не характерна для данной патологии и может предполагать наличие другого миелопролиферативного новообразования.
Диагностика эссенциального тромбоцитоза
Общий анализ крови (ОАК) и мазок периферической крови
Исключение причин вторичного тромбоцитоза
JAK2 мутации диагностируют с помощью полимеразной цепной реакции и, если результат отрицательный, исследуют на мутации CALR или MPL
Возможно исследование костного мозга
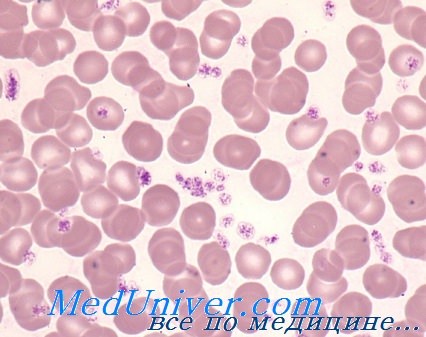
Количество тромбоцитов> 450 000/мкл ( > 450 000 × 10 9 /л), но может составлять > 1 000 000/мкл ( > 1 000 000 × 10 9 /л). Уровень тромбоцитов может снижаться во время беременности. В мазке периферической крови могут обнаруживаться гигантские тромбоциты и фрагменты мегакариоцитов.
При подозрении на идиопатическую тромбоцитемию следует провести общий анализ крови, мазок периферической крови, исследования железа и генетические исследования, включая количественный анализ на JAK2 V617F и анализ на BCR-ABL. Это следует сделать для исключения хронического миелолейкоза Хронический миелолейкоз (ХМЛ) Хронический миелолейкоз (ХМЛ) развивается в результате злокачественной трансформации и клональной пролиферации плюрипотентных стволовых клеток, приводящей к гиперпродукции зрелых и незрелых. Прочитайте дополнительные сведения (ХМЛ, который может проявляться только тромбоцитозом). Если анализы на JAK2 и BCR-ABL отрицательные, должны быть проведены анализы на мутации CALR и MPL. Диагноз эссенциальной тромбоцитемии предполагают на основании нормального гематокрита, количества лейкоцитов, среднего объема эритроцитов (MCV) и исследования уровня железа, а также отсутствия транслокации BCR-ABL
Согласно рекомендациям Всемирной организации здравоохранения, для диагностики эссенциальной тромбоцитемии необходимо, чтобы биопсия костного мозга показывала повышенное количество увеличенных, зрелых мегакариоцитов, но этот критерий никогда не подлежал перспективной валидации, и исследование костного мозга не может дифференцировать эссенциальную тромбоцитопению от истинной полицитемии. Тем не менее, биопсия костного мозга выполняется для определения выраженности фиброза.
Прогноз при эссенциальном тромбоцитозе
Продолжительность жизни близка к нормальной. Хотя заболевание часто сопровождается симптомами, его течение обычно доброкачественное. Серьезные осложнения, обусловленные тромбозом артерий, встречаются редко, но могут представлять угрозу для жизни. Трансформация в лейкоз отмечается у 2% пациентов, но её вероятность может возрастать после применения цитотоксических препаратов, в том числе гидроксимочевины. У некоторых пациентов развивается вторичный миелофиброз, который чаще наблюдается у мужчин с мутацией JAK2V617F или CALR 1 типа.
Лечение эссенциального тромбоцитоза
Препараты, снижающие уровень тромбоцитов (например, гидроксимочевина (в РФ не зарегистрирована), анагрелид)
В редких случаях, цитотоксическое средство
В редких случаях, интерферон
Редко, пересадка гемопоэтических стволовых клеток
При незначительно выраженных вазомоторных симптомах (таких как головная боль, легкая степень ишемии пальцев, эритромелалгия) с целью снижения риска тромбоза у пациентов из группы низкого риска обычно достаточно применения аспирина в дозе 81 мг/день перорально, но при необходимости могут применяться большие дозы. Для контроля тяжелой мигрени может потребоваться снижение количества тромбоцитов. Польза аспирина в период беременности не доказана, его прием может спровоцировать кровотечение у пациенток с эссенциальной тромбоцитемией и мутацией CALR.
Использование аминокапроновой или транексамовой кислот является эффективным в борьбе с кровотечением, вызванным приобретенным синдромом Виллебранда во время проведения незначительных вмешательств, таких как стоматологические процедуры. Проведение более серьезных процедур требует оптимизации количества тромбоцитов.
Снижение количества тромбоцитов
Поскольку прогноз обычно благоприятен и нет корреляции между степенью тромбоцитоза и тромбозом, потенциально токсичных препаратов, снижающих уровень тромбоцитов, следует избегать, чтобы нормализовать количество тромбоцитов у пациентов с отсутствием клинических симптомов. К общепризнанным показаниям для снижения уровня тромбоцитов относятся:
Факторы сердечно-сосудистого риска
Транзиторными ишемическими атаками
Необходимость хирургического вмешательства у пациентов с тяжелым тромбоцитозом и низкой активностью кофактора ристоцетина
Иногда тяжелая мигрень
Тем не менее нет никаких данных, которые подтверждают, что использование цитотоксической терапии для уменьшения количества тромбоцитов снижает риск образования тромбов или улучшает выживаемость. JAK2-положительные и/или пациенты возрастом старше 65 лет подвергаются наибольшему риску развития тромбоэмболических осложнений.
К препаратам, которые снижают уровень тромбоцитов, относятся анагрелид, интерферон альфа-2b и гидроксимочевина. В целом гидроксимочевина считается препаратом выбора для кратковременного использования. Поскольку гидроксимочевина (в РФ не зарегистрирована) и анагрелид проходят через гематоплацентарный барьер, они не используются во время беременности. При необходимости беременным может назначаться интерферон альфа-2a. При условии неэффективности средств для мигрени, самой безопасной терапевтической стратегией для лечения мигрени является применение интерферона. Анагрелид необходимо с осторожностью использовать у пожилых пациентов из-за его влияния на сердечно-сосудистую систему (например, сердцебиение, аритмии) и почки (например, задержка жидкости).
Гидроксимочевину следует назначать только тем специалистам, которые знакомы с особенностями ее использования и мониторинга. Его назначают в начальной дозе от 500 до 1000 мг перорально 1 раз/день. Пациентам еженедельно выполняют общий анализ крови. Если количество лейкоцитов снижается 4000/мкл ( 4 × 10 9 /л), прием гидроксимочевины останавливают и повторно вводят в половинной дозе до нормализации количества лейкоцитов. При достижении стабильного состояния, интервал между проведением ОАК удлиняется до 2 недель, а затем до 4 недель. Целью проводимого лечения является облегчение симптомов, а не нормализация количества тромбоцитов. Слишком резкая отмена приема гидроксимочевины может привести к быстрому скачку количества тромбоцитов.
Действие руксолитиниба, препарата, который используется при истинной полицитемии и первичном миелофиброзе, было изучено на пациентах с эссенциальной тромбоцитемией, резистентной к другим видам лечения.
Удаление тромбоцитов (тромбоцитоферез) применяли в редких случаях у больных с серьезными внутренними кровоизлияниями, при рецидивирующих тромбозах или перед неотложной хирургической операцией, для того чтобы быстро уменьшить количество тромбоцитов. Однако тромбоцитоферез редко необходим. Эти эффекты транзиторные с быстрым восстановлением количества тромбоцитов. Гидроксимочевина или анагрелид не дают немедленный эффект, но начать использовать их необходимо одновременно с тромбоцитоферезом.
Ключевые моменты относительно эссенциального тромбоцитоза
Эссенциальная тромбоцитемия представляет собой клональную аномалию мультипотентных гемопоэтических стволовых клеток, которая приводит к увеличению количества тромбоцитов.
Пациенты находятся под угрозой тромбоза микрососудов, кровоизлияний, и редко макрососудистого тромбоза.
Эссенциальная тромбоцитемия диагностируется методом исключения, в частности, должны быть исключены другие миелопролиферативные неоплазии и реактивный (вторичный) тромбоцитоз.
Для пациентов с асимптоматическим течением болезни терапия не требуется. Аспирин, как правило, эффективен при микрососудистых нарушениях (глазной мигрени, эритромегалии и транзиторных ишемических атаках).
Чтобы контролировать количество тромбоцитов для некоторых пациентов с тяжелым тромбоцитозом может потребоваться более агрессивное лечение; такие меры включают использование гидроксимочевины, анагрелида, интерферона альфа-2b и тромбоцитофереза.
Хронические РН-негативные миелопролиферативные заболевания
Общая информация
Краткое описание
Одобрен объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «28» ноября 2017 года
Протокол №33
Истинная полицитемия – клональное миелопролиферативное заболевание, которое характеризуется пролиферацией эритроидного, гранулоцитарного, мегакариоцитарного ростков кроветворения с преимущественной пролиферацией эритроидного ростка кроветворения, увеличением числа эритроцитов и повышением уровня гемоглобина, тромбоцитозом, лейкоциозом в периферической крови (панмиелоз).
Все больные являются носителями мутации JAK2 V617F и/или CALR, MPL.
Эссенциальная тромбоцитемия – клональное миелопролиферативное заболевание с постоянной повышенной пролиферацией мегакариоцитов и повышенным образованием тромбоцитов, характеризующееся повышенным числом больших, зрелых мегакариоцитов в костном мозге, тромбоцитозом в периферической крови (>450х109/л) и клинически – эпизодами тромбозов и/или кровотечений.
Миелопролиферативное заболевание неклассифицируемое — согласно рекомендациям ВОЗ 2008г данный диагноз следует использовать при наличии клинических, лабораторных и гистологических (в трепанобиоптате костного мозга) признаков МПЗ, не соответствующих какой-либо определенной нозологической форме Ph-негативных миелопролиферативных заболеваний – ИП, ЭТ, ПМФ.
Хронический миеломоноцитарный лейкоз — клональное заболевание кроветворной системы, которое характеризуется хроническим моноцитозом в периферической крови, отсутствием Ph хромосомы, гена BCR-ABL1, а также бластозом в костном мозге ≤20%.
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| D 45.0 | Истинная полицитемия |
| D 47.3 | Эссенциальная (геморрагическая) тромбоцитемия |
| D 47.1 | Хроническая миелопролиферативная болезнь |
Дата разработки/пересмотра протокола: 2017 год.
Пользователи протокола: врачи общей практики, терапевты, онкологи, гематологи.
Категория пациентов: взрослые, беременные.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор рандомизированных клинических исследований (РКИ) или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или |
| Неконтролируемое исследование или | |
| Мнение экспертов | |
| GPP | Наилучшая клиническая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Хронический нейтрофильный лейкоз
2. Истинная полицитемия
3. Первичный миелофиброз
— Префибротическая стадия
— Фибротическая стадия
4. Эссенциальная тромбоцитемия
5. Хронический эозинофильный лейкоз NOS
6. Мастоцитоз
7. Хроническое миелопролиферативное заболевание неклассифицируемое
Миело-/лимфоидные заболевания с эозинофилией и перестройкой PDGFRA, PDGFRB, или FGFR1, или с PCM1-JAK2:
1. Миело-/лимфоидные заболевания с перестройкой PDGFRA
2. Миело-/лимфоидные заболевания с перестройкой PDGFRB
3. Миело-/лимфоидные заболевания с перестройкой FGFR1
4. Миело-/лимфоидные заболевания с перестройкой PCM1-JAK2
Миелодиспластические/миелопролиферативные заболевания (МДС/МПЗ)
1. Хронический миеломоноцитарный лейкоз (ХММЛ)
2. Атипичный хронический миелолейкоз (аХМЛ) bcr-abl1 негативный
3. Ювенильный миеломоноцитарный лейкоз (ЮММЛ)
4. МДС/МПЗ с кольцевыми сидеробластами и тромбоцитозом (МДС/МПЗ-КС-Т)
5. МДС/МПЗ неклассифицируемый
Факторы и группы риска
Истинная полицитемия:
Стратификация риска у больных ИП используется для оценки вероятности тромботических осложнений, превносящих наибольший вклад в структуру смертности и инвалидизации, обусловленную заболеванием, а не для оценки выживаемости или риска трансформации в лейкоз/миелофиброз.
Наиболее устойчивыми факторами риска для тромботических осложнений при ИП являются возраст старше 60 лет и наличие тромбозов в анамнезе. При этом целесообразно также учитывать общие факторы риска для сердечно- сосудистых и тромботических осложнений (табл. 2) (УД – B).
Таблица 2. Стратификация риска развития тромбогеморрагических осложнений при ИП.
| Категории риска | Возраст старше 60 лет и/или тромбозы в анамнезе. | Сердечно-сосудистые факторы риска. |
| Низкий. | — | — |
| Промежуточный. | — | + |
| Высокий. | + | +/— |
*сахарный диабет, артериальная гипертензия, курение
Таблица 4. Прогностическая шкала для пациентов с ИП
| Прогностическая шкала | Группы риска и клиническая значимость |
| Обычная оценка тромбоза (рекомендации Европейского LeukemiaNet) 70 | |
| По меньшей мере 1 из следующих факторов риска: | Низкий риск: возраст |
| • Возраст ≥ 60 лет | высокий риск: возраст ≥60 лет И / ИЛИ наличие тромбоза в анамнезе, по крайней мере, один из факторов риска |
| • Предшествующий тромбоз | Пациентам с низким уровнем риска назначают ацетилсалициловую кислоту с низкой дозой и подвергают регулярной флеботомии, чтобы сохранить гематокрит |
| IPSS для общей выживаемости в PV78 | |
| Факторы риска (вес): | низкий риск: 0 (средняя выживаемость, 28 лет) |
| • Возраст ≥67 лет (5 баллов) | Промежуточный риск: 1-2 балла (средняя выживаемость, 19 лет) |
| • Количество лейкоцитов ≥15 × 109 / L (1 балл) • | |
| • Предшествующий венозный тромбоз в анамнезе (1 балл) |
* Сердечно-сосудистые факторы риска включают гипертонию, диабет и курение.
Прогностическая шкала для Хронического миеломоноцитарного лейкоза: используется для определения группы риска при ХММЛ (данная шкала представлена в виде электронного калькулятора, которым можно воспользоваться пройдя по ссылке 1
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ 12
Диагностические критерии:
Жалобы, анамнез, данные физического исследования имеет значение в диагностике и в дифференциальной диагностике хронических миелопролиферативных заболеваний, но неспецифичны в связи, с чем не относятся к диагностическим критериям.
Жалобы при ИП (характер возникновения и проявления болевого синдрома) на головокружение, головные боли, ухудшение зрения, кожный зуд, приступы стенокардии – плеторический синдром, наиболее характерен для истинной полицитемии.
Кожный зуд, потливость, слабость, повышенная температура тела, боли в костях – миелопролифератитвный синдром;
NB! Плеторический синдром (от слова «плетора» – полнокровие) – характеризуется увеличением массы циркулирующих эритроцитов, что приводит к появлению жалоб на головокружение, головные боли, ухудшение зрения, кожный зуд после мытья, жгучие боли и парестезии в кончиках пальцев, приступы стенокардии. При осмотре кожа и видимые слизистые оболочки с синюшним оттенком (положительный симптом Купермана). Сосудистые осложнения – тромбозы любой локализации, приступы покраснения пальцев рук и ног, которые сопровождаются болью и жжением (эритромелалгия). Увеличение объёма циркулирующих эритроцитов приводит к появлению артериальной гипертензии у пациентов, которые до начала заболевания не жаловались на данный симптом, либо усугубление уже имеющейся гипертонической болезни, которая плохо поддаётся лечению традиционными гипотензивными препаратами. Более выраженными становятся симптомы ишемической болезни сердца, церебрального атеросклероза.
В раннюю стадию заболевания отмечается эритроцитоз, в костном мозге – панмиелоз. Так как заболевание развивается постепенно, от его начала до постановки диагноза проходит от 2 до 4 лет. Длительность данной стали – до 5 лет.
NB! Миелопролиферативный синдром обусловлен гиперплазией трех ростков кроветворения. Проявляется в виде кожного зуда, потливости, слабости, повышенной температуры тела, болей в костях. Повышенный распад гранулоцитов сопровождается нарушением уратового обмена, что проявляется в виде мочекислого диатеза, камнеобразования в почках, подагры, подагрической полиартралгии. Спленомегалия может быть обусловлена увеличением секвестрирующей функции селезенки.
Инструментальные исследования:
· УЗИ органов брюшной полости – с определением объема селезенки, для исключения развития инфаркта селезенки, тромбоза в системе портальных вен.
· трепанобиопсия костного мозга с гистологической оценкой и гистохимическим исследованием для выявления ретикулинового и коллагенового фиброза; также необходимо для оценки эффекта терапии, прогрессирования и трансформации заболевания. Для сопоставления с гистологической картиной в дебюте заболевания (до лечения).
Показания для консультации специалистов:
· консультации других узких специалистов – по показаниям.
Диагностический алгоритм 11:
Дифференциальный диагноз
| (ВОЗ 2016) | Большие критерии | Малые критерии | Подтверждение диагноза |
| ИП | 1. Гемоглобин> 165 г/л у мужчин или более 160 г/л у женщин, или гематокрит> 49% у мужчин или у 48% у женщин, или увеличенная масса эритроцитов (более чем на 25% выше среднего прогнозируемого значения) 2. При биопсии костного мозга – трехростковая гиперплазия (панмиелоз): увеличение пролиферации элементов эритроидного, гранулоцитарного, мегакариоцитарного ростков миелопоэза. 3. Наличие JAK2 (V617F) или JAK2 экзона 12 мутации | 1. Уровень эритропоэтина (ЭПО) сыворотки ниже референсных значений. | Диагноз ИП подтверждается при наличии двух больших и одного малого критерия или при наличии первого большого и двух малых критериев. Примечание: Критерий № 2 (биопсия КМ) может не потребоваться в случаях с устойчивым абсолютным эритроцитозом: уровень гемоглобина > 18,5 г/дл у мужчин (гематокрит, 55,5%) или более 16,5 г/дл у женщин (гематокрит, 49,5%). Однако первичный миелофиброз (имеющийся у 20% пациентов) может быть обнаружен только при проведении биопсии КM; |
| ЭТ | 1. Количество тромбоцитов ≥450 × 109 /л 2. В костном мозге пролиферация мегакариоцитов с увеличением числа зрелых мегакариоцитов с гиперглобулированными ядрами. Не наблюдается сдвига влево в нейтрофильном гранулопоэзе или эритропоэзе и редко увеличение ретикулиновых волокон. 3. Отсутствие критериев BCR-ABL1 + ХМЛ, ЭТ, ПМФ, миелодиспластических синдромов или других миелоидных новообразований 4. Наличие мутации JAK2, CALR или MPL | Наличие клонального маркера или отсутствие доказательств для реактивного тромбоцитоза | Диагностика ЭТ требует наличия всех четырех больших критериев или первых трех больших критериев и малого критерия |
| префибротический ПМФ | 1. Пролиферация и атипия* мегакариоцитов, сочетающиеся с ретикулиновым и/или коллагеновым фиброзом костного мозга; при отсутствии выраженного ретикулинового фиброза – повышенная клеточность костного мозга с пролиферацией клеток гранулоцитарного ряда и угнетением эритропоза (префиброзная клеточная фаза ПМФ). |
2. Отсутствие критериев ИП, BCR/ABL1+ХМЛ, МДС или других миелопролиферативных заболеваний.
3. Наличие мутаций JAK2, CALR или MPL, а при их отсутствии – исключение реактивного фиброза (инфекции, аутоиммунные заболевания, хроническое воспаление, волосатоклеточный лейкоз, другие лимфопролиферативные заболевания, метастазы солидных опухолей, токсические миелопатии)
• Анемия, не связанная с сопутствующим заболеванием
• лейкоцитоз (количество лейкоцитов ≥11 × 109 / л)
• Пальпируемая спленомегалия
• Повышение активности ЛДГ
Примечание: При отсутствии какой-либо из 3 основных клональных мутаций поиск наиболее часто встречающихся сопутствующих мутаций (например, ASXL1, EZH2, TET2, IDH1 / IDH2, SRSF2, SF3B1) помогает в определении клональной природы заболевания
2. Отсутствие критериев для BCR-ABL1 + CML, PV, ET, миелодиспластическим синдромам или другим миелоидным новообразованиям
3. Наличие мутаций JAK2, CALR или MPL, а при их отсутствии – исключение реактивного фиброза (инфекции, аутоиммунные заболевания, хроническое воспаление, волосатоклеточный лейкоз, другие лимфопролиферативные заболевания, метастазы солидных опухолей, токсические миелопатии)
• Анемия, не связанная со сопутствующим заболеванием
• лейкоцитоз (количество лейкоцитов ≥11 × 109 / л)
• пальпируемая спленомегалия
• Уровень ЛДГ увеличен до уровня выше верхней границы нормы
• Лейкоэритробластоз
Примечание: При отсутствии какой-либо из 3 основных клональных мутаций поиск наиболее часто встречающихся сопутствующих мутаций (например, ASXL1, EZH2, TET2, IDH1 / IDH2, SRSF2, SF3B1) помогает в определении клональной природы заболевания
Диагностические критерии МДС/МПЗ с кольцевыми сидеробластами и тромбоцитозом:
| Анемия, ассоциированная с дисплазией эритроидного ростка с/или мультилинейной дисплазией, ≥15% кольцевых сидеробластов, |
| Наличие тромбоцитоза с количеством тромбоцитов ≥450 × 109/L |
| Наличие мутации SF3B1 или, отсутствие мутации SF3B, отсутствие в анамнезе цитотоксической или колони стимулирующей терапии, которые могут быть причиной развития МДС/МПЗ |
| Отсутствие BCR-ABL1, отсутствие перестроек PDGFRA, PDGFRB, или FGFR1; или PCM1-JAK2; отсутствие (3;3)(q21;q26), inv(3)(q21q26) или del(5q) |
| Отсутствие в анамнезе МПЗ, МДС (за исключением MDS-RS), или другие типы МДС/МПЗ |
Диагностические критерии аХМЛ BCR-ABL1−:
| Лейкоцитоз в периферической крови за счет увеличения количества нейтрофилов и их предшественников (промиелоцитов, миелоцитов, метамиелоцитов), включающей ≥10% от лейкоцитов) |
| Дисгранулопоэз, который может включать аномальное содержание хроматина |
| Отсутствие или минимальная абсолютная базофилия; количество базофилов |
| Отсутствие или минимальный абсолютный моноцитоз; моноциты |
| Гиперклеточный КМ с гранулоцитарной пролиферацией и дисплазией гранулоцитов, с/или дисплазией эритроидного и мегакариоцитарного ростков |
| Не доказанные перестройки PDGFRA, PDGFRB, или FGFR1, или PCM1-JAK2 |
| Не соответствует критериям ВОЗ BCR-ABL1+ ХМЛ, ПМФ, ИП, или ЭТ |
Диагностические критерии ХММЛ:
| Персистирующий моноцитоз ≥1 × 109 / L, при этом моноциты составляют ≥10% от количества лейкоцитов |
| Не соответствует критериям ВОЗ для BCR-ABL1 + ХМЛ, ПМФ, ИП или ЭТ |
| Дисплазия в 1 или более миелоидных ростках. Если миелодисплазия отсутствует или минимальна, диагноз ХММЛ может быть выставлен, если присутствуют другие критерии |
| Клональная цитогенетическая и молекулярно-генетическая поломка присутствующая в гемопоэтических клетках |
| или |
| Моноцитоз сохраняется в течение по меньшей мере 3 месяцев |
| Все другие причины моноцитоза были исключены |
Уровень лейкоцитов (> 10 × 109 / л), без ответа на терапию
«Предварительные критерии ответа на терапию ИТК»
Нарастающая спленомегалия, без ответа на терапию
Резистентность к первой линии ИТК
Тромбоцитоз (> 1000 × 109 / л), без ответа на терапию
Резистентность к двум последовательным линиям ИТК
Появление 2 или более мутаций в BCR-ABL1 во время терапии ИТК
20% или более базофилов в КМ
10-19% бластных клеток в периферической крови или КМ
Дополнительные хромосомные абберации в клетках Ph + (трисомия 8, изохромосома 17q, трисомия 19), комплексный кариотип или аномалии 3q26.2
Любая новая клональная хромосомная аномалия в клетках Ph +, которая возникает во время терапии
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Анагрелид (Anagrelide) |
| Ацетилсалициловая кислота (Acetylsalicylic acid) |
| Бусульфан (Busulfan) |
| Гепарин натрия (Heparin sodium) |
| Гидроксикарбамид (Hydroxycarbamide) |
| Иматиниб (Imatinib) |
| Интерферон альфа (Interferon alfa) |
| Клопидогрел (Clopidogrel) |
| Леналидомид (Lenalidomide) |
| Меркаптопурин (Mercaptopurine) |
| Надропарин кальция (Nadroparin calcium) |
| Руксолитиниб (Ruxolitinib) |
| Тиклопидин (Ticlopidine) |
| Цитарабин (Cytarabine) |
| Эноксапарин натрия (Enoxaparin sodium) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ 15: для пациентов с установленным диагнозом, лечение и профилактика осложнений может проводиться в амбулаторных условиях.
Определение тактики терапии при ИП:
Цели терапии ИП (УД – D):
· предотвращение и лечение тромбогеморрагических осложнений;
· контроль симптомов опухолевой интоксикации (снижение веса, потливость, лихорадка, зуд);
· сведение к минимуму риска развития острого лейкоза и пост-ИП МФ;
· предупреждение осложнений в случае беременности, хирургических операций.
Определение тактики терапии при ЭТ:
Цели терапии ЭТ (УД – D):
· предупредить возникновение тромботических или геморрагических осложнений;
· минимизировать риск прогрессирования заболевания с исходом в пост-ЭТ МФ или ОМЛ;
· контроль симптомов интоксикации;
· предупреждение осложнений в случае беременности, хирургических манипуляций. Целевой уровень тромбоцитов менее 400 х 109/л.
Методы терапевтического воздействия при ЭТ:
· Профилактика тромботических осложнений:
— ацетилсалициловая кислота (40-325 мг/сут), клопидогрель (75 мг/сут), тиклопидин (500-750 мг/сут).
· Циторедуктивная терапия:
— Цитостатики: Гидроксимочевина 10-30 мг/кг/сут;
— Интерферон-альфа 1,5-5 млн МЕ 3 раза в неделю;
— Анагрелид 2-10 мг/сут.
· Лечение осложнений заболевания (тромбозы, тромбоэмболии).
Определение тактики терапии при ПМФ:
Цели терапии больных ПМФ (УД – D):
1) Контроль болезни: предупреждение прогрессии, увеличение общей и безрецидивной выживаемости.
2) Облегчение симптоматики: улучшение качества жизни (лечение анемии и другой цитопении, уменьшение спленомегалии, контроль симптомов интоксикации).
3) Предупреждение осложнений в случае беременности, хирургических операций.
Терапия ХФ ПМФ, как правило, проводится с помощью лекарственных препаратов в виде циторедуктивной терапии, интерферонотерапии или их сочетанного применения. В бластной фазе лечение может проводиться по программам лечения острых лейкозов с учетом возраста и коморбидности больных.
После подтверждения диагноза и определения прогностической группы ПМФ должна быть определена тактика специальной терапии. Основными факторами, влияющими на выбор варианта лечения, являются следующие:
· группа риска (по системам IPSS, DIPSS, DIPSS+);
· наличие и степень выраженности симптомов заболевания;
· возраст больного;
· коморбидность;
· наличие совместимых по системе HLA доноров и возможность выполнения алло-ТГСК.
Определение тактики терапии при ХММЛ:
1) Лечение больных ХММЛ с агрессивным типом течения проводится либо в виде монотерапии гидроксимочевиной или этопозидом, либо с использованием различных схем полихимиотерапии, применяемых для лечения острых лейкозов.
2) Дополнительное лечение: как при МДС.
3) Трансплантация аллогенных кроветворных клеток: единственный метод обеспечивающий вылечивания, рекомендуется рассмотреть у молодых пациентов, имеющих совместимого по системе HLA донора; результаты аналогичны к резу льтатам лечения МДС.
4) Циторедуктивная терапия: чаще всего гидроксимочевина, прежде всего при МП-ХММЛ.
5) Гипометилирующие препараты: азацитидин при МД-ХММЛ с бластозом в костном мозге ≥10%.
Определение тактики терапии при хроническом нейтрофильном лейкозе:
Лечение больным ХрНЛ длительное время не проводится, хотя при выраженном гиперлейкоцитозе и нарастании размеров печени и селезенки с целью циторедукции может быть использована гидроксимочевина. Вместе с тем, все больные ХрНЛ должны быть под постоянным наблюдением гематолога.
Определение тактики терапии при атипичном хроническом миелолейкозе:
Заболевание характеризуется крайне агрессивным течением. Длительность жизни больных составляет в среднем 11-18 месяцев. При атипичном хроническом миелолейкозе использование препарата Гливек не эффективно. Единственным эффективным методом лечения является аллогенная трансплантация стволовых клеток. Однако и данный метод лечения обеспечивает длительную безрецидивную выживаемость только у 30% пациентов.
Немедикаментозное лечение 20:
· Режим: общеохранительный;
· Диета: стол №15 (общая).
Медикаментозное лечение
Выбор циторедуктивной терапии
· низкий риск тромбозов – циторедуктивная терапия, как правило, не требуется;
· промежуточный риск:
— возраст 60 лет: 1-ая линия гидроксимочевина, 2-ая линия анагрелид и/или ИФН-альфа;
· высокий риск:
— возраст 40 лет: 1-ая линия гидроксимочевина, 2-ая линия анагрелид и/или ИФН-альфа; Сочетанная терапия (гидроксимочевина + анагрелид, гидроксимочевина + ИФН-альфа)
может стать альтернативой в качестве терапии 2-ой линии у пациентов, если при монотерапии развиваются побочные эффекты, не позволяющие прием дозы препарата, адекватной для контроля уровня тромбоцитов.
Гидроксимочевина
Терапевтический эффект гидроксимочевины заключается в снижении тромбоцитоза, профилактике тромботических осложнений. В исследовании РТ-1 показана большая эффективность гидроксимочевины в сравнении с анагрелидом в предотвращении артериальных тромбозов [22]. Определенные опасения вызывает возможный лейкозогенный эффект при длительном применении, в связи с чем гидроксимочевину в первой линии молодым больным с ожидаемой длительной продолжительностью жизни следует назначать с осторожностью.
Рекомендации (УД – B): гидроксимочевина рекомендуется как препарат выбора в качестве терапии первой линии у больных ЭТ с промежуточным риском развития тромбозов в возрасте > 60 лет и у больных ЭТ с высоким риском развития тромбозов в возрасте > 40 лет. Вторая линия терапии у других категорий больных с промежуточным и высоким риском развития тромбозов.
Гидроксимочевину не следует использовать при беременности или при планировании беременности.
Интерферон-альфа
Лечение препаратами ИФН-альфа является эффективным и безопасным препаратом для лечения. ИФН-альфа не оказывает лейкозогенного или тератогенного действия. Рекомендации (УД – С): ИФН-альфа рекомендуется как препарат выбора в качестве терапии первой линии у больных ЭТ с промежуточным риском развития тромбозов в возрасте
| Фармакологическая группа | Международное непатентованное наименование ЛС | Способ применения, доза | Уровень доказательности |
| Лекарственные средства, профилактирующие тромботические осложнения | ацетилсалициловая кислота или | Внутрь, определяется уровнем тромбоцитов (50, 75, 100мг) | А 33 |
или
или
или
или
или
или
или
или
или
подкожно
или
Эноксапарин
При возникновении осложнений лечение проводится в соответствии с клиническим протоколом данного осложнения.
Хирургическое вмешательство нет.
Дальнейшее ведение: согласно клинического протокола по медицинской реабилитации.
Ведение пациентов с ХМПЗ подразумевает за собой длительный динамический контроль. Профилактика тромбозов и тромбоэмболических осложнений, так как основной причиной, приводящей к инвалидизации и снижению продолжительности жизни, при ЭТ является склонность к тромбозам и тромбоэмболиям.
Стратификация риска у больных ЭТ, как и при ИП предназначена для оценки вероятности тромботических осложнений, в основном обусловливающих инвалидизацию и ограничивающих продолжительность жизни больных.
Из-за риска сердечно-сосудистых осложнений, аритмий и кардиомиопатии, все пациенты должны проходить алвновое обследование сердечно-сосудистой системы (ЭКГ, эхокардиографию).
Индикаторы эффективности лечения [22]
Критерии клиникогематологического ответа при лечении ЭТ:
| Ответ | Критерии ответа | |
| Полный ответ (сохранение ответа в течение 12 недель) | 1 Тромбоциты ≤400 х 109 /л | |
| 2 Нет симптомов, опосредованных заболеванием (микрососудистые нарушения, зуд, головная боль) | ||
| 3 Нормальные размеры селезенки (УЗИ/КТ/МРТ) | ||
| 4 Лейкоциты ≤10 х 109 /л | ||
| Констатация полной ремиссии возможна только при наличии всех 5 критериев. | ||
| Частичный ответ | Пациенты, кто не соответствует критериям полного ответа | |
| (сохранение ответа в течение 12 недель) | 1 Тромбоциты ≤600 х 109 /л или снижение более 50% от исходного уровня. | |
| Нет ответа | Любой ответ, который не удовлетворяет критериям частичного ответа. | |
· нет достоверных рекомендаций по контролю молекулярного ответа (качественный, количественный молекулярный анализ на JAK2V617F).
· исследование костномозгового кроветворения целесообразно проводить только при оценке трансформации в миелофиброз.
Критерии клинико-гематологического ответа при лечении ИП [22]:
| Ответ | Критерии ответа при ИП |
| Полный ответ (ответ в течение 12 недель) | 1 Гематокрит |
| 2 Тромбоциты ≤400 х 109 /л | |
| 3 Лейкоциты ≤10 х 109 /л | |
| 4 Нормальные размеры селезенки (УЗИ/КТ/МРТ) | |
| 5 Нет симптомов, опосредованных заболеванием (микрососудистые нарушения, зуд, головная боль) | |
| Констатация полной ремиссии возможна только при наличии всех 5 критериев. | |
| Частичный ответ (ответ в течение 12 недель) | 1 Гематокрит |
| 2 Ответ по всем другим критериям | |
| Нет ответа | Любой ответ, который не удовлетворяет критериям частичного ответа |
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ [26]: стационарное лечение показано пациентам с развитием жизнеугрожающих тромботических состояний, которое проводится в соответствии с клиническими протоколами: «Венозные тромбозы и тромбофлебиты, посттромбофлебитический синдром», «Тромбоэмболические осложнения в акушерстве», «Тромбоэмболия легочной артерии», «Эмболия и тромбоз аорты и артерий».
Немедикаментозное лечение:
· Режим: общеохранительный.
· Диета: общая.
Медикаментозное лечение: см. Амбулаторный уровень.
Хирургическое вмешательство:
· Спленэктомия – проводится строго по показаниям:
Показания:
· прогрессирующая спленомегалия с компрессионным синдромом (абдоминальный дискомфорт, постоянное чувство тяжести, боль, признаки кишечной непроходимости);
· интоксикация, обусловленная огромной опухолевой массой;
· тяжелые гиперкатаболические симптомы, включая кахексию;
· глубокая анемия, рефрактерный гемолиз, тромбоцитопения, резистентная к традиционным методам терапии;
· обширные инфаркты селезенки с угрозой разрыва;
· внепеченочная портальная гипертензия с угрозой развития кровотечения из желудка и пищевода.
Противопоказания:
· тяжелые сердечно-сосудистые заболевания;
· неконтролируемая коагулопатия;
· отсутствие согласия больного.
Дальнейшее ведение: см. Амбулаторный уровень.
Индикаторы эффективности лечения: см. Амбулаторный уровень.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
· проведение курсов химиотерапии;
· проведение трепанобиопсии гребня подвздошной кости в случае отсутствия возможности проведения в амбулаторных условиях;
· спленэктомия;
· аллогенная трансплантация гемопоэтических стволовых клеток
Показания для экстренной госпитализации:
· соматически тяжелый пациент (ECOG≥3). Госпитализация в отделение паллиативной помощи пациентам с массивной симптоматической спленомегалией, с уровнем тромбоцитов >50 х 109/л.
Информация
Источники и литература
Информация
| АЛТ | – | аланинаминотрансфераза |
| АСТ | – | аспартатаминотрансфераза |
| БФ | – | бластная фаза |
| ГСК | – | гемопоэтические стволовые клетки |
| ГЦ | – | герменативный центр |
| ЗНО | – | злокачественное новообразование |
| ИГХ | – | иммунногистохимия |
| ИП | – | истинная полицитемия |
| ИФα | – | интерферлн-альфа |
| ИФА | – | иммунноферментный анализ |
| ИФТ | – | иммуннофенотипирование |
| КП | – | клинический протокол |
| КТ | – | компьютерная томография |
| ЛДГ | – | лактатдегидрогеназа |
| МПЗ | – | миелопролиферативные заболевания |
| МФ | – | миелофиброз |
| МДС | – | миелодиспластический синдром. |
| МКБ | – | международная классификация болезней |
| МОБ | – | минимальная остаточная болезнь |
| ОАК | – | общий анализ крови |
| ОБП | – | органы брюшной полости |
| ПХТ | – | полихимиотерапия |
| ПЦР | – | |
| РКИ | – | рандомизированное клиническое исследование |
| ТКМ | – | трансплантация костного мозга |
| УД | – | уровень доказательности |
| УЗДГ | – | ультразвуковая доплерография |
| УЗИ | – | ультразвуковое исследование |
| ЭКГ | – | электрокардиограмма |
| ЭТ | – | эссенциальная тромбоцитемия. |
| FISH | – | Fluorescence in situ hybridization |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Кемайкин Вадим Матвеевич – кандидат медицинских наук, Руководитель департамента онкологии Филиала КФ «UMC» Национальный научный центр онкологии и трансплантологии.
2) Вильданова Рузаль Фауатовна – гематолог Филиала КФ «UMC» Национальный научный центр онкологии и трансплантологии.
3) Тусипова Адия Айткалиевна – гематолог Филиала КФ «UMC» Национальный научный центр онкологии и трансплантологии.
4) Смагулова Газиза Ажмагиевна – кандидат медицинских наук, заведующая кафедрой пропедевтики внутренних болезней и клинической фармакологии РГП на ПХВ «Западно-Казахстанский государственный медицинский университет имени М.Оспанова».
Консультант: Рапильбекова Гульмира Курбановна – доктор медицинских наук, профессор, акушер-гинеколог акушерского отделения №1 Филиала КФ «UMC» Национальный научный центр материнства и детства».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Рамазанова Райгуль Мухамбетовна –доктор медицинских наук, заведующая курсом гематологии АО «Казахский медицинский университет непрерывного образования».
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
к типовой структуре
Клинического протокола диагностики и лечения
АЛГОРИТМ ДИАГНОСТИКИ И ЛЕЧЕНИЕ НА ЭТАПЕ СКОРОЙ НЕОТЛОЖНОЙ ПОМОЩИ (схемы)
1) Диагностические мероприятия: сбор жалоб и анамнеза.
2) Медикаментозное лечение: симптоматическая терапия.
Приложение 2
Программа лечения ХМПЗ во время беременности:
В связи с тем, что все Ph-негативные хМПЗ имеют много общих клинико-морфологических характеристик, принципы ведения беременности и лечебная тактика у данной группы пациенток во многом сходны. На основании анализа данных разработан алгоритм обследования женщин с хМПЗ во время беременности, включающий:
— исследование показателей периферической крови и гемостаза, включающее количество тромбоцитов, их функциональную активность, состояние плазменного звена гемостаза, а также исследование содержания маркеров внутрисосудистого свертывания каждые 2 нед.;
— диагностику АФС (волчаночный антикоагулянт, антикардиолипиновые антитела), а также исследование мутаций генов, сопряженных с наследственной тромбофилией, уровня гомоцистеина, в случае если эти исследования не были проведены до беременности;
— УЗИ плода дважды в каждом триместре;
— допплерометрию с исследованием фетоплацентарного и маточно-плацентарного кровотока и кровотока в средней мозговой артерии плода (наиболее информативного показателя для определения гипоксии плода) начиная с 22 нед. каждые 4 нед.;
— кардиотокографию плода с 33 нед. беременности (на 33, 36 и 38-й неделях).



