Хоронит при беременности что это
Что такое антенатальная гибель плода? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кондратенко Юлии Николаевны, гинеколога со стажем в 16 лет.
Определение болезни. Причины заболевания
Опосредованные причины антенатальной гибели плода :
Инфекция может быть вирусной (цитомегаловирусы, вирусы простого герпеса, краснухи, Коксаки, ВИЧ), бактериальной (хламидии, микоплазмы, уреаплазмы, стрептококки группы В, энтеробактерии, кишечная палочка) и грибковой (кандидоз).
Симптомы антенатальной гибели плода
В течение первых трёх дней гибели малыша пациентка может обратить внимание на изменения своего состояния:
Если с момента гибели плода в утробе матери прошло несколько недель, могут присоединяться признаки воспалительной реакции:
Патогенез антенатальной гибели плода
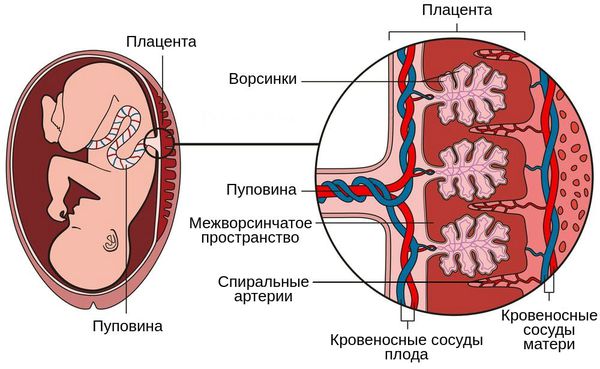
Суть патогенеза заключается в нарушении функции плаценты, развитии хронической плацентарной недостаточности, нарушении кровоснабжения плода, его росте и развитии. Поражаются внутренние органы плода — развивается внутриутробная пневмония, менингит и др. В какой-то момент происходит нарушение нормального функционирования плаценты, развивается острая плацентарная недостаточность и плод погибает.
Профессором И. В. Бариновой в 2015 году были представлены два типа плодовых потерь при внутриутробной гипоксии. Каждому из них характерно своеобразное сочетание патогенетических факторов, связанных с матерью, плацентой и плодом.
Патогенез второго типа обусловлен нарушением циркуляции в плодовой части плаценты, незрелостью ворсин относительно срока беременности, а также васкулопатией сосудов плода и тромбозом ворсин.
Классификация и стадии развития антенатальной гибели плода
Пока не существует общепринятой классификации внутриутробной гибели плода. Однако изучение причин перинатальной смертности привело к появлению двух понятий:
Осложнения антенатальной гибели плода
При своевременном обращении к доктору антенатальная гибель плода не приводит к осложнениям. Если же пациентка обратилась за медицинской помощью спустя больше двух недель после смерти ребёнка, то у неё с большой вероятностью могут развиваться такие осложнения, как:
Чтобы избежать их, необходимо тщательно наблюдать за состоянием пациентки и выполнять профилактические мероприятия:
Диагностика антенатальной гибели плода
После того как женщина обращается к врачу с жалобами на недомогание и отсутствие шевеления плода, врач направляет пациентку на диагностическое обследование. Оно позволяет поставить точный диагноз.
Постановка диагноза внутриутробной гибели плода включает следующие этапы обследования:
Анализы для диагностики внутриутробной гибели плода на позднем сроке беременности не так важны. Отсутствия шевелений плода в течение нескольких дней и сердцебиения по данным УЗИ достаточно для правильной постановки диагноза.
Лечение антенатальной гибели плода
При подтверждённом диагнозе антенатальной гибели плода показана экстренная госпитализация и принятие решения о методе и сроке родоразрешения. Чем меньше интервал между установленным диагнозом и родоразрешением, тем меньше риск возникновения осложнений во время и после родов.
Выбор метода определяется индивидуально, на основании клинических данных и особенностей акушерской ситуации. Оптимальным вариантом родоразрешения при антенатальной гибели плода являются роды через родовые пути. Но иногда выполняется кесарево сечение, например при раннем отделении плаценты от стенок матки, обильном или продолжающемся кровотечении из половых путей.
При родоразрешении беременных с антенатальной гибелью плода, осложнившейся септическим состоянием, показано экстренное оперативное вмешательство. Объём операции решается индивидуально, возможна удаление матки с плодом (экстирпация).
После родов важно тщательно наблюдать за состоянием роженицы, провести профилактику послеродового кровотечения и гнойно-септических осложнений. Необходимо обратить внимание на выделения из половых путей (гнойные или кровянистые ), температуру тела, появление озноба, слабости, тянущих болей внизу живота.
Прогноз. Профилактика
Потеря беременности является показанием к проведению медицинской, психологической и социальной реабилитации пациенток. Необходим полный комплекс диагностических исследований для выяснения причины гибели плода. Выбор алгоритма обследования базируется на данных анамнеза, особенностях течения беременности и результатах патологоанатомического исследования плода и последа.
При неустановленной причине гибели плода в анамнезе необходимо учитывать данный факт при выработке тактики родоразрешения последующих беременностей.
Профилактика антенатальной гибели плода предполагает:
Хориоамнионит — это инфекционное воспаление плодных оболочек и амниотической жидкости, вызванное полимикробными ассоциациями. Проявляется гипертермией, болью в области матки, гнойными или сукровичными выделениями из влагалища. Возможно субклиническое течение заболевания с минимальной симптоматикой. Диагностируется с помощью гинекологического осмотра, КТГ плода, лабораторных исследований, УЗИ малого таза. Тактика ведения беременной предполагает срочное родоразрешение через естественные родовые пути или путем кесарева сечения с одновременным назначением интенсивной антибактериальной, противовоспалительной, инфузионной терапии.
МКБ-10
Общие сведения
Хориоамнионит (интраамниотическая инфекция, амниотический инфекционный синдром) чаще возникает во II триместре и, по данным разных авторов, выявляется у 0,9-10,5% беременных. Развитие заболевания в III триместре обычно связано с длительным безводным периодом после преждевременного излития вод. Патологию чаще обнаруживают у женщин, страдающих хроническими генитальными и экстрагенитальными инфекциями. Актуальность своевременной диагностики и лечения антенатального инфицирования обусловлена тем, что хориоамнионит является одной из наиболее распространенных причин преждевременного прерывания беременности, повышает вероятность возникновения угрожающих жизни осложнений для плода и женщины.
Причины хориоамнионита
Воспаление окружающих плод оболочек — полимикробное инфекционное заболевание, вызванное ассоциацией из двух и более патогенных или условно-патогенных микроорганизмов. Непосредственными возбудителями хориоамнионита могут стать стрептококки группы В, пептострептококки, стафилококки, кишечные палочки, микоплазмы, уреаплазмы, энтерококки, хламидии, трихомонады, гонококки, гарднереллы, кандиды, бактероиды, вирус простого герпеса, цитомегаловирус и др. Для начала воспалительного процесса, как правило, требуется сочетание нескольких предрасполагающих условий, основными из которых являются:
Риск возникновения хориоамнионита также возрастает с началом естественных родов, особенно если в их ходе многократно проводятся пальцевые влагалищные исследования после вскрытия плодных оболочек или выполняется внутренняя кардиотокография плода для получения объективных данных о его состоянии и характеристиках сократительной активности матки.
Патогенез
При нормальном течении беременности развитию воспалительных изменений в хорионе и других плодных оболочках препятствуют естественные плацентарные механизмы защиты, представленные несколькими видами Toll-подобных рецепторов, которые определяют присутствие лигандов микроорганизма и инициируют протективную реакцию в ответ на повреждение эпителия. Выделение дефензинов, секреторных лейкоцитарных ингибиторов протеиназ, элафинов способствует лизису бактерий и инактивации их повреждающих факторов. Массивное восходящее, нисходящее или гематогенное поступление инфекционных агентов провоцирует срыв местного иммунитета, а вырабатываемые ими протеазы разрушают волокна коллагена, входящего в состав плодных оболочек, оказывают прямое повреждающее действие на плаценту.
Опосредованные эффекты, способствующие развитию воспалительного процесса при хориоамнионите, связаны с выделением цитотоксичных цитокинов и матриксных металлопротеаз, апоптозом. Повышенная концентрация микробных фосфолипаз в околоплодной жидкости способствует усиленному синтезу простагландинов из тканевых фосфолипидов, что сопровождается преждевременным началом родовой деятельности. Заглатывая инфицированную амниотическую жидкость, плод внутриутробно заражается. Более чем в 80% случаев заболевания страдает фетоплацентарный комплекс – воспаление распространяется на межворсинчатое пространство, тромбируются сосуды базальной децидуальной оболочки.
Классификация
При систематизации клинических форм хориоамнионита учитывают течение патологического процесса — скорость его развития и выраженность клинических проявлений. С остротой воспаления напрямую связаны морфологические изменения, происходящие в тканях околоплодных оболочек, и вероятность возникновения осложнений. Специалисты в сфере акушерства и гинекологии, различают два вида хориоамнионита:
Симптомы хориоамнионита
При остром течении заболевания у беременной появляются боли различной интенсивности в нижней части живота. Она могут иррадиировать в паховую область, крестец, усиливаться при прощупывании матки через переднюю брюшную стенку. Температура тела зачастую повышена до 38° С и выше, у пациентки возникает выраженный озноб, пульс учащается до 100 сокращений в минуту и выше. Общее самочувствие женщины ухудшается, она испытывает слабость, быструю утомляемость. Могут наблюдаться патологические влагалищные выделения с неприятным запахом — серо-зеленые (гнойные) или с примесью крови. В ряде случаев хориоамнионит протекает бессимптомно и диагностируется после внезапно прервавшейся беременности или по наличию характерных осложнений послеродового периода.
Осложнения
Наиболее серьезными осложнениями хориоамнионита являются фетоплацентарная недостаточность, преждевременный разрыв плодных оболочек, отслоение нормально расположенной плаценты, досрочные роды во 2-3 триместрах. У таких беременных чаще возникают бактериемия, слабость родовой деятельности, атонические послеродовые кровотечения, тромбоэмболии, послеродовые эндометриты, акушерские перитониты, тазовые абсцессы, инфекционные осложнения травматических ран, полученных в родах. Возможны коагулопатии, септический шок, респираторный дистресс-синдром.
Нарушение нормального функционирования фетоплацентарного комплекса при хориоамнионите может спровоцировать задержку развития плода. У новорожденных повышен риск получения травм в родах, развития врожденных неонатальных инфекций (пневмонии, сепсиса, менингита), церебрального паралича и смерти.
Диагностика
Поскольку хориоамнионит представляет серьезную угрозу дальнейшему течению беременности, при подозрении на развитие заболевания все обследования выполняются в экстренном порядке. Диагностический поиск направлен на выявление признаков локального воспаления околоплодных оболочек, оценку состояния плода и определение возможных возбудителей. Наиболее информативны для постановки диагноза:
Дополнительными признаками воспалительного поражения плодных оболочек служат падение уровня эстриола, увеличение содержания хорионического гонадотропина, усиление тромбоагрегации в сочетании с нарушениями плазменного звена гемостаза. После родов наличие воспаления обнаруживается при гистологическом исследовании плодных оболочек. Дифференциальная диагностика проводится с эндометритом, другими воспалительными заболеваниями репродуктивных органов, острой хирургической патологией брюшной полости. При необходимости назначают консультации хирурга, инфекциониста, уролога, неонатолога.
Лечение хориоамнионита
Воспаление оболочек плода является показанием для экстренной госпитализации беременной и ее перевода на постельный режим. Тактика ведения пациентки предполагает как можно более быстрое родоразрешение (стимулированные роды или кесарево сечение) с назначением массивной антибактериальной и симптоматической терапии, которые продолжаются в послеродовом периоде. Выбор метода родоразрешения зависит от выраженности воспалительных изменений, срока безводного периода (при преждевременном излитии околоплодных вод), состояния женщины и плода. Схема медикаментозного лечения направлена на решение таких терапевтических задач, как:
Назначение пациенткам с хориоамнионитом витаминно-минеральных комплексов, иммуностимулирующих средств ускоряет процесс выздоровления и снижает вероятность осложнений. Во время восстановительного периода показано физиотерапевтическое лечение с использованием УВЧ-терапии, инфракрасной лазеротерапии, электроимпульсной терапии.
Прогноз и профилактика
При своевременной постановке диагноза прогноз хориоамнионита для беременной благоприятный. Вероятность положительного исхода для плода повышается по мере увеличения гестационного срока, на котором возникло заболевание. Профилактические мероприятия предполагают раннюю постановку на учет в женской консультации для выявления и лечения генитальных инфекций, экстрагенитальной патологии. Рекомендованы обоснованный подход к назначению инвазивной пренатальной диагностики, экстренная госпитализация и выбор оптимальной тактики ведения беременности и родов при преждевременном отхождении околоплодных вод.
Перинатальные исходы при преждевременном разрыве плодных оболочек
Рассмотрены этиология и перинатальные и постнатальные исходы при преждевременном разрыве плодных оболочек (ПРПО), акушерская тактика ведения недоношенной беременности, осложненной ПРПО, показания к досрочному прерыванию недоношенной беременности, осложнен
Etiology, and ante-natal and post-natal outcomes in premature breaking of waters (PBW) were considered, as well as obstetrical practice of managing incomplete pregnancy complicated with PBW, and indications for premature abortion of incomplete pregnancy complicated with PBW.
Преждевременным называется разрыв околоплодных оболочек до начала родовой деятельности независимо от срока беременности, клинически проявляющийся излитием околоплодных вод. Популяционная частота преждевременного разрыва плодных оболочек (ПРПО) составляет около 12% [1, 6], однако в структуре причин преждевременных родов эта патология достигает 35–60% [2].
Этиология
Данные эпидемиологических исследований свидетельствуют о многообразии этиологических факторов ПРПО. Выявлена взаимосвязь ПРПО с высоким паритетом, а также преждевременными родами, привычным невынашиванием и ПРПО в анамнезе [5]. Причиной разрыва оболочек могут быть приобретенные или врожденные формы дефицита коллагена (синдром Элерса–Данлоса), дисбаланс микроэлементов, в том числе дефицит меди, являющейся кофактором матриксных металлопротеиназ (ММП) и их ингибиторов, влияющих на свойства компонентов соединительнотканного матрикса плодных оболочек. Одним из факторов, способствующих повреждению плодных оболочек, является оксидантный стресс, связанный с продукцией реактивных кислородных радикалов нейтрофилами и макрофагами при их вовлечении в процесс микробной элиминации, которые вызывают локальную дегенерацию коллагена, истончение и разрыв оболочек путем активизации ММП, а хлорноватистая кислота непосредственно разрушает коллаген I типа, являющийся структурной основой плодных оболочек [11, 19].
Подтверждена роль отслойки плаценты как в индукции преждевременных родов, так и ПРПО, связанная с выбросом большого количества простагландинов, высокой утеротонической активностью тромбина [27] и наличием питательной среды для роста бактериальной микрофлоры.
На протяжении последних лет утвердилось обоснованное мнение о том, что ведущей причиной ПРПО является восходящее инфицирование околоплодных оболочек и микробная инвазия амниотической полости, частота которой в течение первых суток после ПРПО составляет от 37,9% до 58,5% [12]. Подтверждают восходящий путь передачи инфекции многочисленные исследования, указывающие на идентичность штаммов микроорганизмов, выделенных у плодов и в мочеполовых путях беременных [7, 12, 21]. Среди инфекционных агентов, которые служат непосредственной причиной восходящего воспалительного процесса, преобладают Еscherichia сoli, Staphilococcus aureus, Streptococcus faecalis, Streptococcus группы B, Bacteroides fragilis, Corinobacter, Campylobacter, Clebsiella pneumoniae [7]. Ряд авторов подчеркивают роль анаэробных бактерий в этиологии восходящего инфицирования, в частности Fusobacterium [22]. К часто встречающимся представителям микробных ассоциаций относятся Ureaplasma urealiticum, Mycoplasma hominis и Gardnerella vaginalis. Однако широкое распространение урогенитальных микоплазм, стертая клиническая картина и трудности диагностики затрудняют определение роли этих микроорганизмов в этиологии и патогенезе преждевременных родов и ПРПО [3]. Риск ПРПО значительно возрастает при наличии истмико-цервикальной недостаточности и пролапса плодного пузыря в связи с нарушением барьерной функции цервикального канала, а также укорочении шейки матки менее 2,5 см [14].
Степень повреждения околоплодных оболочек связана с видом патогена и его способностью активизировать ММП. Тесная взаимосвязь увеличения концентрации большинства ММП (ММП-1, 7, 8 и 9) и снижения тканевого специфического ингибитора металлопротеиназ (ТИММП-1) в околоплодных водах с внутриамниальной бактериальной инвазией и отслойкой плаценты не подвергается сомнению [11, 19]. Механизм бактериального действия на плодные оболочки опосредован, с одной стороны, стимулирующим влиянием микробных протеиназ и эндотоксинов на экспрессию ММП и выработку провоспалительных цитокинов (ИЛ-2, ИЛ-6, ИЛ-12, фактора некроза опухоли) с последующей локальной деградацией коллагена оболочек, а с другой стороны, повышением бактериальными фосфолипазами синтеза простагландинов с развитием гипертонуса миометрия и увеличения внутриматочного давления [19].
Таким образом, ведущую роль в этиологии и патогенезе ПРПО при недоношенной беременности играют факторы, стимулирующие апоптоз, разрушение фосфолипидов и деградацию коллагена соединительнотканного матрикса околоплодных оболочек, преимущественно связанные с действием инфекции.
Перинатальные и постнатальные исходы
Более 30% пери- и неонатальной заболеваемости и смертности при преждевременных родах связаны с беременностью, осложненной ПРПО [1, 3]. В структуре заболеваемости и смертности основное место занимают синдром дыхательных расстройств (СДР) (до 54%), внутриутробная инфекция и гипоксическое поражение головного мозга, в виде перивентрикулярной лейкомаляции (ПВЛ) головного мозга (до 30,2%) и внутрижелудочковых кровоизлияний (ВЖК) [1, 3, 31].
Синдром дыхательных расстройств
СДР новорожденных представляет совокупность патологических процессов, формирующихся в пренатальном и раннем неонатальном периодах и проявляющихся нарастанием симптомов дыхательной недостаточности на фоне угнетения жизненно важных функций организма. Основной причиной развития СДР является дефицит сурфактанта или его инактивация. К предрасполагающим факторам следует отнести внутриутробные инфекции (ВУИ) и перинатальную гипоксию. Степень тяжести и частота реализации СДР прогрессивно снижается с увеличением срока беременности и степени зрелости плода и составляет около 65% до 30 недель беременности, 35% — в 31–32 недели, 20% в 33–34 недели, 5% в 35–36 недель и менее 1% — в 37 недель и более [1, 15, 31].
Существует мнение, что интраамниальная инфекция, связанная с длительным безводным промежутком, способствует созреванию легких плода и снижает частоту респираторных нарушений [28]. В эксперименте на овцах показано, что интраамниальное введение эндотоксина E. coli достоверно в большей степени повышает концентрацию липидов и протеинов сурфактанта, при применении бетаметазона, и в 2–3 раза увеличивает воздушный объем легких [15]. Однако клинические исследования не подтвердили предположение о стимулирующем влиянии ПРПО на зрелость легочной ткани, и оно требует дальнейшего изучения [31].
Врожденная инфекция плода
Наиболее значимым фактором риска неблагоприятного пери- и постнатального исхода, усугубляющим течение пневмопатий и патологии центральной нервной системы, является ВУИ. Это понятие объединяет инфекционные процессы (пневмония, сепсис и др.), которые вызывают различные возбудители, проникшие к плоду от инфицированной матери. Для недоношенных детей, находящихся на длительном стационарном лечении, большую опасность представляют и нозокомиальные инфекции. Мертворождаемость и ранняя неонатальная смертность при ВУИ связана со степенью тяжести воспалительного процесса, зависящего от гестационного возраста плода, типа и вирулентности возбудителя, защитных факторов околоплодных вод и неспецифического иммунитета, и составляет по данным литературы 14,9–16,8% и 5,3–27,4% соотвественно [2, 33].
Преобладающей клинической формой неонатальной инфекции при ПРПО, составляющей от 42% до 80%, является пневмония, как правило, связанная с аспирацией инфицированными водами, часто сочетающаяся с признаками язвенно-некротического энтероколита. Прогрессирование очагов первичного воспаления в легких или кишечнике плода обусловливает возможность развития метастатического гнойного менингита, перитонита, а также внутриутробного сепсиса, частота которого при ПРПО до 32 недель колеблется от 3% до 28%. Основными факторами риска неонатального сепсиса являются гестационный срок и развитие хориоамнионита (ХА) [29, 33].
Влияние ВУИ на отдаленный исход не однозначно. Есть данные, указывающие на риск развития детского церебрального паралича, связанного с интраамниальной инфекцией и гестационным возрастом плода [10, 26]. В то же время ряд исследований не подтвердили достоверной связи между ВУИ и нарушением умственного и психомоторного развития детей [17, 22].
Постгипоксические поражения головного мозга
Основные гипоксические повреждения головного мозга недоношенных детей включают ПВЛ и ВЖК.
ПВЛ представляет собой коагуляционный некроз белого вещества, с последующей дегенерацией астроцитов с пролиферацией микроглии, вследствие гипоксемии и ишемии головного мозга. При экстремально низкой и очень низкой массе тела при рождении патологоанатомическая частота ПВЛ варьирует от 25% до 75%, а in vivo — от 5% до 15%. Осложения ПВЛ в виде деструкции афферентных волокон таламокортикальных и кортикокортикальных путей отрицательно влияют на формирование межнейрональных ассоциативных связей, процессы миелинизации белого вещества и могут стать причиной развития когнитивных нарушений [2, 26]. Прогностическим критерием развития ПВЛ и отдаленных неврологических нарушений является значительное повышение концентрации в околоплодных водах и пуповинной крови новорожденных провоспалительных цитокинов, в том числе ИЛ-6, что подтверждает гипотезу о цитокин-опосредованном повреждении мозга и косвенно свидетельствует о роли ВУИ в развитии ПВЛ [13, 26].
ВЖК составляют в структуре перинатальной смертности недоношенных новорожденных от 8,5% до 25% [2, 13]. К основным факторам риска их развития относят острую гипоксию плода и ХА [26]. Частота тяжелых степеней ВЖК снижается с увеличением гестационного возраста и при родоразрешении путем операции кесарева сечения. Некоторые исследования подтверждают роль глюкокортикоидной терапии в уменьшении риска развития ВЖК и ПВЛ [17, 20]. В то же время разработка достоверно эффективных методов профилактики ВЖК до настоящего времени остается в поле внимания научных исследований.
Инфекционные осложнения беременных, рожениц и родильниц при недоношенной беременности, осложненной ПРПО
Пролонгирование недоношенной беременности при ПРПО представляет значительный риск для матери, в первую очередь в связи с присоединением инфекционного процесса и развитием гнойно-септических осложнений (ГСО), в большинстве случаев ХА, послеродового эндомиометрита и, реже, — сепсиса. К факторам риска реализации ГСО следует отнести хирургические внутриматочные вмешательства, хроническую урогенитальную инфекцию, разрыв плодных оболочек на фоне пролабирования плодного пузыря, а также антенатальной гибели плода [1, 5].
Риск гнойно-септических инфекций (ГСИ) матери имеет достоверную связь с длительностью безводного промежутка и сроком гестации. Общая частота реализованного ХА при недоношенной беременности, осложненной ПРПО, составляет 13–74%, а при разрыве оболочек до 28 недель 28,8–33% [4, 7, 13]. Однако, по нашим данным, основанным на анализе течения 912 беременностей, осложненных ПРПО в сроке 22–34 недели, частота ХА до 31 недели беременности и продолжительности латентного периода более 2 суток — времени, необходимого для эффективной экспозиции глюкокортикоидов с целью профилактики СДР, — достоверно не меняется. В то же время при пролонгировании беременности после 31-й недели риск реализации ХА увеличивается. Таким образом, на наш взгляд, оптимальным подходом при ведении беременности, осложненной ПРПО, следует считать максимальное пролонгирование беременности до 31-й недели беременности, а при разрыве оболочек в более поздние сроки — только на период проведения глюкокортикоидной профилактики СДР. В то же время необходимо помнить, что вопрос о возможности длительного пролонгирования беременности при ПРПО должен решаться индивидуально с учетом возможностей акушерской и, в большей степени, неонатальной служб, а также факторов риска ГСИ у беременной.
К прогностическим критериям инфекционных осложнений и ХА относят маловодие и косвенные признаки воспаления плаценты [23]. По нашим данным, при нормальном объеме околоплодных вод с индексом амниотической жидкости более 8 см частота реализации ХА составляет 4,9%. В то же время при снижении индекса амниотической жидкости менее 5 см риск развития ХА возрастает в 2 раза.
Послеродовая заболеваемость родильниц проявляется эндометритом в 3,5–11,1% случаях [4]. Частота развития сепсиса по данным разных авторов достигает 1,7%, а материнская летальность, связанная с ведением недоношенной беременности, осложненной ПРПО, — 0,85% [4, 23].
Клинико-лабораторная диагностика и прогностические критерии хориоамнионита и системной воспалительной реакции
Раннее выявление признаков ХА представляет определенные трудности в связи с изменением реактивности организма во время беременности и склонности к формированию латентных форм воспалительных заболеваний. Типичными симптомами ХА являются лихорадка, тахикардия матери и плода, специфический запах околоплодных вод или патологические выделения из влагалища. К сожалению, гипертермия до 38 °С и выше часто является единственным индикатором развития ХА, а значения традиционных маркеров воспалительного процесса — количества лейкоцитов и сегментоядерных нейтрофилов — при беременности имеют широкую вариабельность, зависимы от медикаментов, в том числе стероидов и антибиотиков и, по данным некоторых исследований, имеют невысокое диагностическое значение [4, 30]. Из рутинных клинико-лабораторных критериев ХА высокую диагностическую ценность имеют гипертермия более 37,5 °С, лейкоцитоз более 17 × 10 9 /л и палочкоядерный сдвиг лейкоцитарной формулы до 10% и более. Развитие указанных симптомов необходимо использовать в качестве показаний для родоразрешения со стороны матери при пролонгировании недоношенной беременности, осложненной ПРПО [2, 4, 6].
Наибольшие трудности представляет ранняя диагностика септических состояний. За последние годы достигнут большой прогресс в изучении и использовании белков плазмы крови, принимающих участие в так называемом острофазном ответе — совокупности системных и местных реакций организма на тканевое повреждение, вызванное различными причинами (травма, инфекция, воспаление, злокачественное новообразование и пр.). В качестве прогностического критерия инфекции при ПРПО широко используется определение концентрации С-реактивного белка (СРБ), повышение которого в сыворотке крови более 800 нг/мл является индикатором интраамниальной инфекции и тесно коррелирует с фуниситом, гистологически и клинически выраженным ХА с чувствительностью 92% и специфичностью 96% [9]. Кроме того, концентрация СРБ в околоплодных водах может косвенно отражать состояние плода, так как он продуцируется гепатоцитами и не проникает через плаценту. В то же время ряд авторов считают СРБ малоспецифичным, а повышение его концентрации возможным при физиологическом течении беременности [30].
Среди биомаркеров сепсиса наиболее высокой диагностической точностью обладает прокальцитонин (ПКТ) — предшественник гормона кальцитонина, вырабатываемый несколькими типами клеток различных органов под влиянием бактериальных эндотоксинов и провоспалительных цитокинов. При системном инфекционном поражении его уровень возрастает в течение 6–12 часов и может служить ранним диагностическим критерием сепсиса и системной воспалительной реакции. Вирусные инфекции, местные инфекции, аллергические состояния, аутоиммунные заболевания и реакции отторжения трансплантата обычно не приводят к повышению концентрации ПКТ, а его высокие уровни свидетельствуют о бактериальной инфекции с системной воспалительной реакции [4, 25]. По нашим данным, средние уровни ПКТ при нормальном течении беременности и реализованном ХА составляют 0,29 и 0,72 нг/мл (p
В. Н. Кузьмин, доктор медицинских наук, професcор
ГБОУ ВО МГМСУ им. А. И. Евдокимова, Москва
Перинатальные исходы при преждевременном разрыве плодных оболочек/ В. Н. Кузьмин
Для цитирования: Лечащий врач № 3/2018; Номера страниц в выпуске: 34-38
Теги: недоношенная беременность, осложнения, акушерская тактика