Хорошо что во время появления пенициллина
Новости Барнаула
Опросы
Спецпроекты
Прямой эфир
Лекарство, которое спасло миллионы. 10 удивительных фактов о пенициллине
Пенициллин / Фото: ru-static.z-dn.net
13 сентября мир празднует день рождения пенициллина. Открыл это лекарство Александр Флеминг. За всю историю человечества не было другого лекарства, которое спасло бы столько человеческих жизней. «Для победы во Второй мировой войне пенициллин сделал больше, чем 25 дивизий!» Именно такие слова прозвучали при вручении Флемингу, Чейну и Флори Нобелевской премии по биологии и медицине. ИА «Амител» подготовило подборку интересных фактов об этом удивительном лекарстве.
Факт №1
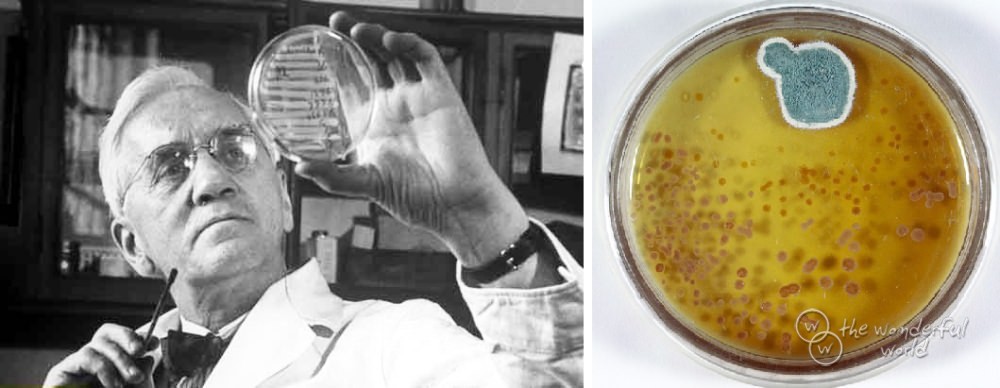
Неряшливость шотландского микробиолога Александра Флеминга явилась причиной открытия пенициллина. Когда 3 сентября 1928 года он возвратился в свою лабораторию, после того как целый месяц отсутствовал, то обратил внимание на чашку Петри, внутри которой образовался участок с плесенью. Ученый заметил, что вокруг плесени исчезли все микробные колонии. Этот феномен заинтересовал Флеминга, и он провел исследование содержимого чашки. Плесень принадлежала к роду пеницилловых, а вещество, погубившее микробов, ученый назвал пенициллином.
Отчет о своем новом открытии Флеминг опубликовал в 1929 году в одном британском журнале, который был посвящен экспериментальной патологии. В этом же году он все еще занимался исследованиями и вскоре обнаружил, что осуществлять работу с пенициллином сложно, его выработка чрезвычайно трудоемка и выделить в чистом виде его невозможно. К тому же экстракт плесени оказался нестойким, быстро выводился из тканей, и создать нужную концентрацию для полного уничтожения бактерий не получалось.
Флеминг продолжал в больнице свои опыты по местному применению пенициллина, используя экстракт плесени наружно для лечения воспалительных очагов. Результаты были довольно благоприятными, но отнюдь не чудодейственными, так как в нужный момент лекарство теряло свою активность. В 1931 году, выступая в Королевской зубоврачебной клинике, он снова охарактеризовал пенициллин как перспективный препарат. В 1932 году в журнале «Патология и бактериология» Флеминг опубликовал результаты своих опытов лечения инфицированных ран.
В середине 1939 года молодой английский профессор Хоуард Уолтер Флори, заведующий кафедрой патологии в Оксфордском университете, и биохимик Эрнест Чейн по просьбе Флеминга попытались получить в чистом виде пенициллин. Только после двух лет разочарований и поражений им удалось получить несколько граммов коричневого порошка.
Когда 3 сентября 1939 года Англия объявила войну Германии, Оксфордская группа, опасаясь немецкой оккупации, решила любой ценой спасти чудодейственную плесень. Чейн и Флори вывезли свой препарат на анализ в США контрабандным способом: они пропитали коричневой жидкостью подкладку своих пиджаков и карманов. Достаточно было выжить одному из них, чтобы сохраненные споры плесневых грибков позволили возобновить работу. Только в середине 1940 года пенициллин удалось получить в необходимом для исследований количестве.
Первые инъекции нового средства были сделаны человеку 12 февраля 1941 года. Один из лондонских полицейских во время бритья порезался. Развилось заражение крови. Первый укол пенициллина сделали умирающему пациенту. Состояние больного сразу улучшилось. Но пенициллина было слишком мало, запас его быстро иссяк. Болезнь возобновилась, и пациент умер. Несмотря на это, наука торжествовала, так как было убедительно доказано, что пенициллин прекрасно действует против заражения крови. Через несколько месяцев ученым удалось накопить такое количество пенициллина, которого могло с избытком хватить для спасения человеческой жизни. Счастливцем был пятнадцатилетний мальчик, больной заражением крови, которое не поддавалось лечению. Это был первый человек, которому пенициллин спас жизнь.
В 1941 году СССР запросил у союзников образец лекарства. Однако ответа не последовало. Тогда в 1942 году под руководством главы всесоюзного института экспериментальной медицины Зинаиды Виссарионовны Ермольевой из плесени, собранной со стен бомбоубежища, в тяжелейших условиях был получен отечественный пенициллин. Советский препарат был назван «пенициллин-крустозин». Его выпуск был начат в 1944 году на предприятиях химико-фармацевтической промышленности методом поверхностного культивирования гриба.
В 1943-м впервые пенициллин начали выпускать в массовом количестве в Пеории, штат Иллинойс, на заводе Хайрама Уолкера. Когда-то здесь с большим знанием дела «варили» виски, и на винодельческой фирме имелось превосходное оборудование для ферментации. Но вскоре выяснилось, что эти помещения слишком тесные для наращивания производства лекарства, что потребовало расширения бизнеса.
Потребность в пенициллине росла с каждым днем. Важно было увеличить не только количество препарата, но и его активность. Интересное испытание антибиотиков произошло в январе 1944 года, когда в Москву с группой зарубежных ученых приехал профессор Флори. Он привез свой пенициллин и решил сравнить его с российским. Наш препарат оказался активнее зарубежного: 28 единиц против 20 в 1 мл. Тогда профессор Флори и американский ученый Сандерс предложили провести клинические испытания по оценке действия препарата на больных. И вновь победу одержал наш отечественный пенициллин.
По просьбе профессора Флори предоставить для дальнейших исследований русский пенициллин ему намеренно, якобы как его образец, был выдан американский штамм. Вернувшись в Америку, Флори исследовал полученный материал и был разочарован. В своем отчете он написал: «Советская плесень оказалась не crustosum, а notatum, как у Флеминга. Ничего нового русские не открыли». А вот советские ученые как раз и «утерли нос» американским коллегам, но только наладить широкомасштабное производство этого препарата в разрушенной стране было непросто.
Сам пенициллин по настоянию Флеминга не был запатентован. Он считал, что лекарство, спасающее людям жизнь, не должно служить источником дохода.
Случайности не случайны: как был открыт первый антибиотик?
Историю открытия первого антибиотика, пенициллина, часто называют случайностью, реже – «научным анекдотом», а кто-то считает, что это было провидение. Первооткрывателем вещества считается микробиолог и бактериолог Александр Флеминг.
Правда, ученый всегда говорил о себе, что он всего лишь заметил свойства пенициллина и придумал ему название. Как бы то ни было, это лекарство, спасло тысячи жизней и оказало человечеству неоценимую помощь в борьбе с тяжёлыми бактериальными инфекциями.
Открытие Флеминга
Быть может, он плохо помыл лабораторную посуду, или споры залетели из соседнего помещения, важен тот факт, что, когда Флеминг пригляделся к испорченным образцам, оказалось, что стафилококков в чашках нет, плесень уничтожила их. После изучения этого случая Флеминг занялся выделением действующего вещества из плесени.
В сентябре 1929 г. в университетском медицинском клубе Лондона он сделал доклад о новом веществе Penicillium notatum, указав помимо достоинств и недостатки. Вещество было нестойким и включало в себя множество белковых примесей, затрудняющих его использование в медицине.
Опыты по очистке длились до 1941 года. Выделить пенициллин в чистом виде удалось учёным Э. Флори и Г. Чейну, и тогда же препарат начал успешно применяться в терапии. Именно 1941 г. считается началом эры антибиотиков.
В 1945 г. Флеминг, Чейн и Флори получили нобелевскую премию, но сразу отказались от патента, решив, что лекарство, спасающее тысячи жизней, не должно становиться средством материального обогащения.
В аптеках «Столички» представлен большой выбор качественных современных препаратов для борьбы с вирусами и инфекциями. Перед применением некоторых, требуется консультация специалиста.
Гайморит: симптомы, особенности лечения и правила профилактики
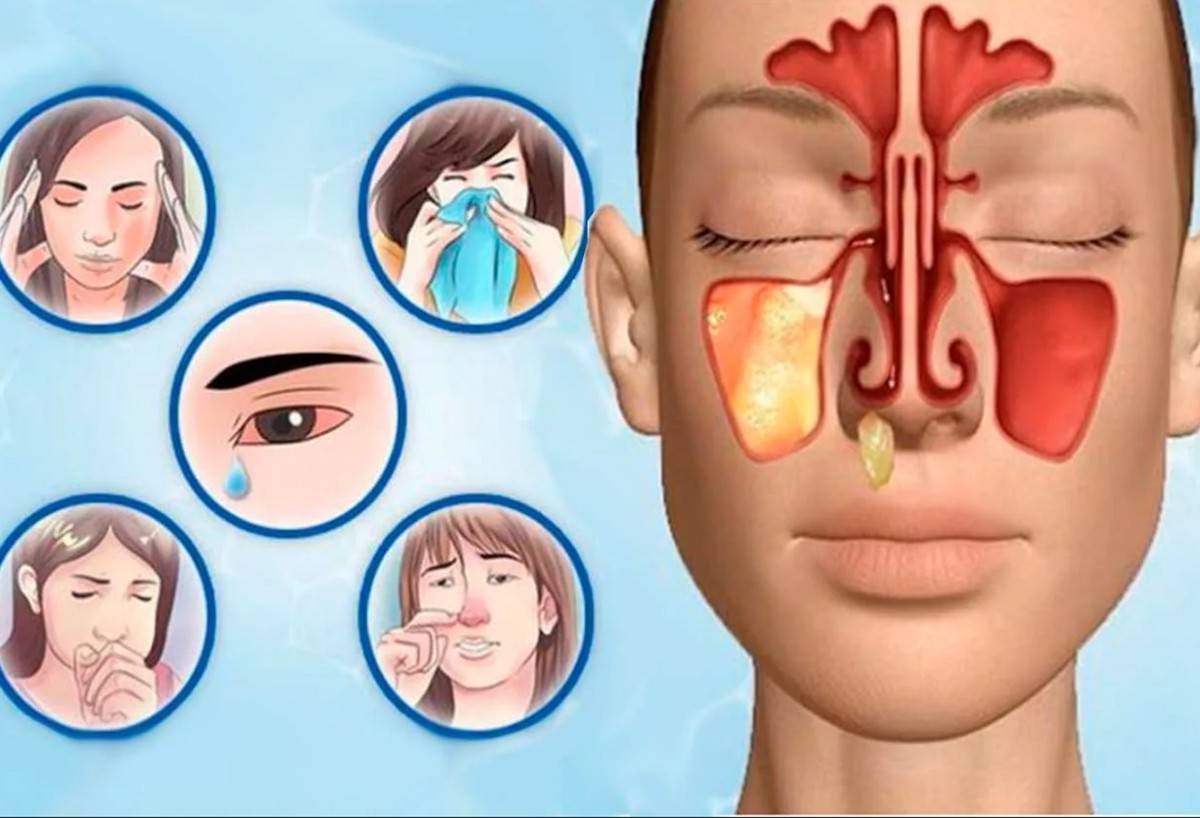
Гайморит – это воспалительный процесс в области гайморовой пазухи, расположенной в толще черепной кости над верхней челюстью, слева и справа. Этот процесс является одной из разновидностей синуситов (это общее название для воспалительных процессов в области придаточных пазух – лобной, гайморовой, решетчатой или клиновидной). Обычно воспалительный процесс затрагивает слизистые оболочки, выстилающие пазухи изнутри, реже затрагиваются более глубокие слои тканей, вплоть до костных структур. Обычно процесс возникает как осложнение вирусных или бактериальных инфекций в области носоглотки и верхних дыхательных путей.
Исходя из причины развития, механизмов формирования и симптомов, гайморит бывает нескольких типов. Выделение каждого из них важно для определения тактики лечения, прогноза и разработки мер профилактики.
Острый – развивается быстро, как осложнение ОРВИ, насморков, простудных заболеваний, воспаления в области корней зубов на верхней челюсти. Возбудители проникают через каналы, соединяющие пазухи с полостью носа с гайморовыми пазухами, размножаются в полости. Тело начинает активно вырабатывать иммунные клетки и слизь, чтобы обезвредить патогенные организмы. Если слизь закупорит проток пазухи, возникает давление на стенки, усиление воспалительного процесса. По мере очищения пазухи от содержимого воспалительный процесс постепенно затухает.
Хронический – воспалительный процесс, который длится более 4 недель, имеет вялое или волнообразное течение, с периодами обострений. Обычно возникает из-за не долеченной острой формы, наличия аденоидов, тонзиллитов, отитов.
Гнойный – обычно становится осложнением острой формы либо обострения хронического процесса, если процесс не лечится, предпринимаются попытки самолечения или пациент переносит инфекцию на ногах. Патогенные бактерии накапливаются в пазухах, в смеси с лейкоцитами образуют гнойное содержимое. Самое опасное осложнение при этой форме – прорыв гноя в полость черепа, поражение костных тканей, мозга.
Двусторонний – одна из тяжелых форм, поражение локализовано сразу в обеих пазухах – левой и правой. Нередко возникает как осложнение инфекций в полости рта и носоглотки, обычно грибковой или бактериальной. Обычно имеет острое течение, редко переходит в хроническую форму.
Аллергическое поражение возникает у пациентов, страдающих от чрезмерно активной реакции иммунной системы на различные вещества. Особенно часто эта форма синусита бывает при поллинозе, круглогодичном рините, реакции на плесень, пылевых клещей.
Катаральный – преимущественно бывает у детей. Он развивается при проникновении в полость пазух патогенных организмов, что формирует отек и раздражение слизистых. Считается самой легкой формой болезни, проходящей при активном лечении без осложнений и последствий.
Полипозная форма формируется при образовании полипозных разрастаний слизистых из-за чрезмерно быстрого деления клеток. Рост полипов могут провоцировать инфекции, травмы, велика роль наследственности.
Одонтогенный – формируется как результат серьезных проблем зубов, особенно 4-6 зуба на верхней челюсти, корни которых расположены в непосредственной близости от пазухи. Если возникают проблемы в области корней этих зубов, воспаление и нагноение может переходить на пазуху, она заполняется секретом и воспаляется.
Причины
Придаточные пазухи, включая гайморовы, созданы как естественный барьер на пути инфекций, фильтр для различных опасных веществ в воздухе. Они помогают согревать воздух, увлажнять его и очищать от примесей перед попаданием в гортань, и ниже по респираторному тракту. Основная причина воспаления и появления признаков гайморита – это проникновение бактерий, грибков или вирусов, аллергенов. Реже инфекция попадает с током крови из других, отдаленных очагов.
Нарушать работу пазух могут патологии иммунной системы, частые ОРВИ, респираторная форма аллергии, носительство патогенных бактерий в носоглотке (стафило-, стрепто- или менингококк).
Среди ключевых причин, которые могут привести к развитию гайморита, можно выделить:
Осложнения
Не все люди знают, как начинается гайморит, поэтому многие принимают симптомы за тяжелую простуду и лечатся самостоятельно. Это может привести к определенным осложнениям, отдаленным последствиям. Среди ключевых осложнений можно выделить поражения бронхов и распространение инфекции на легкие, развитие отитов (поражение среднего уха), переход болезни в хроническую форму.
Тяжелый и запущенный, своевременно не вылеченный гайморит может привести к воспалению внутренних органов – сердца, глаз, почек, поражению суставов и мозга, его оболочек. Если образуются гнойные полости в гайморовых пазухах, возможен прорыв гноя в кровь (возникает сепсис), проникновение его в соседние пазухи с развитием пансинусита, воспаление мозговых оболочек с явлениями менингита. Всех этих осложнений можно избежать при полноценном лечении гайморита под руководством лор-врача.
Симптомы и диагностика
Конечно, при развитии гайморита нужно немедленно обращаться к врачу, но как понять, что гайморит начался? Начальные признаки неспецифичные – это повышение температуры от незначительной до высокой, сильная слабость, заложенность носа или обильные густые выделения, болезненность в проекции пазух или в области лица.
Боль при гайморите может быть различной – от тупой, давящей до сильной, мучительной. Она локализуется в подглазничной области, может отдавать в область переносицы, лобную зону или верхние зубы. При надавливании на область пазух или наклонах головы вперед она усиливается, распространяясь по подглазничной области. Могут краснеть и отекать веки.
Врачи отмечают некоторые особенности того, как проявляется болезнь в определенных возрастных группах. Так, у взрослых самым ключевым признаком могут быть болевые ощущения, головная боль, нарушение восприятия запахов. Может меняться голос, он становится гнусавым, нос сильно заложен, выделяется полупрозрачная или желто-зеленая слизь. Высокая лихорадка типична для острой формы, при хроническом или аллергическом гайморите болезнь может протекать без температуры.
На фоне поражения пазух возможно слезотечение, неприятный привкус во рту, слабость, постоянное утомление, нарушения аппетита, расстройства сна, ознобы и приступы кашля.
Заразен ли гайморит? Само по себе воспаление – это результат влияния патогенных факторов, и это не заразно. Бактерии или вирусы, которые спровоцировали заболевание, могут передаваться от человека к человеку, но не обязательно вызовут поражение пазух.
Диагноз гайморита ставит лор-врач после проведения ряда тестов и осмотра пациента. Важно подробно рассказать, как началось заболевание, какие жалобы были ранее и имеются в данный момент. Врач осмотрит полость носа и глотку, прощупает проекцию пазух, определяя болезненность.
Дополнительно могут понадобиться КТ или МРТ придаточных пазух, рентгенограмма, УЗИ исследование, эндоскопия носоглотки, при необходимости – биопсия полипозных образований. Назначаются анализы крови, посевы отделяемой из носа слизи для определения флоры, чтобы подобрать необходимые препараты.
Как лечить у взрослого
Терапия болезни должна быть комплексной. Она направлена на борьбу с инфекцией, устранение воспаления, налаживание оттока слизи из пазух и улучшение носового дыхания. В неосложненных случаях возможно лечение гайморита дома под постоянным контролем оториноларинголога. В тяжелых случаях и при необходимости хирургического лечения пациент госпитализируется в стационар.
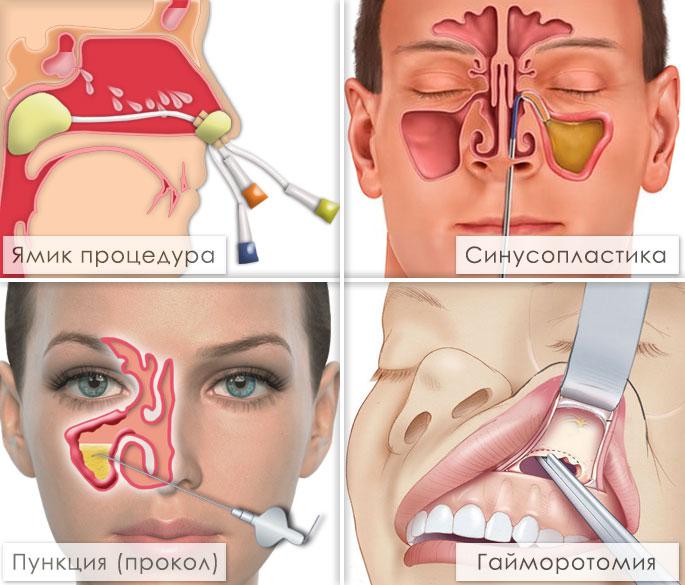
Возможно консервативное лечение с назначением антибактериальных препаратов, противовоспалительных средств, антигистаминных препаратов и различных капель, спреев для носа. Также применяют пункционное лечение или хирургические вмешательства. Выбор зависит от возраста пациента, вида патологии, тяжести состояния и возможных осложнений.
Многим пациентам назначают пункции (с местным обезболиванием) – они помогают удалить гнойное содержимое, помочь в оценке характера воспаления, плюс приносят существенное облегчение. После удаления содержимого пазухи промывают физраствором или фурациллином, вводят растворы антибиотиков и противовоспалительные препараты. Минус подобной тактики – не всегда достаточно одного прокола, поэтому требуется курс процедур в течение нескольких недель. Метод достаточно неприятный, имеет ряд противопоказаний и осложнений, процедура болезненна как во время прокола, так и после него.
Ошибки в антибактериальной терапии инфекций дыхательных путей в амбулаторной практике
Проблема рациональной антибактериальной терапии инфекций дыхательных путей не теряет актуальности и в настоящее время. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой
Проблема рациональной антибактериальной терапии инфекций дыхательных путей не теряет актуальности и в настоящее время. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой — требует от врача-клинициста осведомленности о многочисленных антибиотиках и их свойствах (спектр действия, фармакокинетика, побочные эффекты и т. д.), умения ориентироваться в вопросах микробиологии, клинической фармакологии и других смежных дисциплинах.
Согласно И. В. Давыдовскому, «врачебные ошибки — род добросовестных заблуждений врача в его суждениях и действиях при исполнении им тех или иных специальных врачебных обязанностей». Ошибки в антибактериальной терапии инфекций дыхательных путей имеют наибольший удельный вес в структуре всех лечебно-тактических ошибок, совершаемых в пульмонологической практике, и оказывают существенное влияние на исход заболевания. Кроме того, неправильное назначение антибактериальной терапии может иметь не только медицинские, но и различные социальные, деонтологические, экономические и другие последствия.
При выборе способа антибактериальной терапии в амбулаторной практике необходимо учитывать и решать как тактические, так и стратегические задачи. К тактическим задачам антибиотикотерапии относится рациональный выбор антибактериального препарата, обладающего наибольшим терапевтическим и наименьшим токсическим воздействием.
Стратегическая задача антибиотикотерапии в амбулаторной практике может быть сформулирована как уменьшение селекции и распространения резистентных штаммов микроорганизмов в популяции.
В соответствии с этими положениями следует выделять тактические и стратегические ошибки при проведении антибактериальной терапии инфекций дыхательных путей в амбулаторной практике (см. таблицу 1).
Тактические ошибки антибактериальной терапии
I. Необоснованное назначение антибактериальных средств
Особую категорию ошибок представляет неоправданное применение антибактериальных препаратов (АП) в тех ситуациях, когда их назначение не показано.
Показанием для назначения антибактериального препарата является диагностированная или предполагаемая бактериальная инфекция.
Наиболее распространенная ошибка в амбулаторной практике — назначение антибактериальных препаратов при острых респираторных вирусных инфекциях (ОРВИ), имеющее место как в терапевтической, так и в педиатрической практике. При этом ошибки могут быть обусловлены как неправильной трактовкой симптоматики (врач принимает ОРВИ за бактериальную бронхолегочную инфекцию в виде пневмонии или бронхита), так и стремлением предотвратить бактериальные осложнения ОРВИ.
При всех трудностях принятия решения в подобных ситуациях необходимо отдавать себе отчет в том, что антибактериальные препараты не оказывают влияния на течение вирусной инфекции и, следовательно, их назначение при ОРВИ не оправдано (см. таблицу 2). В то же время предполагаемая возможность предотвращения бактериальных осложнений вирусных инфекций с помощью назначения антибактериальных препаратов не находит себе подтверждения в клинической практике. Кроме того, очевидно, что широкое неоправданное применение антибактериальных препаратов при ОРВИ чревато формированием лекарственной устойчивости и повышением риска возникновения нежелательных реакций у пациента.
Одной из распространенных ошибок при проведении антибактериальной терапии является назначение одновременно с антибиотиком противогрибковых средств с целью профилактики грибковых осложнений и дисбактериоза. Следует подчеркнуть, что при применении современных антибактериальных средств у иммунокомпетентных пациентов риск развития грибковой суперинфекции минимален, поэтому одновременное назначение антимикотиков в этом случае не оправдано. Комбинация антибиотика с противогрибковым средством целесообразна только у больных, получающих цитостатическую или противоопухолевую терапию или у ВИЧ-инфицированных пациентов. В этих случаях оправдано профилактическое назначение антимикотиков системного действия (кетоконазол, миконазол, флуконазол), но не нистатина. Последний практически не всасывается в желудочно-кишечном тракте и не способен предотвратить грибковую суперинфекцию иной локализации — полости рта, дыхательных или мочевыводящих путей, половых органов. Часто практикующееся назначение нистатина с целью профилактики дисбактериоза кишечника вообще не находит логического объяснения.
Часто врач назначает нистатин или другой антимикотик в случае обнаружения в полости рта или в моче грибов рода Сandida. При этом он ориентируется лишь на данные микробиологического исследования и не учитывает наличие или отсутствие симптомов кандидоза, а также факторов риска развития грибковой инфекции (тяжелый иммунодефицит и др.).
Выделение грибов рода Сandida из полости рта или мочевых путей пациентов в большинстве случаев служит свидетельством бессимптомной колонизации, не требующей коррегирующей противогрибковой терапии.
II. Ошибки в выборе антибактериального препарата
Пожалуй, наибольшее число ошибок, возникающих в амбулаторной практике, связано с выбором антибактериального средства. Выбор антибиотика должен производиться с учетом следующих основных критериев:
Определяющим фактором выбора препарата должен быть спектр природной активности антибиотика: необходимо, чтобы он охватывал основных возбудителей внебольничных инфекций дыхательных путей (см. таблицу 3).
Кроме того, при выборе препарата следует учитывать уровень приобретенной резистентности возбудителей в популяции. Основные тенденции, касающиеся резистентности возбудителей, отмеченной в последние годы, отражены в таблице 4. Наиболее значимые проблемы, связанные с применением основных антибактериальных средств при инфекциях дыхательных путей, могут быть сформулированы следующим образом.
С учетом вышесказанного, оптимальными средствами для лечения внебольничных инфекций дыхательных путей в настоящее время могут быть признаны β-лактамные антибиотики и новые фторхинолоны (см. таблицу 5). Использование макролидов должно быть ограничено — препараты можно назначать при нетяжелой пневмонии у детей или пациентов молодого возраста, особенно при наличии признаков атипичного течения (микоплазменная, хламидийная).
 |
| Таблица 5. Значение антибактериальных средств при инфекциях нижних дыхательных путей в амбулаторной практике. |
Следует подчеркнуть, что назначение некоторых антибактериальных препаратов, применяемое в амбулаторной практике при респираторных инфекциях, нельзя признать рациональным. К таким препаратам прежде всего относятся:
В таблице 6 приведены современные рекомендации по антибактериальной терапии внебольничных респираторных инфекций, с учетом всех требуемых критериев и доказанной эффективности в контролируемых клинических исследованиях.
Представленные рекомендации имеют наиболее общий характер. В то же время с практических позиций выбор оптимального антибактериального препарата также должен осуществляться с учетом особенностей пациента и заболевания. Так, например, у больных пневмонией молодого и среднего возраста без отягощающих факторов терапевтический эффект оказывают амоксициллин, макролиды, защищенные пенициллины и новые фторхинолоны. Однако у больных пожилого возраста в этиологии заболевания большее значение приобретают S. aureus и грамотрицательные бактерии, что объясняет снижение эффективности амоксициллина и макролидов у этой категории больных.
Также распространенной во врачебной практике ошибкой является отказ от назначения антибактериальной терапии при пневмонии беременным женщинам из-за опасения негативного влияния препаратов на плод. Следует отметить, что перечень антибактериальных препаратов, прием которых нежелателен во время беременности из-за риска эмбриотоксического действия, ограничен — тетрациклины, хлорамфеникол, сульфаниламиды, ко-тримоксазол, фторхинолоны, аминогликозиды. Другие антибиотики, в частности β-лактамы, макролиды, могут применяться у беременных женщин.
Другие возможные факторы, влияющие на выбор антибактериального препарата, представлены в таблице 7.
 |
| Таблица 7. Особые клинические ситуации при внебольничных инфекциях нижних дыхательных путей. |
Нередки ошибки при выборе антибактериального препарата в случае неэффективности первоначального. Здесь необходимо также остановиться на ошибках антибактериальной терапии, которые касаются несвоевременной оценки неэффективности первоначального антибиотика. Общепринятым критическим сроком оценки эффективности (или неэффективности) антибактериальной терапии считаются 48—72 ч с момента его назначения. К сожалению, приходится нередко сталкиваться с такими случаями, когда больной продолжает получать назначенный антибиотик в течение недели и более, несмотря на отсутствие очевидного клинического эффекта. Обычно критерием эффективности антибактериальной терапии является снижение или нормализация температуры тела больного, уменьшение признаков интоксикации. В тех случаях (не столь частых), когда лихорадка с самого начала заболевания отсутствует, приходится ориентироваться на другие признаки интоксикации (головная боль, анорексия, общемозговая симптоматика и т. д.), а также на отсутствие прогрессирования заболевания за период проводимого лечения.
Продолжение антибактериальной терапии, невзирая на ее неэффективность, имеет немало негативных последствий. При этом затягивается назначение другого, более адекватного антибиотика, что ведет к прогрессированию воспаления (особенно важно при тяжелых пневмониях, у больных с сопутствующей патологией) и развитию осложнений, а также удлиняет сроки лечения. Кроме того, повышается риск возникновения побочных (токсических) эффектов препаратов, а также развития и усиления антибиотикорезистентности. Продолжение лечения, несмотря на неэффективность проводимой терапии, подрывает доверие больного и его родственников к лечащему врачу. Очевидна и неэкономичность такой ошибочной тактики антибактериальной терапии (напрасный расход неэффективного АП, дополнительные затраты на лечение токсических эффектов и др.).
Кроме того, ошибки встречаются при замене неэффективного антибиотика на другой, т. е. при смене препарата. При этом врач забывает, что принцип выбора антибактериального препарата остается прежним, т. е. ориентироваться следует на клиническую ситуацию с учетом, однако, неэффективности первоначального препарата и ряда других дополнительных признаков. Отсутствие эффекта от первоначально назначенного антибиотика в известной степени должно служить дополнительным ориентиром, позволяющим обосновать выбор второго препарата. Так, например, отсутствие эффекта от применения β-лактамных антибиотиков (пенициллины, цефалоспорины) у больного с внебольничной пневмонией позволяет предполагать атипичную этиологию пневмонии (микоплазменной, хламидийной или легионеллезной) с учетом, разумеется, других клинических признаков.
Клинические признаки атипичной пневмонии, вызванной Mycoplasma pneumoniae или Chlamydia pneumoniae:
Наличие клинических признаков атипичной пневмонии делает обоснованным назначение антибактериальных препаратов из группы макролидов, доксициклина или фторхинолонов (левофлоксацин, моксифлоксацин, офлоксацин).
III. Ошибки в выборе режима дозирования антибактериального препарата
Ошибки в выборе оптимальной дозы антибактериального средства могут заключаться в назначении как недостаточной, так и избыточной дозы препарата. И те и другие ошибки чреваты негативными последствиями.
Если доза антибиотика недостаточна и не создает в крови и тканях дыхательных путей концентрацию, превышающую минимальную дозу для подавления основных возбудителей инфекции, что является условием эрадикации соответствующего возбудителя, то это не только может служить одной из причин неэффективности терапии, но и создает реальные предпосылки для формирования резистентности микроорганизмов. Ошибки в выборе оптимальной дозы могут быть связаны как с назначением недостаточной разовой дозы, так и с неправильным режимом дозирования (недостаточная кратность введения).
В качестве примера неадекватного режима дозирования антибиотиков при внебольничной пневмонии можно привести амоксициллин, который ранее рекомендовался в суточной дозе до 1 г. Однако современные рекомендации предполагают назначение амоксициллина в суточной дозе 1,5 и даже 3 г для преодоления возможной резистентности S. pneumoniae. Примеры неадекватных режимов дозирования антибиотиков в амбулаторной практике при респираторных инфекциях приводятся в таблице 8.
 |
| Таблица 8. Неадекватные режимы дозирования пероральных антибактериальных препаратов в амбулаторной практике при респираторных инфекциях у взрослых. |
Неправильный выбор интервалов между введениями антибактериальных препаратов обычно обусловлен не столько сложностями парентерального введения препаратов в амбулаторных условиях или негативным настроем больных, сколько неосведомленностью практикующих врачей о некоторых фармакодинамических и фармакокинетических особенностях препаратов, которые должны определять режим их дозирования. Типичной ошибкой является назначение в амбулаторной педиатрической практике при пневмонии бензилпенициллина с кратностью введения два раза в сутки, так как более частое его введение неудобно для пациента. Следует отметить, что при нетяжелом течении пневмонии вряд ли оправдано стремление некоторых врачей к обязательному назначению парентеральных антибиотиков. Современные антибактериальные препараты характеризуются хорошей биодоступностью при приеме внутрь, а также одинаковой клинической эффективностью с парентеральными препаратами, поэтому в подавляющем большинстве случаев оправдано лечение пероральными препаратами. Если назначение парентеральных антибиотиков действительно необходимо, следует выбрать препарат с длительным периодом полувыведения (например, цефтриаксон), что позволяет назначать его один раз в сутки.
IV. Ошибки при комбинированном назначении антибиотиков
Одной из ошибок антибактериальной терапии внебольничных респираторных инфекций является необоснованное назначение комбинации антибиотиков. Врачи старших поколений помнят то время (50—70-е гг. прошлого столетия), когда при лечении пневмонии обязательным считалось назначение пенициллина и стрептомицина, о чем свидетельствовали многие учебные пособия и руководства. Это был своеобразный стандарт лечения пневмоний для того времени. Несколько позднее одновременно с антибиотиками рекомендовалось назначение сульфаниламидов, с учетом полученных в свое время З. В. Ермольевой данных о химиотерапевтическом синергизме сульфаниламидов и пенициллина.
В современной ситуации, при наличии большого арсенала высокоэффективных антибактериальных препаратов широкого спектра, показания к комбинированной антибактериальной терапии значительно сужены, и приоритет в лечении респираторных инфекций остается за монотерапией. В многочисленных контролируемых исследованиях показана высокая клиническая и бактериологическая эффективность адекватных антибактериальных средств при лечении респираторных инфекций в режиме монотерапии (амоксициллин, амоксициллин/клавуланат, цефалоспорины II-III поколений, новые фторхинолоны). Комбинированная антибактериальная терапия не имеет реальных преимуществ ни в выраженности эффекта, ни в предотвращении развития резистентных штаммов.
Основными показаниями к комбинированной антибактериальной терапии являются тяжелое течение пневмонии — в этом случае общепринятым стандартом лечения становится комбинированное назначение парентерального цефалоспорина III поколения (цефотаксим или цефтриаксон) и парентерального макролидного антибиотика (эритромицин, или кларитромицин, или спирамицин); последние включаются в комбинацию для воздействия на вероятных атипичных микроорганизмов (легионелла или микоплазма). Следует отметить, что в настоящее время в клинической практике появились новые антибактериальные препараты (левофлоксацин, моксифлоксацин) с высокой активностью в отношении как типичных, так и атипичных возбудителей, что позволяет назначать их в режиме монотерапии даже при тяжелой пневмонии.
Другой клинической ситуацией, оправдывающей комбинированное назначение антибиотиков, является пневмония у иммунокомпрометированных пациентов (лечение цитостатиками, СПИД), при которой имеется высокая вероятность ассоциации возбудителей (см. таблицу 7).
К сожалению, часто в амбулаторной практике приходится сталкиваться с ситуациями, при которых больным с нетяжелым течением пневмонии, при отсутствии осложнений, тяжелой фоновой патологии назначается два антибиотика. Логичного обоснования этой тактики лечения нет, при этом следует учитывать возможный антагонизм препаратов, более высокий риск нежелательных реакций и увеличение стоимости лечения.
Следует отметить, что нерациональные комбинации антибактериальных препаратов имеют и официальные лекарственные формы, которые выпускаются отечественной фармацевтической промышленностью, например ампиокс, олететрин. Разумеется, применение таких препаратов недопустимо.
V. Ошибки, связанные с длительностью антибактериальной терапии и критериями клинической эффективности
В некоторых случаях проводится необоснованно длительная антибактериальная терапия. Такая ошибочная тактика обусловлена, прежде всего, недостаточным пониманием цели самой антибактериальной терапии, которая сводится прежде всего к эрадикации возбудителя или подавлению его дальнейшего роста, т. е. направлена на подавление микробной агрессии.
Собственно воспалительная реакция легочной ткани, которая проявляется различными клинико-рентгенологическими признаками (аускультативная картина, сохраняющаяся рентгенологическая инфильтрация, ускорение СОЭ) регрессирует медленнее и не требует продолжения антибактериальной терапии (см. таблицу 9). В связи с этим следует считать ошибочной тактику, согласно которой у больногос сохраняющимися рентгенологическими признаками легочной инфильтрации, крепитирующими хрипами (crepitacio redux), увеличением СОЭ при нормализации температуры тела и исчезновении (или уменьшении) признаков интоксикации продолжают проводить антибактериальную терапию.
 |
| Таблица 9. Сроки исчезновения симптомов при эффективной антибактериальной терапии внебольничной пневмонии. |
Еще более ошибочна тактика замены одного антибиотика на другой в подобных ситуациях, расцениваемых врачом как неэффективность назначенной антибактериальной терапии. У некоторых больных после исчезновения признаков интоксикации и даже регрессии воспалительных изменений в легких в течение длительного времени может сохраняться слабость, потливость, субфебрильная температура. Последняя расценивается врачом как проявление не полностью купированной бронхолегочной инфекции, что «подтверждается» рентгенологическими данными в виде изменения легочного рисунка или «остаточными явлениями пневмонии» и обычно влечет за собой назначение антибактериального препарата, несмотря на отсутствие изменений со стороны крови. Между тем подобная клиническая ситуация часто обусловлена вегетативной дисфункцией после легочной инфекции (постинфекционная астения) и не требует антибактериальной терапии, хотя, разумеется, в каждом конкретном случае необходимы тщательное обследование больного и расшифровка всей имеющейся симптоматики.
Рекомендованная длительность применения антибактериальных препаратов при бронхолегочных инфекциях приведена в таблице 10.
 |
| Таблица 10. Длительность антибактериальной терапии бактериальных респираторных инфекций в амбулаторной практике. |
Л. И. Дворецкий, доктор медицинских наук, профессор
С. В. Яковлев, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва