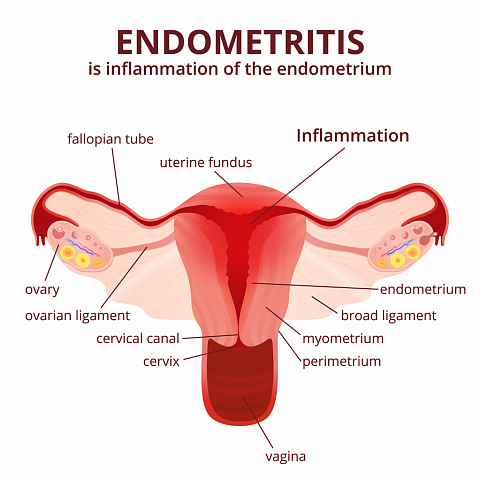
Хронический неспецифический эндометрит что это такое и как лечить
Хронический эндометрит — проблема и решения
Рассмотрены факторы риска развития хронического эндометрита, клинические симптомы заболевания, методы диагностики и подходы к комплексной терапии.
An examination was performed on the factors of the risk of the development of chronic endometritis, clinical symptoms of disease, methods of diagnostics and approaches to complex therapy.
.jpg)
В настоящее время актуальность проблемы ХЭ приобретает не только медицинское, но и социальное значение, поскольку данное заболевание часто приводит к нарушению репродуктивной функции, являясь причиной бесплодия, неудачных попыток экстракорпорального оплодотворения (ЭКО), невынашивания беременности (НБ), осложненного течения беременности и родов [1].
Хронический эндометрит — клинико-морфологический синдром, характеризующийся комплексом морфофункциональных изменений эндометрия воспалительного генеза, приводящих к нарушению нормальной циклической трансформации и рецептивности ткани.
Среди пациенток с ХЭ 97,6% составляют женщины репродуктивного периода, что подчеркивает особую значимость данной патологии с точки зрения влияния на репродуктивную функцию [2].
У женщин с бесплодием ХЭ встречается в 12–68% случаев, достигая своего максимума при наличии трубно-перитонеального фактора бесплодия. У больных с неудачными попытками ЭКО и переноса эмбрионов (ПЭ) частота ХЭ возрастает до 60% и более. Наибольшие показатели распространенности ХЭ отмечены у больных с привычным невынашиванием беременности и составляют более 70% [5, 6].
По данным различных авторов, факторами риска развития ХЭ являются все инвазивные вмешательства в полости матки (гистероскопия, выскабливание полости матки, биопсия эндометрия, гистеросальпингография, манипуляции в программах вспомогательных репродуктивных технологий и др.), инфекционно-воспалительные осложнения после беременностей и родов, использование внутриматочных спиралей (ВМС), инфекции влагалища и шейки матки, бактериальный вагиноз, деформации полости матки с нарушением циклического отторжения эндометрия, лучевая терапия в области органов малого таза [1, 7, 8].
В современных условиях эндометрит характеризуется рядом особенностей: изменением этиологической структуры с увеличением значимости вирусной и условно-патогенной флоры, ростом резистентности флоры к фармакотерапии, трансформацией клинической симптоматики в сторону стертых форм и атипичного течения, длительными сроками терапии и высокой ее стоимостью [9]. Современная общепризнанная классификация ХЭ, выстроенная по этиологическому фактору, претерпела в последнее десятилетие значительные изменения в сторону расширения перечня специфических форм заболевания. Существуют вирусные (вирус папилломы человека — ВПЧ, цитомегаловирус, вирус иммунодефицита человека), хламидийные, микоплазменные, грибковые, протозойные и паразитарные специфические эндометриты, отдельно выделен саркоидоз эндометрия [1, 10]. Для идентификации инфекционного агента обязательно проводить тщательное микробиологическое исследование соскоба эндометрия с определением чувствительности флоры к антибактериальным препаратам. В одной трети случаев при гистологически верифицированном ХЭ выявляются стерильные посевы эндометрия, что может свидетельствовать о важной роли условно-патогенной флоры в развитии воспалительного процесса или недостаточной детекции возбудителя, особенно в случае вирусной инвазии [11]. Длительная и часто бессимптомная персистенция инфекционных агентов в эндометрии приводит к выраженным изменениям в структуре ткани, препятствуя нормальной имплантации и плацентации, формируя патологический ответ на беременность, а также вызывает нарушение пролиферации и нормальной циклической трансформации ткани [12]. По различным данным, у больных с бесплодием частота ХЭ составляет в среднем 10% (от 7,8 до 15,4%). Среди женщин с верифицированным ХЭ в 60% случаев диагностируется бесплодие (в 22,1% — первичное бесплодие, в 36,5% — вторичное бесплодие), неудачные попытки ЭКО и переноса эмбрионов в анамнезе отмечены у 40% женщин [4, 12]. Клиническая картина ХЭ в значительной степени отражает глубину структурных и функциональных изменений в ткани эндометрия. Неполноценная циклическая трансформация эндометрия на фоне воспалительного процесса, нарушение процессов десквамации и регенерации функционального слоя эндометрия приводят к появлению основного симптома заболевания — маточных кровотечений (перименструальные, межменструальные). Достаточно постоянными являются жалобы на тянущие боли внизу живота, дисменорею и диспареунию, нередко отмечаются серозные и серозно-гноевидные бели. Среди клинических симптомов особое место занимает бесплодие (преимущественно вторичное), неудачные попытки ЭКО и НБ. Более половины пациенток в анамнезе имеют инвазивные вмешательства в полости матки и на органах малого таза. Часто хронический эндометрит сочетается с хроническим сальпингоофоритом и спаечным процессом в малом тазе. Важно отметить, что использование минимальных критериев для диагностики воспалительных заболеваний органов малого таза (ВЗОМТ), предложенных CDC (Centers for Disease Control and Prevention, США, 1993), информативно в случае с хроническим эндометритом только в 33% [7]. В целом у 35–40% пациенток какие-либо клинические симптомы заболевания отсутствуют [8, 13]. Диагностика ХЭ основана на анализе клинических симптомов, данных анамнеза, эхографической картины [2, 11]. Обязательным этапом диагностики заболевания является морфологическое исследование эндометрия [14].
Эхографические критерии ХЭ впервые разработаны профессором В. Н. Демидовым с соавт. (1993 г.). Исследование проводят дважды на 5–7 и 17–21 день менструального цикла. Часто при ХЭ полость матки после менструации расширена до 0,4–0,7 см, в ряде случаев имеется асимметричность расширения полости матки и неровность внутренней поверхности эндометрия. Изменение структуры эндометрия также выражается в возникновении в зоне срединного М-эха участков повышенной эхогенности различной величины и формы. Внутри участков выявляются отдельные зоны неправильной формы и сниженной эхогенности. Другой важный признак — наличие пузырьков газа, иногда с характерным акустическим эффектом «хвоста кометы». В базальном слое эндометрия часто визуализируются четкие гиперэхогенные образования диаметром до 0,1–0,2 см, представляющие собой очаги фиброза, склероза или кальциноза. Довольно редким, но важным признаком эндометрита является асимметрия толщины передней и задней стенок эндометрия. О наличии патологии свидетельствует также истончение М-эха во второй трети менструального цикла менее 0,6 см. У каждой пятой больной отмечается наличие нескольких из перечисленных признаков [15].
В настоящее время для диагностики внутриматочной патологии широко используется гистероскопия [16]. Наиболее частыми признаками воспалительного процесса в эндометрии являются: неравномерная толщина эндометрия — 30% случаев, полиповидные нарастания — 32,2%, неравномерная окраска и гиперемия слизистой оболочки — 23% и 11,8%, точечные кровоизлияния — 9%, очаговая гипертрофия слизистой оболочки — 7%. Трудности гистероскопической интерпретации данных связаны с отсутствием типичных макроскопических признаков хронического эндометрита, с очаговым характером воспалительного процесса и стертыми формами заболевания [17]. По разным данным гистероскопия позволяет по макроскопическим признакам точно идентифицировать хронический эндометрит только в 16–35% случаев [7, 16]. При подозрении на ХЭ гистероскопия важна для исключения всего спектра внутриматочной патологии, но для верификации диагноза во всех случаях необходимо проведение морфологического исследования эндометрия [8].
«Золотым стандартом» диагностики ХЭ является морфологическое исследование эндометрия, которое должно быть обязательным звеном алгоритма обследования [7, 13]. Диагностическое выскабливание слизистой оболочки матки производят в среднюю и позднюю фазу пролиферации, на 7–10 день менструального цикла. В последние годы общепринятыми критериями морфологической диагностики ХЭ являются [1]:
Несмотря на значительное развитие фармакологической основы терапии, лечение ХЭ в настоящее время представляет значительные трудности для клиницистов [4].
Комплексная терапия ХЭ должна быть этиологически и патогенетически обоснованной, поэтапной и базироваться на результатах максимально тщательного обследования [5]. Алгоритм лечения должен учитывать все звенья патогенеза заболевания.
Необходимость использования этиотропных препаратов для элиминирования повреждающего агента или снижение вирусной активности не вызывает сомнения. Принимая во внимание, что почти в 70% случаев ВЗОМТ применение рутинных методов диагностики не позволяет выявить этиологический фактор, эмпирическая антимикробная терапия при ХЭ всегда оправдана и приводит к достоверному уменьшению частоты клинических симптомов. При этом она должна обеспечивать элиминацию широкого спектра возможных патогенных микроорганизмов, включая хламидии, гонококки, трихомонады, грамотрицательные факультативные бактерии, анаэробы, стрептококки и вирусы. Оправдано назначение нескольких курсов этиотропной терапии со сменой групп препаратов [5, 18].
Выбор группы лекарственных препаратов зависит от данных микробиологического исследования содержимого влагалища и полости матки, анамнестических указаний на использование антибактериальных препаратов в течение последнего года, от выраженности клинической симптоматики и обширности воспалительного процесса [16].
Основу базовой антибактериальной терапии должны составлять комбинации фторхинолонов и нитроимидазолов; цефалоспоринов III поколения, макролидов и нитроимидазолов, а также сочетание защищенных пенициллинов (амоксициллин/клавулановая кислота) с макролидами. При наличии вирусной инфекции (чаще вируса простого герпеса) в зависимости от клинической картины применяют современные аналоги нуклеозидов (Ацикловир или Валтрекс), как правило, в длительном режиме — в течение не менее 3–4 месяцев [3, 19].
Одновременно на основании данных иммунного и интерферонового статуса проводится коррекция иммунных нарушений [20].
Второй этап лечения ХЭ направлен на восстановление морфофункционального потенциала ткани и устранение последствий вторичных повреждений: коррекция метаболических нарушений и последствий ишемии, восстановление гемодинамики и активности рецепторного аппарата эндометрия. Данный этап лечения крайне важен, должен быть продуманным и достаточно продолжительным [11].
Метаболическая терапия при ХЭ направлена на усиление тканевого обмена, активацию энергетических процессов в клетках, устранение последствий гипоксии ткани, в том числе угнетение анаэробного гликолиза [4, 12]. С этой целью используются комплексные метаболические препараты, длительность приема которых должна составлять не менее 3–4 недель. Представителем данной группы препаратов является Актовегин, полученный посредством диализа и ультрафильтрации, в состав которого входят низкомолекулярные пептиды и дериваты нуклеиновых кислот. Актовегин активирует клеточный метаболизм путем увеличения транспорта, накопления и усиления внутриклеточной утилизации глюкозы и кислорода, что приводит к ускорению метаболизма аденозинтрифосфата (АТФ) и повышению энергетических ресурсов клетки. Актовегин удобен для приема. Его выпускают и в таблетках, и в растворе для инъекций. Поэтому женщины, которые по каким-либо причинам не могут лечь в стационар или систематически приезжать на прием, принимают его дома по схеме, расписанной врачом. Актовегин таблетки принимают, не разжевывая, перед едой, запивая небольшим количеством жидкости, по 1 таблетке 2 раза в день в течение 30 дней [21]. При введении в форме инфузии к 200–300 мл основного раствора (0,9% раствор хлорида натрия или 5% раствор декстрозы) добавляют 10–20 мл Актовегина, раствор используют по следующей схеме: внутривенно через день в течение не менее двух недель. Скорость введения: около 2 мл/мин [22].
Положительное влияние Актовегина на кровообращение связано с улучшением доставки и утилизации кислорода, увеличением перфузии глюкозы и восстановлением аэробного метаболизма как в периферических тканях, так и в нейрональных структурах. Путем активации фермента супероксиддисмутазы препарат оказывает выраженное антиоксидантное и противоишемическое действие. Актовегин хорошо сочетается с другими лекарственными средствами, что очень удобно для комплексного лечения хронического эндометрита.
Традиционно в комплексной терапии ХЭ применяются физические факторы. Наиболее часто в комплексной терапии ХЭ применяют электроимпульсную терапию, интерференционные токи, переменное магнитное поле низкой частоты, ток надтональной частоты. Задачи физиотерапии при ХЭ заключаются в улучшении гемодинамики органов малого таза, стимуляции функции рецепторов, ускорении процессов регенерации эндометрия, повышении иммунологических свойств [4].
Дискуссионными остаются вопросы о целесообразности использования в комплексном лечении ХЭ циклической гормональной терапии. В настоящее время считается, что при хроническом эндометрите оправдано только дифференцированное назначение гормонотерапии при наличии гипофункции яичников или ановуляции. Потенциал к патологической регенерации ткани, который таит в себе хроническое воспаление, при назначении циклической заместительной гормональной терапии может быть усилен и реализован [3, 8].
Контроль эффективности терапевтических мероприятий должен проводиться не ранее чем через 2 месяца после окончания лечения с учетом эффекта последействия физиотерапии [2, 5]. При этом оценивается динамика клинических симптомов, проводится ультразвуковое исследование матки (допплерометрия сосудов матки) и аспирационная биопсия эндометрия (на 7–10 день менструального цикла) с последующим морфологическим исследованием эндометрия [1, 11].
Литература
А. З. Хашукоева, доктор медицинских наук, профессор
Н. Д. Водяник, кандидат медицинских наук, доцент
С. А. Хлынова, кандидат медицинских наук
Е. А. Цомаева
ГБОУ ВПО РНИМУ им. Н. И. Пирогова Минздравсоцразвития России, Москва
Эндометрит: симптомы и лечение у женщин
Что такое эндометрит матки?
Эндометритом называется воспаление слизистой оболочки матки, которое начинается из-за паразитирования микроорганизмов: они повреждают слизистую, активируют иммунную систему и мигрируют в область воспаления. Есть несколько видов таких «вредителей»:
Симптомы и лечение эндометрита связаны со сложностью заболевания. При тяжелом течении эндометрита (помимо стандартного воспаления) развивается гнойный процесс. Гной образуется из погибших «бойцов» в борьбе за здоровье организма — микроорганизмов и лейкоцитов — и значительно утяжеляет течение заболевания. Иногда у больных проявляется пиометра — состояние, при котором полость матки заполняется гноем.
Возбудители проникают в матку двумя путями: восходящим и нисходящим. В первом случае бактерии попадают в полость из влагалища через шейку матки. Нисходящий путь бывает гематогенным или лимфогенным: иными словами, если в организме уже запущен какой-то воспалительный процесс, возбудитель попадает в матку через кровь или лимфу.
На развитие и течение воспаления влияет ряд провоцирующих факторов:
Другие, не менее опасные факторы — появление в полости матки остатков плаценты после кесарева сечения или родов, а также наличие там децидуальной (отпадающей) ткани, сгустков крови, плодного яйца. Поэтому аборт (особенно в нестерильных условиях) и выскабливание могут привести к воспалению.
Симптомы эндометрита матки
Лейкоциты — клетки иммунной системы — вырабатывают медиаторы воспаления простагландины. Этот процесс проявляется в ряде симптомов:
При эндометрите проявляется острое либо хроническое воспаления: первое характеризуется яркой симптоматикой, второе нередко протекает бессимптомно. Острый воспалительный процесс чаще связан с воздействием сразу нескольких микроорганизмов. Реже слизистая оболочка поражается изолированно: обычно воспаляется мышечная оболочка матки наравне с развитием миоэндометрита.
При остром эндометрите симптомы проявляются на 3-4 день: повышается температура, наблюдается слабость, головная боль и боль внизу живота, гнойные и (или) кровянистые выделения. Острая стадия длится от 8 до 10 дней и полностью проходит при правильном и своевременном лечении. Если же этого не произошло, острая форма может перетечь в хроническую.
Хронический эндометрит легко не заметить: часто женщины узнают о заболевании только на приеме у гинеколога или при планировании беременности. Наиболее яркий симптом заболевания — нарушение менструального цикла. Температура у пациенток обычно нормальная, иногда бывают ноющие боли в пояснице и внизу живота. Поэтому окончательный диагноз ставится только на основе гистологического исследования эндометрия.
При обсуждении репродуктологии важнее говорить о хроническом эндометрите (ХЭ). Острая патология замечается почти сразу и потому оперативно устраняется. А вот хроническая фаза требует долгого лечения в течение нескольких месяцев, ведь при такой форме заболевания эндометрий сильно видоизменяется, не может трансформироваться и обновляться.
Чаще всего болезнь проявляется у женщин от 26 до 35 лет. Национальный центр контроля заболеваемости сообщает, что каждый год в США регистрируют около 1 млн воспалительных заболеваний органов малого таза. В России такие диагнозы ставятся от 28 до 34 % пациенток гинекологии. При хроническом эндометрите часто развивается бесплодие или привычное невынашивание беременности: до 65 % и до 70 % случаев соответственно. Плодное яйцо не может прикрепиться к измененному эндометрию, из-за чего беременность не наступает или протекает неудачно.
Клинические проявления хронического эндометрита таковы:
Однако единого мнения насчет клинической картины хронического эндометрита не существует. Даже при явных симптомах невозможно понять, какова глубина функциональных и структурных изменений эндометрия.
Лечение эндометрита у женщин разного возраста
Симптомы и лечение эндометрита у женщин мало связаны с возрастом. После 40 лет острый эндометрит обычно проявляется более ярко: на это влияют изменения гормонального фона из-за предстоящего климакса. Переход острой формы в хроническую в этом возрасте происходит намного быстрее, однако формат лечения в 25 и 45 лет не различается.
Борьба с заболеванием — сложная, но важная задача, особенно у женщин, переживших выкидыш или неудачное ЭКО. Чтобы поставить точный диагноз и подобрать индивидуальное лечение, врачи МЦРМ собирают детальный анамнез. Необходимо выяснить информацию о менструальной функции, течении и исходе беременностей, абортах и выкидышах. Это позволит верно диагностировать патологию и подготовить эндометрий к беременности с помощью специально подобранных препаратов.
В комплексное лечение входят антибиотики широкого спектра с высокой способностью проникновения в клетку, а также (в зависимости от вида возбудителя) противогрибковые (антимикотики) и противовирусные препараты, местные комбинированные лекарства, системная энзимотерапия (применение ферментов) и физиотерапия в момент реабилитации. Для профилактики кандидоза на фоне антибиотиков назначаются противогрибковые препараты.
Следующий этап — гормональная терапия: комбинированные оральные контрацептивы. Во вторую фазу цикла при планировании беременности врач назначает прогестерон. Лечение начинается с первого дня менструации.
Перед назначением препаратов в нашей клинике проходит комплексная диагностика:
После диагностики мы подбираем индивидуальное лечение. На первом этапе необходимо уничтожить инфекционного агента, на втором — восстановить функционал эндометрия: благодаря лечению устраняются повреждения, завершается регенерация, восстанавливается локальная гемодинамика (движение крови в сосудах) и активность рецепторов эндометрия.
В стенах клиники мы много лет разрабатывали схемы, которые помогают наиболее эффективно бороться с заболеванием. Прежде всего на весь период лечения (два-три менструальных цикла) прописываются следующие препараты:
Препараты в первый месяц лечения:
1. При обнаружении патогена по результатам фемофлор-скриннинга с первого дня менструального цикла назначается антибактериальная либо противовирусная терапия — в зависимости от вида возбудителя. Если в результате фемофлор-скрининга патоген не найден, антибиотики пить не нужно!
2. Также важна поддержка нормальной флоры желудочно-кишечного тракта и влагалища, поэтому:
Препараты во второй месяц лечения:
1. Активная иммунотерапия: 10 дней после менструации принимается Генферон — 250 тыс. ед. два раза в сутки интравагинально.
2. Препараты, которые активируют обмен веществ в тканях, улучшают трофику (питание клеток) и стимулируют процесс регенерации: Актовегин — одно драже 3 раза в сутки перед приемом пищи на протяжении 30 дней.
3. Физиотерапевтические методы благоприятно влияют на пораженные ткани, помогают снять воспалительные процессы, улучшить состояние сосудов и эндометрия.
В третий месяц лечения важно закрепить результат: лучше всего отправиться на санаторно-курортное лечение. Можно поехать в «Балтийский Берег» в Зеленогорске (50 км от центра Санкт-Петербурга): там работают врачи-партнеры, сопровождающие наших пациентов на месте. Специалисты будут знать всё о вашем диагнозе и дадут своевременный совет. Стоимость индивидуальной программы составляет от 2060 рублей в сутки.
Хронический эндометрит и беременность
Как уже было сказано ранее, при хроническом эндометрите часто наблюдается бесплодие или привычное невынашивание беременности. Необходимо, чтобы слой эндометрия постоянно регенерировался: только тогда зародыш будет успешно имплантирован в матку. При хроническом эндометрите регенерация невозможна из-за воспалительного процесса, поэтому плодное яйцо не может закрепиться на эндометрии.
Даже если это происходит, беременность редко оказывается успешной: риск выкидыша сохранится на протяжении вынашивания. Такую беременность сопровождают нарушения и осложнения: в частности, возбудители заболевания могут поразить ткани плода, что приведет к его гибели.
Нарушение развития эмбриона — еще одно возможное последствие беременности при эндометрите. Поврежденному эндометрию не хватает поступления крови из-за застоя: ткань не получает кислород, витамины, питательные вещества и не передает их эмбриону. Из-за этого ребенок может родиться с патологиями. Кроме того в несколько раз повышается вероятность рождения раньше срока, может нарушиться формирование плаценты, так что при планировании беременности следует немедленно начать лечение этого заболевания.
В общей сложности выкидыши и бесплодие из-за хронического эндометрита связаны сразу с несколькими причинами:
Поэтому перед планированием беременности необходимо пройти полный курс лечения от эндометрита: в таком случае вероятность забеременеть может возрасти до 100 %. В случае с ЭКО основная проблема связана именно с закреплением половых клеток в матке, поэтому для эффективности стоит сделать несколько попыток подсадить оплодотворенную яйцеклетку. Помимо приема препаратов необходимо поберечь себя: постараться исключить стрессы, ограничить физическую нагрузку и не поднимать тяжести.
Современные методы лечения хронического эндометрита (обзор литературы)
Хронический эндометрит встречается у женщин преимущественно в репродуктивном возрасте и ведет к нарушению менструальной, секреторной и генеративной функций. На сегодняшний день продолжается активный поиск оптимального и эффективного комплекса мероприятий
Chronic endometritis is common among women in their reproductive age and leads to malfunction of menstrual, secretory and generative function. Currently, active search of optimal and efficient complex of measures for the treatment of this disease is proceeded. All the well-known, including the most modern methods of treatment of chronic endometritis, are presented in this article.
Хронический воспалительный процесс в эндометрии является одной из основных причин невынашивания беременности, бесплодия, неудачных попыток экстракорпорального оплодотворения (ЭКО). Лечение хронического эндометрита представляет собой достаточно сложную, но очень важную задачу, особенно у женщин с бесплодием и репродуктивными потерями в анамнезе [1].
Лечение хронического эндометрита — непростая задача. Сложности ведения больных связаны со следующими причинами. Преобладание стертых форм заболевания и отсутствие специфических клинических симптомов. Хроническое воспаление в любой ткани имеет волнообразно-прогрессирующий характер, поэтому при отсутствии адекватного лечения повреждение ткани во времени (за счет каскада вторичных повреждений) всегда имеет нарастающий характер. Сложности идентификации микробных агентов в эндометрии, особенно при вирусной инвазии, приводят к проблеме выбора этиотропных препаратов. В ходе лечения возможна смена ведущего микробного фактора (например, на представителя условно-патогенной микрофлоры). Элиминация повреждающего агента из эндометрия часто не приводит к самовосстановлению ткани, особенно при длительности заболевания более 2 лет, поэтому с целью устранения каскада вторичных повреждений ткани необходимы целенаправленные терапевтические мероприятия. Контроль эффективности лечебных мероприятий на основании динамики клинических симптомов и неинвазивных методов исследования не дает точных представлений о восстановлении рецептивности эндометрия [2].
Таким образом, лечение хронического эндометрита (ХЭ) должно быть комплексным, этиологически и патогенетически обоснованным, поэтапным и базироваться на результатах максимально тщательного и точного обследования состояния эндометрия. Большинство ученых сходятся во мнении о целесообразности проведения комплексной терапии ХЭ в два этапа [3].
Сущность первого этапа заключается в элиминации повреждающего эндометрий микробного фактора и/или снижении активности вирусной инвазии посредством проведения этиотропной терапии антибиотиками широкого спектра действия, анаэробными средствами и/или противовирусными препаратами [4, 5]. При стерильных посевах эндометрия или невозможности проведения микробиологического исследования у пациенток с признаками ХЭ допустимо проведение эмпирической антибактериальной и противовирусной терапии препаратами широкого спектра действия со сменой групп препаратов в течение нескольких курсов в случае необходимости.
Столкнувшись с проблемой лекарственной резистентности и роста числа нежелательных лекарственных реакций, в последние годы возобновился интерес клиницистов во многих странах мира к использованию фагов с лечебной и профилактической целью. Некоторые предлагают вводить в полость матки поливалентный бактериофаг в сочетании с инфракрасным лазером накожно, что позволяет реализовать антимикробный эффект путем специфического направленного действия на большой спектр возможных возбудителей воспалительного процесса в полости матки в отсутствие значительного системного влияния, а также добиться иммуномодулирующего эффекта, улучшить гемодинамику в органах малого таза и стимулировать рецепторную активность эндометрия [6].
Цель второго этапа лечения ХЭ заключается в восстановлении морфофункционального потенциала эндометрия путем устранения результатов вторичных повреждений ткани — коррекции фиброзирующих и склеротических процессов, последствий ишемии, восстановлении гемодинамики и активности рецепторного аппарата эндометрия. Характер терапии ХЭ на данном этапе зависит от морфологического состояния эндометрия и наличия сочетанной гинекологической патологии. Первый аспект сводится к выраженности воспалительной реакции и наличию обширных участков склероза и/или атрофии в эндометрии, что определяется длительностью течения ХЭ и приводит к нарушению рецептивности эндометрия при продолжительности заболевания более 2 лет.
Научно доказаны морфофункциональные изменения эндометрия у всех женщин с неудачными попытками ЭКО в анамнезе. При обнаружении у таковых совпадений в 3 и более локусах системы генов тканевой совместимости (HLA) II класса целесообразным является проведение подготовительных мероприятий с использованием иммуноглобулинотерапии [7].
Второй этап терапии нередко является продолжительным (2–3 мес), но очень важным, так как позволяет добиться завершения воспалительного процесса — регенерации поврежденной слизистой оболочки тела матки. Для этого используют различные варианты метаболической терапии, преформированные физические и бальнеологические факторы, гормональные препараты, иммуномодуляторы [8–10]. Многие авторы отмечают важность включения в данный этап лечения препарата Лонгидаза, что значительно повышает эффективность терапии и купирование клинической симптоматики [11, 12].
Традиционно в комплексной терапии ХЭ применяются физические факторы [13]. Наиболее часто в комплексной терапии ХЭ применяют электроимпульсную терапию, интерференционные токи, переменное магнитное поле низкой частоты, ток надтональной частоты [14]. Подробно изучено применение низкочастотной электроимпульсной терапии при абдоминально-вагинальном расположении электродов, которая позволяет улучшить имплантационный потенциал эндометрия и увеличить частоту наступления беременности у женщин с «тонким» эндометрием в 3,4 раза [15].
Возможно применение низкоинтенсивного импульсного лазерного излучения красного спектра в комплексной терапии хронического эндометрита с помощью аппарата «Матрикс» по оригинальной методике. Данный вид физического воздействия оказывает противовоспалительный, иммунокоррегирующий, вазоактивный эффекты [16].
Задачами физиотерапии при ХЭ являются улучшение гемодинамики органов малого таза, стимуляция функции рецепторов, ускорение процессов регенерации эндометрия, повышение иммунологических свойств.
В литературе имеются данные о высокой эффективности использования экзогенного оксида азота в комплексном лечении хронического эндометрита. Доказано, что NO-терапия нормализует нарушенную микроциркуляцию, снижает микробную обсемененность, активирует фагоцитоз и функцию макрофагов, усиливает рост фибробластов, сосудов. Работой Н. Г. Грищенко доказана эффективность внутривлагалищного введения оксида азота с целью оптимизации подготовки пациенток с ранее безуспешными программами ЭКО на фоне «тонкого» эндометрия [17].
Кроме оксида азота в практической медицине нашло применение газовой смеси (СО2 и N2) в процессе подготовки «тонкого» эндометрия к программе ЭКО. Углекислый газ оказывает сосудорасширяющее действие, которое сопровождается усилением метаболизма и восстановлением рецепторной чувствительности. Азот — один из основных химических элементов биологически активных веществ, необходим для обеспечения дыхания и жизнедеятельности клеток. Методика предусматривает проведение трех орошений в течение первой фазы менструального цикла и демонстрирует положительный эффект в отношении роста эндометрия, достигающего приемлемой величины к моменту переноса эмбриона. Применение метода орошения газовой смесью в период одного менструального цикла у женщин с «тонким» эндометрием позволяет существенно увеличить толщину эндометрия. Данный способ можно рекомендовать для подготовки эндометрия к последующим переносам эмбрионов у пациенток с неуспешными попытками ЭКО, причиной которых было нарушение имплантации, обусловленное «тонким» эндометрием [18].
Зарубежные авторы отмечают высокую эффективность в лечении гипопластичного эндометрия внутриматочным введением гранулоцитарного колониестимулирующего фактора (Г-КСФ), препарата Филграстим [19–21]. Механизм его действия в отношении пролиферации и дифференцировки клеток эндометрия до конца не ясен. По имеющимся на сегодняшний день данным, Г-КСФ повышает концентрацию в эндометрии тромбоцитарного фактора роста эндотелиальных клеток, играющего ключевую роль в стимуляции ангиогенеза [22, 23]. Такая же положительная корреляция наблюдалась при изучении концентраций интегрина альфа-V/бета-3. Как известно, интегрины задействованы во всех стадиях имплантации, наибольшая концентрация интегрина альфа-V/бета-3 совпадает с максимальной рецепторной активностью эндометрия. Данный гликопротеин выделяется железистыми эпителиальными клетками после 19?го дня цикла при открытии окна имплантации. В нескольких работах было показано, что недостаток интегрина альфа-V/бета-3 характерен для женщин с тонким эндометрием и встречается также у пациенток, перенесших многочисленные безуспешные попытки ЭКО [24]. Внутриматочные перфузии Г-КСФ сопровождаются увеличением толщины эндометрия в течение 72 часов после применения, что определяет кратность его введения в первой фазе менструального цикла вплоть до овуляции [25–27].
Исследованиями М. Malinova и соавт. уставлен положительный эффект на рост эндометрия в циклах ЭКО у бесплодных женщин вагинального или орального приема вазодилятаторов типа силденафила цитрата совместно с кломифеном цитратом [28, 29].
С целью подготовки эндометрия к программе вспомогательных репродуктивных технологий (ВРТ) и преодоления проблемы недостаточной толщины и рецептивности эндометрия в клиниках мира используются разные методики лечения, такие как гистероскопия с адгезиолизисом, эстрогены, агонисты гонадотропин-релизинг-гормона, Аспирин, витамин Е, пентоксифиллин, L-аргинин, β-блокаторы типа атенолола, глюкокортикоиды и дигидроэпиандростендион [30, 31]. Крайне интересны работы последних лет, связанные с применением антагонистов рецепторов окситоцина, индол-3 карбинола и интерферона [32, 33].
Некоторыми авторами с целью увеличения толщины эндометрия при низком уровне сосудисто-эндотелиального фактора роста (СЭРФ) в сыворотке крови предложено в состав комплексной предгестационной подготовки вводить метилпреднизолон в дозировке 8 мг в сутки с 1?го по 25?й день менструального цикла, что ведет к увеличению уровня СЭРФ и соответственно толщины эндометрия [34].
В последние годы широко изучаются возможности клеточной терапии стволовыми клетками в регенеративной медицине. Одними из наиболее перспективных являются мезенхимальные стволовые клетки, происходящие из костного мозга, пуповинной крови, жировой ткани. Описан новый источник таких клеток — менструальная кровь. Среди преимуществ их использования: доступность, неинвазивный способ получения исходного материала, а также отсутствие иммунных реакций при аллогенном применении. Отсутствие спонтанной трансформации при длительном культивировании клеток — важный фактор, подтверждающий безопасность использования метода.
Мезенхимальные стволовые клетки секретируют ряд цитокинов (интерлейкины-6, 7, 8, 11, 12, 14, 15, 27, фактор, угнетающий лейкемию (leukemia inhibitory factor), фактор роста стволовых клеток (stem cell factor), макрофагальный колониестимулирующий фактор (macrophage colony stimulating factor)). Некоторые из них обеспечивают критическое взаимодействие «клетка–клетка», приводя к ускорению дифференцировки гемопоэтических стволовых клеток. По другим данным, мезенхимальные стволовые клетки in vitro синтезируют различные ростовые факторы, включая СЭРФ, интерлейкины-1 и 6, фактор некроза опухоли, а также гепатоцитарный фактор роста (hepatocyte growth factor), который индуцирует митогенную и антиапоптогенную активность в различных системах, ускоряет заживление ран. Мезенхимальные стволовые клетки обладают рецепторами эпидермального фактора роста (epidermal growth factor), инсулиноподобного фактора роста 1 (insulin-like growth factor 1) и др., иммуномодулирующими эффектами, индуцируют Т-регуляторные клетки, косвенно способствуя переключению Th1 клеточного иммунитета на Th2 гуморальный ответ. При этом описываются антибактериальные свойства мезенхимальных стволовых клеток, а их системное введение значительно уменьшает персистенцию хронической инфекции, снижает циркуляцию нейтрофилов по отношению к макрофагам.
Появляются работы, посвященные применению эндометриальных мезенхимальных стволовых клеток в лечении синдрома Ашермана. После их введения наблюдалась неоваскуляризация стенки матки, сопровождающаяся утолщением эндометрия, достаточным для успешной имплантации и вынашивания беременности. В случаях отсутствия ответа эндометрия на гормональную терапию внутриматочное введение мезенхимальных стволовых клеток в начале менструального цикла непосредственно после кюретажа может решить задачу роста эндометрия и в последующем способствовать наступлению беременности в программе ЭКО. Подобные публикации пока носят характер описания единичных случаев. Тем не менее следует признать высокий потенциал клеточных технологий в преодолении невосприимчивости тонкого эндометрия и связанных с ней бесплодия и невынашивания беременности.
Важным методом коррекции нарушения трофики является применение прямых метаболических активаторов, что приводит к усилению тканевого обмена, активации энергетических процессов в клетках, устранению последствий гипоксии в ткани, в том числе угнетению анаэробного гликолиза и стабилизации цикла Кребса в аэробных параметрах функционирования. С этой целью используются комплексные метаболические препараты, длительность приема которых должна составлять не менее 3–4 недель. Ярким представителем данной группы препаратов является депротеинизированный гемодериват крови телят.
Аутоплазменное лечение хронического эндометрита нашло широкое применение как в России, так и за рубежом. В нашей стране применяется парацервикальное введение аутоплазмы. Иностранные авторы сообщают об успешном лечении хронического эндометрита при внутриматочном введении PRP-плазмы (Platelet Rich Plasma) [35, 36].
Из нетрадиционных методов лечения хронического эндометрита применяют контрастный массаж, иглорефлексотерапию, йоготерапию. Кроме положительного воздействия последнего метода лечения на эндометрий авторы отмечают снижение депрессии и уровня стресса, что очень важно, так как сам по себе стресс способен провоцировать гемодинамические нарушения, способствовать поддержанию высокого уровня провоспалительных цитокинов в эндометрии [37, 38].
Дискуссионными остаются вопросы о целесообразности использования в комплексном лечении ХЭ циклической гормональной терапии. В настоящее время считается, что при ХЭ оправдано только дифференцированное назначение гормонотерапии при наличии гипофункции яичников или ановуляции [39]. Потенциал к патологической регенерации ткани, который таит в себе хроническое воспаление, при назначении циклической заместительной гормональной терапии может быть усилен и реализован [40]. Хотя некоторые авторы отмечают успешность лечения гипопластичного эндометрия циклическими гормональными препаратами [41–43].
В предполагаемом фертильном цикле, особенно при проведении стимуляции функции яичников, обосновано применение эстрогенных препаратов. При этом трансдермальные формы эстрогенов обладают рядом преимуществ перед оральным приемом эстрадиола ввиду высокой по сравнению с оральным приемом биодоступности, создания постоянной концентрации в кровотоке, отсутствия конверсии в неактивные метаболиты и возможности легкого варьирования дозы. Справедливости ради надо отметить, что препараты эстрадиола могут назначаться и на этапе подготовки к фертильному циклу в случаях, когда причиной тонкого эндометрия является овариальная недостаточность. Эстрогены назначаются по 21?дневной схеме, в течение последних десяти дней их сочетают с прогестинами (дидрогестерон 10–20 мг/сут, микронизированный прогестерон 200 мг/сут, раствор прогестерона 1% — 2 мл или 2,5% — 1 мл внутримышечно через день). Реакция эндометрия в индивидуальных случаях значительно отличается, поэтому возможность увеличивать или уменьшать дозу становится принципиальным фактором успеха подготовки эндометрия к фертильному циклу и обусловливает предпочтение в пользу трансдермальных форм эстрогенов [44–46].
Недостаточная эффективность гормональной терапии эстрогенами объясняется сниженной рецептивностью тонкого эндометрия и сохраняет актуальность поиска дополнительных путей увеличения его роста.
Задача улучшения ростовых функций эндометрия оказывается непростой для решения, так как экзогенные эстрогены усиливают пролиферативные процессы с одновременной активацией воспалительной реакции, что неблагоприятно для последующего наступления и течения беременности.
Альтернативные способы ускорения процессов созревания эндометрия активно изучаются, но универсального средства для решения этой задачи пока не найдено. Соблюдение принципа «пролиферация без воспаления» возможно при системном действии лекарственных средств, в состав которых входит набор цитокинов и факторов роста, обеспечивающих активацию Th2 клеточного иммунитета и рост слизистой оболочки матки. В этой связи представляет интерес использование гидролизата плаценты человека в виде раствора для внутривенных инъекций Лаеннека [47].
Критериями эффективности проведенной терапии являются: купирование клинических симптомов заболевания при их наличии, восстановление эхографической картины эндометрия, улучшение васкуляризации эндометрия при допплерометрии сосудов матки, элиминация или снижение активности инфекционного агента, восстановление морфологической структуры эндометрия, восстановление функционального состояния эндометрия, нормализация менструального цикла с полноценной лютеиновой фазой [48].
Проводится контрольная аспирационная биопсия эндометрия на 7–11 день менструального цикла не ранее чем через 2–3 мес после лечения с последующим морфологическим и бактериологическим исследованиями состояния эндометрия.
Хронический эндометрит является клинически значимой нозологической формой с позиций репродуктологии и требует обязательной диагностики и лечения у женщин с патологией репродуктивной системы, а также при использовании программ вспомогательных репродуктивных технологий. Комплексная этиопатогенетическая терапия хронического эндометрита позволяет восстановить нарушенный тканевый гомеостаз и рецептивность эндометрия, что приводит к восстановлению репродуктивной функции.
Литература
* ГУЗ УОКБ, Ульяновск
** ФГБОУ ВПО УлГУ, Ульяновск