Цитомегаловирус в чем опасность
Цитомегаловирус: что за инфекция и чем опасна?
Цитомегаловирус — вирус герпеса 5 типа.
Цитомегаловирусная (ЦМВ) инфекция, или цитомегалия — хроническое герпесвирусное заболевание человека с возможностью поражения практически всех органов и систем: ЖКТ, бронхо-легочной и мочеполовой систем.
До 80% всех людей на свете инфицированы ЦМВ, но у большинства с ним нет хлопот. Если только речь не идет об иммунодефицитах, беременности и внутриутробном развитии.
Чем же так коварен ЦМВ?
1. ЦМВ отличается высоким тропизмом (любовью) к клеткам слюнных желез и в локализованной форме находится только там.
2. Вирус способен поражать любые клетки практически всех внутренних органов.
3. ЦМВ — хроническая персистирующая инфекция человека. Однажды заразившись, человек инфицирован навсегда, но для здоровых это не опасно.
4. Развитие цитомегалии связано с потерей иммунного контроля над латентным состоянием ЦМВ.
5. Инкубационный период составляет от 20 до 60 дней.
6. Цитомегаловирус передается через близкий физический контакт человека с человеком. Это может происходить через жидкости организма:
Во время беременности заражение происходит через плаценту или непосредственно во время родов.
Инфицирование возможно при поцелуе или при контакте с предметами, на которых есть частички слюны или мочи больного человека.
Основная часть людей заражается в детстве, обычно в яслях или детском саду, т.е. там, где есть много контактов между детьми. Реже инфицирование происходит в возрасте 10-35 лет.
Выделяют следующие формы заболевания:
1. Приобретенная ЦМВ:
3. ЦМВ у ВИЧ-инфицированных и др. лиц с ослабленным иммунитетом.
Что же происходит когда мы инфицируемся ЦМВ?
Первая встреча с вирусом чаще всего протекает бессимптомно. Только в 2% случаев отмечают симптомы, похожие на ОРВИ (повышение температуры, боль в горле, в суставах и мышцах, увеличение лимфатических узлов). У людей с нормальным иммунитетом инфекция обычно не вызывает серьезных осложнений.
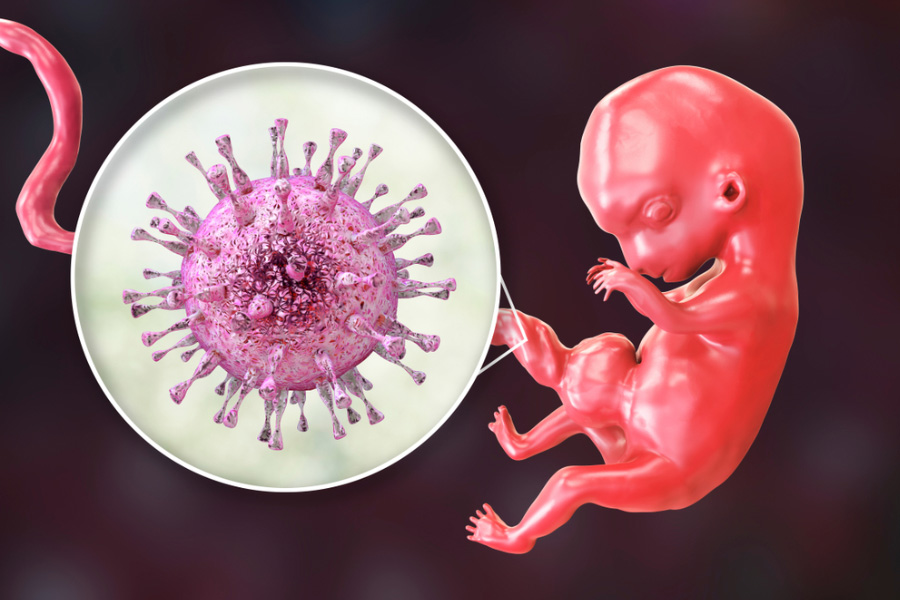
Гораздо опаснее врожденная ЦМВ. Чаще всего беременные женщины получают ЦМВ от больных детей младшего возраста. Различные врожденные патологии диагностируют у 10% детей, инфицированных во время внутриутробного развития. Вирус существенно увеличивает риск преждевременных родов, задержки внутриутробного развития, спонтанного прерывания беременности.
ЦМВ относят к группе так называемых TORCH-инфекций, чаще всего связываемых с аномалиями развития плода и патологией беременности. Заражение вирусом может произойти до беременности или непосредственно во время внутриутробного развития ребенка. В первом случае нет клинических проявлений, а в крови выявляются только специфические «поздние» антитела. Такая ситуация не опасна ни для плода, ни для женщины, риск осложнений не превышает 1%.
Первичное инфицирование матери во время беременности связано с большим риском для плода (30–50%).
В результате 10–15% детей могут иметь нарушения слуха или зрения, судороги, замедление внутриутробного развития, микроцефалию (уменьшение размера мозга). После рождения возможны неврологические симптомы, задержка умственного и физического развития, поражение печени, которое чаще всего проявляется желтухой, увеличение селезенки. ⠀ Вот такая вроде как «неопасная» инфекция.
Как же можно заподозрить, что у человек инфицирован ЦМВ?
Симптомы вирусных инфекций, если ты не врач, кажутся одинаковыми.
У здоровых людей заболевание может себя вообще ничем себя не проявлять и человек может даже не узнать, что заразился. Реже болезнь протекает в виде острой ЦМВ, по симптомам напоминающей инфекционный мононуклеоз:
Как правило, выздоровление наступает за 2 недели.
У больных с иммунодефицитом ЦМВ протекает более тяжело, так как вирус быстро распространяется по организму и вызывает:
Заподозрить инфекцию можно по общему анализу крови, где уровень лимфоцитов превышает 50% ( у взрослых) и 72% (у детей до 4,5 лет), и появляются атипичные лимфоциты (мононуклеары).
Точную диагностику ЦМВ проводят с помощью анализа:
ИФА позволяет определить антитела к ЦМВ в сыворотке крови. Оценивают наличие иммуноглобулинов — IgG и IgM.
Высокий уровень IgM в крови больного обычно свидетельствует о первичном инфицировании. При реактивации вируса количество IgM может расти.
Если определяют IgG, то встреча организма с ЦМВ уже не первая; эти антитела остаются на всю жизнь. Их количество может расти при активации вируса.
Расшифровка результатов анализов ведется врачом.
ПЦР определяет наличие специфических для ЦМВ участков ДНК в образцах слюны, грудного молока и т.д.
Как лечить цитомегаловирусную инфекцию?
Вопрос на самом деле сложный. Так как специфического лечения и профилактики ЦМВ-инфекции нет.
В тяжелых случаях применяется посиндромная терапия (в зависимости от вовлечения в инфекционный процесс внутренних органов).
Обоснованием включением в терапевтический комплекс противовирусных средств иммунного действия (интерферонов) является то, что клинические проявления инфекции обычно связаны с иммунодефицитными состояниями различной степени выраженности.
При ЦМВ инфекции всегда наблюдается сниженная выработка собственного интерферона. Учитывая, что ЦМВ является хроническим, персистирующим возбудителем, интерферонотерапия может быть рекомендована и в качестве профилактики обострений.
Но данную терапию назначает врач.
Профилактика ЦМВ
Специфическая профилактика ЦМВ инфекции отсутствует.
Эффективной и безопасной вакцины против ЦМВ пока не существует.
Вирус передается при половых контактах, поцелуях, совместном использовании столовых приборов, игрушек, зубных щеток. Поэтому соблюдение общих правил гигиены, мытье рук с мылом перед приготовлением еды, после похода в туалет или смены подгузника поможет предотвратить заражение. При контакте с биологическими жидкостями (спермой, мочой) необходимо использовать резиновые перчатки.
Уязвимым группам пациентов — например, принимающим иммунодепрессанты после пересадки органов или беременным — нужно более тщательно соблюдать гигиенические правила.
По возможности нужно избегать контакта с маленькими детьми (особенно до 5 лет) и тем более не целовать их, не есть с ними из одной посуды.
Чем опасен цитомегаловирус
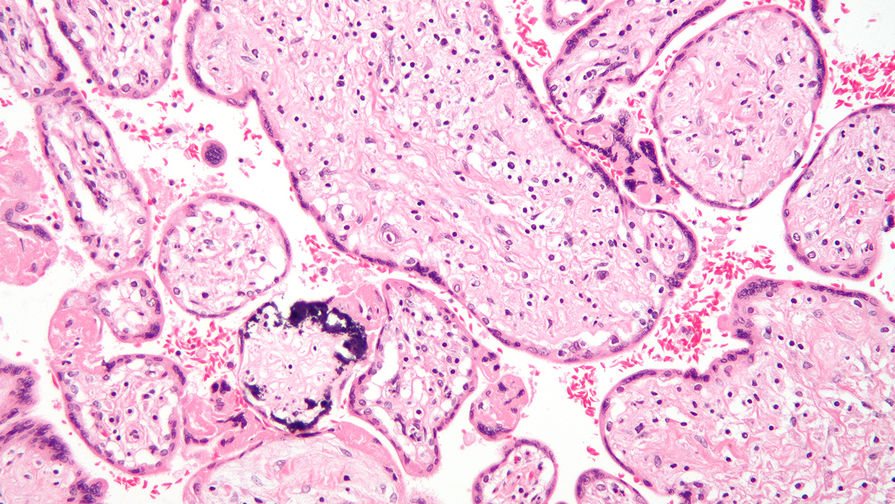
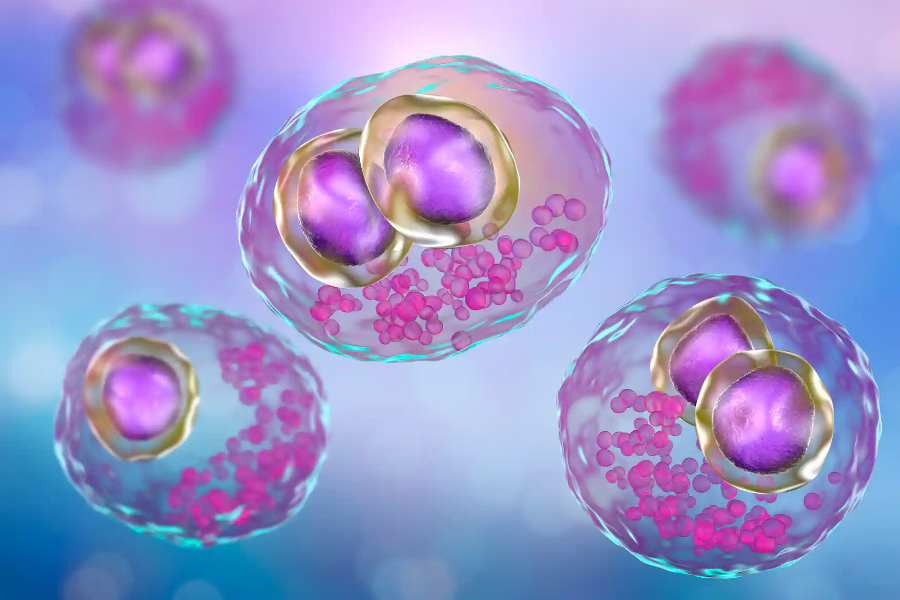
Цитомегаловирус (ЦМВ) — это двухцепочечный ДНК-вирус, представитель подсемейства бета-герпесвируса. Он известен человеку немногим более полусотни лет — его открыли в середине XX века. Однако еще до этого у мертворожденных младенцев были описаны клетки, похожие на «совиные глаза», — позже стало понятно, что они были заражены вирусом. Спустя 50 лет такие же клетки были обнаружены у пациентов, которым проводили трансплантации органов.
Цитомегаловирус — крупный вирус размером в 150–200 нм, что делает его одним из самых больших по размеру вирусов, известных современной науке. Его геном представлен двухцепочечной ДНК, содержащей информацию для производства более 230 белков.
После заражения вирусные белки начинают синтезироваться в клетке хозяина с вирусной ДНК — ЦМВ так распространяется и поддерживает свою жизнедеятельность.
Один из таких белков (ДНК-полимераза, необходимая для прохождения жизненного цикла вируса) играет роль мишени для использующихся сейчас противовирусных препаратов.
Встречаемость вируса высока везде. Однако этот показатель колеблется в зависимости от возраста, места проживания и социально-экономического статуса: зараженность выше в развивающихся странах и неблагополучных группах населения. Согласно результатам обследований, в среднем в США половина населения от 6 до 49 лет инфицирована ЦМВ. Среди 75–80-летних американцев носителями являются уже девять человек из десяти. В развивающихся же странах среди детей от одного года до пяти лет инфицирован примерно каждый пятый, а у пожилых людей этот показатель может достигать 90–100%.
Поскольку вирус может вызывать врожденные дефекты у детей, эти цифры заставляют специалистов бить тревогу.
Как же вирус так успешно распространяется? Оказывается, ЦМВ эволюционирует именно так, чтобы скрыться от нашей иммунной системы и дать о себе знать лишь в подходящий для него момент, рассказывает Рич Берри, один из авторов исследования по этой теме, опубликованного в журнале Cell. «Однако еще не все потеряно, — продолжает доктор Берри, — иммунная система тоже не бездействует, она тоже эволюционирует и перестраивается так, как это необходимо для продолжения выживания нашего вида». Таким образом, возникла эволюционная «гонка вооружений» между вирусом и иммунной системой человека, и пока что вирус, кажется, идет впереди.
Кто в группе риска?
Судя по статистике, в группу риска заражения попадает практически любой. Однако серьезные осложнения от вируса грозят в основном людям с пониженной функцией иммунитета: например, пациентам с трансплантированными органами, со СПИДом или новорожденным. Особенно восприимчивы к инфицированию недоношенные дети с низким весом, поскольку их иммунные системы еще не до конца сформированы. Более того, ученые выяснили, что уязвимость для вируса могут повысить некоторые генетические мутации.
Вирус может передаться через выделения из организма инфицированных больных: через слюну, слезы, мочу, фекалии, грудное молоко, сперму и т.д.
Также заразиться можно при переливании крови либо трансплантации органов. Кроме того, на некоторых поверхностях ЦМВ остается жизнеспособным до шести часов, и поэтому изредка можно заразиться и через контакт с предметами.
После первичного попадания ЦМВ остается в организме носителя на всю жизнь. Проявления его присутствия обычно зависят от состояния иммунной системы. «ЦМВ не похож на вирус гриппа, который наша иммунная система может успешно вычистить из наших органов, — комментирует Питер А. Барри, профессор из школы медицины Калифорнийского университета в Дэвисе. — Как только вы заразились, это уже навсегда».
У здоровых людей симптомов заражения часто нет, и вирус не дает о себе знать. Однако вирус может реактивироваться, и тогда болезнь может проявлять себя в осложнениях различной степени тяжести, от неспецифической фебрильной лихорадки до даже смертельного исхода.
Более того, некоторые ученые считают, что на самом деле вирус сильно недооценен и связан с гораздо большим количеством осложнений, чем можно найти в стандартном описании для врачей.
Клиническую диагностику ЦМВ можно за короткие сроки провести в лаборатории, причем методов обнаружения вируса множество. Диагностика вируса улучшилась и у беременных женщин, хотя, согласно самым последним исследованиям, стандартный тест выявляет отнюдь не все случаи заражения. Одобренного лечения для будущих матерей сейчас нет. Новорожденным с умеренным проявлением симптомов заражения обычно прописывают валганцикловир. Здоровые люди, зараженные ЦМВ, чаще всего не нуждаются в лечении. Лечение обычно назначают пациентам с ослабленной иммунной системой.
ЦМВ и беременность
Как отмечает Эми Армстронг-Хеймсот из Университета Северной Аризоны, лишь 13% женщин слышали об этом вирусе. Про то, что его передача от матери ребенку может обернуться трагедией, исследовательница узнала от коллеги с недиагностированным ЦМВ.
«У ее сына теперь церебральный паралич и потеряны слух и зрение», — рассказывает она.
Особое внимание направлено на женщин и с ВИЧ, и с ЦМВ, поскольку при таком двойном вирусном заражении риск инфицирования младенца вырастает в разы. Согласно исследованиями, ВИЧ-инфицированные женщины с ЦМВ в моче при родах в пять раз чаще передают ВИЧ младенцам, чем женщины с ВИЧ, но без ЦМВ. Также они в 30 раз чаще заражают новорожденных ЦМВ.
Лучшим методом борьбы с вирусом в перспективе специалисты называют вовсе не лекарства, а вакцины. Они помогут контролировать вирус на уровне популяции — с помощью всеобщей иммунизации. В первую очередь такая стратегия была бы направлена на женщин детородного возраста для предотвращения заражения плода. Однако, конечно, они необходимы и для пациентов с трансплантированными органами и гематопоэтическими стволовыми клетками.
Хотя вакцины пока нет, у исследователей, по-видимому, уже есть достаточное количество фундаментальных знаний для ее создания.
Разработок с различными стратегиями сейчас много — занимаются ими даже такие гиганты фармбизнеса, как Merck и GSK.
Удивительно, как борьба с цитомегаловирусом еще не стала одним из приоритетов международных здравоохранительных учреждений. Разработки вакцин можно было бы ускорить привлечением общественного внимания к этой проблеме и обращением к политическим и экономическим организациям за помощью. Остается надеяться, что многочисленные разработки ученых по созданию эффективной и безопасной вакцины уже близки к успеху — ведь они избавят многие семьи от бремени последствий заражения вирусом и спасут множество жизней.
Цитомегаловирус
Цитомегаловирус — возбудитель инфекционной патологии цитомегалии. Основной признак заболевания — так называемая «упорная простуда» — постоянная заложенность носа, сопровождающаяся головными и суставными болями, общей слабостью, увеличением слюнных желёз, обильным слюноотделением.
Общие сведения
Заболевание, развивающееся после инфицирования человека цитомегаловирусом, обладает различными названиями. В медицинских справочниках можно найти описание цитамегаловирусной инфекции, инклюзивной цитомегалии, вирусной болезни слюнных желёз и т. д. Перечисленные термины характеризуют одно патологическое состояние, диагностируемое у детей и взрослых.
Многие пациенты входят в число носителей цитомегаловируса, но не знают об этом. Антитела к соответствующему патогену присутствуют в крови 15% подростков и 55–60% взрослых. Бессимптомное течение цитомегалии отмечается у 80% носителей возбудителя.
Причины проявления цитомегаловируса
Цитомегаловирус относится к семейству герпесвирусов. Клетки, поражённые этим патогеном, начинают интенсивно расти. Передача инфекции от носителя к здоровому человеку осуществляется при длительных телесных контактах. Основные пути передачи возбудителя:
Цитомегаловирус может находиться в организме десятилетиями. Проявление симптомов заболевания происходит при ослаблении иммунитета. В группу риска входят лица, принимающие иммунодепрессанты после трансплантации костного мозга или внутренних органов. Наибольшую опасность для пациентов представляет врождённая цитомегалия, которая может стать причиной гибели наворожённого.
Симптоматика патологии
Признаки патологии специфичны и зависят от способа инфицирования ребёнка или взрослого. Так, врождённая цитомегалия не проявляется у 95% новорождённых. Оставшиеся 5% младенцев могут столкнуться со следующими симптомами патологии:
Около 20% случаев внутриутробного инфицирования плода цитомегаловирусом заканчиваются летальным исходом. Выжившие пациенты страдают от задержки умственного развития, необратимых повреждений органов зрения и слуха.
Пациенты, родившиеся неинфицированными, могут заразиться цитомегалией от родственников в первые месяцы жизги. Дети и взрослые, обладающие нормальным иммунитетом, часто страдают от мононуклеозоподобного синдрома. Это состояние развивается под действием цитомегаловируса, а клиническая картина напоминает патологии, вызываемые вирусом Эпштейна-Барр. Пациенты жалуются на следующие проявления цитомегалии:
В редких случаях течение цитомегалии осложняется желтухой, основным признаком которой становится увеличение концентрации печёночных ферментов в крови. В 6% случаев цитомегаловирус приводит к развитию пневмонии, протекающей без клинических проявлений.
Диагностика заболевания
Постановка диагноза осуществляется педиатром, терапевтом или инфекционистом. Необходимо сдать кровь на наличие антител к возбудителю цитомегалии. Тип обнаруженного иммуноглобулина укажет на присутствие цитомегаловируса, но не позволит оценить текущую стадию инфекционного процесса.
ПЦР-тесты направлены на установление пределов активности патогена. В качестве биоматериалов могут выступать соскобы из уретры или цервикального канала, мокрота, слюна и другие жидкости. Полимеразная цепная реакция даёт врачам возможность выявить причины активности цитомегаловируса и разработать тактику лечения инфицированного лица.
Пациентам могут потребоваться дополнительные консультации специалистов, занимающихся лечением патологий, поражённых цитомегалией органов. Мужчинам и женщинам репродуктивного возраста необходимы консультации урологов и гинекологов. В качестве вспомогательных диагностических мер выступают ультразвуковая диагностика, магнитно-резонансная томография, гастроскопия и т. д.
Лечение цитомегаловируса
Неосложненное течение цитомегалии не требует специфической терапии. Лечение направлено на устранение симптомов простуды и интоксикации. Пациенту назначаются жаропонижающие, антигистаминные, сосудосуживающие препараты и обильное питьё.
Осложнённая цитомегалия лечится с помощью противовирусных препаратов на основе ганцикловира. Раствор вливается внутривенно, поскольку таблетированная форма состава не позволяет доставить в организм достаточное количество действующего вещества.
Прогноз
При неосложнённом течении заболевания полное купирование симптомов наступает через 7–10 дней после начала лечения. У беременных женщин цитомегалия может стать причиной самопроизвольного аборта или мертворождения. По этой причине пациенткам репродуктивного возраста, планирующим зачатие ребёнка, необходимо сдавать анализы для выявления цитомегаловируса и прохождения последующего лечения.
Вопросы и ответы
Источники
При подготовке статьи использованы следующие материалы:
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
История
Исходя из теории ко-эволюции вирусов с их хозяевами, считается, что герпетические вирусы появились в кембрийский период. В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
Характеристика возбудителя
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Патогенез
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Клиника ЦМВИ
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
У новорожденного антенатальная ЦМВИ проявляется симптомами «тяжелой инфекции» с полисистемным поражением: задержкой внутриутробного развития, часто — недоношенностью, гепатоспленомегалией, затяжной неконъюгационной и конъюгационной желтухой, тромбоцитопенической пурпурой, анемией, ДВС-синдромом с кровоизлиянием во внутренние органы, прежде всего в мозг, пневмонией, микроцефалией, хориоретинитом, увеитом, кардитом, различными вариантами поражения центральной нервной системы, в том числе продуктивным вентрикулоэнцефалитом с прогрессирующей гидроцефалией, а также — кортикальными или мозжечковыми пороками развития [13]. В дальнейшем этим детям присущи недостаточная прибавка веса, задержки психического и моторного развития, мышечная слабость, часто — длительная субфебрильная температура, стойкая анемия и тромбоцитопения, длительный гепатит с холестатическим синдромом и высоким риском фиброза и цирроза печени, мальабсорбция.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование