Цитотоксичность что это такое
цитотоксичность
Смотреть что такое «цитотоксичность» в других словарях:
цитотоксичность — Свойство химических веществ или иммунных агентов быть токсичными для клеток [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN cytotoxicity … Справочник технического переводчика
цитотоксичность — rus цитотоксичность (ж), цитотоксическое действие (с) eng cytotoxicity, cytotoxic action, cytotoxic effect fra cytotoxicité (f), action (f) cytopathogène, action (f) cytotoxique deu zellschädigende Wirkung (f), zytopathogene Wirkung (f),… … Безопасность и гигиена труда. Перевод на английский, французский, немецкий, испанский языки
цитотоксичность Т-киллеров — Клетки иммунной системы [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN cytotoxic killer lymphocyte … Справочник технического переводчика
Аллергия — I Аллергия (allergia; греч. allos другой + ergon действие) повышенная чувствительность организма к воздействию некоторых факторов окружающей среды (химических веществ, микроорганизмов и продуктов их жизнедеятельности, пищевых продуктов и др.),… … Медицинская энциклопедия
10993.5 — ГОСТ Р ИСО 10993.5 < 99>Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследование на цитотоксичность: методы in vitro. ОКС: 11.020 КГС: Р20 Классификация, номенклатура и общие нормы Действие: С 01.01.2002… … Справочник ГОСТов
Мабтера — Действующее вещество ›› Ритуксимаб* (Rituximab*) Латинское название Mabthera АТХ: ›› L03AX06 Моноклональные антитела 17 1а Фармакологические группы: Иммунодепрессанты ›› Противоопухолевые средства — моноклональные антитела Нозологическая… … Словарь медицинских препаратов
ГОСТ Р 53485-2009: Материалы текстильные. Метод определения токсичности — Терминология ГОСТ Р 53485 2009: Материалы текстильные. Метод определения токсичности оригинал документа: индекс токсичности : Величина, характеризующая степень цитотоксического действия. Определения термина из разных документов: индекс… … Словарь-справочник терминов нормативно-технической документации
Медиа́торы — (лат. mediator посредник: синоним нейромедиаторы) биологически активные вещества, секретируемые нервными окончаниями и обусловливающие передачу нервных импульсов в синапсах. В качестве М. могут выступать самые различные вещества. Всего… … Медицинская энциклопедия
Алка-Зельтцер — Действующее вещество ›› Ацетилсалициловая кислота + (Лимонная кислота + Натрия гидрокарбонат) (Acetylsalicylic acid + [Citric acid + Sodium hydrocarbonate]) Латинское название Alka Seltzer АТХ: ›› N02BA51 Ацетилсалициловая кислота в комбинации с… … Словарь медицинских препаратов
Цитотоксичность что это такое
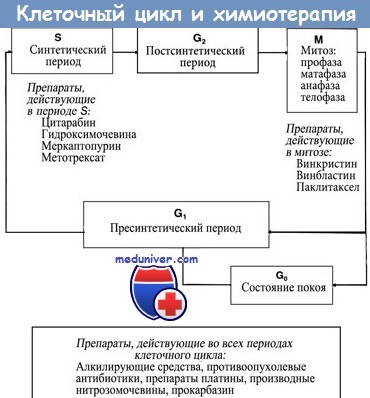
Цитотоксические вещества блокируют клеточный цикл. Все цитотоксические противоопухолевые лекарства препятствуют прохождению клетками клеточного цикла, приводя к синхронизации и замедлению пролиферации быстро размножающихся клеток. Результатом является снижение чувствительности к лекарствам в S-фазе.
Цитотоксичность пропорциональна общей лекарственной экспозиции. Фармакокинетика противоопухолевых лекарств — это сложный процесс, т.к. цитотоксичность для злокачественных клеток пропорциональна общей лекарственной экспозиции (площадь под кривой; ППК), а не концентрации препарата в плазме на пике. Сначала вещество должно проникнуть в отдельные злокачественные клетки, а затем взаимодействовать со своими молекулярными мишенями. Поскольку это взаимодействие часто обратимо, по крайней мере сначала, цитотоксическая концентрация должна сохраняться все это время.
Кроме того, число индивидуальных взаимодействий между лекарством и молекулами-мишенями, необходимое для киллинга одиночной клетки, может быть очень велико. Подсчитано, что для киллинга одной клетки с ее ДНК должен связаться как минимум 1 млн молекул цисплатина.
Комбинации противоопухолевых препаратов стали применять после того, как было обнаружено, что использование одного препарата не дает значительной ремиссии или не излечивает пациента (за исключением метотрексата при лечении хориокарциномы). Это явление объясняет гипотеза log-киллинга.
Лекарства, используемые для комбинированной терапии, должны обладать определенными свойствами:
• оказывать некоторый эффект при использовании в отдельности;
• вызывать преимущественно полный ответ (гибель всех клеток опухоли), а не частичный (гибель менее 50% клеток);
• биохимические механизмы действия препаратов должны быть разными для воздействия на опухоль, содержащую гетерогенную клеточную популяцию;
• препараты не должны обладать сходным побочным действием, т.к. в этом случае необходимо снижать их дозы, что приводит к утрате аддитивного эффекта комбинации.
По многим показателям различные опухоли являются гетерогенными, включая чувствительность к лекарственным веществам, в результате нестабильности их генетической конституции. Злокачественные клетки способны мутировать, что крайне важно для терапии, поскольку такие мутации могут привести к возникновению резистентности к лекарствам. В большинстве случаев такая резистентность определяется свойствами конкретного типа опухолей.
Клинически резистентность может стать очевидной, когда чувствительные клоны опухоли погибают, а резистентные выживают и становятся доминирующими. Излечимость пропорциональна числу злокачественных клеток, и, в соответствии с гипотезой Голди-Колдмана, существует более высокая вероятность мутации, приводящих к лекарственной резистентности, в более многочисленной клеточной популяции.
ЦИТОТОКСИНЫ
Цитотоксины (греческий kytos вместилище, здесь — клетка + токсины) — антитела, вызывающие повреждение клеток. Иногда в качестве синонима понятия «цитотоксины» употребляют термин «цитолизины», который имеет более широкое значение, так как применим к любым веществам, способным растворять клеточные элементы. Антитела, разрушающие эритроциты, обычно называют гемолизинами (см. Гемолиз), разрушающие лейкоциты — лейколизинами, инактивирующие сперматозоиды—сперматолизинами. К цитотоксинам относят также бактериолизины — антитела к бактериальным антигенам, способные в присутствии комплемента вызывать бактериолиз (см.).
Цитотоксины образуются при иммунизации животного антигенами клеточного происхождения, которые могут принадлежать к тканям животного другого вида (гетероцитотоксины), того же вида, но другой генетической линии (гомоцитотоксины), к тканям животного той же линии, что и иммунизируемое (изоцитотоксины), и к собственным тканям иммунизируемого животного (аутоцитотоксины). Чем больше антигены донора отличаются от антигенов реципиента, тем легче образуются антитела. Поэтому на практике цитотоксины получают, иммунизируя животное клеточной взвесью или антигенным материалом органов животного другого вида. Полученные при этом иммунные сыворотки содержат разные типы антицеллюлярных антител (антицеллюлярные сыворотки) или антиорганных антител (антиорганные сыворотки), как способствующих, так и не способствующих возникновению цитотоксического действия. В связи с этим термины «антицеллюлярная сыворотка» и «антиорганная сыворотка» являются более широкими, чем термин «цитотоксическая сыворотка», применяемый к тем сывороткам, цитотоксическое действие которых подтверждено.
Установлено, что при аллотрансплантации тканей в крови реципиента появляются гомоцитотоксины, которые, очевидно, играют определенную роль в механизме отторжения аллотрансплантата. При изотрансплантации, вероятно, образуется незначительное количество цитотоксинов, их значение в механизме отторжения трансплантата несущественно, и изотрансплантаты, как правило, приживают (см. Трансплантация).
В 1898 году Ж. Борде в лаборатории И. И. Мечникова показал, что иммунизация гетерогенными эритроцитами сопровождается образованием специфических антител — гемолизинов. Этим была доказана возможность получения антител не только против микроорганизмов, но и против клеточных элементов макроорганизма, что легло в основу учения о цитотоксинах. В 1900 году, иммунизируя морских свинок тканями кроличьего семенника, И. И. Мечников получил спермоцитотоксическую сыворотку, обездвиживающую сперматозоиды морской свинки. И. И. Мечников и А. М. Безредка изготовили лейкотоксическую и гемолитическую сыворотки. Лейкотоксическая сыворотка была получена при иммунизации морской свинки клетками лимфоидных органов кролика, гемолитическая сыворотка — при иммунизации эритроцитами. Обе сыворотки проявляли специфическое действие, избирательно направленное в первом случае на лейкоциты (иммобилизация и распад их), во втором — на эритроциты (гемолиз). Введение этих сывороток в больших дозах снижало соответственно число лейкоцитов и эритроцитов, инъекции малых доз, наоборот, приводили к увеличению их числа в крови. Таким образом, в лаборатории Мечникова было не только заложено учение о цитотоксинах, но и показано принципиальное различие в действии больших и малых доз цитотоксических сывороток: большие дозы проявляли токсическое действие, малые дозы действовали как активаторы.
После И. И. Мечникова спермоцитотоксины были получены С. И. Метальниковым (1900), Е. С. Лондоном (1901), М. П. Тушновым (1911) и др. В дальнейшем рядом исследователей были получены тестикулоцитотоксины, овариоцитотоксины и плацентоцитотоксины, применение которых в больших дозах приводило к дистрофическим процессам соответственно в семенниках, яичниках и плаценте. Были получены гепатоцитотоксины, вызывавшие в печени жировую дистрофию, развитие цирроза и некротические изменения; нефроцитотоксины, при введении которых развивались тяжелые изменения в почках. Вводимые в больших дозах нейротоксины вызывали тяжелые поражения головного мозга и периферических нервов. Аналогичные изменения в тканях глаза возникали под влиянием офтальмоцитотоксинов, приготовленных С. С. Головиным (1904) и др. Были получены цитотоксины, действующие на ткани сердца, желудка, селезенки, кожи, желез внутренней секреции и других органов.
В 1909 году А. А. Богомолец доказал возможность стимуляции функции надпочечников малыми дозами супрареноцитотоксинов. С помощью морфологических и физиологических методов исследования он установил, что введение кошке малых доз супрареноцитотоксической сыворотки вызывает повышение АД, учащение пульса и дыхания. Микроскопические изменения в надпочечниках свидетельствовали об усилении под влиянием цитотоксинов их гормональной активности. Эту работу А. А. Богомольца следует считать началом физиологического периода в изучении цитотоксинов в отличие от предшествовавшего, преимущественно морфологического. В 1925 году Л. А. Варшамовым и И. А. Леонтьевым в лаборатории А. А. Богомольца была впервые получена цитотоксическая сыворотка к активным элементам соединительной ткани, названная А. А. Богомольцем антиретикулярной цитотоксической сывороткой (см.).
В. К. Линдеман, H. Н. Нефедьев и П. А. Герцен показали, что при повреждении одной из почек в организме подопытного животного возникают аутоцитотоксины, оказывающие повреждающее действие на здоровую почку. Аутоцитотоксины в большем или меньшем количестве продуцируются при распаде любой ткани в организме в результате заболевания или экзогенного повреждения (лучевое воздействие, ожог и др.); при этом в кровь больного поступают аутоантигены. Аутоиммунизация, приводящая к возникновению аутоцитотоксинов (аутоантител), играет существенную роль в механизме дальнейшего развития патологического процесса. При воспалительных, дистрофических и других заболеваниях щитовидной железы установлено наличие в крови аутотиреоцитотоксинов.
Цитотоксины получают так же, как и другие высокоактивные и специфические препараты антител. Специфичность цитотоксинов достигается иммунизацией животных органоспецифическими очищенными антигенами или тщательной адсорбцией иммунной сыворотки органоспецифическими антигенами, присутствовавшими в использованном для иммунизации материале. Проблема получения узкоспецифических цитотоксинов, как и других высокоспецифических антител, решается в настоящее время на основе гибридомной техники (см. Гибридома), позволяющей получать моноклональные антитела.
Степень нарушения функции органа зависит от дозы, биологической активности цитотоксина и функциональной лабильности клеточного субстрата. Часть клеток гибнет под действием цитотоксинов у сохранившихся клеток нарушается функция.
Механизм действия малых доз цитотоксинов, стимулирующих функцию органа сложнее. В связи с образованием на мембране клетки комплекса антиген — антитело функция соответствующих клеток органа нарушается, часть тканевых элементов, очевидно, наименее стойких, погибает, но одновременно идет процесс восстановления, сопровождающийся выраженной функциональной активизацией органа. Такое объяснение действия малых доз цитотоксинов, в частности антиретикулярной цитотоксической сыворотки, дал А. А. Богомолец. В настоящее время оно является общепринятым.
Механизм действия цитотоксинов заключается в активации системы комплемента (см.) образующимся комплексом антиген—антитело (см. Антиген— антитело реакция). Цитотоксическим действием обладают антитела, принадлежащие к иммуноглобулинам (см.), с выраженной комплемент связывающей способностью. Цитотоксины принадлежат преимущественно к иммуноглобулину класса G. Изменение пространственной структуры молекулы антитела в результате связывания с антигеном приводит к обнажению на антителе участков, связывающих комплемент. Этапы последовательной активации компонентов комплемента, ведущие к цитолизу, наиболее полно изучены на эритроцитах на примере иммунного гемолиза (см.) и подтверждены на других клетках. Разрушение клеточных мембран при действии цитотоксинов и комплемента установлено с помощью электронной микроскопии. Повреждения, возникающие в мембранах эритроцитов, представляют собой круглые отверстия диаметром 8—10 нм. В ядросодержащих клетках происходит инвагинация клеточных мембран, набухание митохондрий и мембран эндоплазматической) ретикулума. Повышение проницаемости клеточной мембраны проявляется потерей внутриклеточных ионов калия, аминокислот и рибонуклеотидов. Клетки набухают, и в результате осмотического лизиса из них высвобождаются белки и нуклеиновые кислоты. Собственно лизис клеточной мембраны осуществляется на последнем этапе активации системы комплемента декамолекулярным комплексом с вовлечением компонентов комплемента C5 — C9. Декамолекулярный комплекс (по одной молекуле С5, С6, С7, С8 и 6 молекул С9) имеет молекулярный вес (массу) около 995 000. Возможно, что повреждение возникает в результате взаимодействий этого комплекса с липидами клеточной мембраны. Морфологические признаки повреждения клеточной мембраны становятся заметными после фиксации С5 вследствие детергентного действия активированной формы этого компонента (C5), который проявляет резко выраженные гидрофобные свойства по отношению к фосфолипидам мембраны. Взаимодействие других компонентов комплемента усиливает детергентное действие С5, что приводит к расплавлению участков клеточной мембраны.
Цитотоксины применяют в экспериментальных исследованиях для изучения функции отдельных органов и систем. Методы цитотоксической стимуляции и цитотоксического подавления функции различных органов и физиологических систем вошли в арсенал патофизиологических методов. Аналогичное действие цитотоксины оказывают in vitro при добавлении их в питательную среду. Так, малые дозы цитотоксинов усиливают пролиферацию соответствующих клеточных элементов, большие дозы подавляют размножение клеток.
Цитотоксины, специфичные к поверхностным антигенам определенных клеток, применяют для идентификации этих клеток в цитотоксическом тесте in vitro в присутствии комплемента. Примером может служить использование иммунных сывороток и моноклональных антител для идентификации популяций и субпопуляций лимфоидных клеток.
В клинической практике применяют в малых дозах антиретикулярную цитотоксическую сыворотку с целью повышения защитных функций организма при инфекционных и опухолевых процессах. Для усиления эритроцитопоэза, лейкоцитопоэза или тромбоцитопоэза вводят цитотоксические сыворотки, полученные при иммунизации животного соответственно эритроцитами, лейкоцитами или тромбоцитами. Для ускорения восстановления нормального состава крови у доноров, а также при гипорегенераторной анемии (см.) используют миелоцитотоксическую сыворотку.
Оценка цитотоксичности in vitro как критерий рационального выбора слезозаместительных препаратов
Полный текст:
Аннотация
Цель: сравнительный анализ цитотоксического действия широкой линейки препаратов слезозаместительной терапии в отношении эпителиальных клеток роговицы в условиях in vitro.
Материалы и методы. Объектом исследования явились 11 препаратов «искусственных слез» с различными системами консервантов и 9 бесконсервантных слезозаместителей. В качестве тест-систем были использованы клетки постоянной трансформированной клеточной линии эпителия роговицы (HCEC) человека. Цитотоксичность «искусственных слез» оценивали по жизнеспособности клеток, культивируемых в питательной среде, содержащей в своем составе исследуемые препараты.
Результаты. Наиболее токсичными в отношении клеток эпителия роговицы из слезозаместителей, содержащих консерванты, оказались Лакрисифи, Слезин, Гипромелоза- П и Офтолик®. Близкими к ним по токсичности были Катионорм®, Артелак® Баланс и Оптив®. Глазные капли Стиллавит, Систейн®Ультра и Блинк®контактс проявили умеренную токсичность. Визмед® Лайт из группы слезозаместителей с консервантами не оказывал цитотоксического действия на клетки в условиях in vitro, так же как и бесконсервантные слезозаместители Хилабак®, Теалоз®, Теалоз Дуо® и Эво Тиарс™. Цитотоксический эффект в отношении клеток эпителия роговицы выявлен у препаратов Хилозар-Комод® и Хило®Фреш, несмотря на отсутствие в их составе консерванта.
Заключение. Проведенное исследование показало принципиальную возможность использования систем in vitro для сравнительной оценки цитотоксического действия препаратов в целях рационального выбора слезозаместителей.
Ключевые слова
Об авторах
Тихорецкий пр., 4, Санкт-Петербург, 194064, Российская Федерация
младший научный сотрудник отдела клеточных культур, лаборатория биологии клетки в культуре, группа клеточной биотехнологии
ул. Я. Гашека, 21, Санкт-Петербург, 192283, Российская Федерация
кандидат медицинских наук, заведующий клинико-бактериологической лабораторией
Тихорецкий пр., 4, Санкт-Петербург, 194064, Российская Федерация
лаборант-исследователь, отдел клеточных культур, лаборатория биологии клетки в культуре, группа клеточной биотехнологии
ул. Я. Гашека, 21, Санкт-Петербург, 192283, Российская Федерация
доктор медицинских наук, профессор, зам. директора по научной работе
Тихорецкий пр., 4, Санкт-Петербург, 194064, Российская Федерация
кандидат биологических наук, ведущий научный сотрудник отдела клеточных культур, лаборатория биологии клетки в культуре, группа клеточной биотехнологии
Список литературы
1. Baudouin C., Labbe A., Liang H., Pauly A., Brignole-Baudouin F. Preservatives in eye drops: the good, the bad and the ugly. Prog Retin Eye Res. 2010;9:312–34. DOI: 10.1016/j.preteyeres.2010.03.001
2. Whitson J., Petroll W. Corneal epithelial cell viability following exposure to ophthalmic solutions containing preservatives and/or antihypertensive agents. Adv Ther. 2012;29:874–88. DOI: 10.1007/s12325-012-0057-1
3. Tu E. Balancing antimicrobial efficacy and toxicity of currently available topical ophthalmic preservatives. Saudi J Ophthalmol. 2014;28(3):182–7. DOI: 10.1016/j.sjopt.2014.06.006
4. Elder D., Crowley P. Antimicrobial Preservatives Part One: Choosing a Preservative System. American Pharmaceutical Review. 2012, available from http://www.americanpharmaceuticalreview.com/Featured-Articles/38886-Antimicrobial-Preservatives-Part-One-Choosing-a-Preservative-System/
5. Freeman P., Kahook M. Preservatives in Topical Ophthalmic Medications: Historical and Clinical Perspectives. Expert Review of Ophthalmology 2009;4(1):59–64.
6. Ammar D., Noecker R., Kahook M.. Effects of benzalkonium chloride-preserved, polyquad- preserved, and sofZia-preserved topical glaucoma medications on human ocular epithelial cells. Adv Ther. 2010 Nov; 27(11):837–45. DOI: 10.1007/s12325-010-0070-1.
7. Schiffman R., Christianson M., Jacobsen G., Hirsch J., Reis B. Reliability and validity of the ocular surface disease index. Arch Ophthalmol. 2000;118:615–21.
8. Management and therapy of dry eye disease: report of the Management and Therapy Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf. 2007 Apr;5(2):163–78.
9. Данченко Е.О. Оценка цитотоксичности фармацевтических субстанций с использованием клеточных культур. Иммунология, аллергология, инфектология. 2012;2:22–31. [Danchenko E.O. Evaluation of cytotoxicity of pharmaceutical substances using cell cultures. Immunopathology, allergology, infectology=Immunopatologija, Allergologija, Infektologija. 2012;2:22–31. (In Russ.)]
10. Еропкин М.Ю., Еропкина Е.М. Клеточные культуры как модельная система исследования токсичности и скрининга цитопротекторных препаратов. Санкт-Петербург: Морсар, 2003. [Eropkin M.Ju., Eropkina E.M. The cell cultures as a model system toxicity studies and screening of cytoprotective drugs. St. Petersburg: Morsar AV, 2003. (In Russ.)]
11. Аникина Л.В., Пухов С.А., Дубровская Е.С., Афанасьева С.В., Клочков С.Г. Сравнительное определение жизнеспособности клеток с помощью МТТ и ресазурина. Фундаментальные исследования. 2014;12:1423–1427. [Anikina L.V., Puhov S.A., Dubrovskaja E.S., Afanas’eva S.V., Klochkov S.G. Comparative determination of cell viability using the MTT and Resazurin. Fundamental research=Fundamental’nye issledovaniya. 2014;12:1423–1427. (In Russ.)]
12. Urcan E., Haertel U., Styllou M., Hickel R., Scherthan H., Reichl F. Real-time xCELLigence impedance analysis of the cytotoxicity of dental composite components on human gingival fibroblasts. Dent Mater. 2010;26:1:51–8. DOI: 10.1016/j.dental.2009.08.007
13. Александрова О.И., Околов И.Н., Тахтаев Ю.В., Хорольская Ю.И., Хинтуба Т.С., Блинова М.И. Сравнительная оценка цитотоксичности антимикробных глазных капель. Офтальмологические ведомости. 2015;8(1):89–97. [Aleksandrova O.I., Okolov I.N., Tahtaev Ju.V., Horol’skaja Ju.I., Hintuba T.S., Blinova M.I. Competitive evaluation of cytotoxicity of antibacterial eye drops. Sravnitel’naja ocenka citotoksichnosti antimikrobnyh glaznyh kapel’. Oftal’mologicheskie vedomosti. 2015;8(1):89–97. (In Russ.)]
14. Александрова О.И., Хорольская Ю.И., Майчук Д.Ю., Блинова М.И. Исследование общей цитотоксичности антибиотиков аминогликозидного и фторхинолонового ряда на клеточных культурах. Вестник офтальмологии. 2015;5:39–48. [Aleksandrova O.I., Horol’skaja Ju.I., Majchuk D.Ju., Blinova M.I. Study of the general cytotoxicity of antibiotics of aminoglycoside fluoroquinolone groups on cell cultures. Annals of Ophthalmology=Vestnik oftal’mologii 2015;5:39– 48. (In Russ.)] DOI: 10.17116/oftalma2015131543-53
15. Александрова О.И., Околов И.Н., Хорольская Ю.И., Блинова М.И., Чураков Т.K. Оценка влияния бензалкония хлорида на цитотоксичность глазных капель Неттацин и Тобрекс в условиях in vitro. Cовременные технологии в офтальмологии. 2016;3:163–166. [Aleksandrova O.I., Okolov I.N., Horol’skaja Ju.I., Blinova M.I., Churakov T.K. Evaluation of BAK influence on cytotoxicity of eye drops Nettacin and Tobrex in vitro. Ocenka vlijanija benzalkonija hlorida na citotoksichnost’ glaznyh kapel’ Nettacin i Tobreks v uslovijah in vitro. Sovremennye tehnologii v oftal’mologii, 2016;3:163–166. (In Russ.)]
16. Александрова О.И., Околов И.Н., Хорольская Ю.И., Панова И.Е., Блинова М.И. Возможности клеточных технологий для рациональной фармакотерапии глазных патологий. Cовременные технологии в офтальмологии. 2017;7:5–7. [Aleksandrova O.I., Okolov I.N., Horol’skaja Ju.I., Panova I.E., Blinova M.I. Possibilities of cell technologies for rational pharmacotherapy of eye pathologies. Vozmozhnosti kletochnyh tehnologij dlja racional’noj farmakoterapii glaznyh patologij. Sovremennye tehnologii v oftal’mologii. 2017;7:5–7. (In Russ.)]
17. Александрова О.И., Околов И.Н., Хорольская Ю.И., Панова И.Е., Блинова М.И. Оценка цитотоксичности слезозаместительных препаратов с использованием системы in vitro. Офтальмология. 2017;14(1):59–64). [Aleksandrova O.I., Okolov I.N., Horol’skaja Ju.I., Panova I.E., Blinova M.I. Cytotoxicity evaluation of tear substitutes using in vitro system. Ocenka citotoksichnosti slezozamestitel’nyh preparatov s ispol’zovaniem sistemy in vitro. Оphthalmology in Russia=Oftal’mologiya. 2017;14(1):59–64). DOI: 10.18008/1816-5095- 2017-1-59-66. (In Russ.).] DOI: http://dx.doi.org/10.18008/1816-5095-2017-1-59-66
18. Александрова О.И., Околов И.Н., Хорольская Ю.И., Панова И.Е., Блинова М.И. Влияние нестероидных противовоспалительных глазных капель на клетки эпителия роговицы и конъюнктивы человека в условиях in vitro. Офтальмология. 2017;15(3):251– 259. [Aleksandrova O.I., Okolov I.N., Horol’skaja Ju.I., Panova I.E., Blinova M.I. Influence of NSAID eye drops on corneal epithelial cells in vitro. Оphthalmology in Russia=Oftal’mologiya. 2017;15(3):251– 259. (In Russ.)] DOI: 10.18008/1816-5095-2017-3-251-259
19. Cancer cell culture: methods and protocols / Ser. Methods in Molecular Medicine. Vol. 88. (Ed. S.P. Langdon). Totowa, NJ: Humana Press, 2003. 165–169 p.,
20. Kahook M. Preservatives in Topical Ophthalmic Medications: Historical and Clinical Perspectives. Expert Review of Ophthalmology. 2009;4(1):59–64.
21. Epstein S., Ahdoot M., Marcus E., Asbell P. Comparative toxicity of preservatives on immortalized corneal and conjunctival epithelial cells. J Ocul Pharmacol Ther 2009;25(2):113–9.
22. Noecker R. Effects of common ophthalmic preservatives on ocular health. Adv Ther. 2001 Sep-Oct; 18(5):205–15.
23. Schrage N., Frentz M., Spoeler F. The Ex Vivo Eye Irritation Test (EVEIT) in evaluation of artificial tears: Purite-preserved versus unpreserved eye drops. Graefes Arch Clin Exp Ophthalmol. 2012 Sep; 250(9):1333–40. DOI: 10.1007/s00417-012-1999-3
24. Samar K. Basak Preservatives and Ocular Surface Diseases. Kerala Journal of Ophthalmology. 2016;18(4):311–6.
25. Schrage N., Frentz M., Reim M. Changing the composition of buffered eye-drops prevents undesired side effects. Br J Ophthalmol. 2010;94:1519–22. DOI: 10.1136/bjo.2009.177386
26. Mueller-Lierheim. Traenenersatz- und Kontaktlinsenbenetzungsloesungen. In: Köln Biermann, ed. Aktuelle Kontaktologie. 2015:8–15.
27. Houlsby R., Ghajar M., Chavez G. Antimicrobial activity of boratebuffered solutions. Antimicrob Agents Chemother. 1986;29:803–6.
28. Lehmann D., Cavet M., Richardson M. Nonclinical safety evaluation of boric acid and a novel borate-buffered contact lens multi-purpose solution, Biotrue™ multipurpose solution. Cont Lens Anterior Eye. 2010 Dec; 33 Suppl 1:S24–32. DOI: 10.1016/j.clae.2010.06.010
29. Graupner O., Hausmann C. The alternation of the pH in the anterior chamber of the rabbits eye burned with smallest volumes of high concentrated acid and base [in German]. Albrecht Von Graefes Arch Klin Exp Ophthalmol. 1968;176:48–53.
Для цитирования:
Александрова О.И., Околов И.Н., Хорольская Ю.И., Панова И.Е., Блинова М.И. Оценка цитотоксичности in vitro как критерий рационального выбора слезозаместительных препаратов. Офтальмология. 2018;15(2):167-175. https://doi.org/10.18008/1816-5095-2018-2-167-175
For citation:
Aleksandrova O.I., Okolov I.N., Khorolskaya Yu.I., Panova I.E., Blinova M.I. Cytotoxicity Evaluation Using in vitro System as a Criteria of Rational Choice of Tear Substitutes. Ophthalmology in Russia. 2018;15(2):167-175. (In Russ.) https://doi.org/10.18008/1816-5095-2018-2-167-175