бцж и неонатальный скрининг в один день
Обследование проводится на такие болезни как: врожденный гипотиреоз, муковисцидоз, фенилкетонурия, адреногенитальный синдром, галактоземия. Раннее выявление этих заболеваний позволяет врачу вовремя назначить необходимое дообследование, лечение или специализированную диету.
Остановимся немного подобнее на каждом из этих заболеваний.
В рамках неонатального скрининга эти пять заболеваний включены еще и потому, что при ранней диагностике их можно вылечить, или, по крайней мере, значительно облегчить последствия и тяжесть течения процесса.
Как проводится данное обследование?
Обычно кровь на анализ берут у малышей, родившихся в срок не ранее 4-го дня жизни, недоношенным деткам тест проводится не ранее 7-го дня жизни. Но точная дата обследования может существенно меняться в зависимости от обстоятельств. Такое раннее обследование объяснимо тем, что некоторые генетически обусловленные болезни могут проявляться в первые недели жизни и крайне важно вовремя диагностировать их, чтобы начать необходимую терапию, с целью минимизировать риски тяжелых последствий заболевания.
Среди родителей скрининг на наследственные заболевания принято называть «пяточным тестом»- потому, что кровь для теста берут через маленький прокол на пяточке малыша (у ребенка старше 3 месяцев кровь на обследование берется из пальчика).
Чтобы результаты теста были максимально точными, кровь следует сдавать натощак, через 3 часа после последнего кормления ребенка (у новорожденных перед очередным кормлением).
В Детском Диагностическом центре появилась уникальная возможность сдать анализ крови на 5 наследственных заболеваний. Подробнее
Неонатальный скрининг
Неонатальный скрининг, ласково именуемый в нашей стране «пяточка», является одним из первых важных исследований новорожденного. В России скрининг преимущественно направлен на выявление пяти наследственных болезней обмена: фенилкетонурии, врожденного гипотиреоза, врожденной дисфункции коры надпочечников (ВДКН), галактоземии и муковисцидоза. За рубежом этот список расширен до 50 различных заболеваний, в некоторых штатах Америки их свыше 60. Здоровый доношенный новорожденный допускается к скринингу на 4–5 сутки, недоношенный — на седьмой день после рождения. Заболевания, на выявление которых направлен скрининг, никак не проявляют себя в периоде новорожденности, но их ранняя диагностика и своевременно начатое патогенетическое лечение существенно влияют на прогноз и качество жизни ребенка. Помимо исследования крови проводится аудиометрия для оценки слуха и пульсоксиметрия для скрининга пороков сердца, но в данной статье мы преимущественно сосредоточимся на тестировании крови.
Разработка программы скрининга началась в шестидесятых годах прошлого века, когда Роберт Гатри создал технологию тестирования сухих отпечатков крови на фильтровальной бумаге. Первым заболеванием, которое стало кандидатом для массовой диагностики, была фенилкетонурия, так как ее раннее выявление и коррекция питания способны предотвратить развитие тяжелых неврологических нарушений. Затем к скринингу добавилось еще несколько заболеваний: врожденный гипотиреоз, ВДКН, галактоземия и муковисцидоз. Тандемная масс-спектрометрия (ТМС) позволила значительно расширить список заболеваний, добавив к болезням обмена веществ гемоглобинопатии, спинальную мышечную атрофию, тяжелый комбинированный иммунодефицит и др.
Таблица 1 | Рекомендуемая The American College of Obstetricians and Gynecologists (ACOG) скрининг-панель для врожденных заболеваний
В данной статье будут рассмотрены два скрининга, доступные в нашей стране: обязательный, включающий тестирование на пять заболеваний (врожденный гипотиреоз, ВДКН, фенилкетонурия, галактоземия, муковисцидоз) и расширенный скрининг на наследственные нарушения метаболизма.
Обязательный скрининг
На 4–5 сутки после рождения здорового доношенного ребенка или на седьмые сутки жизни недоношенного ребенка проводится тестирование методом «сухого пятна».
Фенилкетонурия (в современной классификации ― ФАГ-зависимая ФКУ) обусловлена мутацией гена фенилаланингидроксилазы и относится к числу аминокислотных аминоацидопатий. В норме фенилаланин (ФА) путем реакций гидроксилирования превращается в тирозин, однако в случае мутации вышеназванного гена активность превращающего фермента снижается, создается дефицит тирозина одновременно с избытком ФА, образующего токсичные метаболиты (фенилацетат, фенилпируват, фениллактат). Снижение образования тирозина влечет за собой нарушение синтеза гормонов щитовидной железы, нейротрансмиттеров и пигментов меланоцитов, а избыток ФА приводит к дисбалансу аминокислот в тканях мозга, обусловленному торможением их всасывания в желудочно-кишечном тракте или нарушением реабсорбции из почечных канальцев, нарушению образования или стабилизации полирибосом, снижению синтеза миелина, норадреналина и серотонина. Также за счет конкурентного ингибирования создается дефицит тирозиназы, что в совокупности с дефицитом тирозина приводит к снижению образования меланина и гипопигментации.
Основной проблемой пациентов с ФКУ являются нарушения функции ЦНС: от сонливости, вялости, отсутствия аппетита в период манифестации в 2–6 месяцев до тяжелых нарушений психомоторного развития в будущем; нередко развиваются атаксия, гиперкинезы, тремор рук, парезы по центральному типу. Единственный способ предотвратить развитие вышеназванных нарушений — назначение гипофенилаланиновой диеты с момента рождения с поддержанием низкого уровня фенилаланина в течение всей жизни.
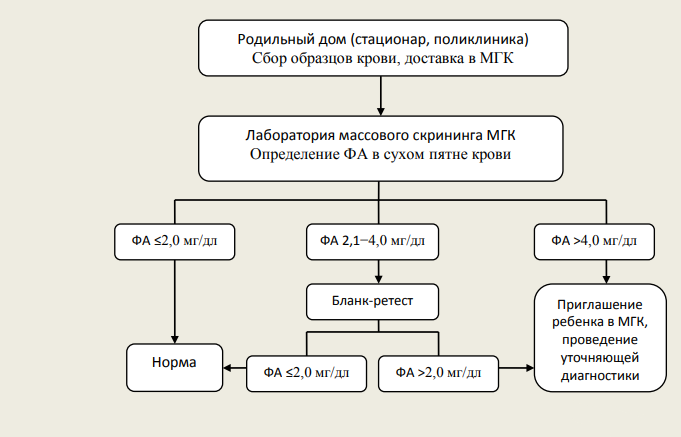
Рисунок 1 | Интерпретация результатов исследования на наличие фенилкетонурии
ВДКН обусловлена дефицитом ферментов и транспортных белков, участвующих в биосинтезе кортизола. Наиболее часто встречается дефицит 21-гидроксилазы, что в свою очередь приводит к дефициту кортизола и альдостерона и ответному увеличению секреции АКТГ и гиперплазии коры надпочечников. В условиях дефицита фермента происходит значительное накопление предшественников гормонов, что приводит к увеличению синтеза тестостерона, не зависящего от 21-гидроксилазы. В итоге у пациента формируется надпочечниковая недостаточность и гиперандрогения. Гормональным маркером дефицита 21-гидроксилазы является уровень 17-гидроксипрогестерона (17-ОНП), определяемый в рамках неонатального скрининга. Результат трактуется как положительный, если при двукратном тестировании образца уровень 17-ОНП у доношенных новорожденных составляет ≥ 20 нг/мл. У недоношенных детей при заборе крови на 7–8 сутки после рождения скрининговый результат трактуется как положительный при следующих уровнях 17-ОНП: на сроке 23–32 недели гестации ― ≥ 65 нг/мл; на сроке 33–36 недель гестации ― ≥ 40 нг/мл.
Врожденный гипотиреоз в большинстве случаев вызван дефектами самой щитовидной железы (первичный гипотиреоз). Причины первичного врожденного гипотиреоза можно в широком смысле классифицировать как неспособность щитовидной железы нормально развиваться (дисгенезия) или неспособность структурно нормальной щитовидной железы производить нормальные количества гормона (дисгормоногенез). Дисгенезия щитовидной железы, охватывающая весь спектр агенеза, гипоплазии и эктопии, является наиболее частой причиной врожденного гипотиреоза. В то время как это заболевание остается наиболее частой причиной врожденного гипотиреоза, частота возникновения дисгормоногенеза за последние несколько десятилетий увеличилась. В то время как на дисгормоногенез приходится только 15 % врожденного гипотиреоза, диагностированного в первые дни скрининга новорожденных, у 30–40 % младенцев, прошедших скрининг по современным протоколам, имеется эктопическая щитовидная железа, соответствующая одной из форм дисгормоногенеза. В отличие от дисгенезии щитовидной железы, при которой моногенная причина присутствует только у небольшого количества пациентов, дисгормоногенез часто возникает из-за генетического дефекта на каком-либо этапе синтеза тиреоидных гормонов.
Учитывая разнообразие функций тиреоидных гормонов в организме человека, врожденный гипотиреоз характеризуется разнообразием клинических проявлений с поражением всех органов и систем. При отсутствии своевременного лечения на первый план выходит задержка психомоторного и речевого развития, затем наступают отставание в физическом развитии и задержка полового развития. Основной задачей скрининга является наиболее раннее выявление детей с подозрением на врожденный гипотиреоз.
Рисунок 2 | Интерпретация результатов исследования на наличие врожденного гипотиреоза
Галактоземия — аутосомно-рецессивное наследственное нарушение обмена углеводов, при котором в организме накапливается избыток галактозы и ее метаболитов. В норме галактоза образуется в результате гидролиза лактозы в кишечнике либо в процессе ферментных реакций, обмена гликопротеинов и гликолипидов. Галактоза является материалом для образования клеточных мембран, нервной ткани, нервных окончаний и т. д. В результате ферментных реакций она превращается в глюкозу, и именно дефицит галактозо-1-фосфатуридилтрансферазы лежит в основе патогенеза данного заболевания. Метаболиты галактозы обладают повреждающим действием. Так, галактитол проникает в хрусталик глаза, приводя к повышению осмотического давления, электролитным нарушениям и денатурации белка с формированием катаракты. Другие метаболиты обладают гепато-, нейро- и нефротоксическим действиями, а также вызывают гемолиз эритроцитов. Тормозящее влияние метаболитов галактозы на углеводный обмен приводит к гипогликемии.
Рисунок 3 | Интерпретация результатов исследования на наличие галактоземии
Муковисцидоз — аутосомно-рецессивное заболевание, связанное с мутацией гена МВТР (трансмембранного регулятора муковисцидоза). МВТР является хлорным каналом, мутации гена которого нарушают не только транспорт, но и секрецию ионов хлора. При затруднении их прохождения через клеточную мембрану увеличивается реабсорбция натрия железистыми клетками, нарушается электрический потенциал просвета, что вызывает изменение электролитного состава и дегидратацию секрета желез внешней секреции. В результате выделяемый секрет становится чрезмерно густым и вязким. Поражаются все экзокринные железы организма: печень, поджелудочная железа, мочеполовая система, но наиболее ярко муковисцидоз проявляет себя со стороны органов дыхания, провоцируя бронхообструкцию, дыхательную и сердечную недостаточность, легочную гипертензию.
Рисунок 4 | Интерпретация результатов исследования на наличие муковисцидоза
Расширенный скрининг
Органические ацидемии — группа аутосомно-рецессивных наследственных заболеваний обмена, в основе патогенеза которых лежит дефицит ферментов, участвующих в метаболизме белков, что приводит к повышению уровня кетоновых тел, обладающих токсическим действием на различные органы и ткани, в частности, на ЦНС. Данные заболевания манифестируют уже в стадии декомпенсации, как правило, в период с первой недели до первого года жизни. Триггерами служат стресс, длительное голодание, инфекционные заболевания, иммунизация, реже — чрезмерное употребление белковой пищи. Проявляются преимущественно неврологической симптоматикой: нарушение сознания вплоть до комы, эпилептические приступы, нарушение мышечного тонуса, у детей старшего возраста — нарушения психоречевого развития, атаксия, очаговые неврологические симптомы, синдром Рейе (острая печеночная недостаточность, сочетающаяся с энцефалопатией), психические расстройства.
Нарушения окисления жирных кислот — врожденный дефект метаболизма из-за нарушения либо митохондриального β-окисления, либо транспорта жирных кислот с использованием карнитинового транспортного пути. Проявления зависят от нарушения метаболизма конкретной кислоты, но все они имеют общие черты и требуют схожей тактики лечения. В периоде новорожденности метаболические нарушения проявляются тяжелой кардиомиопатией, гипокетотической гипогликемией, дисфункцией печени в первые несколько дней или недель жизни, часто заканчиваясь летально. В младенческом и детском возрасте характерны эпизоды летаргии и рвоты, развивается дисфункция печени и гипокетотическая гипогликемия, энцефалопатия, что может привести к внезапной младенческой смерти. У подростков и во взрослом возрасте дебютируют эпизодическим рабдомиолизом, мышечной слабостью, миалгией. Лечение включает отказ от голодания, симптоматическую терапию развившихся осложнений и включение в рацион добавок, если это необходимо.
Аминоацидопатии
Болезнь кленового сиропа (она же лейциноз) — наследственное заболевание, обусловленное дефицитом дегидрогеназы кетокислот с разветвленной цепью и нарушением метаболизма лейцина, изолейцина, валина (аминокислоты с разветвленной цепью, АКЦР). Повышение уровня АКЦР и их метаболитов, в частности, кетокислот, приводит к кетоацидозу, атрофии ткани головного мозга, нарушению окислительного фосфорилирования в дыхательной цепи митохондрий. Избыток лейцина обладает нейротоксическим эффектом, вызывая дисфункцию астроцитов, апоптоз нейронов и блокируя транспорт через гематоэнцефалический барьер аминокислот, важных для синтеза нейротрансмиттеров.
Гомоцистеинурия — наследственное заболевание из группы аминоацидопатий, обусловленное нарушением метаболизма серосодержащих аминокислот, в частности, метионина. Дефицит цистатион-b-синтазы нарушает преобразование метионина в цистеин. Высокий уровень гомоцистеина связан с образованием некротически-дегенеративных участков в почках, селезенке, слизистой оболочке желудка и сосудах, активацией XII фактора свертывания, способствующего тромбообразованию.
Тирозинемия 1 типа — заболевание, обусловленное дефицитом фумарилацетоацетатгидролазы, в результате чего происходит накопление высокотоксичных фумарил- и малеилацетоацетата, обладающих гепатотоксическим и канцерогенным действием. Конечные метаболиты — сукцинилацетон и сукцинилацетоацетат — являются митохондриальными токсинами, тормозящими фосфорилирование и блокирующими цикл Кребса. Накопление токсинов приводит к прогрессирующему заболеванию печени с развитием печеночной недостаточности, цирроза, тубулопатии с формированием ренальной тубулопатии, гипофосфатемического рахита, синдрома Фанкони. Острая тирозинемия сопровождается развитием гипертрофической кардиомиопатии. Кроме того, нарушается путь синтеза порфирина, ингибируется синтез порфобилиногена, что приводит к кризам, проявление которых напоминает порфирию. Все пациенты подвержены высокому риску развития гепатоцеллюлярной карциномы, вторичной по отношению к циррозу. Без своевременного лечения дети погибают в возрасте 10 лет.
Бцж и неонатальный скрининг в один день
В настоящее время вы встречаетесь с целым рядом новых методов диагностики туберкулезной инфекции, введение которых в практику привели к изменению подходов к применению уже известных методов и к изменению нормативных документов.
Информация, представленная в данном обращении, позволит вам найти ответы на многие вопросы относительно профилактики, диагностики и лечения туберкулезной инфекции у детей.
Традиционно вакцинация против туберкулеза с применением БЦЖ или БЦЖ-М (ослабленной вакцины), когда вводится другой вид микобактерий – микобактерии M.bovis-BCG, проводится на 3-7 день жизни ребенка в родильном доме для создания противотуберкулезного иммунитета, при отсутствии противопоказаний.
Вы должны знать, что существуют абсолютные и относительные противопоказания к вакцинации против туберкулеза.
Абсолютными противопоказаниями к иммунизации против туберкулеза являются:
— генерализованная БЦЖ инфекция (лимфаденит, БЦЖ-остит), выявленные у других детей в семье;
— ВИЧ инфекция у ребенка.
Относительными противопоказаниями являются:
— масса тела при рождении менее 2500 г. (при вакцинации БЦЖ);
— менее 2300 г. (при вакцинации БЦЖ-М);
— острые инфекционные заболевания;
— ВИЧ инфекция у матери.
Дети, которые не были вакцинированы против туберкулеза, должны наблюдаться педиатром. Согласно нормативным документа, необходимо проводить пробу Манту с 2ТЕ один раз в 6 месяцев до проведения прививки против туберкулеза.
Детям, старше 2-х месяцев, перед вакцинацией БЦЖ необходима постановка реакции Манту с 2ТЕ. В случае отрицательного результата по пробе Манту с 2 ТЕ можно проводить вакцинацию против туберкулеза.
Интервал между постановкой пробы Манту с 2ТЕ и вакцинацией должен быть не менее 3-х дней и не более 2-х недель.
Эффективность вакцинации БЦЖ определяют по двум параметрам:
формирование постпрививочного рубчика (до 10мм);
положительная чувствительность к туберкулину по пробе Манту с 2ТЕ в возрасте 1 год.
Необходимо помнить, что у 10% детей от числа вакцинированных БЦЖ, при наличии сформировавшегося постпрививочного рубца, впервые положительная чувствительность к туберкулину возникает в возрасте 3-х лет.
Иммунодиагностика туберкулеза.
В Российской Федерации до настоящего времени проводится скрининг туберкулезной инфекции. Всем детям в возрасте от 1 до 14 лет ежегодно проводятся иммунологические тесты, у подростков – возможно сочетание иммунодиагностики и рентгенологического обследования. Взрослому населению необходимо проведение флюорографического обследования один раз в два года. Группам риска необходимо проведение рентгенологического обследования один раз в год или один раз в полгода с учетом степени риска заболеть туберкулезом.
В возрасте от 1 года до 7 лет включительно детям по-прежнему проводится постановка пробы Манту с 2 ТЕ ежегодно, если ребенок вакцинирован БЦЖ и при отсутствии противопоказаний для постановки пробы.
Необходимо знать, что проба Манту не является прививкой! Это иммунологический, а именно специфический аллергический тест, внутрикожное введение смеси антигенов, при реакции на которые может развиться кожная аллергическая реакция при наличии в организме микобактерий различного типа, в том числе и туберкулезных. До настоящего времени проба Манту рекомендована для применения ВОЗ в странах с низким и среднем уровнем жизни, так как является признанным и дешевым способом иммунодиагностики туберкулеза.
Условно, реакция на пробу Манту с 2 ТЕ отражает развитие поствакцинальной аллергии после вакцинации БЦЖ. Поствакцинальная аллергия определяется оценкой динамики реакции Манту2ТЕ с 12 месячного возраста и до 7 лет. К 7 годам отмечается снижение чувствительности к туберкулину, вплоть до отрицательного результата реакции на Манту 2ТЕ. При нарастании результатов пробы более 5 мм в год или при наличии контакта с больным туберкулезом необходима постановка более информативных тестов для диагностики туберкулезной инфекции.
Необходимо помнить, что в условиях скрининга пробу Манту 2ТЕ, как и другие тесты, проводят только здоровым детям. Ели возникают сомнения в состоянии ребенка или выборе теста – обратитесь к специалисту.
Перенесенные заболевания и предшествующие прививки могут влиять на чувствительность кожи ребенка к туберкулину, в связи с этим, пробу Манту с 2 ТЕ ставят через 1 месяц после выздоровления ребенка и через 1 месяц после любой профилактической прививки.
С учетом роста сопутствующей патологии у детей может возникнуть ситуация, когда постановка пробы Манту с 2 ТЕ может быть противопоказана. В подобных ситуациях мы рекомендовали бы обратиться к специалистам (педиатру, иммунологу или фтизиатру), чтобы выбрать наиболее оптимальный иммунологический тест, который будет информативен и безопасен при его проведении для ребенка.
Новые иммунологические тесты.
За последние десять лет в практической работе врачей появились три новых иммунологических теста, которые могут применяться для диагностики туберкулезной инфекции. В Российской Федерации был разработан и внедрен новый кожный тест – Диаскинтест. В странах Европы, Америки и Канады были внедрены тесты, которые проводятся в лабораторных условиях – IGRA- тесты (ELISPOT и QuantiferonTBGold тест).
Диаскинтест — аллерген туберкулезный рекомбинантный в стандартном разведении, не обладает сенсибилизирующим действием, нетоксичен.
Препарат Диаскинтест © или аллерген туберкулезный рекомбинантный представляет собой комплекс рекомбинантных белков, соединенных вместе (ESAT6/CFP10), который предназначен для внутрикожного введения с целью получения реакции гиперчувствительности замедленного типа.
Основными задачами, которые ставили перед собой ученые, явилась высокая диагностическая информативность нового теста, превышающая таковую у пробы Манту с 2 ТЕ; простота в использовании и доступность.
Все перечисленные задачи были выполнены, и уже первые результаты клинических исследований, проведенных в 2009 году, продемонстрировали не только высокую специфичность теста (90-100%), но и его безопасность.
Следует знать, что не стоит проводить пробу у детей с отягощенным аллергологическим анамнезом, с эндокринными нарушениями и с иммунодефицитом.
Важно знать, что у детей, вакцинированных БЦЖ и не инфицированных МБТ, тесты нового поколения (проба с диаскинтестом, ELISpot и QFT) должны быть отрицательными. В связи с этим, данный препарат эффективен для дифференциальной диагностики поствакцинальной и инфекционной аллергии.
Получение положительного результата при проведении любого из данных тестов требует проведения комплексного обследования для исключения заболевания туберкулезом.
Обращаем ваше внимание на необходимость качественного проведения обследования ребенка с положительным иммунологическим тестом, из контакта с больным туберкулезом, а также при наличии клинической симптоматики или рентгенологических изменений, характерных для туберкулеза.
Комплексное обследование должно обязательно включать лабораторный комплекс обследования, МСКТ и эндоскопическое исследование трахеобронхиального дерева.
Мы будем рады ответить на все ваши вопросы о состоянии здоровья вас и ваших детей, провести комплексное обследование на уровне ведущих клиник Европы и мира с применением всех современных методов диагностики.
Что нужно и нельзя делать до и после прививки
Прививки — это важный шаг в жизни ребенка и серьезное испытание для родителей. Существует множеством мифов, которые не только осложняют уход за ребенком до и после вакцинации, но и отвлекают внимание родителей от действительно важных моментов, связанных с прививками.
Перед тем как сделать прививку
Принимая во внимание тот факт, что в подавляющем большинстве случаев, прививки хорошо переносятся здоровыми детьми без всякой подготовки и предварительного лечения, самым важным пунктом в подготовке ребенка к прививке является определение противопоказаний к прививкам, то есть тех случаев болезни у ребенка, при которых прививка может дать серьезные побочные реакции. Противопоказания и предосторожности для вакцинации, в некоторых случаях проведение вакцинации у детей либо категорически запрещено, либо должно быть отложено на более поздний срок. Чтобы правильно оценить противопоказания и предосторожности для проведения вакцинации у ребенка важно следовать календарю вакцинации и знать заранее, какая прививка и когда должна быть поставлена ребенку. Перед тем как поставить ребенку прививку и в день вакцинации прочтите, какие противопоказания и предосторожности связаны с введением той или иной прививки и убедитесь в том, что у ребенка нет никаких противопоказаний для введения прививки. Если определение некоторых противопоказаний или предосторожностей вызывает у вас затруднение (например, насколько опасна у ребенка простуда или кашель) – покажите его врачу. Вслепую отказываться от прививки из-за легкого насморка или кашля не следует – это только сорвет план вакцинации.
Подготовка ребенка к прививке Необходимая подготовка ребенка к прививке обычно гораздо проще, чем принято считать
Питание ребенка За несколько дней до вакцинации не следует вводить в рацион ребенка новые продукты питания. Если ребенок находится на грудном вскармливании – матери лучше отказаться от новых продуктов и питаться как обычно. Это поможет избежать возникновения аллергических реакций, которые могут быть спутаны с действием прививки. Профилактический прием антигистаминных лекарств и жаропонижающих средств Прием антигистаминных препаратов (например, Супрастин) за день до прививки рекомендуется только в случае детей, страдающих различными проявлениями аллергии (крапивница, атопический дерматит, астма), или у которых прошлая доза прививки вызвала появление сильного отека, покраснения и боли на месте инъекции. Назначение антигистаминных препаратов ребенку следует обсудить с врачом. Для того чтобы профилактическое лечение было эффективным важно правильно подобрать дозу лекарства в зависимости от силы аллергии и массы тела ребенка. Профилактический прием жаропонижающих средств не рекомендуется. Исключение составляют только дети склонные к фебрильным судорогам, которым следует дать жаропонижающее средство непосредственно перед прививкой или сразу после прививки. Перед тем как пойти на прививку убедитесь в том, что лекарства есть у вас дома (Парацетамол в свечах или в сиропе в дозировке соответствующей возрасту ребенка и Супрастин).
Сразу перед прививкой
Непосредственно перед прививкой расспросите врача о том, какую прививку или прививки получит ребенок и том, какие побочные реакции могут возникнуть после такой прививки и что следует предпринять по их поводу.
В момент прививки и сразу после прививки
В момент прививки постарайтесь подержать ребенка и успокоить его после инъекции. Обычно дети грудного возраста быстро успокаиваются, если их приложить к груди (после живой оральной прививки против полиомиелита нельзя кормить или поить ребенка в течении часа), а дети постарше – если им предложить игрушку (игрушкой лучше запастись из дому).
Сразу после прививки
Сразу после прививки не спешите покидать поликлинику. Если врач не предложил вам – вам следует по собственной инициативе остаться в поликлинике еще на 10-15 минут. Такая предосторожность связана с риском возникновения коллапса или сильных аллергических реакций на прививку (анафилактический шок). Несмотря на то, что такие реакции возникают исключительно редко, возможность их развития всегда следует иметь в виду.
Уход за ребенком в последующие дни после прививки Уход за ребенком после прививки заключается в следующем
Питание ребенка после прививки В течение нескольких дней после прививки следует воздержаться от введения в рацион ребенка или кормящей матери новых продуктов. После прививки, особенно если у ребенка есть температура, понос или рвота, следите за тем, чтобы ребенок получал достаточно жидкости. Не переживайте, если в течение 2-3 дней после прививки у ребенка нет аппетита.
Лечение температуры и профилактика аллергии после прививки
Повышение температуры это нормальная реакция организма ребенка на прививку, которая означает, что иммунная система отреагировала на прививку и начинает вырабатывать иммунитет (однако отсутствие повышенной температуры после прививки не означает, что прививка оказалась неэффективной). В случае совершенно здоровых детей не следует сбивать температуру после прививки, если она не превышает 38, 5С. В случаях более значительного повышения температуры, а также когда температура держится на уровне 38,5 С вечером, ребенку следует дать жаропонижающее. Для лечения температуры после прививки рекомендуется использовать Парацетамол. В качестве жаропонижающего средства у детей ни в коем случае нельзя использовать Аспирин.
В случае детей со склонностью к фебрильным судорогам следует начать лечение температуры при повышении ее выше 37,5 или дать ребенку жаропонижающее до появления температуры, если так посоветовал невропатолог, наблюдающий ребенка.
Профилактика аллергических реакций после прививок показана только в случае детей склонных к развитию аллергии. В таких случаях рекомендуется использовать Супрастин или другое антигистаминное лекарство по назначению врача.
Лечение покраснения и отека на месте инъекции
Большинство прививок приводят к появлению более или менее выраженного покраснения или отека на месте инъекции. Наиболее выжженная местная реакция на введение прививки наблюдается в случае АКДС (покраснение, отек и болезненность на месте инъекции) и БЦЖ (образование долго незаживающей язвочки). В случае всех типов прививок рекомендуется воздержаться от любого локального лечения покраснения или отека на месте инъекции. Если ребенок расчесывает место инъекции, его можно покрыть легкой марлевой повязкой. На месте АКДС нередко образуется уплотнение, располагающееся в глубине мышцы – «шишка». Часто такое уплотнение бывает болезненным, и ребенок легко прихрамывает на одну ножку (если прививка была введена в бедро). Образование плотной «шишки» после АКДС считается нормальной реакцией и не требует никакого лечения. В течение нескольких недель шишка самостоятельно рассасывается.
Можно ли купать ребенка после прививки?
Если после прививки у ребенка нет температуры, его можно купать, без всяких опасений намочить прививку. Место прививки, однако, лучше не растирать мочалкой. Исключение составляет только проба Манту (это не прививка) которую нельзя мочить или растирать до чтения результатов.
Можно ли гулять с ребенком после прививки?
Прививка не является противопоказанием для прогулок и игр на улице. Прогулки после прививок совершенно безопасны, если у ребенка нет температуры и он хорошо себя чувствует.
Понос и рвота после прививки
Из-за высокой чувствительности вегетативной нервной системы детей к любым раздражителям после прививок нередко наблюдаются отдельные эпизоды рвоты или короткие эпизоды поноса. Ни однократная рвота, ни кратковременный понос не должны вызывать беспокойства и не требуют никакого специального лечения.