Чем восстановить слизистую носа после ожога
Лечение местных лучевых повреждений
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов, как следствие воздействия ионизирующего излучения в суммарной очаговой дозе 60—70 Гр., проявляются в виде хронических эпителиитов и дерматитов, с прогрессированием их в лучевые язвы кожи, лучевые проктиты, циститы и т. п. В патогенезе таких повреждений, наряду с нарушением микроциркуляции, ведущее значение играет прямое воздействие излучения на клетки и подавление репаративных процессов. В дальнейшем на передний план выходят присоединение инфекции поврежденных тканей и усугубление негативных процессов заживления поврежденных тканей [1]. Вот почему в комплекс медикаментозных средств при лечении местных лучевых повреждений включаются вещества, воздействие которых направлено на улучшение тканевой микроциркуляции, повышение репараторных процессов и подавление инфекционного процесса. Для лечения местных лучевых повреждений апробированы практически все известные медикаментозные средства, удовлетворяющие перечисленным требованиям. Низкая терапевтическая эффективность имеющихся средств явилась основанием для поиска новых методов лечения. В отделении лечения лучевых повреждений МРНЦ РАМН ежегодно проходит лечение значительное число больных с лучевыми язвами конечностей и других областей тела, лучевыми повреждениями кишечника, мочевого пузыря и др. Основным компонентом местного лечения является препарат димексид (диметилсульфоксид, или ДМСО), применяющийся в виде перевязок раствора 5—10% или мази 10%. Это базовое лечение, назначаемое с учетом конкретных особенностей каждого больного, может дополняться назначением других антисептиков (диоксидин, хлоргексидин и др.), протеолитических ферментов, средств, стимулирующих репараторные процессы (куриозин, витаминизированные масла и др.). Разработанные схемы местного и общего лечения позволяют добиться благоприятных результатов у 57% пациентов [1, 2].
С сентября 2002 г. мы исследовали терапевтическую эффективность препарата гепон для лечения больных местными лучевыми повреждениями (см. таблицу 1).
 |
| Таблица 1. Применение гепона при лечении местных лучевых повреждений. |
Лучевые язвы у больных развились после лучевой терапии злокачественных опухолей (рак кожи — 16 пациентов, рак молочной железы — шесть, саркомы — четыре). Суммарная очаговая доза (СОД) составляла 45—70 Гр. Лучевые проктиты явились следствием лучевой терапии рака шейки и тела матки (13), рака мочевого пузыря (3) и прямой кишки (2). Лучевые циститы также наблюдались после лучевой терапии рака шейки и тела матки (13) и рака мочевого пузыря (4). Пневмофиброз — это следствие лучевой терапии лимфогранулематоза (6) и рака молочной железы (5 больных).
При лечении лучевых язв гепон применялся на первом этапе (7—10 дней) в виде орошения язвы раствором. Гепон (0,002) растворяли перед употреблением в 5 мл стерильного физиологического раствора. Орошение полученным раствором 0,04% гепона производилось ежедневно. На втором этапе, по мере развития грануляции, применялась мазь 0,04% (10—18 дней). Результаты лечения лучевых язв гепоном сопоставлялись с динамикой течения раневого процесса у более 800 больных, которым терапию проводили с принятыми в отделении методами лечения, состоящими в местном применении раствора 10% димексида (аппликации или электрофорез), электрофореза протеолитических ферментов и гепарина, использовании мазей левомиколя, ируксола, куриозина и эплана.
Эффективность применения гепона оценивалась клинически по состоянию раневой поверхности (уменьшение экссудации, скорости развития грануляций и скорости эпителизации язвы по Л. Н. Поповой (см. таблицу 2)), исчисляемой по формуле:
СЗ= (S-St)/St х 100, где
СЗ — скорость заживления
S — площадь лучевой язвы (мм 2 перед началом лечения)
St — площадь язвы (мм 2 ) в день измерения
t — время в сутках от начала лечения
 |
| Таблица 2. Скорость заживления лучевых язв. |
Положительный терапевтический эффект использования гепона мы склонны связывать в первую очередь с благоприятным его действием на микрофлору, что способствовало снижению воспалительного процесса и его негативных последствий (отек окружающих тканей, нарушение микроциркуляции и т. п.). Кроме того, важным аспектом действия гепона является его иммуномоделирующее действие, проявляющееся в активизации секреторного иммуноглобулина, снижении уровня противовоспалительных цитокинов, активизации a-интерферона, снижении адгезивной функции клеток и их апоптоза, прекращении вирусной репликации и повышении резистентности организма к бактериальной флоре.
В настоящее время, когда ранозаживляющее действие гепона доказано, лечение больных лучевыми язвами начинается с применения гепона, а затем дополняется, по показаниям, другими лекарственными средствами. Лечение лучевых ректитов (18 больных) и лучевых циститов (17 больных) проводилось в виде ежедневных двукратных микроклизм или инстилляций водного раствора 0,04% в течение 12—18 дней. Результаты применения гепона также сравнивались с результатами «традиционного» лечения, практиковавшегося в отделении в течение последних 25—30 лет (микроклизмы димексида 5—10%, эмульсии синтозона, витаминизированных масел и т. п.). Внутриполостное введение гепона уменьшало интенсивность болей и геморрагий и сокращало продолжительность лечения с 28—36 до 15—23 дней. Применение гепона активировало показатели иммунитета и у этой группы больных.
Таким образом, иммуномодулятор гепон в лечении больных с местными лучевыми повреждениями (лучевые язвы, лучевые ректиты и циститы) проявил себя как эффективное медикаментозное средство, способствующее быстрому снижению выраженности воспалительного процесса в поврежденных облучением тканях и ускорению репараторных процессов в них.
Литература
М. С. Бардычев, доктор медицинских наук, профессор
Медицинский радиологический научный центр РАМН (г. Обнинск)
Коррекция сухости слизистой оболочки полости носа
Большинству современных людей довольно часто приходится испытывать неприятные ощущения, характеризуемые как «сухость слизистой оболочки носа». Она выражается в заложенности носа, часто попеременной, зудом, жжением, образованием корок в&nb
Большинству современных людей довольно часто приходится испытывать неприятные ощущения, характеризуемые как «сухость слизистой оболочки носа». Она выражается в заложенности носа, часто попеременной, зудом, жжением, образованием корок в носовой полости, снижением обоняния. Кроме ощущения дискомфорта, сухость слизистой оболочки полости носа негативно сказывается на фильтрационной функции носа — частицы пыли, бактерии и вирусы, содержащиеся в воздухе, в процессе дыхания практически беспрепятственно попадают в легкие.
К возникновению сухости слизистой оболочки полости носа могут приводить различные факторы. Довольно часто «сухость в носу» является побочным действием некоторых лекарственных средств, в первую очередь антигистаминных препаратов и препаратов, содержащих атропин. Самым распространенным является неблагоприятное воздействие климата и экологии, пребывание в помещениях с центральным отоплением и кондиционированным воздухом. Негативное влияние на влажность слизистой оболочки носа оказывает вдыхание горячего воздуха, в частности при табакокурении, разряженный воздух (при авиаперелетах и отдыхе в горах), запыленность воздуха на ряде производств — цементном, химическом и т. д. Кроме того, такое состояние может быть и симптомом общего заболевания.
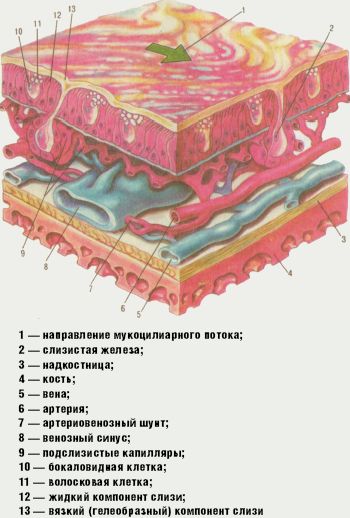
Слизистая оболочка полости носа покрыта особым мерцательным эпителием, состоящим из реснитчатых клеток, обеспечивающих транспорт слизистого секрета (рис. 1).
Реснитчатые клетки имеют по 250–300 ресничек длиной 7 и высотой 0,3 микрона. Каждая ресничка состоит из 9 пар микротрубочек, расположенных в виде кольца и окружающих две непарные центральные микротрубочки. Движение ресничек мерцательного эпителия слизистой оболочки носа осуществляется посредством скольжения микротрубочек (Satir P., 1974). Энергия для движения обеспечивается АТФ, расщепляющейся динеином. Динеин — это Са/Мg-зависимая АТФаза. Двигательный цикл начинается с присоединения АТФ к молекуле динеина. Расщепление фосфатного кольца в процессе гидролиза АТФ приводит к соединению молекулы динеина и тубулиновой молекулы соседнего наружного дублета и сопровождается конформационными изменениями молекулы динеина — сгибанием и смещением микротрубочки на определенном расстоянии. Это, в свою очередь, приводит к присоединению новой молекулы АТФ к динеину и разрыву её связей с тубулином, в результате чего динеиновая ручка принимает первоначальную форму. Весь цикл повторяется заново (Киселев А. С., Ткачук И. В., 2006).
Движение ресничек строго направлено — от преддверия полости носа в сторону носоглотки. Мукоцилиарный клиренс обеспечивается назальным секретом. Источником секрета, покрывающего эпителий полости носа, являются слизистые железы слизистой оболочки носа, бокаловидные клетки, транссудация из субэпителиальных капилляров, слезных желез, секрет специализированных Боумановых желез из ольфакторной зоны носа. Объем назальной секреции за 24 ч составляет от 100 мл до 1–2 л. Слизистый покров задних двух третей носа обновляется каждые 10–15 мин. Функция ресничек оптимальна при температуре 28–33 °C, достаточном количестве секрета с рН 5,5–6,5. Потеря влаги, понижение температуры до 7–10 °C, увеличение рН секрета более 6,5 вызывает прекращение колебания ресничек.
Устранению сухости слизистой оболочки носа способствует нанесение на нее изотонического раствора. При этом нормализуются реологические свойства слизи. Считается, что содержащиеся в изотоническом растворе микроэлементы, такие как Са, Fе, К, Мg, Сu, способствуют повышению двигательной активности ресничек, активизации репаративных процессов в клетках слизистой оболочки носа и нормализации функции ее желез. Перечисленные микроэлементы содержатся в препаратах, которые готовят из морской воды, стерилизуя ее и доводя содержание солей до изотонической концентрации (Отривин Море, Маример, Аква Марис, Салин и др.), и из воды минеральных источников, обладающей лечебными свойствами (сальц).
Одним из новых препаратов этой группы является Отривин Море, представляющий собой очищенный, обеззараженный изотонический раствор океанической воды из Бретани, добываемой в экологически чистом районе Атлантического океана, богатой натуральными микроэлементами. Он содержит 18 минералов и микроэлементов.
Нами проведено обследование и лечение 50 больных обоего пола в возрасте от 21 года до 43 лет с жалобами на «сухость в носу», вызванную длительным пребыванием в помещениях с сухим и/или разряженным воздухом. В лечении основной группы (25 больных) применялся Отривин Море в виде орошений слизистой оболочки носа 2 раза в день в течение 10 дней, во второй (контрольной) группе (25 больных) в течение 10 дней использовали масляный раствор токоферола ацетата и ретинола пальмитата в виде капель 2 раза в день. Распределение больных по полу и возрасту, а также по выраженности клинических проявлений в обеих группах было сравнимо. Каждые три дня проводилась оценка динамики основных симптомов: затруднение носового дыхания, сухость в полости носа (в том числе субъективные ощущения пациента), характер и количество отделяемого из носа, состояние мукоцилиарного транспорта (сахариновый тест).
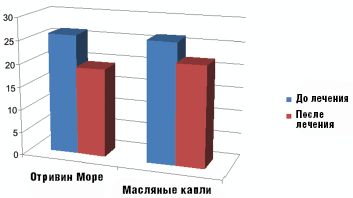
По окончании курса лечения положительный клинический эффект получен у 42 больных, из них 23 из основной и 19 из контрольной группы. У 8 (16%), в том числе 6 из контрольной группы (24%), положительной динамики зарегистрировано не было. В группе больных, получавших Отривин Море, регресс патологических признаков был значительно более быстрым по сравнению с контрольной группой, что подтверждалось результатами исследования мукоцилиарного транспорта. В среднем уменьшение времени мукоцилиарного транспорта на фоне применения препарата составило 6,9 мин. В контрольной группе этот показатель составил 4,3 мин (рис. 2).
Изменение показателей мукоцилиарного транспорта коррелировало с данными риноманометрии и изменениями клинической картины, учитывавшей субъективную симптоматику, оценивавшуюся с использованием опросника для пациентов. Препарат хорошо переносился всеми больными. Кроме того, все больные отметили удобство применения препарата, тогда как использование масляных капель большинством пациентов второй группы (24 человека) характеризовалось как «неудобное».
Таким образом, Отривин Море можно рекомендовать в качестве средства для ухода за полостью носа не только больным с ринитами, в том числе атрофическими, но и как средство ежедневного гигиенического ухода за полостью во время отопительного сезона, а также людям, длительно пребывающим в помещениях с сухим и/или разряженным воздухом.
Литература
О. В. Зайцева, кандидат медицинских наук ФГУ НКЦ оториноларингологии ФМБА России, Москва
Комплексное лечение больных с обострением хронического гипертрофического фарингита
Локальная боль в горле является основным, а иногда и единственным симптомом при целом ряде острых и хронических заболеваний глотки. Сопутствующий синдром интоксикации у пациентов с обострением хронических заболеваний глотки
Локальная боль в горле является основным, а иногда и единственным симптомом при целом ряде острых и хронических заболеваний глотки. Сопутствующий синдром интоксикации у пациентов с обострением хронических заболеваний глотки и связанные с ним повышение температуры тела, слабость и утомляемость могут быть не выражены. Напротив, болевой синдром — интенсивный, длительный, вызывающий затруднения при глотании и зачастую резистентный к самостоятельному лечению — является главной причиной обращения пациентов к врачу.
Терапия болевого синдрома при обострениях хронических воспалительных процессов глотки традиционно сводится к комбинации местных процедур: теплые щелочные полоскания, ингаляции, вяжущие средства, ментол и пр., с антисептическими или антибактериальными препаратами. Кроме этого, в состав антисептических средств некоторыми фармацевтическими производителями включены местноанастезирующие препараты, например ксилокаин.
Назначение средств, обладающих системным обезболивающим, противовоспалительным и жаропонижающим действием (нестероидных противовоспалительных препаратов (НПВП)), при хронических заболеваниях глотки не имеет широкого распространения ввиду невысокой эффективности и невозможности проведения длительного лечения.
Более перспективным представляется использование уникального по составу препарата стрепфен (флурбипрофен), производимого фармацевтической компанией Бутс Хелскэр Интернейшнл (Великобритания).
Флурбипрофен относится к группе неселективных НПВС: ингибируя ферменты циклооксигеназу 1 типа и циклооксигеназу 2 типа, он приводит к угнетению синтеза простагландинов — медиаторов боли и воспаления. Анальгезирующий и противовоспалительный эффект флурбипрофена развивается значительно быстрее по сравнению с воздействием селективных НПВП (ингибиторами циклооксигеназы 2 типа). Данное свойство препарата нашло применение в офтальмологии и ревматологии, где флурбипрофен назначается в наружных формах.
В состав одной таблетки стрепфена входит 8,75 мг флурбипрофена, что вполне достаточно для развития стойкого (до 3 ч) противовоспалительного и анальгетического эффекта уже в течение 15–30 мин. Данной дозировки препарата достаточно для развития выраженного местного действия. В то же время она незначительна для развития системного эффекта и связанных с ним нежелательных побочных действий, свойственных препаратам группы НПВП. Несмотря на высокую абсорбцию и аффинность флурбипрофена к белкам плазмы крови (99%), системные побочные эффекты могут наблюдаться только при превышении рекомендуемой дневной дозы в 3–6 раз.
В проведенном нами исследовании приняли участие 40 пациентов с обострением хронического гипертрофического фарингита: 28 женщин и 12 мужчин в возрасте от 16 до 68 лет. Давность обострения хронического гипертрофического фарингита колебалась во временном промежутке от 5 дней до 3 нед.
Все пациенты предъявляли жалобы на различную по интенсивности боль в горле. У 23 человек боль была постоянной и сопровождалась ощущением «отека слизистых» или ощущением наличия «инородного тела» в горле. У 27 пациентов боль усиливалась при глотании. У основной части больных обращению предшествовало самостоятельно начатое лечение (полоскания горла, местные антисептики, антибактериальная терапия), имевшее незначительный и кратковременный эффект. Почти у половины пациентов (19 человек) в анамнезе была двусторонняя тонзиллэктомия.
Локализация гипертрофического процесса в глотке распределялась следующим образом: гипертрофия боковых столбов глотки — 17 человек, гипертрофия островков лимфоидной ткани на задней стенке глотки (гранулезный фарингит) — 9 человек, небные ниши (у больных с тонзиллэктомией в анамнезе) — 2 человека, смешанной локализации — 12 человек. У 19 пациентов локальное воспаление лимфоидной ткани сочеталось с выраженным катаральным воспалением слизистой ротоглотки.
Критериями исключения из исследования служили: эрозивно-язвенные поражения желудочно-кишечного тракта в фазе обострения; бронхиальная астма, крапивница и ринит, спровоцированные приемом НПВП; выраженные нарушения функции печени и почек; беременность и период лактации; а также повышенная чувствительность к флурбипрофену или компонентам препарата в анамнезе.
Пациенты были разделены на две группы. Всем больным было проведено двукратное прижигание лимфоидных гранул ротоглотки 10%-ным раствором нитрата серебра (ляписа) с интервалом один день (первый и третий день лечения). Половине пациентов (20 человек) — основная группа исследования — назначался стрепфен в дозировке 8,75 мг (1 таблетка) 5 раз в день (с интервалом 3 ч). Больным рекомендовалось рассасывать таблетку в полости рта до полного ее растворения. Лечение начинали за 5–6 ч до первой процедуры прижигания раствором нитрата серебра. Курс лечения составил 3 дня.
Выраженность болевого синдрома в горле пациенты оценивали по визуальной аналоговой шкале (ВАШ) от 0 до 10 баллов. При этом за 0 принимали отсутствие признака, а за 10 — максимальную его выраженность. По окончании лечения пациенты характеризовали общую динамику симптомов (боль в горле, ощущение першения, сухости, чувство инородного тела в горле)(ВАШ 0–10 баллов), а также переносимость препарата (хорошая, удовлетворительная, неудовлетворительная). Врач оценивал гиперемию и степень инфильтрации гранул лимфоидной ткани ротоглотки (0–5 баллов).
У всех получавших стрепфен пациентов уже спустя 10 мин после первого приема препарата отмечалось уменьшение болей в горле, в большинстве случаев значительное, вплоть до полного купирования болевого синдрома (у 5 пациентов). На следующий день после процедуры прижигания (второй день лечения) пациенты обеих групп отмечали уменьшение болей в горле, более значительное в группе пациентов, получавших стрепфен (почти в 2 раза). На третий день лечения, перед вторым прижиганием гранул лимфоидной ткани ротоглотки, также оценивалась выраженность болевого синдрома. Пациенты первой группы, получающие стрепфен, отметили дальнейшее значительное снижение болей в горле по сравнению с предыдущим днем (почти на 50%). Во второй группе пациентов, не получавших стрепфен, также сохранялась незначительная положительная динамика, хотя двое больных отметили некоторое усиление болей, по сравнению с предыдущим днем. На следующий день после второй процедуры прижигания (4-й день наблюдения) больные обеих групп отмечали уменьшение болей в горле по сравнению с предыдущим днем, причем более выраженная положительная динамика наблюдалась во второй группе обследованных — в первой группе пациентов на 4-й день лечения был отменен стрепфен (табл. 1, рис. 1).
 |
| Таблица 1. Динамика интенсивности болей в горле на фоне лечения стрепфеном (группа I) и без применения препарата (группа II) (ВАШ 0–10 баллов) |
 |
| Рисунок 1. Динамика интенсивности болей в горле на фоне лечения стрепфеном (группа I) и без применения препарата (группа II) ВАШ 0–10 баллов) |
При визуальном осмотре ротоглотки пациентов обеих групп выявлялось уменьшение степени инфильтрации лимфоидной ткани, подвергшейся прижиганию нитратом серебра. Положительная динамика этого показателя была несколько выше в группе пациентов, получавших стрепфен (табл. 2, рис. 2). Интенсивность гиперемии гранул лимфоидной ткани ротоглотки, как основного показателя выраженности воспаления, значительно уменьшалась в ходе лечения у пациентов, получавших стрепфен (на 80%) (табл. 3, рис. 3).
 |
| Таблица 2. Динамика степени инфильтрации гранул лимфоидной ткани глотки на фоне лечения стрепфеном (группа I) и без применения препарата (группа II)(ВАШ 0–5 баллов) |
 |
| Рисунок 2. Выраженность инфильтрации лимфоидной ткани после прижиганий на фоне лечения стрепфеном (группа I) и без применения препарата (группа II)(ВАШ 0–5 баллов) |
Учитывая приведенные выше данные, можно с уверенностью утверждать, что применение флурбипрофена в комплексе с химическими прижиганиями 10%-ным раствором нитрата серебра в лечении обострений хронического гипертрофического фарингита, обеспечивает значительно более выраженный регресс симптомов воспаления и обеспечивает высокий анальгетический эффект.
 |
| Таблица 3. Динамика выраженности гиперемии гранул лимфоидной ткани глотки на фоне лечения стрепфеном (группа I) и без применения препарата (группа II)(ВАШ 0–5 баллов) |
 |
| Рисунок 3. Выраженность гиперемии гранул лимфоидной ткани на фоне лечения стрепфеном (группа I) и без применения препарата (группа II)(ВАШ 0–5 баллов) |
Анализ результатов лечения показал, что применение местной противовоспалительной терапии флурбипрофеном значительно повышает эффективность химического прижигания воспаленных гипертрофированных участков лимфоидной ткани ротоглотки. Полная ремиссия после 3 дней лечения достигалась почти в 2 раза чаще по сравнению с контрольной группой (табл. 4).
Переносимость препарата стрепфен в большинстве случаев расценивалась как хорошая. У одного пациента (5%), на второй день лечения отмечалось появление металлического привкуса во рту, что не послужило поводом для отмены препарата.
 |
| Таблица 4. Исход заболевания после курса лечения стрепфеном (группа I) и без применения препарата (группа II) |
Из вышеизложенного можно сделать следующие выводы.
А. В. Божко, кандидат медицинских наук
Городская поликлиника № 124, Москва
Гайморит: симптомы, особенности лечения и правила профилактики
Гайморит – это воспалительный процесс в области гайморовой пазухи, расположенной в толще черепной кости над верхней челюстью, слева и справа. Этот процесс является одной из разновидностей синуситов (это общее название для воспалительных процессов в области придаточных пазух – лобной, гайморовой, решетчатой или клиновидной). Обычно воспалительный процесс затрагивает слизистые оболочки, выстилающие пазухи изнутри, реже затрагиваются более глубокие слои тканей, вплоть до костных структур. Обычно процесс возникает как осложнение вирусных или бактериальных инфекций в области носоглотки и верхних дыхательных путей.
Исходя из причины развития, механизмов формирования и симптомов, гайморит бывает нескольких типов. Выделение каждого из них важно для определения тактики лечения, прогноза и разработки мер профилактики.
Острый – развивается быстро, как осложнение ОРВИ, насморков, простудных заболеваний, воспаления в области корней зубов на верхней челюсти. Возбудители проникают через каналы, соединяющие пазухи с полостью носа с гайморовыми пазухами, размножаются в полости. Тело начинает активно вырабатывать иммунные клетки и слизь, чтобы обезвредить патогенные организмы. Если слизь закупорит проток пазухи, возникает давление на стенки, усиление воспалительного процесса. По мере очищения пазухи от содержимого воспалительный процесс постепенно затухает.
Хронический – воспалительный процесс, который длится более 4 недель, имеет вялое или волнообразное течение, с периодами обострений. Обычно возникает из-за не долеченной острой формы, наличия аденоидов, тонзиллитов, отитов.
Гнойный – обычно становится осложнением острой формы либо обострения хронического процесса, если процесс не лечится, предпринимаются попытки самолечения или пациент переносит инфекцию на ногах. Патогенные бактерии накапливаются в пазухах, в смеси с лейкоцитами образуют гнойное содержимое. Самое опасное осложнение при этой форме – прорыв гноя в полость черепа, поражение костных тканей, мозга.
Двусторонний – одна из тяжелых форм, поражение локализовано сразу в обеих пазухах – левой и правой. Нередко возникает как осложнение инфекций в полости рта и носоглотки, обычно грибковой или бактериальной. Обычно имеет острое течение, редко переходит в хроническую форму.
Аллергическое поражение возникает у пациентов, страдающих от чрезмерно активной реакции иммунной системы на различные вещества. Особенно часто эта форма синусита бывает при поллинозе, круглогодичном рините, реакции на плесень, пылевых клещей.
Катаральный – преимущественно бывает у детей. Он развивается при проникновении в полость пазух патогенных организмов, что формирует отек и раздражение слизистых. Считается самой легкой формой болезни, проходящей при активном лечении без осложнений и последствий.
Полипозная форма формируется при образовании полипозных разрастаний слизистых из-за чрезмерно быстрого деления клеток. Рост полипов могут провоцировать инфекции, травмы, велика роль наследственности.
Одонтогенный – формируется как результат серьезных проблем зубов, особенно 4-6 зуба на верхней челюсти, корни которых расположены в непосредственной близости от пазухи. Если возникают проблемы в области корней этих зубов, воспаление и нагноение может переходить на пазуху, она заполняется секретом и воспаляется.
Причины
Придаточные пазухи, включая гайморовы, созданы как естественный барьер на пути инфекций, фильтр для различных опасных веществ в воздухе. Они помогают согревать воздух, увлажнять его и очищать от примесей перед попаданием в гортань, и ниже по респираторному тракту. Основная причина воспаления и появления признаков гайморита – это проникновение бактерий, грибков или вирусов, аллергенов. Реже инфекция попадает с током крови из других, отдаленных очагов.
Нарушать работу пазух могут патологии иммунной системы, частые ОРВИ, респираторная форма аллергии, носительство патогенных бактерий в носоглотке (стафило-, стрепто- или менингококк).
Среди ключевых причин, которые могут привести к развитию гайморита, можно выделить:
Осложнения
Не все люди знают, как начинается гайморит, поэтому многие принимают симптомы за тяжелую простуду и лечатся самостоятельно. Это может привести к определенным осложнениям, отдаленным последствиям. Среди ключевых осложнений можно выделить поражения бронхов и распространение инфекции на легкие, развитие отитов (поражение среднего уха), переход болезни в хроническую форму.
Тяжелый и запущенный, своевременно не вылеченный гайморит может привести к воспалению внутренних органов – сердца, глаз, почек, поражению суставов и мозга, его оболочек. Если образуются гнойные полости в гайморовых пазухах, возможен прорыв гноя в кровь (возникает сепсис), проникновение его в соседние пазухи с развитием пансинусита, воспаление мозговых оболочек с явлениями менингита. Всех этих осложнений можно избежать при полноценном лечении гайморита под руководством лор-врача.
Симптомы и диагностика
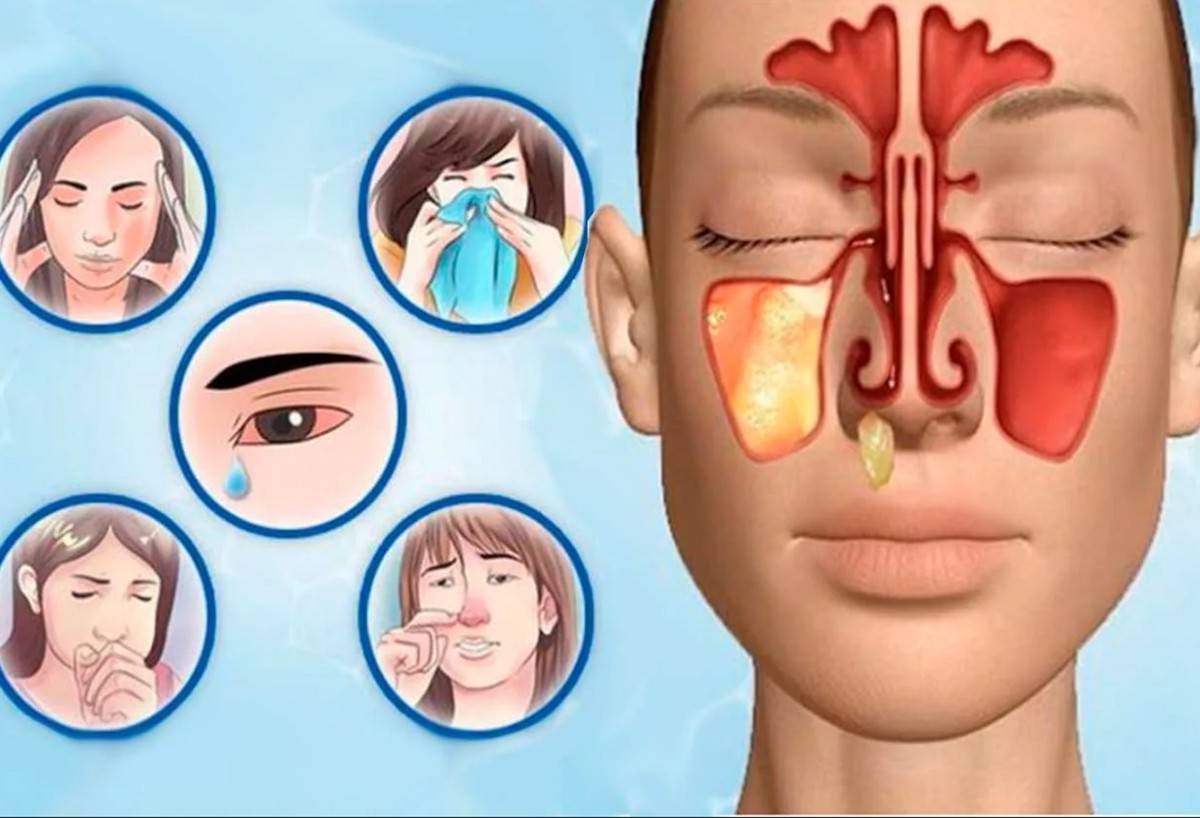
Конечно, при развитии гайморита нужно немедленно обращаться к врачу, но как понять, что гайморит начался? Начальные признаки неспецифичные – это повышение температуры от незначительной до высокой, сильная слабость, заложенность носа или обильные густые выделения, болезненность в проекции пазух или в области лица.
Боль при гайморите может быть различной – от тупой, давящей до сильной, мучительной. Она локализуется в подглазничной области, может отдавать в область переносицы, лобную зону или верхние зубы. При надавливании на область пазух или наклонах головы вперед она усиливается, распространяясь по подглазничной области. Могут краснеть и отекать веки.
Врачи отмечают некоторые особенности того, как проявляется болезнь в определенных возрастных группах. Так, у взрослых самым ключевым признаком могут быть болевые ощущения, головная боль, нарушение восприятия запахов. Может меняться голос, он становится гнусавым, нос сильно заложен, выделяется полупрозрачная или желто-зеленая слизь. Высокая лихорадка типична для острой формы, при хроническом или аллергическом гайморите болезнь может протекать без температуры.
На фоне поражения пазух возможно слезотечение, неприятный привкус во рту, слабость, постоянное утомление, нарушения аппетита, расстройства сна, ознобы и приступы кашля.
Заразен ли гайморит? Само по себе воспаление – это результат влияния патогенных факторов, и это не заразно. Бактерии или вирусы, которые спровоцировали заболевание, могут передаваться от человека к человеку, но не обязательно вызовут поражение пазух.
Диагноз гайморита ставит лор-врач после проведения ряда тестов и осмотра пациента. Важно подробно рассказать, как началось заболевание, какие жалобы были ранее и имеются в данный момент. Врач осмотрит полость носа и глотку, прощупает проекцию пазух, определяя болезненность.
Дополнительно могут понадобиться КТ или МРТ придаточных пазух, рентгенограмма, УЗИ исследование, эндоскопия носоглотки, при необходимости – биопсия полипозных образований. Назначаются анализы крови, посевы отделяемой из носа слизи для определения флоры, чтобы подобрать необходимые препараты.
Как лечить у взрослого
Терапия болезни должна быть комплексной. Она направлена на борьбу с инфекцией, устранение воспаления, налаживание оттока слизи из пазух и улучшение носового дыхания. В неосложненных случаях возможно лечение гайморита дома под постоянным контролем оториноларинголога. В тяжелых случаях и при необходимости хирургического лечения пациент госпитализируется в стационар.
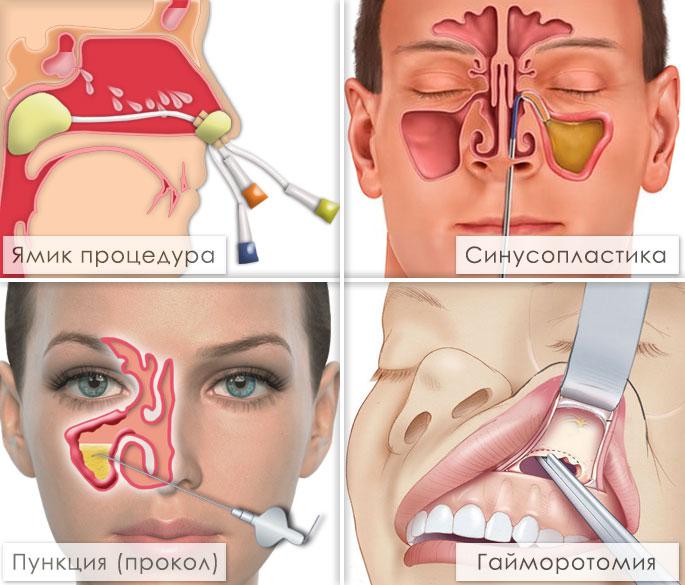
Возможно консервативное лечение с назначением антибактериальных препаратов, противовоспалительных средств, антигистаминных препаратов и различных капель, спреев для носа. Также применяют пункционное лечение или хирургические вмешательства. Выбор зависит от возраста пациента, вида патологии, тяжести состояния и возможных осложнений.
Многим пациентам назначают пункции (с местным обезболиванием) – они помогают удалить гнойное содержимое, помочь в оценке характера воспаления, плюс приносят существенное облегчение. После удаления содержимого пазухи промывают физраствором или фурациллином, вводят растворы антибиотиков и противовоспалительные препараты. Минус подобной тактики – не всегда достаточно одного прокола, поэтому требуется курс процедур в течение нескольких недель. Метод достаточно неприятный, имеет ряд противопоказаний и осложнений, процедура болезненна как во время прокола, так и после него.