Фрагмин или гепарин что лучше
Фрагмин или гепарин что лучше
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Ведение беременных с тромбофилией
Журнал: Российский вестник акушера-гинеколога. 2013;13(4): 79-81
Краснопольский В. И., Петрухин В. А., Мельников А. П. Ведение беременных с тромбофилией. Российский вестник акушера-гинеколога. 2013;13(4):79-81.
Krasnopol’skiĭ V I, Petrukhin V A, Mel’nikov A P. Management of pregnant women with thrombophilia. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(4):79-81.
Московский областной НИИ акушерства и гинекологии
На основании результатов опубликованных работ и трехлетнего опыта Московского областного НИИ акушерства и гинекологии (проведено наблюдение 570 беременных с тромбофилией, обусловленной в основном сочетанием гетерозиготного носительства генов метилентетрагидрофолатредуктазы и ингибитора активатора плазменного I типа) представлена тактика ведения беременных, страдающих тромбофилией. Приведены показания к обследованию пациенток, методы диагностики тромбофилий. Обращено внимание на особенности лечения беременных как препаратами нефракционированного гепарина, так и низкомолекулярными гепаринами, предотвращающими тяжелейшие осложнения.
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Понятие «тромбофилия» объединяет все наследственные и приобретенные нарушения гемостаза, при которых возникает предрасположенность к раннему проявлению и рецидивированию тромбозов, тромбоэмболии, ишемии и инфарктов органов [2]. Для практических целей очень важно выделять врожденную тромбофилию, поскольку речь идет о тромбогенных факторах, сопровождающих пациентов на протяжении всей жизни. Врожденной тромбофилией называется склонность к тромбозу в силу врожденных предрасполагающих факторов [13], независимо от причины. На протяжении многих лет к приобретенным формам тромбофилии относили антифосфолипидный синдром (АФС), однако в настоящее время имеются данные о генетической природе происхождения АФС [5], что, впрочем, не мешает относить это состояние по-прежнему к тромбофилиям. У пациенток с тромбофилией тромботические осложнения возникают в ситуациях, когда у других людей подобные осложнения не наблюдаются: при назначении пероральных контрацептивов, при беременности, при неосложненных хирургических операциях, при длительных путешествиях и сохраненной неудобной позе и т.д.
Клиническими проявлениями тромбофилии служат тромботические осложнения или акушерские потери, о чем имеются соответствующие публикации в медицинской литературе [1, 3, 11]. Этим тромбофилия отличается от простого полиморфизма генов, число различных комбинаций которых превышает 1,5 млн. Поэтому полиморфизм генов фибриногена, фактора VIII (FVIII), фактора XIII (FXIII) и др. следует считать простым полиморфизмом генов, поскольку к настоящему времени не доказана их связь с клинической патологией.
К врожденным тромбофилиям относятся следующие состояния:
— дефицит содержания белков-антикоагулянтов: антитромбина III (АТ III) ниже 70% (по активности), протеина С (ПС) ниже 65%, протеина S (ПS) ниже 55%;
— антифосфолипидный синдром (АФС), диагностированный согласно современным диагностическим критериям 2006 г. [10];
АФС может быть диагностирован в случае, если имеются 1 клинический и 1 лабораторный критерии. Клинические критерии:
1. Артериальный или венозный тромбоз без воспаления сосудистой стенки.
2. Патология беременности:
а) одна гибель плода после 10 нед беременности и более;
б) эклампсия, гестоз или фетоплацентарная недостаточность в сроке менее 34 нед беременности;
в) 3 самопроизвольных аборта и более в сроки менее 10 нед беременности без анатомических, гормональных, хромосомных нарушений.
1. Дважды положительный тест на волчаночный антикоагулянт с интервалом 12 нед;
2. Антикардиолипиновые антитела в высоких титрах (более 40 ед.), определенные методом ELISA с интервалом 12 нед;
3. Наличие антител к β-2-гликопротеину-I.
Следует помнить, что АФС не должен диагностироваться в тех случаях, когда временной интервал между клиническими и лабораторными проявлениями составляет менее 12 нед и более 5 лет, а поверхностные венозные тромбозы не включаются в критерии диагностики АФС.
Показания к обследованию пациенток
Обследование пациенткам назначается при возникновении идиопатических тромбозов, инсультов, инфарктов, наличии выкидыша, тяжелого гестоза, преждевременной отслойки нормально расположенной плаценты, преждевременных родов в сроках до 34 нед гестации, синдрома задержки роста плода в анамнезе, тромбозов на фоне приема пероральных контрацептивов или заместительной гормональной терапии (ЗГТ). На основании 3-летнего опыта Московского областного НИИ акушерства и гинекологии (проведено наблюдение 570 беременных с тромбофилией, в основном обусловленной сочетанием гетерозиготного носительства генов МТГФР и PAI-I), считаем целесообразным обследование для выявления тромбофилии при осложненном течении настоящей беременности даже в отсутствие акушерских осложнений в анамнезе, что позволяет обосновать лечение антикоагулянтами и предупредить прогрессирование осложнений.
Диагностика тромбофилий
Обследование на тромбофилию включает:
— определение процента активности белков-антикоагулянтов: АТ III, ПС, ПS;
— исследование полиморфизма генов: FV Лейден, FIIG20210A, МТГФРС677Т, PAI-I;
— определение содержания гомоцистеина натощак;
— исследование волчаночного антикоагулянта, антител к кардиолипинам и антител к β2-гликопротеину I.
Лечение беременных с тромбофилиями
Пациенток следует делить на две группы:
— имеющих акушерские потери в анамнезе;
— имеющих тромботические осложнения в анамнезе и при настоящей беременности.
При наличии акушерских потерь в анамнезе лечение начинают с ранних сроков гестации для обеспечения адекватной плацентации с 4-5 нед до 34 нед беременности, обычно НФГ подкожно по 5000 ЕД 2 раза в день с интервалом 12 ч. Для исключения гепарининдуцированной тромбоцитопении на 4, 8 и 15-й дни лечения НФГ следует определять число тромбоцитов в клиническом анализе крови. После 34 нед гестации в плаценте наступают естественные инволютивные изменения, и применение гепарина не улучшает исход беременности, теоретически увеличивая риск геморрагических осложнений. В виде ингаляций гепарин применяется в дозировке 500-700 ЕД/кг через 12 ч. При большой массе пациентки (более 90 кг) возможно использование гепарина в той же дозе через 8 ч.
При наличии тромботических осложнений у пациентки с тромбофилией при настоящей беременности и в анамнезе после лечения у сосудистых хирургов проводится терапия НФГ по 5000 ЕД через 12 или 8 ч без лабораторного контроля. Ввиду роста числа тромботических осложнений у беременных в III триместре и в послеродовом периоде, особенно в первые 4 нед, целесообразно назначение режима 5000 ЕД 3 раза в день. Применение НФГ в суточной дозе до 20 000 ЕД не требует лабораторного контроля. Родоразрешение, операции и пункция перидурального пространства безопасны, если показатели тромбинового и активированного частичного тромбопластинового времени нормальны, а количество тромбоцитов у пациентки соответствует норме [12].
При лечении НМГ беременных достижение уровней профилактического лечения (0,3-0,5 ЕД активности анти-Xа-фактора) затруднено ввиду увеличения скорости клубочковой фильтрации и объема распределения по мере прогрессирования беременности, поэтому рекомендованный уровень активности анти-Ха-фактора может быть достигнут только при индивидуальном подборе дозы пациентке [4, 8]. Нередко лечение НМГ не предотвращает развития гипотрофии плода, и применение НФГ является предпочтительным.
Лечение пациенток с тромботическими осложнениями требует минимального перерыва в использовании препаратов на период родоразрешения. При проведении программированных родов и планового кесарева сечения последняя инъекция гепарина проводится накануне вечером, до 15 ч следующего дня проводится родоразрешение и через 3 ч после родов возобновляется гепаринотерапия по 5000 ЕД через 12 ч в течение всего послеродового периода. Назначение полной терапевтической дозы гепарина возможно через сутки после родов и контролируется по уровню активированного частичного тромбопластинового времени для НФГ и уровню анти-Ха-фактора для НМГ. Поскольку при нормально протекающей беременности и ее осложнениях содержание D-димера повышено, этот показатель не может быть использован ни в диагностических целях, ни для контроля эффективности лечения НМГ [9].
На фоне профилактического лечения гепарином пациенток с тромбофилией, как правило, не требуется назначения других препаратов, активно действующих на свертывающую систему крови. Назначение прочих лекарственных веществ не противопоказано.
Подобная практика ведения беременных с тромбофилией позволяет добиться благоприятного исхода беременности.
Применение аспирина или гепарина или и того и другого для улучшения исходов беременности у женщин с персистенцией антифосфолипидных антител и привычным невынашиванием беременности
Актуальность: Аспирин и гепарин широко используются в качестве профилактической стратегии для снижения высокого риска привычного невынашивания беременности у женщин с антифосфолипидными антителами (АФА). Этот обзор заменяет предыдущий, устаревший обзор, в котором оценивали все потенциальные методы лечения для привычного невынашивания беременности у женщин с АФА. В настоящем обзоре основное внимание уделяется более узкой области применения, поскольку в настоящее время клиническая практика ограничивается использованием аспирина или гепарина или обоих препаратов у женщин с АФА в попытке уменьшить осложнения беременности.
Цель исследования: Оценить влияние применения аспирина или гепарина, или того и другого для улучшения исходов беременности у женщин с персистенцией (наличием в двух отдельных пробах) АФА, либо с волчаночным антикоагулянтом (ВА), с антикардиолипином (АКЛ) или с антителами к aß2-гликопротеину-I (aß2GPI) или с их комбинацией, а также с привычным невынашиванием беременности (два или более случая, которые не обязательно должны быть последовательными).
Методы поиска: Был выполнен поиск в электронных базах данных Кокрановского реестра по беременности и родам, ClinicalTrials.gov, международной платформе реестра клинических исследований ВОЗ (ICTRP) (3 июня 2019 г.) и библиографических списках извлеченных исследований. Там, где это было необходимо, мы пытались связаться с авторами исследований.
Критерии включения: В обзор включали рандомизированные, кластерно-рандомизированные и квази-рандомизированные контролируемые исследования, оценивающие влияние применения аспирина, гепарина (либо низкомолекулярного гепарина (НМГ), либо нефракционированного гепарина (НФГ)) или комбинации аспирина и гепарина по сравнению с отсутствием лечения, с применением плацебо или других препаратов на исходы беременности у женщин с персистенцией АФА и привычным невынашиванием беременности. Были рассмотрены все схемы лечения.
Сбор и анализ данных: Два автора обзора независимо оценивали результаты исследований на предмет соответствия критериям включения и систематической ошибки. Два автора обзора независимо друг от друга извлекали данные и проверяли их на точность, а достоверность доказательств оценивали с использованием системы GRADE.
В целом качество доказательства было низким или очень низким из-за небольшого числа женщин в исследованиях и систематической ошибки. Доза и тип гепарина и аспирина различались в разных исследованиях. Одно исследование сравнивало применение только аспирина с использование плацебо; ни одно исследование не сравнивало применение только гепарина с использованием плацебо, и не было ни одного исследования, в котором не было группы, принимающей препараты сравнения во время беременности; пять исследований изучали эффективность использования гепарина (либо НФГ, либо НМГ) в сочетании с аспирином по сравнению с применением только аспирина; одно исследование сравнивало применение НМГ с использованием аспирина; в двух исследованиях сравнивали комбинацию НМГ плюс аспирин с комбинацией НФГ плюс аспирин; в двух исследованиях оценивали комбинацию различных доз гепарина в сочетании с аспирином. Во всех исследованиях использовали применение низких доз аспирина. Аспирин по сравнению с плацебо.
Мы не уверены, оказывает ли аспирин какое-либо влияние на частоту живорождения по сравнению с применением плацебо (отношение рисков (ОР) 0,94; 95% доверительный интервал (ДИ) 0,71-1,25; 1 исследование; 40 женщин; доказательства очень низкого качества). Мы не уверены, оказывает ли применение аспирина какое- либо влияние на риск развития преэклампсии, прерывания беременности, преждевременных родов с рождением живого плода, задержки внутриутробного роста или неблагоприятных событий у ребенка по сравнению с применением плацебо. Мы не уверены, оказывает ли применение аспирина какое-либо влияние на побочные явления (кровотечение) у матери по сравнению с использованием плацебо (ОР 1,29; 95% ДИ 0,60-2,77; 1 исследование; 40 женщин).
Качество доказательств этих результатов очень низкое из-за неточности, из-за малого числа включенных женщин и широкого 95%-ного ДИ, а также из-за систематической ошибки. Во включенных исследованиях не были зарегистрированы венозная тромбоэмболия и артериальная тромбоэмболия. Гепарин плюс аспирин по сравнению с применением только аспирина. Применение гепарин плюс аспирин может увеличить частоту живорождения (ОР 1,27; 95% ДИ 1,09- 1,49; 5 исследований; 1295 женщин; доказательства низкого качества). Мы не уверены, оказывает ли применение гепарин плюс аспирин какое-либо влияние на риск развития преэклампсии, преждевременных родов с рождением живого плода или задержки внутриутробного роста плода по сравнению с применением только аспирина из-за систематической ошибки и неточности вследствие небольшого количества включенных женщин и широкого 95%-ного ДИ. Мы не уверены, оказывает ли применение гепарин плюс аспирин какое-либо влияние на побочные явления (кровотечение) у матери по сравнению с применением только аспирина (ОР 1,65; 95% ДИ 0,19-14,03; 1 исследование; 31 женщина). Ни у одной женщины из группы «гепарин плюс аспирин» или группы «только аспирин» не было гепарин- индуцированной тромбоцитопении, аллергических реакций или венозной или артериальной тромбоэмболии. Точно так же ни у одного ребенка не было врожденных пороков развития. Применение гепарин плюс аспирин может уменьшить риск прерывания беременности (ОР 0,48; 95% ДИ 0,32-0,71; 5 исследований; 1295 женщин; доказательства низкого качества). При сравнении применения НМГ плюс аспирин и использования только аспирина общее ОР для частоты живорождения составило 1,20 (95% ДИ 1,04-1,38; 3 исследования; 1155 женщин). При сравнении применения НФГ плюс аспирин с использованием только аспирина ОР частоты живорождения составило 1,74 (95% ДИ 1,28-2,35; 2 исследования; 140 женщин).
Заключение авторов: Комбинация гепарина (НФГ или НМГ) и аспирина в течение беременности может увеличить частоту живорождения у женщин с персистенцией АФА по сравнению с применением только аспирина. Наблюдаемый положительный эффект гепарина был обусловлен одним большим исследованием, в котором применение НМГ плюс аспирин сравнивали с применением только аспирина. Во включенных исследованиях побочные явления не были зарегистрированы или были редкими. Для дальнейшей оценки потенциальных рисков и преимуществ этой стратегии лечения, особенно среди женщин с АФА и привычным невынашиванием беременности, необходимы дополнительные исследования, чтобы достичь консенсуса относительно идеальной профилактики привычного невынашивания беременности на основе профиля риска.
Низкомолекулярные гепарины в современной системе управления свертываемостью крови
Цель обзора: анализ современных принципов применения низкомолекулярных гепаринов (НМГ) в различных клинических ситуациях.
Основные положения. Современный арсенал антикоагулянтов позволяет использовать различные по механизму действия препараты для профилактики и долгосрочной терапии тромботических осложнений. В целях длительной профилактики тромбозов механических протезов клапанов сердца обязательным остается применение ингибиторов витамина К.
НМГ являются эффективными препаратами для рутинной профилактики венозных тромбозов в хирургии и ортопедии, а также для их долгосрочной терапии. Оригинальные НМГ — предпочтительные антикоагулянты у беременных.
Парнапарин (Флюксум) обладает наибольшей средней молекулярной массой и наиболее высокой относительной антитромбиновой активностью среди НМГ, применяющихся в отечественной практике. Нефракционированный гепарин остается незаменимым препаратом для терапии тяжелых тромбозов глубоких вен, тромбоэмболии легочной артерии, а также для обеспечения экстракорпоральной циркуляции крови.
Заключение. Традиционно НМГ рассматривают как множество однотипных взаимозаменяемых препаратов. Однако их относительная антитромбиновая активность серьезно различается в зависимости от средней молекулярной массы (прямая зависимость). Наиболее активным ингибитором тромбина из числа НМГ, доступных в отечественной клинической практике, является Флюксум (парнапарин). Высокий уровень безопасности и эффективность этого препарата делают целесообразным его широкое клиническое применение.
Кричевский Лев Анатольевич — д. м. н., заведующий отделением анестезиологии и реаниматологии № 4 ГБУЗ «ГКБ № 15 им. О. М. Филатова ДЗМ»; ведущий научный сотрудник ФГБНУ «НИИОР им. В. А. Неговского» ФАНО. 107031, г. Москва, ул. Петровка, д. 25, стр. 2. E-mail: levkrich72@gmail.com
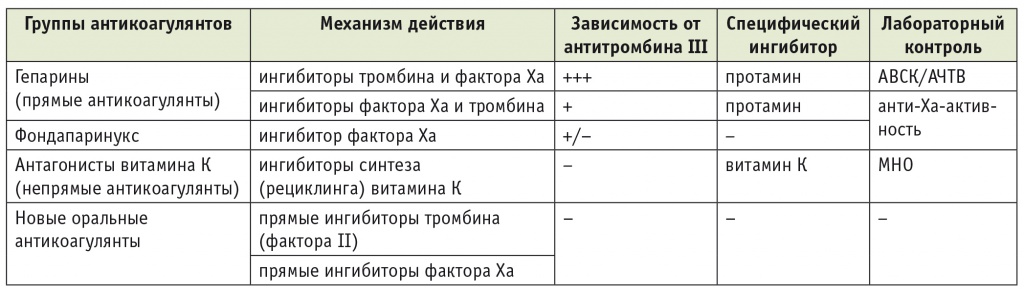
Таблица 1
Фармакодинамические и клинические особенности антикоагулянтов, распространенных в современной клинической практике
Примечание. АВСК — активированное время свертывания крови; АЧТВ — активированное частичное тромбопластиновое время; МНО — международное нормализованное отношение.
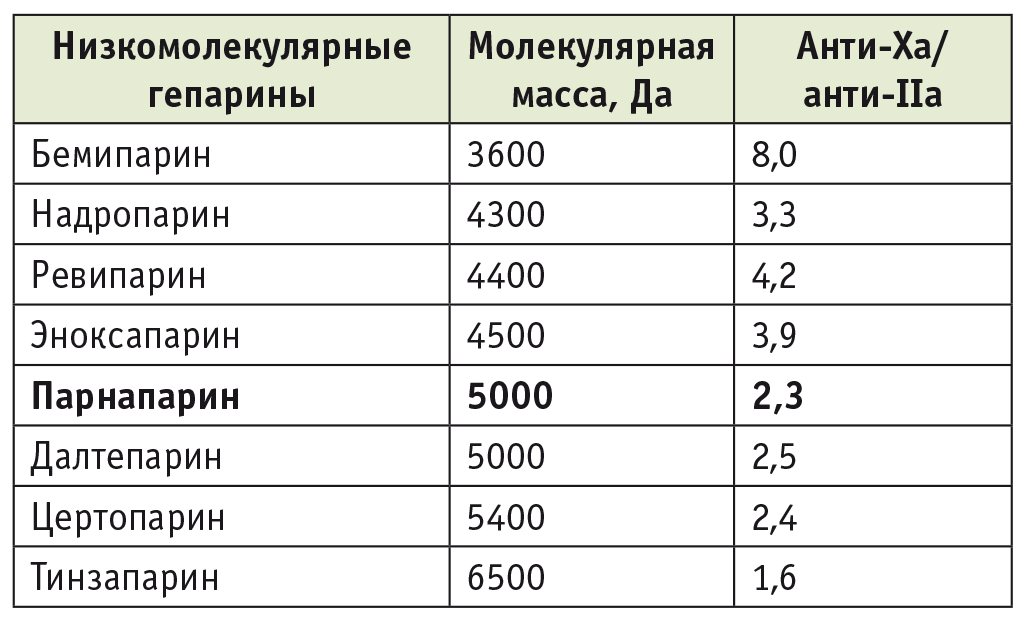
Создание фракционированных, или низкомолекулярных, гепаринов сделало возможным более удобное и безопасное применение прямых антикоагулянтов. Эти препараты гарантированно всасываются при подкожном введении. В связи с их ослабленным или практически отсутствующим влиянием на тромбин кровотечения при назначении НМГ достаточно редки. Во многих клинических ситуациях НМГ не требуют лабораторного контроля. Вполне закономерно, что эти препараты прочно заняли нишу рутинной профилактики тромбозов у самых разных категорий больных, прежде всего хирургических, ортопедических пациентов и больных, находящихся в отделениях реанимации. Подчеркнем также сравнительную безопасность длительного использования НМГ у беременных. Все это привело к достаточно формальному, упрощенному отношению клиницистов к НМГ как к однородной группе фармакологических средств, которые хороши для рутинной профилактики тромбозов, но недостаточно эффективны для лечения серьезных тромботических осложнений. Однако реальная ситуация не совсем такова. Разброс молекулярной массы НМГ достаточно велик — от 3 до 7 кДа. В свою очередь, молекулярная масса (или длина гепариновой цепочки) определяет выраженность ингибирующего влияния препарата на тромбин. Поскольку анти-Xа-активность является стабильным свойством всех НМГ, различную выраженность ингибирования тромбина выражают в виде отношения анти-Xа/анти-IIа. Чем оно меньше, тем антитромбиновая активность выше ( табл. 2 ).
Таблица 2
Молекулярная масса и относительная антитромбиновая активность низкомолекулярных гепаринов
Таким образом, особенности механизма действия того или иного антикоагулянта определяют целесообразность его применения в различных клинических ситуациях. Рассмотрим возможности эффективного и дифференцированного применения традиционной группы препаратов — НМГ.
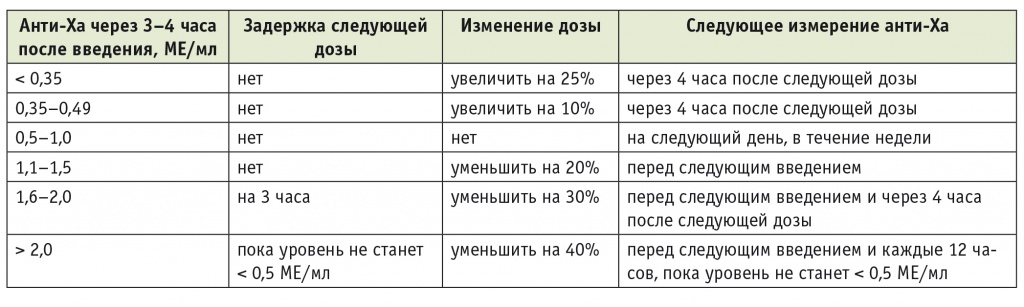
Таблица 3
Контроль анти-Xа-активности при терапии низкомолекулярными гепаринами [3]
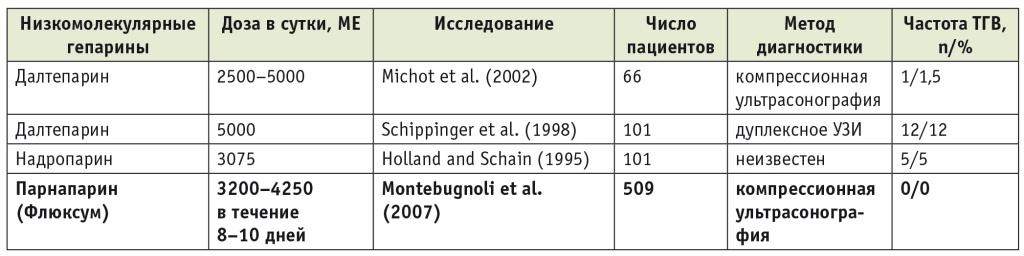
Таблица 4
Результаты применения низкомолекулярных гепаринов
Примечание. ТГВ — тромбоз глубоких вен.
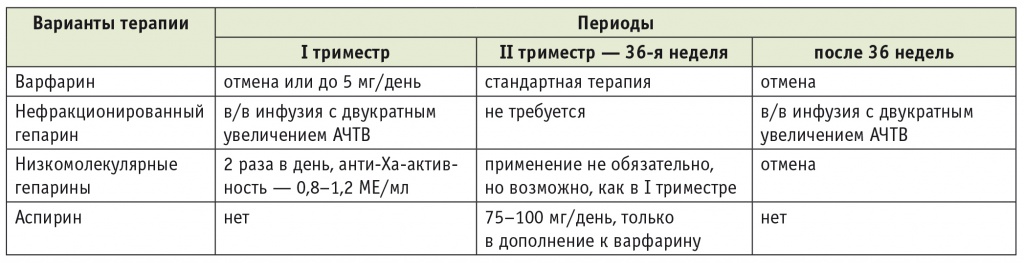
Таблица 5
Профилактика тромбоза механических протезов клапанов сердца во время беременности
Примечание. АЧТВ — активированное частичное тромбопластиновое время.
Таким образом, НМГ прочно занимают свою нишу в общем спектре антикоагулянтных средств, прежде всего при профилактике тромботических осложнений, лечении различных форм тромбофлебитов и, конечно, у беременных. Фармакологическая группа НМГ не является однородной. Важнейшим отличительным свойством препаратов является их антитромбиновая активность, прямо зависящая от молекулярной массы и обратно выражаемая величиной анти-Xа/анти-IIа.
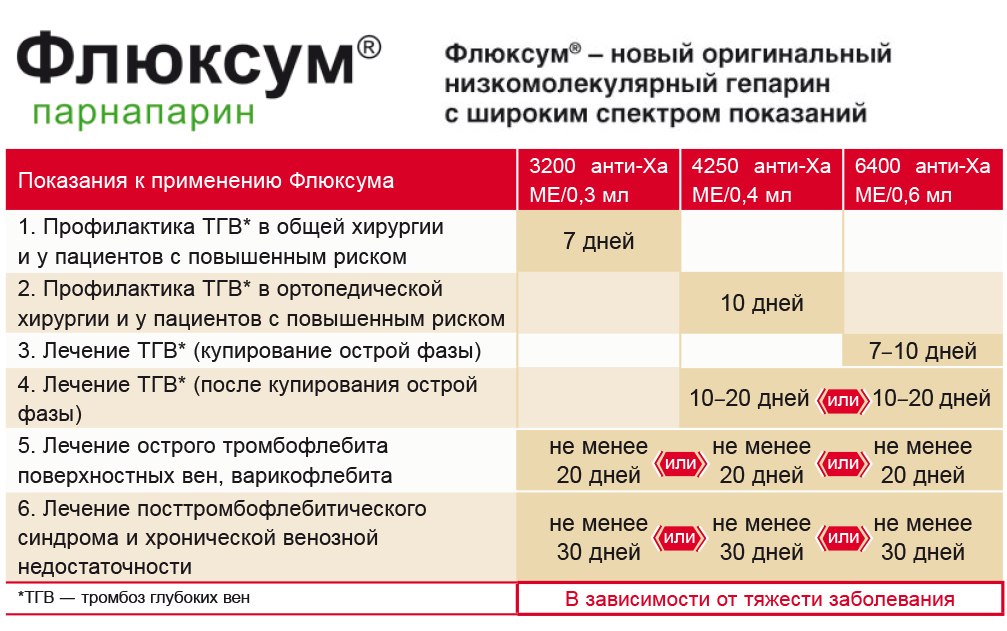
Рис. Тактика применения препарата парнапарин (Флюксум)
Несмотря на создание все новых средств для антикоагулянтной терапии, низкомолекулярные гепарины (НМГ) остаются препаратами выбора для рутинной профилактики и долгосрочного лечения тромбозов. Именно эта группа антикоагулянтов предпочтительна у такой сложной категории пациентов, как беременные. Традиционно НМГ рассматривают как множество однотипных взаимозаменяемых препаратов. Однако их относительная антитромбиновая активность серьезно различается в зависимости от средней молекулярной массы (прямая зависимость). Наиболее активным ингибитором тромбина из числа НМГ, доступных в отечественной клинической практике, является парнапарин (Флюксум). Высокий уровень безопасности и эффективность этого препарата делают целесообразным его широкое клиническое применение.
АНТИКОАГУЛЯНТЫ, ДЕЙСТВУЮЩИЕ НА ПРОЦЕСС ТРОМБООБРАЗОВАНИЯ
Ч. 1 Тромбоэмболия легочной артерии и тромбоз глубоких вен — самые распространенные причины смертности и инвалидности при сердечно–сосудистых заболеваниях.
Преферанская Нина Германовна
Доцент кафедры фармакологии образовательного департамента Института фармации и трансляционной медицины Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Единственным доказательным по эффективности методом профилактики тромбозов и тромбоэмболических осложнений является применение антикоагулянтов, изменяющих вязкость крови, способствующих разжижению и повышению текучести крови. Стандартная схема лечения рекомендует начинать использовать антикоагулянты сразу после диагностирования таких заболеваний. Применение антикоагулянтов с момента появления симптомов позволяет предотвратить формирование сгустка крови, его увеличение и закупоривание сосудов. Большинство антикоагулянтов оказывают влияние не на сам кровяной сгусток, а на активность свертывающей системы крови.
Низкомолекулярные гепарины для парентерального введения (селективные ингибиторы фактора Ха)
Низкомолекулярные гепарины состоят из фрагментов гепарина с молекулярной массой от 2000 до 10 000 (в среднем 4000–5000 Да), получают путем фракционирования, гидролиза или деполимеризации обычного нефракционированного гепарина. В отечественной практике используют следующие препараты низкомолекулярных (фракционированных) гепаринов:
Эти препараты неоднородны по своему составу, т.к. содержат разные фракции гепарина и отличаются друг от друга антикоагулянтной активностью, физико-химическими и фармакокинетическими свойствами, но обладают антикоагулянтным и антитромботическим действием. Антикоагулянтный эффект продолжительный и зависит от действующего вещества (от 6 до 18 час.). При выборе антикоагулянта не учитывается возраст больных, тяжесть сопутствующих заболеваний, уровень тромбоза и степень нарушения внутрисердечной гемодинамики.
Низкомолекулярные гепарины блокируют процесс свертывания крови, угнетая в большей степени преимущественно активность фактора Ха, некоторые из них незначительно оказывают влияние на снижение образования протромбиназы (активатора протромбина) и активность фактора IIа. Протромбиназа (prothrombinase complex) — сложный комплекс, состоящий из активированных факторов свертывания Ха и Vа и др. факторов, который формируется на поверхности мембран тромбоцитов в присутствии ионов кальция. В процессе свертывания крови образуется как тканевая, так и кровяная протромбиназа. При применении антикоагулянтов количество образовавшейся протромбиназы очень мало, оно недостаточно для перевода протромбина в тромбин.
Прямые антикоагулянты катализируют образование комплекса с антитромбином III, тромбином и др. активированными факторами. Образуется тройной комплекс с антитромбином III, они необратимо изменяют его конфигурацию и сокращают период его полужизни до 3–6 часов. Связывание с антитромбином III усиливает угнетающее действие на активность фактора Ха, тем самым снижается переход протромбина в тромбин. В результате нейтрализации происходит ингибирование тромбина и формирование тромбов. В отличие от гепарина низкомолекулярные гепарины не связываются с фактором фон Виллебранда, легко инактивируются на поверхности тромбоцитов, что снижает риск геморрагических осложнений, реже развивается тромбоцитопения и остеопороз.
Низкомолекулярные гепарины, так же, как и гепарин, действуют на факторы свертывания через антитромбин III, но отличаются от гепарина следующими свойствами:
Низкомолекулярные гепарины способны блокировать каскад коагуляции на более ранних его этапах, обладают быстрым, выраженным, стабильным и более предсказуемым антикоагулянтным эффектом. Они имеют меньшее сродство к фактору 4 тромбоцитов и поэтому реже, чем стандартный гепарин, вызывают побочные эффекты. Фактор 4 тромбоцитов — антигепариновый, обладает выраженной антигепариновой активностью, устраняет эффект гепарина, его влияние на образование протромбиназы и на увеличение проницаемости сосудов. Антигепариновой активностью обладают также разрушенные и интактные тромбоциты, что связано со способностью тромбоцитов адсорбировать гепарин и его фрагменты и выделять фактор 4 тромбоцитов в плазму крови.
Применяют низкомолекулярные гепарины в основном для профилактики и лечения тромбоза глубоких вен (после хирургического вмешательства), для предупреждения тромбоэмболии легочной артерии. Низкомолекулярные гепарины показаны при нестабильной стенокардии, остром ишемическом инсульте и инфаркте миокарда, для профилактики и терапии тромбозов в акушерско–гинекологической практике, колоректальной и ортопедической хирургии. Их используют для профилактики свертывания крови в системе экстракорпорального кровообращения при длительном проведении гемодиализа или гемофильтрации.
Важно! При применении низкомолекулярных гепаринов могут возникать кровотечения. В первые дни лечения возможна умеренная тромбоцитопения. Низкомолекулярные гепарины в ряде случаев повышают активность печеночных ферментов, могут вызвать аллергические реакции и при длительном применении возникает опасность развития остеопороза. При передозировке протамин сульфат полностью не устраняет эффекты низкомолекулярных гепаринов (≤ 60%). Противопоказанием к их применению является повышенная чувствительность к тому или иному препарату, тяжелая почечная дисфункция, внутричерепное кровоизлияние, беременность, кормление грудью и др.
Формы выпуска низкомолекулярных гепаринов – специальные шприцы-дозаторы разового использования (в блистере по 2 шприца одноразового применения, упак. — 10 шт.).
Доза действующего вещества выражается в международных единицах (МЕ) с активностью подавления фактора Ха в плазме крови и выпускается в виде раствора для инъекций в мл.
Выпускается в растворе для п/к и в/в введения 2,5 м/0,5 мл. 0,5 мл помещают в специальный шприц с иглой вместимостью 1 мл, снабженный автоматической системой безопасности. После подкожной инокуляции Фондапаринукс полностью всасывается из места инъекции, выводится почками в течение 3 суток.
Важно! Применяют с осторожностью при повышенном риске развития кровотечений и гиперчувствительности к препарату. Препарат не рекомендуется смешивать с другими медикаментами.
ПРЯМЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ АНТИКОАГУЛЯНТЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ
К пероральным антикоагулянтам, прямым ингибиторам фактора свертывания крови Ха (активированного фактора Стюарта–Прауэра) относят Апиксабан (Эликвис), Ривароксабан (Ксарелто).
Апиксабан (Эликвис, тб., покр. обол., 2,5 мг и 5 мг) является мощным прямым ингибитором фактора свертывания крови Xa. Он избирательно и обратимо блокирует активный центр фермента, угнетает активность протромбиназы. Для реализации его антитромботического действия не требуется наличия антитромбина III. В результате ингибирования фактора свертывания крови Xa изменяются значения показателей системы свертывания крови: удлиняется активированное тромбопластиновое время и протромбиновое время. Препарат опосредованно влияет на агрегацию тромбоцитов, оказывая антиагрегантный эффект. Апиксабан быстро всасывается из желудочно–кишечного тракта. Абсолютная биодоступность при приеме 10 мг достигает 50%, максимальная концентрация достигается в течение 3 час. после приема внутрь. Период полувыведения (Т½) составляет около 12 час. Прием пищи не оказывает влияния на фармакокинетические показатели. С белками плазмы крови связывается на 87%. Основным путем выведения является кишечник.
Важно! При временном перерыве в терапии Апиксабаном (преднамеренном или случайном) возрастает риск тромбоза. Пациентов следует проинструктировать о необходимости избегать таких перерывов. При временной остановке антикоагуляционного лечения по любым причинам оно должно быть возобновлено как можно скорее.
Не рекомендуется применять у пациентов с заболеванием печени и с повышенным риском кровотечений, во время беременности и в период грудного вскармливания.
Ривароксабан (Ксарелто, тб., покр. обол., 2,5 мг, 10 мг, 15 мг, 20 мг) — высокоселективный дозозависимый прямой ингибитор фактора Ха. Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Высокая биодоступность (80–100%) наблюдается при приеме в дозе 10 мг, которая не зависит от приема пищи. При приеме натощак 20 мг препарата биодоступность составляла всего F=66%. Максимальная концентрация достигается через 2–4 час. после приема. Большая часть Ривароксабана (92–95%) связывается с белками плазмы крови.
Ривароксабан, 2,5 мг, применяют с целью профилактики смертности вследствие сердечно–сосудистых осложнений, инфаркта миокарда у пациентов после острого коронарного синдрома; 10 мг — в профилактике венозной тромбоэмболии у пациентов, которым проводят обширные ортопедические хирургические вмешательства на нижних конечностях, 15 и 20 мг – для лечения тромбоза глубоких вен и тромбоэмболии легочной артерии, а также с целью профилактики их рецидивов и для профилактики системной тромбоэмболии и инсульта у пациентов с фибрилляцией предсердий неклапанного происхождения.
Важно! Не рекомендуется применять препарат во время беременности, в период грудного вскармливания, детям и подросткам до 18 лет, при наличии болезней почек, при наличии злокачественных новообразований и гиперчувствительности у пациентов.