Хиазмально селлярная область что это
Пояснения к проведению исследований для специалистов
При исследовании головного мозгавизуализируются структуры головного мозга, ликворная система, частично придаточные пазухи носа и ротовая полость, макроскопические изменения гипофиза и орбит. Могут быть визуализированы крупные аневризмы сосудов и большие мальформации. Для определения изменений гипофиза (микроаденома) необходимо отдельное исследование хиазмально-селлярной области прицельно. Для исключения изменений в глазницах, в том числе зрительных нервах – прицельно орбит. Для чёткой визуализации структур артерий головного мозга проводится исследование в сосудистом (артериальном) режиме. При необходимости визуализировать венозные синусы – вены головного мозга.
Хиазмально-селлярная область (гипофиз)
Визуализируются следующие анатомические структуры, входящие в понятие хиазмально-селлярной области: гипофиз, турецкое седло, хиазма (перекрест зрительных нервов), сифоны сонных артерий, прилежащие структуры мозга и ликворной системы.
Орбиты
Можно определить анатомическое строение следующих структур: глазные яблоки, глазодвигательные мышцы, слёзные железы, зрительные нервы, хиазма, периорбитальная клетчатка, костные границы глазниц и прилежащих участков головного мозга.
Артерии головного мозга (исследование головного мозга в сосудистом режиме)
После трёхмерной реконструкции видны артерии головного мозга, их анатомическое строение, положение, отхождение от соответствующих участков, размеры просветов, можно оценить проходимость (полная или частичная), симметричность одноимённых артериях, отсутствие или наличие ангиодисплазий (аневризм и сосудистых мальформаций).
Венозные синусы головного мозга.
Визуализируются венозные синусы головного мозга, крупные вены: их наличие, анатомические варианты строения и проходимость.
Исследование позвоночника.
Исследование суставов
В зону диагностического интереса попадает сам исследуемый сустав и околосуставные мягкие ткани. Определяются изменения связок, хрящевых структур (в том числе, менисков), суставной капсулы, состояние костных структур (в некоторых случаях для уточнения костных изменений рекомендуется КТ исследование), мышц. Тазобедренные суставы (левый и правый) всегда исследуются вместе, остальные суставы (локтевой, голеностопный, коленный и т.д.) по одному.
Исследование органов брюшной полости и забрюшинного пространства.
Оценка органов брюшной полости и забрюшинного пространства с определением их размеров, местоположения, изменений. «Неподвижные» органы (печень, селезёнка, желчный пузырь, почки, надпочечники, нижняя полая вена, лимфатические узлы, крупные артерии) визуализируются достаточно хорошо для детального описания. Желудок и кишечник по причине своей подвижности (перистальтики), а также пульсирующая брюшная аорта определяются недостаточно чётко.
Органы малого таза
Визуализируются органы малого таза, оцениваются их размеры, положение относительно друг друга. Для получения максимального количества диагностической информации надо проконсультироваться с врачом кабинета МРТ о подготовке пациента к исследованию. Наличие некоторых видов внутриматочной спирали может затруднить визуализацию из-за появления артефактов.
Мягкие ткани
Исследование мягких тканей конечностей целесообразно при подозрении на наличие патологических изменений и/или пальпации образований, после предшествующих ультразвукового или рентгенологического исследований. В направлении рекомендуется указывать зону диагностического интереса (проксимальная, средняя, дистальная треть, бедра, голени, плеча, предплечья). Непосредственно перед сканированием в районе предполагаемой патологии прикрепляется «маячок». Его роль выполняет капсула с жировым раствором, хорошо видная на всех программах сканирования. Требования для исследования мягких тканей шеи такие же, как для шейного отдела позвоночника.
ВАЖНО! При необходимости выполнить МР исследование области тела, не указанной в списке, проконсультируйтесь с врачом кабинета МРТ!
Аденомы гипофиза. Выступление врача-нейрохирурга Лещинского А.В.
Опухоли гипофиза. Врач-нейрохирург Лещинский Андрей Владиславович.
Краткое содержание:
Здравствуйте, уважаемые слушатели!
Я сам врач-нейрохирург, оперирую опухоли гипофиза. Хиазмально-селлярная область — это место, где находится гипофиз и патологические процессы, которые исходят из него.
Гипофиз — это центральный орган эндокринной системы, который регулирует весь гормональный обмен в организме.
Когда я объясняю пациентам по поводу того, что это такое, я обычно говорю, что гипофиз — это как генерал, который контролирует все железы внутренней секреции, выделяя соответствующие гормоны.
Некоторые гормоны действуют на весь организм, некоторые только прицельно на какие-то органы-мишени.
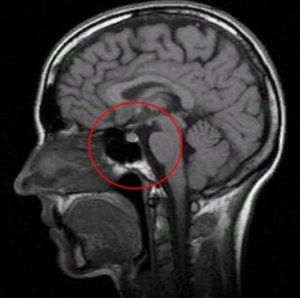
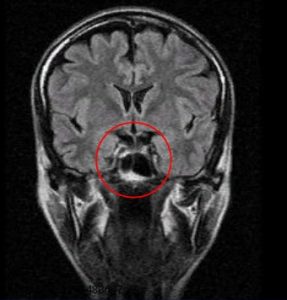
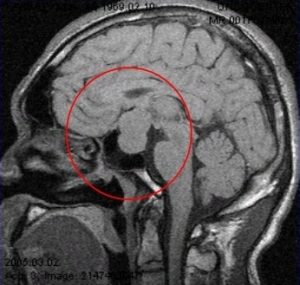
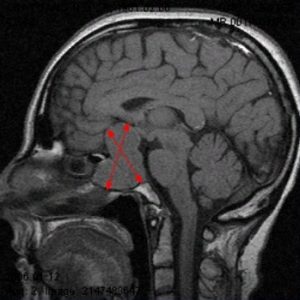
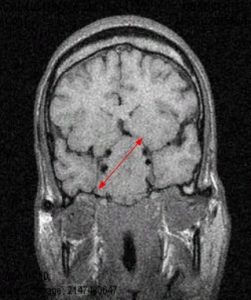
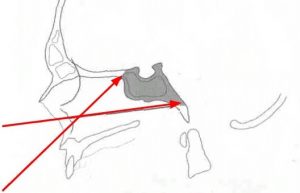
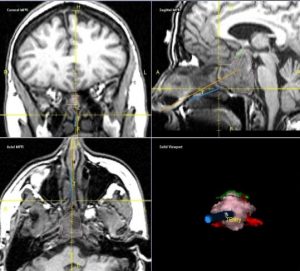
Рис.1 и 2. Нормальная анатомия хиазмально-селлярной области. МРТ
Вот это гипофиз, вот это хиазма, между ними ножка гипофиза или стебель гипофиза. Это нормальная анатомия.
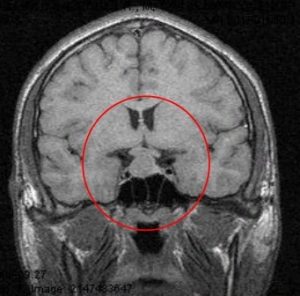
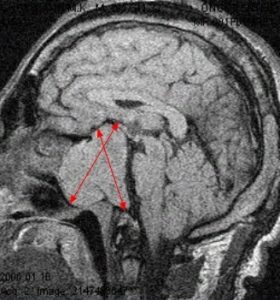
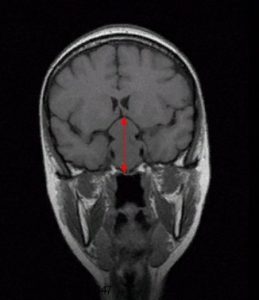
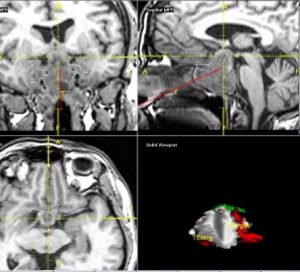
Рис. 3 и 4. Аденома гипофиза. МРТ
На рисунках 3 и 4 показана патологическая анатомия. Из этого маленького органа выросла вот такая большая аденома гипофиза.
Рост опухоли может быть кверху, он называется супраселлярный, может быть книзу, он называется инфраселлярный. Может быть кзади — ретроселлярный, кпереди — антеселлярный. Или вправо или влево — это называется латероселлярный рост в соответствующую сторону, вправо или влево.
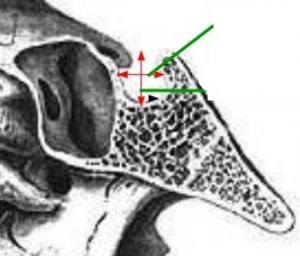
Доступ осуществляется через полость носа, если мы говорим про трансназальный подход. Далее хирург попадает в такую воздухоносную пазуху. Это полость в кости, которая называется основная кость. В ней внутри есть некоторые перегородки. Хирург их убирает и оказывается перед турецким седлом. Турецкое седло — это костный карман, в котором как раз находится гипофиз. То есть хирург делает как бы трепанацию вот здесь вот, убирает косточку, и вот здесь. И попадает в то место, где производится оперативное лечение.
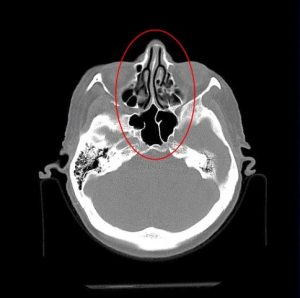
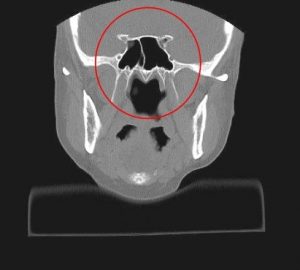
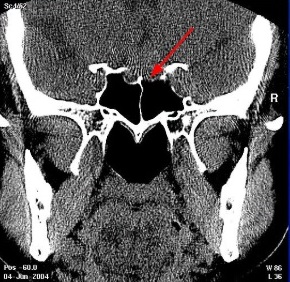
Рис. 5 и 6 Компьютерная томография головного мозга
До этого была магнитно-резонансная томография головного мозга. Это компьютерная томография головного мозга. Просто еще раз хочу показать. Доступ осуществляется через полость носа. Это передняя стенка пазухи. Черное — это воздух. Это задняя стенка пазухи. И хирург оказывается в области турецкого седла. Иногда внутри пазухи существуют дополнительные перегородки.
По размерам нам важно знать, что бывает:
Главное, чтобы размер был минимум в двух проекциях измерен.
Рис.7 Примеры гигантских аденом гипофиза
Вот гигантская аденома гипофиза с супраселлярным ростом кверху, с инфраселлярным ростом книзу. Тут латероселлярный рост в одну из сторон (вправо). И также видите, какой огромный узел. Все это можно удалить.
Рис. 8 Рентгенография черепа (оценка турецкого седла)
Рис. 9 Компьютерная томография
По компьютерной томографии : мы специально иногда ее назначаем, с той точки зрения, чтобы посмотреть, не разрушены ли костные структуры, потому что на КТ очень хорошо видны именно костные структуры.
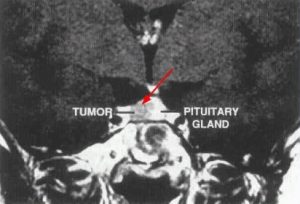
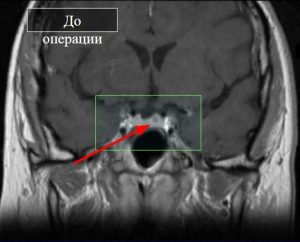
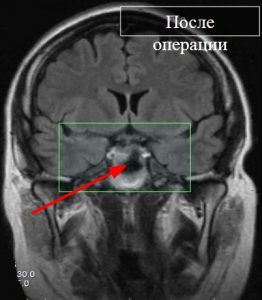
Рис. 10 МРТ с контрастным усилением
Но, тем не менее, золотой стандарт, как я уже сказал, — это МРТ, обязательно с контрастным усилением. На рисунке 10: серое — это опухоль, а эта часть — нормальный гипофиз. Показана стрелкой опухоль. Особенно это актуально для микроаденом гипофиза, которые находятся в толще нормального, неизменённого гипофиза, и которые иными способами выявить невозможно. Это характерно для гормонально активных опухолей, например.
При подозрении на опухоль хиазмально-селлярной области существует следующий алгоритм :
Бывают гормонально активные опухоли и гормонально неактивные.
Гормонально активные опухоли.
Клиническая картина гиперпролактинемии
| Женщины | Мужчины |
| Нарушение менструального цикла: аменорея, олигоменорея, ановуляторные циклы, укорочение лютеиновой фазы | Снижение или отсутствие либидо и потенции |
| Бесплодие | Уменьшение выраженности вторичных половых признаков (особенно при начале заболевания в постпубертатном возрасте) |
| Лакторея | Бесплодие, вследствие олигоспермии |
| Снижение либидо, фригидность | Гинекомастия |
| Гиперандрогения: гирсутизм, акне | Лакторея |
| Метаболические нарушения: остеопороз, ожирение, гиперинсулинемия (вследствие снижения печёночной и периферической резистентности) | |
| Психоэмоциональные нарушения: повышенная утомляемость, слабость | |
Клиническая картина акромегалии:
Клиническая картина гиперкортицизма:
Исходя из того, что бывают опухоли гормонально активные, с уществуют частные показания к операции.
Соматотропиномы — это синдром акромегалии, в качестве первого этапа, иногда при отсутствии эффекта от медикаментозного лечения. Но хирургия все-таки является помощью первой линии.
Пролактинома — при отсутствии эффекта от медикаментозного лечения, при непереносимости препаратов, аллергической реакции, например, на них. Все-таки мы считаем, что первая линия лечения — это медикаментозное лечение. Иногда бывают случаи, когда очень поздно выявили пролактиному у пациента. Она большого или гигантского размера. Очень сильно сдавила окружающие структуры мозга, вызвала, например, нарушение зрения, называется хиазмальный синдром. В этом случае совместно с эндокринологом проводится консилиум и в определенных ситуациях мы отказываемся от медикаментозной терапии, по крайней мере дооперационной, и берем сразу на операцию.
Тиреотропиномы и гонадотропиномы — это редкий вариант опухоли. Их не будем пока обсуждать.
Клиническая картина гормонально неактивных аденом состоит из воздействия массы опухоли на окружающие структуры.
Так как опухоли не выделяют гормоны, пациенты начинают чувствовать, или почувствуют ее намного позже, чем гормонально активные опухоли.
Половые нарушения : аменорея, олигоопсоменорея, лакторея, бесплодие, эректильная дисфункция у мужчин.
Гипопитуитарные нарушения : вторичный гипокортицизм, вторичный гипотиреоз.
Абсолютное показание к операции — это:
Рис. 11 Трансназальный доступ (угол хирургического действия)
Транскраниальные доступы нужны только в отдельно взятых случаях и это обсуждается отдельно с пациентами.
Как я уже говорил, доступ осуществляется через полость носа. Это основная пазуха, воздухоносоная, основная кость, в которой находится вот такая полость. Осуществляется трепанация передней стенки пазухи и задней стенки пазухи. И мы попадаем вот в этот костный кармашек, который называется турецкое седло, где лежит гипофиз, из которого могут развиваться большие опухоли. Стрелками показано, что даже через полость носа можно убирать большие опухоли, которые могут далеко выходить за полость турецкого седла. Это угол хирургического действия, который позволяет нам широко удалять большие опухоли с различными вариантами роста.
То есть существуют некоторые методики, которые позволяют нам удалять распространенные сложные опухоли, большие, например, или те, которые имеют какой-то интересный рост в сторону: вправо, влево, вверх, вниз, которые не видны обычным взглядом, например, через микроскоп.
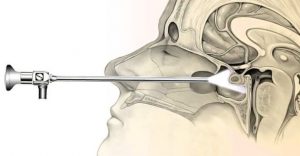
Рис. 11. Применение эндоскопической техники
В данном случае, если вы видите, то зелененькое сверху — это хиазма, то есть зрительные нервы, а красненькое — это сонные артерии. И на нижнем снимке видно, как хирург удаляет часть опухоли. И видно, что это происходит около сонной артерии и он тут должен быть внимательным, собранным, чтобы не повредить данный сосуд. И также это позволяет увидеть часть инструментов, которые могут быть зарегистрированы этой операционной системой, нейронавигацией. Хирург знает, где они расположены. Это очень важный момент.
12 и 13 Использование операционной нейронавигации
Рис. 14. Использование операционной нейронавигации
Применение нейроэндоскопии, системы операционной нейронавигации позволяют:
— Свободно ориентироваться в условиях узкой и глубокой операционной раны (мы говорим про трансназальную хирургию).
— Эта система, все вместе — позволяет улучшить общее состояние пациента после операции и как можно быстрее пациент возвращается к обычной жизни и быстрее выписывается из стационара. Что, мне кажется, является очень важным для пациента.
Некоторые клинические случаи я вам покажу.
Рис. 15 Клинический случай, гигантская аденома гипофиза
Рис. 16 Клинический случай, питуитарная апоплексия
Рис. 17. Клинический случай, небольшие образования
Рис. 18 Клинический случай, микроаденома (кортикотропинома)
Среднее пребывание в палате реанимации у пациентов в основном не более суток. Пациент прооперирован, на следующий день переводится в свою палату. На 3-6 сутки он может быть выписан.
Фотография сделана на третьи сутки после операции. Это типичные пациенты с акромегалией, у которых были удалены опухоли, выделяющие гормон роста, соматотропиномы.
Производится в это время:
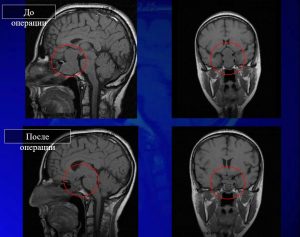
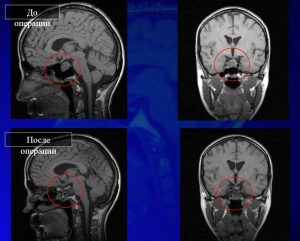
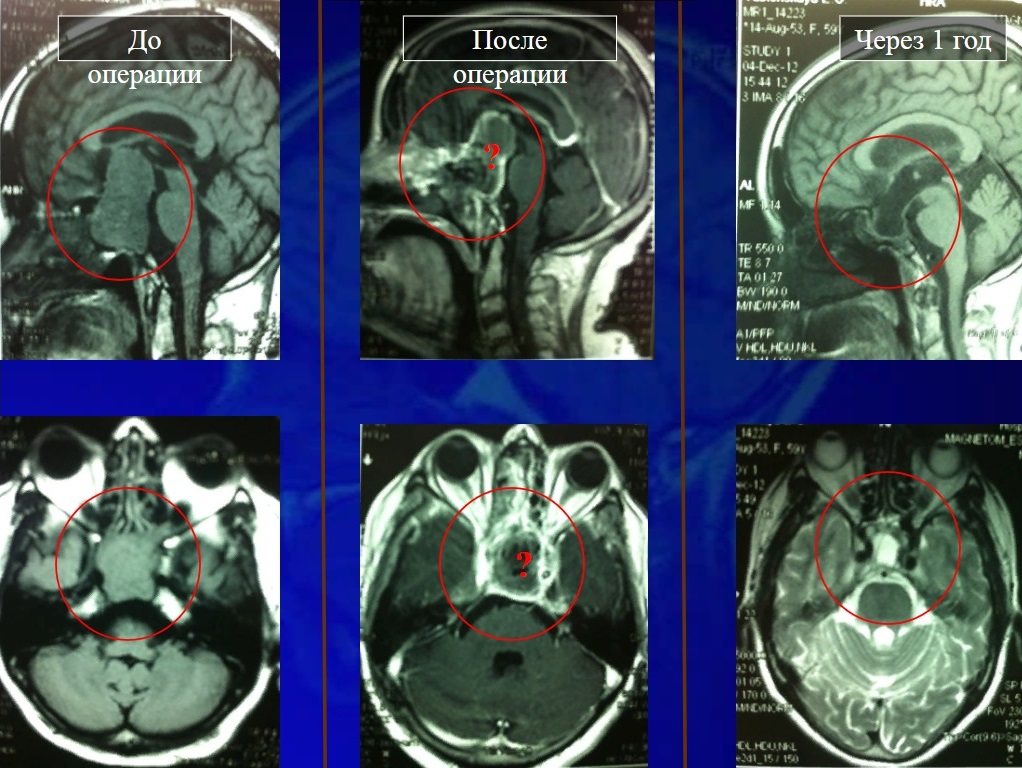
Рис. 19 Снимки МРТ до операции, сразу после и через год
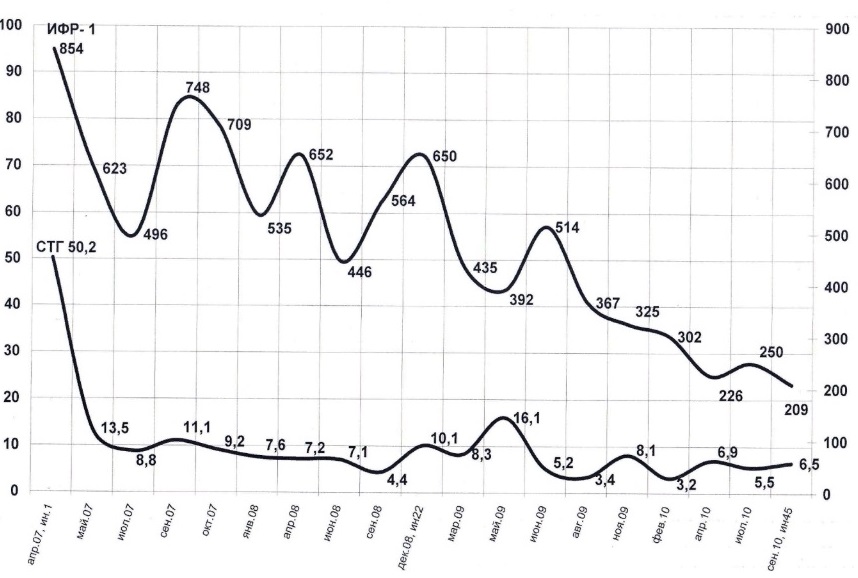
Рис. 20 Динамика СТГ, ИРФ-1 после операции
Конечно же, это командная работа : то есть это офтальмолог, невролог, эндокринолог, нейрохирург, рентгенолог, лор-врач, иногда радиотерапевт, если будет требоваться лучевая терапия.
Показания к радиохирургии:
Радиохирургических установок очень много, самая распространенная — это гамма-нож или кибер-нож. (Рисунок 21)
Рис. 21 Радиохирургические установки
Благодарю вас за внимание, если у вас будут какие-то вопросы — задавайте. Если есть какие-то личные вопросы, пожалуйста, тут моя почта, мой телефон.
Диагностика и лечение метастатических опухолей в хиазмально – селлярную область
Анализ результатов диагностики и нейрохирургического лечения метастатических опухолей, локализованных в хиазмально – селярную область
Введение
Клинически метастазы в ХСО проявляются общемозговой симптоматикой, нарушением секреции гормонов гипофиза, глазодвигательными и зрительными нарушениями, симптомами поражения ветвей тройничного нерва (Bagan, 1980).
Диагностика метастазов в ХСО сложна. По литературным данным в 56% случаев метастатические опухоли ХСО являются первыми проявлениями онкологического заболевания (Abrams, 1950). Отсутствие онкологического анамнеза, патогномоничных симптомов, специфических признаков нейровизуализации усложняют дифференциальную диагностику между метастатическим поражением ХСО и первичными опухолями данной локализации (Bell, 2001; Buonaguidi, 1983). Окончательная диагностика возможна только на основе патоморфологического и иммуногистохимического исследований (ИГХ) (Nelson, 1987).
Лечение метастазов в ХСО комбинированное. В большинстве случаев первым этапом является нейрохирургическое вмешательство, направленное на гистологическую верификацию опухоли и на декомпрессию зрительных и глазодвигательных нервов, с последующей химиотерапией, лучевой терапией или стереотаксической радиохирургией (Roessmann, 1970). Многие авторы считают, что удаление опухолей не существенно влияет на продолжительность жизни, но в сочетании с последующими лучевыми методами лечения улучшает качество жизни больных (Bell, 2001; Gsponer, 1999).
Материал и методы
С 2007 по 2013 гг. в НИИ нейрохирургии им. акад. Н. Н. Бурденко наблюдались 163 больных с метастатическими опухолями основания черепа. В 19 (20, 4%) случаях метастазы локализовались в ХСО. Соотношение М: Ж было около 1: 2; Женщин в данной группе было 12 (63, 2%), мужчин – 7 (36, 8%). Средний возраст больных с метастазами в ХСО составлял 40 лет (минимальный возраст 13 лет, максимальный – 72 года). Предоперационно всем больным выполнялось МРТ головного мозга с внутривенным контрастированием.
Всем больным выполнено нейроофтальмологическое обследование, оценивались острота зрения, поля зрения, осматривалось глазное дно.
Проводилось исследование гормонов аденогипофиза. Наличие или отсутствие несахарного мочеизнурения оценивалось клинически, а также на основе осмолярности и электролитного состава мочи и крови.
Окончательная диагностика выполнялась на основе патоморфологического и или иммуногистохимического исследования биоптата или аутопсийного материала в одном случае. Иммуногистохимическое исследование выполнялось в 14 наблюдениях.
19 больным были выполнены оперативные вмешательства с целью гистологической верификации опухоли, и уменьшения ее размеров. Оперативные вмешательства выполнялись 2 способами – транскраниальным и трнсназальным. В большинстве случаев трансназальные оперативные вмешательства выполнялись с применением эндоскопической техники.
В 5 случаях после оперативных вмешательств выполнялись стереотаксическая рад
Результаты
Диагностика метастатических опухолей ХСО основывалась на анамнезе, клинической картине, данных нейровизуализации и результатов патоморфологического и иммуногистохимического исследований.
Клиническая картина складывалась из дисфункции гипофиза, зрительных, глазодвигательных нарушений, симптомов поражения лобной и височной долей и общемозговой симптоматики. Нарушения функций аденогипофиза в нашем наблюдении отмечались в 5 (26, 3%) случаях. У 2 (10, 5%) пациентов гормональные нарушения проявлялись в виде гипокортицизма и гипотиреоза, в 3 (15, 8%) случаях в виде пангипопитуитаризма. Картина поражения нейрогипофиза с синдромом несахарного мочеизнурения наблюдалось у 3 (15, 8%) больных. Сочетание несахарного мочеизнурения и дисфункция аденогипофиза наблюдались у 2 (10, 5%) больных.
Дисфункция ветвей тройничного нерва в виде снижения чувствительности на лице наблюдалась у 3 больных.
Общемозговая симптоматика проявлялась в 4 (23, 5%) случаях в виде головных болей. У 1 больного с преимущественно супраселлярным ростом опухоли с компрессией дна 3 желудочка наблюдался Корсаковский синдром.
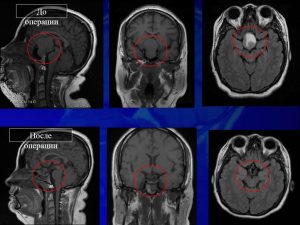
Всем больным была выполнена МРТ головного мозга с внутривенным контрастированием, оценивались МР характеристики опухоли, локализацию, соотношение с окружающими структурами (рис. 1). В 15 (79%) наблюдениях из 19 дооперационно установлен диагноз метастаз в ХСО, как наиболее вероятный на основе онкологического анамнеза и данных МРТ. В 4 случаях больные поступали с результатами КТ головного мозга, на которой определялись образования ХСО, вызывающие деструкцию турецкого седла, ската (рис. 2).
В нашем наблюдении в 7 (36, 8%) случаях метастазы имели эндо – супра – латероселлярный рост с односторонним распространением в кавернозный синус. В остальных 12 (63, 2%) случаях опухоли распространялись эндо – супраселлярно. Характер роста опухоли определял хирургическую тактику.
Редко при метастатическом поражении ХСО в морфологическом препарате возможно визуализировать ткань метастаза с тканью гипофиза (рис. 3)
19 больным выполнено 23 оперативных вмешательств. Срок от момента проявления симптомов поражения структур ХСО до хирургического вмешательства составлял в среднем 5, 4 месяца (от 1 месяца до 1 года).
В 19 (82, 6%) случаях производились эндоскопические трансназальные оперативные вмешательства, 9 из которых описаны как «парциальное удаление», 5 «удаление», 4 «биопсия опухоли». В одном случае проводилась пластика ликворной фистулы аутотканями. Одному больному с метастазом почечноклеточного рака выполнена трехкратная трансназальная резекция опухоли через 12 месяцев после первой и через 4 месяца после второй операций, в связи с увеличением размеров опухоли ХСО и нарастанием зрительных нарушений.
Одной больной через 19 месяцев после транскраниальной операции в связи с продолженным ростом опухоли выполнена трансназальная резекция рецидива опухоли.
Неврологический статус оценивался у всех больных в раннем послеоперационном периоде к моменту выписки из клиники. В 15 (88, 2%) случаях больные были выписаны из клиники без неврологического ухудшения, а улучшение в виде регресса головных болей наблюдалось у 3 пациентов.
Улучшения гормонального статуса больных после оперативных вмешательств не отмечалось. У 2 (11, 8%) больных было усугубление электролитных нарушений, которые регрессировали на фоне заместительной терапии. Предсуществующий несахарный диабет не регрессировал.
После нейрохирургических вмешательств по поводу метастатических опухолей ХСО не наблюдается драматического улучшения зрительных и глазодвигательных функций, характерного для хирургии доброкачественных образований (менингиом, аденом) данной локализации. Из 19 случаев, зрительные функций в раннем послеоперационном периоде оценивалось у 15 (79%) больных. Из них зрительные и глазодвигательные функций остались без динамики в 8 (53, 3%) случаях, ухудшение наблюдалось в 4 (26, 7%) наблюдениях, и улучшение у 3 (15, 8%) пациентов. В отдаленном периоде (более чем 3 месяцев) зрительная и глазодвигательная функций оценивались в 7 (36, 8%) случаях. Среди них улучшение отмечалось в 3 случаях, прогрессивное ухудшение в 3 наблюдениях, и в 1 случае не отмечалось динамики. Отсутствие изменений а так же ухудшение зрительной функции при хирургии метастазов основания черепа обусловлено невозможностью радикального удаления данных опухолей и инфильтативным тесным соотношением в зрительными и глазодвигательными нервами, вследствие чего излишняя радикальность приводит к отрицательным результатам.
Интраоперационные и ранние послеоперационные осложнения наблюдались у 5 (26%) пациентов. В 2 случаях была интраоперационная кровопотеря до 2, 5 литров (рак почки и рак простаты). У 1 больной в раннем послеоперационном периоде возникла назальная ликворея. В раннем послеоперационном периоде неврологическое ухудшение наблюдалось в 2 случаях при транскраниальных оперативных вмешательствах. В одном наблюдении отмечалось нарастание пареза отводящего нерва, регрессировавшего после проведенного лечения. У 1 больной после транскраниальной резекции метастаза рака молочной железы возник стойкий правосторонний амавроз.
Летальных исходов вследствие оперативных вмешательств не было.
В послеоперационном периоде в 2 случаях проводилась СТРХ, еще 3 пациентам проводилась лучевая терапия на хиазмально – селлярную область. В одном наблюдении через 6 месяцев после проведения лучевой терапии было снижение зрения с 0, 7 до 0, 1 вследствие лучевых изменений в зрительном нерве.
Обсуждение
В различных сочетаниях встречаются нарушения секреторной функции аденогипофиза. Гипопитуитаризм проявляется гипотиреозом в 33, 3%, гипокортицизмом в 30, 6%, гипопролактинемией в 11, 1% случаев, низким уровнем тестостерона в 11, 1% наблюдений. В 22, 2% случаев описывается пангипопитуитаризм (Bell, 2001).
При метастазах ХСО зрительные нарушения в виде снижения зрения, а так же сужения и выпадения полей зрения встречается в 7-50% случаев (Branch, 1987).
Вследствие частой и прогрессирующей инвазии метастазов в кавернозный синус наблюдается быстро нарастающая головная боль в сочетании с глазодвигательными нарушениями и выпадениями чувствительности на лице (Bell, 2001). Частота глазодвигательных нарушений при метастатических поражениях ХСО достигает 15-43% (Cox, 1979), при менингиомах кавернозного синуса встречаются в 42% (Gasponer, 1999), при хордомах основания черепа – в 70% (Bagan, 1980). Глазодвигательные нарушения при аденомах гипофиза встречаются значительно реже: в 6, 7% случаев по данным Калинина П. Л. и в 8, 3% по наблюдениям Шкарубо А. Н (Калинин, 2009; Шкарубо, 2007).
Лечение метастазов ХСО комплексное, включает хирургические вмешательства, лучевую терапию, химиотерапию (Шкарубо, 2007). Тотальное удаление метастазов ХСО практически невозможно ввиду интенсивной васкуляризации опухоли, локальной инвазии в окружающие костные структуры и в кавернозный синус, инфильтрации гипоталамуса и зрительных путей (Gsponer, 1999). В наблюдаемой нами серии больных в 12 случаях опухоль была удалена парциально или была выполнена биопсия, в 10 случаях было достигнуто субтотальное удаление.
Вероятность осложнений при хирургических вмешательствах по поводу метастазов ХСО значительно выше по сравнению с доброкачественными образованиями той же локализации (Kattah, 1985). По данным литературы из 21 больных, прооперированных по поводу метастазов в ХСО отмечены такие осложнения как, ликворея в 2 (9, 5%) случаях, карциноматозный менингит у 1 (4, 6%) пациента, ухудшение эндокринной функции в 3 наблюдениях (Bell, 2001).
Продолжительность жизни пациентов с метастазами в ХСО колеблется от 6 месяцев до 5 лет (с момента выявления метастаза) и зависит от распространенности онкологического процесса, локализации других метастазов, возраста пациента, проведенного лечения (Molinatti, 1985). Так, наименьшая продолжительность жизни наблюдается в группе больных старше 65 лет, с мелкоклеточным раком легкого, при обнаружении метастаза в ХСО в период до 1 года с момента диагностики первичной опухоли (Cox, 1979).
По литературным данным метастазы в ХСО становятся непосредственной причиной летального исхода в около 14 % (Molinatti, 1985).
Заключение
В клинической практике метастатические опухоли ХСО встречаются редко. Ввиду отсутствия онкологического анамнеза, патогномоничных клинических признаков и характерных данных нейровизуализации, окончательная диагностика возможна только на основе результатов патоморфологического и иммуногистохимического исследований.
Метастатические опухоли ХСО в основном доступны для трансназальных оперативных вмешательств, однако при преимущественно супраселлярном или латероселлярном росте солитарных метастазов предпочтительны транскраниальные операций.
При единичном метастазе, исходном хорошем состоянии больного, ожидаемой большой продолжительности жизни показана широкая резекция опухоли. В противоположных случаях нейрохирургическое вмешательство выполняется только с целью гистологической верификации опухоли.
Как правило, нейрохирургические вмешательства не улучшают функций гипофиза и только в редких случаях приводят к улучшению зрительных и глазодвигательных функций.
Продолжительность жизни больше при агрессивной хирургической тактике с последующим лечением химиотерапией и лучевой терапией. При исходно тяжелом состоянии больных, которым проводилась только биопсия для верификации диагноза без последующего лечения, летальный исход наступал в течение 3 месяцев после оперативного вмешательства вследствие прогрессии опухоли ХСО.
Список литературы:
Дис. …доктора мед. наук: 14. 00. 28 / НИИ нейрохирургии им. акад Н. Н. Бурденко. Москва. 2007. 389 с.